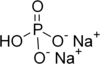Фосфаты натрия - Sodium phosphates
Фосфат натрия является общим термином для множества соли из натрий (Na+) и фосфат (PO43−). Фосфат также образует семейства или конденсированные анионы, включая ди-, три-, тетра- и полифосфаты. Большинство этих солей известны как в безводной (безводной), так и в гидратированной формах. Гидраты встречаются чаще, чем безводные формы.[1]
Использует
Фосфаты натрия находят множество применений в пищевых продуктах и для очистки воды. Например, фосфаты натрия часто используются в качестве эмульгаторы (как в плавленный сыр ),[2] загустители, и разрыхлители для выпечки. Они также используются для контроля pH обработанных пищевых продуктов.[3] Они также используются в медицине для запор и подготовить кишечник к медицинским процедурам. Кроме того, они используются в моющих средствах для смягчения воды и как эффективное средство против ржавчины.
Побочные эффекты
Фосфаты натрия популярны в торговле отчасти потому, что они недорогие, и потому, что они нетоксичны при нормальном уровне потребления.[4] Однако пероральный прием фосфатов натрия в высоких дозах для подготовка кишечника за колоноскопия может у некоторых людей нести риск повреждения почек в виде фосфатная нефропатия. Существует несколько пероральных фосфатных композиций, которые готовятся экстемпорально. Препараты для перорального приема фосфатов были отменены в США, хотя доказательства их причинно-следственной связи неоднозначны.[5] Поскольку доступны безопасные и эффективные заменители фосфатных слабительных средств, некоторые медицинские авторитеты рекомендовали полностью отказаться от пероральных фосфатов.[6]
Монофосфаты
Распространены три семейства монофосфатов натрия, производные ортофосфата (PO43−), гидрофосфат (HPO42−) и дигидрофосфат (H2PO4−). Некоторые из наиболее известных солей показаны в таблице.
| имя | формула | Регистрационный номер CAS |
|---|---|---|
| мононатрий фосфат (безводный) | Неа2PO4 | 7558-80-7 |
| мононатрий фосфат (моногидрат) | Неа2PO4(ЧАС2O) | 10049-21-5 |
| мононатрий фосфат (дигидрат) | Неа2PO4(ЧАС2O)2 | 13472-35-0 |
| динатрий фосфат (безводный) | Na2HPO4 | 7558-79-4 |
| динатрий фосфат (дигидрат) | HNa2PO4(ЧАС2O)2 | 10028-24-7 |
| динатрий фосфат (гептагидрат) | HNa2PO4(ЧАС2O)7 | 7782-85-6 |
| динатрий фосфат (октагидрат) | HNa2PO4(ЧАС2O)8 | |
| динатрий фосфат (додекагидрат) | HNa2PO4(ЧАС2O)12 | 10039-32-4 |
| тринатрийфосфат (безводный, гексагональный) | Na3PO4 | |
| тринатрийфосфат (безводный, кубический) | Na3PO4 | 7601-54-9 |
| тринатрийфосфат (полугидрат) | Na3PO4(ЧАС2O)0.5 | |
| тринатрийфосфат (гексагидрат) | Na3PO4(ЧАС2O)6 | |
| тринатрийфосфат (октагидрат) | Na3PO4(ЧАС2O)8 | |
| тринатрийфосфат (додекагидрат) | Na3PO4(ЧАС2O)12 | 10101-89-0 |
Ди- и полифосфаты
Помимо этих фосфатов, натрий образует ряд полезных солей с пирофосфаты (также называемые дифосфатами), трифосфатами и высокополимерами. Из этих солей соли дифосфатов особенно распространены в продаже.
| имя | формула | Регистрационный номер CAS |
|---|---|---|
| мононатрия дифосфат (безводный) | Неа3п2О7 | |
| динатрий дифосфат (безводный) | Na2ЧАС2п2О7 | 7758-16-9 |
| динатрия дифосфат (гексагидрат) | Na2ЧАС2п2О7(ЧАС2O)6 | |
| тринатрийдифосфат (безводный) | Na3HP2О7 | |
| тринатрийдифосфат (моногидрат) | Na3HP2О7(ЧАС2O) | |
| тринатрийдифосфат (нонагидрат) | Na3HP2О7(ЧАС2O)9 | |
| тетранатрий дифосфат (безводный) | Na4п2О7 | 7722-88-5 |
| тетранатрий дифосфат (декагидрат) | Na4п2О7(ЧАС2O)10 | 13472-36-1 |
Помимо дифосфатов, соли натрия известны как трифосфаты, например трифосфат натрия и тетрафосфаты. Циклические полифосфаты, называемые метафосфатами, включают тример триметафосфат натрия и тетрамер Na3п3О9 и Na4п4О12, соответственно.
Полимерные фосфаты натрия образуются при нагревании смесей NaH2PO4 и Na2HPO4, что индуцирует реакция конденсации. Конкретный образующийся полифосфат зависит от деталей нагрева и отжига. Одна производная - это стеклянный (т.е. аморфный) Соль Грэма. Это линейный полифосфат средней формулы NaO (NaPO3) Na2. Кристаллические полифосфаты с высокой молекулярной массой включают: Соль Куррола и Соль Мэддрелла (CAS № 10361-03-2). Эти виды имеют формулу [NaPO3]п[NaPO3(ОЙ)]2 где n может достигать 2000. По своей структуре эти полимеры состоят из ПО3− «мономеры», цепи которых заканчиваются протонированными фосфатами.[1][7]
Рекомендации
- ^ а б Клаус Шредтер; Герхард Беттерманн; Томас Стаффель; Фридрих Валь; Томас Кляйн; Томас Хофманн (2012). «Фосфорная кислота и фосфаты». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a19_465.pub3.
- ^ http://www.sodiumphosphateformula.com/tag/monosodium-phosphate
- ^ Лампила, Лучина Е. (2013). «Применение и функции пищевых фосфатов». Анна. N.Y. Acad. Наука. 1301 (1): 37–44. Bibcode:2013НЯСА1301 ... 37л. Дои:10.1111 / nyas.12230.
- ^ Раззак, М. С. (2011). «Фосфатная токсичность: новый взгляд на старую проблему». Клиническая наука. 120 (3): 91–97. Дои:10.1042 / CS20100377. ЧВК 3120105. PMID 20958267.
- ^ Маркавиц, Великобритания; Парезелли, Массачусетс (12 августа 2007 г.), «Острый фосфатный нефропатил», Kidney Int., 76 (10), стр. 1027–34, Дои:10.1038 / ки.2009.308, PMID 19675530
- ^ Макки, AC; Брин, L; Amand, KS; Эвиган, М. (август 2007 г.), «Таблетки фосфата натрия и острая фосфатная нефропатия», Am J Gastroenterol, 104 (8), стр. 1903–6, Дои:10.1038 / ajg.2009.342, PMID 19661931
- ^ Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. п. 530. ISBN 978-0-08-037941-8.
внешняя ссылка
- Белл, Рассел Н. (апрель 1973 г.), «Эмульгирующий агент для сыра на основе фосфата натрия и алюминия», Патент США 3726960
- Лиен, Ю. Х. (16 июля 2008 г.), «Является ли подготовка кишечника перед колоноскопией рискованным делом для почек?», Природа Клиническая Практика Нефрология, 4 (11): 606–14, Дои:10.1038 / ncpneph0939, PMID 18797448