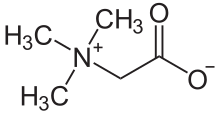
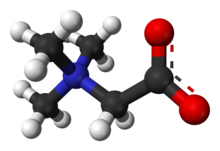
Триметилглицин - Trimethylglycine
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК 2-триметиламмониоацетат | |
Другие имена
| |
| Идентификаторы | |
3D модель (JSmol ) | |
| 3537113 | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.003.174 |
| Номер ЕС |
|
| 26434 | |
| КЕГГ | |
| MeSH | Бетаин |
PubChem CID | |
| UNII | |
| |
| |
| Свойства | |
| C5ЧАС11Нет2 | |
| Молярная масса | 117.146 |
| Внешность | Белое твердое вещество |
| Температура плавления | 180 ° С (356 ° F, 453 К)[1] (разлагается) |
| Растворимый | |
| Растворимость | Метанол |
| Кислотность (пKа) | 1.84 |
| Фармакология | |
| A16AA06 (КТО) | |
| Данные лицензии | |
| Опасности | |
| Пиктограммы GHS |  |
| Сигнальное слово GHS | Предупреждение |
| H315, H319 | |
| P264, P280, P302 + 352, P305 + 351 + 338, P321, P332 + 313, P337 + 313, P362 | |
| Родственные соединения | |
Связанный аминокислоты | Глицин Метилглицин Диметилглицин |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Триметилглицин (TMG) является производное аминокислоты что происходит в растениях. Триметилглицин был первым бетаин обнаружен; первоначально это называлось просто бетаин потому что в 19 веке он был обнаружен в сахарная свекла.[2] С тех пор было открыто много других бетаинов, и более конкретное название глицин бетаин отличает этот.
Структура и реакции
Триметилглицин - это N-метилированная аминокислота. Это цвиттерион поскольку молекула содержит как четвертичный аммоний группа и карбоксильная группа. Карбоксильная группа будет частично протонирована в водном растворе ниже pH 4, то есть ниже pH, равного (pKа − 2).
- (CH
3)
3N+
CH
2CO−
2 (водн.) + ЧАС+
⇌ (CH
3)
3N+
CH
2CO
2ЧАС (водн.)
Деметилирование TMG дает диметилглицин.
Производственные и биохимические процессы
Обработка сахароза из сахарной свеклы дает глицин бетаин в качестве побочный продукт. Значение[требуется разъяснение ] TMG соперничает с содержанием сахара в сахарной свекле.[3]
Биосинтез
У большинства организмов глицин бетаин биосинтезируется путем окисления холин в два шага. Промежуточный, бетаиновый альдегид, образуется под действием фермента митохондриальной холиноксидазы (холиндегидрогеназа, EC 1.1.99.1). Бетаиновый альдегид далее окисляется в митохондрии у мышей к бетаину ферментом бетаинальдегиддегидрогеназой (EC 1.2.1.8).[4][5] У человека активность бетаинового альдегида осуществляется неспецифическим ферментом цистозоловым альдегиддегидрогеназой (EC 1.2.1.3). [6]
Биологическая функция
TMG - это органический осмолит. Свеклу выращивали из морская свекла, которому необходимы осмолиты для выживания в засоленных почвах прибрежных районов. TMG также встречается в высоких концентрациях (~ 10 мМ) у многих морских беспозвоночных, таких как ракообразные и моллюски. Он служит мощным аттрактантом для хищников широкого профиля, таких как хищные морская улитка Плевробранхеи калифорнийские.[7]
TMG - важный кофактор в метилирование, процесс, который происходит в каждой клетке млекопитающего, отдающей метильные группы (–CH3) для других процессов в организме. Эти процессы включают синтез нейротрансмиттеры такие как дофамин и серотонин. Метилирование также необходимо для биосинтеза мелатонин и электронная транспортная цепь составляющая коэнзим Q10, а также метилирование ДНК для эпигенетики.
Главный этап цикла метилирования - реметилирование гомоцистеин, соединение, которое естественным образом образуется при деметилировании незаменимой аминокислоты. метионин. Несмотря на его естественное образование, гомоцистеин связан с воспалением, депрессией, определенными формами деменции и различными типами сосудистых заболеваний. Процесс реметилирования, который детоксифицирует гомоцистеин и преобразует его обратно в метионин, может происходить одним из двух путей. Путь, присутствующий практически во всех клетках, включает фермент метионинсинтаза (MS), что требует витамин B12 как кофактор, а также косвенно зависит от фолиевая кислота и другие Витамины группы B. Второй путь (ограниченный печенью и почками у большинства млекопитающих) включает: бетаин-гомоцистеинметилтрансфераза (BHMT) и требует TMG в качестве кофактора. В нормальных физиологических условиях эти два пути в равной степени способствуют удалению гомоцистеина из организма.[8]. Дальнейшее расщепление бетаина с помощью фермента диметилглициндегидрогеназа производит фолиевую кислоту, тем самым возвращая метионинсинтазу. Таким образом, бетаин участвует в синтезе многих биологически важных молекул и может быть даже более важным в ситуациях, когда основной путь регенерации метионина из гомоцистеина нарушен генетическими полиморфизмами, такими как мутации в гене MS.
TMG в сельском хозяйстве и аквакультуре
Заводские фермы дополнение корм с TMG и лизин увеличить поголовье мышечная масса (и, следовательно, «выход туши», количество годного к употреблению мяса).
Лососевые фермы применяйте TMG для снятия осмотического давления на клетки рыб, когда рабочие переводят рыбу из пресной в соленую.[3][9]
Добавка TMG снижает количество жировая ткань у свиней; однако исследования на людях не показали влияния на массу тела, состав тела или расход энергии в состоянии покоя.[10]
TMG в рационе человека
| Еда | TMG (мг / 100 г) |
|---|---|
| Лебеда | 630 |
| Шпинат | 577 |
| Пшеницы отруби | 360 |
| Баранина | 332 |
| Свекла | 256 |
Биологически активная добавка
Хотя добавление TMG снижает количество жировая ткань у свиней исследования на людях не показали влияния на массу тела, состав тела или расход энергии в состоянии покоя при использовании в сочетании с низкокалорийной диетой.[10] В Управление по контролю за продуктами и лекарствами Соединенных Штатов одобрил безводный триметилглицин (также известный под торговой маркой Цистадан) для лечения гомоцистинурия, заболевание, вызванное аномально высоким гомоцистеин уровни при рождении.[11] TMG также используется как гидрохлорид поваренная соль (продается как бетаин гидрохлорид или бетаин HCl). Бетаина гидрохлорид когда-то разрешался в лекарства, отпускаемые без рецепта (OTC) как желудочная помощь в Соединенных Штатах. Кодекс федеральных нормативных актов США, раздел 21, раздел 310.540, который вступил в силу 10 ноября 1993 г., запретил использование бетаина гидрохлорида в безрецептурных продуктах из-за недостаточности доказательств, чтобы классифицировать его как «общепризнанный как безопасный и эффективный».[12]
Добавка TMG может вызвать понос, расстройство желудка или тошнота. Добавка TMG снижает уровень гомоцистеина, но также повышает уровень холестерина ЛПНП.[13]
Другое использование: ПЦР
Триметилглицин может действовать как адъювант из полимеразной цепной реакции (ПЦР) процесс и другие ДНК-полимераза -основанные анализы, такие как Секвенирование ДНК. По неизвестному механизму он помогает предотвратить образование вторичных структур в молекулах ДНК и предотвращает проблемы, связанные с амплификацией и секвенированием областей, богатых GC. Триметилглицин делает гуанозин и цитидин (сильные связующие) ведут себя с термодинамикой, подобной термодинамике тимидин и аденозин (слабые связующие). Экспериментально установлено, что его лучше всего использовать при конечной концентрации 1 М.[14]
Спекулятивное использование
Лабораторные исследования и два клинических испытания показали, что TMG является потенциальным средством лечения безалкогольных стеатогепатит.[15][16][17]
TMG был предложен для лечения депрессии. Теоретически это увеличило бы S-аденозилметионин (SAMe) реетилированием гомоцистеина. Тот же результат преобразования гомоцистеина в метионин может быть достигнут при добавлении фолиевой кислоты и витамина B12, метионина затем служит предшественником синтеза SAMe. Показано, что SAMe в качестве пищевой добавки действует как неспецифический антидепрессант.[18]
Исследования с целью разработки экологически безопасных биомиметические покрытия для судов использует TMG, среди прочего, в качестве нетоксичного противообрастающего покрытия[нужна цитата ].
Ионообменная хроматография IEX
В книге Amersham Biosciences / GE Healthcare, Ионообменная хроматография и хроматофокусирование - Принципы и методы, стр. 48. «Цвиттерионные добавки, такие как бетаин, могут предотвращать осаждение и могут использоваться в высоких концентрациях, не влияя на градиентное элюирование»[нужна цитата ]
использованная литература
- ^ Acheson, R.M .; Бонд, Дж. Дж. Ф. (1956). «52. Реакции присоединения гетероциклических соединений. Часть II. Фенантридин и метилацетилендикарбоксилат в метаноле». J. Chem. Soc. 1956: 246. Дои:10.1039 / JR9560000246.
- ^ Schiweck, Hubert; Кларк, Маргарет; Поллах, Гюнтер. «Сахар». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a25_345.pub2.
- ^ а б Мякеля, П. (2004). «Агропромышленное использование глицинбетаина». Sugar Tech. 6 (4): 207–212. Дои:10.1007 / BF02942500. HDL:10138/312331. S2CID 25219649.
- ^ Kempf, B .; Бремер, Э. (1998). «Поглощение и синтез совместимых растворенных веществ в качестве реакции микробного стресса на среду с высокой осмоляльностью». Arch. Микробиол. 170 (5): 319–330. Дои:10.1007 / s002030050649. PMID 9818351. S2CID 8045279.
- ^ «BRENDA - Информация по EC 1.2.1.8 - бетаин-альдегиддегидрогеназа». Brenda-enzymes.org. Получено 2016-07-07.
- ^ Черн, М. К .; Петрушко, Р. (1999). «Доказательства митохондриальной локализации бетаинальдегиддегидрогеназы в печени крысы: очистка, характеристика и сравнение с цитоплазматическим изоферментом E3 человека». Биохимия и клеточная биология. 77 (3): 179–187. Дои:10.1139 / o99-030. PMID 10505788.
- ^ Gillette, R .; Huang, R.C .; Hatcher, N .; Мороз, Л. Л. (март 2000 г.). «Потенциал анализа затрат и выгод при кормлении хищной улитки путем интеграции голода, вкуса и боли». Proc. Natl. Акад. Sci. Соединенные Штаты Америки. 97 (7): 3585–3590. Bibcode:2000PNAS ... 97.3585G. Дои:10.1073 / пнас.97.7.3585. ЧВК 16283. PMID 10737805.
- ^ Финкельштейн, Дж. Д. (1998-03-24). «Метаболизм гомоцистеина: пути и регуляция». Европейский журнал педиатрии. 157 (S2): S40 – S44. Дои:10.1007 / пл00014300. ISSN 0340-6199. PMID 9587024.
- ^ Xue, M .; Xie, S .; Цуй, Ю. (2004). «Влияние стимулятора кормления на пищевую адаптацию карпа гибеля». Carassius auratus gibelio (Блох), кормил диетами с заменой рыбной муки мясо-костной ». Aquacult. Res. 35 (5): 473–482. Дои:10.1111 / j.1365-2109.2004.01041.x.
- ^ а б Schwab, U .; Törrönen, A .; Toppinen, L .; и другие. (Ноябрь 2002 г.). «Добавка бетаина снижает концентрацию гомоцистеина в плазме, но не влияет на массу тела, состав тела или расход энергии в состоянии покоя у людей». Am. J. Clin. Нутр. 76 (5): 961–967. Дои:10.1093 / ajcn / 76.5.961. PMID 12399266.
- ^ Holm, P. I .; Ueland, P.M .; Vollset, S.E .; и другие. (Февраль 2005 г.). «Статус бетаина и фолиевой кислоты как кооперативные детерминанты гомоцистеина плазмы у людей». Артериосклер. Тромб. Васк. Биол. 25 (2): 379–385. Дои:10.1161 / 01.ATV.0000151283.33976.e6. PMID 15550695.
- ^ "CFR - Свод федеральных правил, раздел 21". Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США.
- ^ Olthof MR, van Vliet T, Verhoef P, Zock PL, Katan MB (2005). «Влияние нутриентов, снижающих уровень гомоцистеина, на липиды крови: результаты четырех рандомизированных плацебо-контролируемых исследований на здоровых людях». PLOS Med. 2 (5): e135. Дои:10.1371 / journal.pmed.0020135. ЧВК 1140947. PMID 15916468.
- ^ Henke, W .; Herdel, K .; Юнг, К .; Schnorr, D .; Лёнинг, С. А. (октябрь 1997 г.). «Бетаин улучшает ПЦР-амплификацию GC-богатых последовательностей ДНК». Нуклеиновые кислоты Res. 25 (19): 3957–3958. Дои:10.1093 / nar / 25.19.3957. ЧВК 146979. PMID 9380524.
- ^ Angulo, P .; Линдор, К. Д. (2001). «Лечение неалкогольной жировой болезни печени: современные и новые методы лечения». Семин. Печень Dis. 21 (1): 81–88. Дои:10.1055 / с-2001-12931. PMID 11296699.
- ^ Абдельмалек, М. Ф .; Sanderson, S.O .; Angulo, P .; и другие. (Декабрь 2009 г.). «Бетаин при неалкогольной жировой болезни печени: результаты рандомизированного плацебо-контролируемого исследования». Гепатология. 50 (6): 1818–26. Дои:10.1002 / hep.23239. PMID 19824078.
- ^ Miglio, F .; Rovati, L.C .; Санторо, А .; Сетникар И. (август 2000 г.). «Эффективность и безопасность перорального бетаин-глюкуроната при неалкогольном стеатогепатите. Двойное слепое рандомизированное плацебо-контролируемое проспективное клиническое исследование в параллельных группах». Arzneimittelforschung. 50 (8): 722–7. Дои:10.1055 / с-0031-1300279. PMID 10994156.
- ^ Мишулон Д., Фава М. (2002). «Роль S-аденозил-L-метионина в лечении депрессии: обзор доказательств». Am. J. Clin. Нутр. 76 (5): 1158С – 61С. Дои:10.1093 / ajcn / 76.5.1158s. PMID 12420702.
внешние ссылки
- База данных USDA по содержанию холина в общих продуктах питания - включая данные о метаболитах холина, таких как бетаин, в 434 пищевых продуктах.
