Ортонитрат - Orthonitrate
 | |
| Имена | |
|---|---|
| Название ИЮПАК Ортонитрат | |
| Идентификаторы | |
3D модель (JSmol ) | |
PubChem CID |
|
| |
| |
| Характеристики | |
| НЕТ3− 4 | |
| Молярная масса | 78.006 |
| Конъюгированная кислота | Ортонитриновая кислота |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
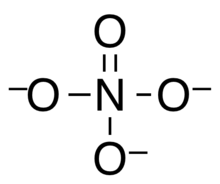
Ортонитрат четырехгранный оксоанион азота по формуле НЕТ3−
4. Впервые был обнаружен в 1977 году.[1] и в настоящее время известен только в двух соединениях: ортонитрат натрия (Na3НЕТ4) и ортонитрат калия (K3НЕТ4). Соответствующая оксокислота, ортоназотная кислота (H3НЕТ4), является гипотетическим и никогда не наблюдалось. Ортонитрат натрия и калия можно получить путем сплавления нитрата и оксида металла при высоких температурах.[2] и в идеале высокие давления (несколько ГПа ).[3]
- NaNO3 + Na2O → Na3НЕТ4 (300 ° C в течение 3 дней)[4]
Получающиеся ортонитраты представляют собой белые твердые вещества, чрезвычайно чувствительные к влаге и CO.2, разлагаясь в течение нескольких минут до гидроксида натрия, карбоната натрия и нитрата натрия при контакте с воздухом.[1]
- Na3НЕТ4 + CO2 → NaNO3 + Na2CO3
- Na3НЕТ4 + H2O → NaNO3 + 2NaOH
Ортонитрат-ион является тетраэдрическим с длиной связи N – O 139 пм, что неожиданно коротко, что указывает на то, что полярные взаимодействия укорачивают связь.[4] Эта короткая длина связи параллельна оксоанионам, содержащим элементы третьего ряда, такие как PO43− и так42−, для которого связь pπ-dπ ранее была предложена в качестве объяснения короткой длины связи. Поскольку 3d-орбитали азота имеют слишком большую энергию, чтобы участвовать в случае ортонитрата, короткая связь N – O в ортонитрате указывает на то, что связывание pπ-dπ, вероятно, не является самым важным объяснением длин связей этих более тяжелых анионы тоже.[2] (См. Статью о гипервалентность для обсуждения моделей склеивания)
Другие оксоанионы азота
Рекомендации
- ^ а б Янсен, Мартин (август 1977 г.). "Обнаружение ортонитрата методом вибрационной спектроскопии: Na3НЕТ4". Angewandte Chemie International Edition на английском языке. 16 (8): 534–535. Дои:10.1002 / anie.197705341.
- ^ а б Янсен, Мартин (1979-08-31). «Кристаллическая структура Na3НЕТ4". Angewandte Chemie International Edition на английском языке. 18 (9): 698–699. Дои:10.1002 / anie.197906982.
- ^ Кесада Кабрера, Р .; Sella, A .; Bailey, E .; Leynaud, O .; Макмиллан, П.Ф. (Апрель 2011 г.). «Синтез под высоким давлением и структурное поведение ортонитрата натрия Na3НЕТ4" (PDF). Журнал химии твердого тела. 184 (4): 915–920. Bibcode:2011JSSCh.184..915Q. Дои:10.1016 / j.jssc.2011.02.013.
- ^ а б Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
