Альдозоредуктаза - Aldose reductase
| Альдозоредуктаза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 | |||||||||
| Идентификаторы | |||||||||
| Номер ЕС | 1.1.1.21 | ||||||||
| Количество CAS | 9028-31-3 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| БРЕНДА | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| |||||||||
В энзимология, альдозоредуктаза (или же альдегидредуктаза) (EC 1.1.1.21 ) является цитозольным НАДФН -зависимый оксидоредуктаза который катализирует восстановление различных альдегидов и карбонилов, включая моносахариды. Он известен прежде всего тем, что катализирует снижение глюкоза к сорбитол, первый шаг в путь полиола метаболизма глюкозы.[1]
Реакции
Альдозоредуктаза катализирует НАДФН-зависимое превращение глюкоза к сорбитол, первый шаг в путь полиола метаболизма глюкозы. Второй и последний этап этого пути катализируется сорбитолдегидрогеназа, который катализирует NAD-связанное окисление сорбита до фруктозы. Таким образом, путь полиола приводит к превращению глюкозы во фруктозу со стехиометрическим использованием NADPH и выработкой NADH.[1]
Галактоза также является субстратом для пути полиола, но соответствующий кетосахар не вырабатывается, поскольку сорбитолдегидрогеназа не способна окислять галактит.[2] Тем не менее, альдозоредуктаза может катализировать восстановление галактозы до галактита.
- галактоза + НАДФН + Н+ галактитол + НАДФ+
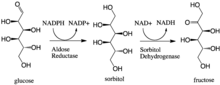
Функция
Реакция альдозоредуктазы, в частности продуцируемого сорбита, важна для функционирования различных органов тела. Например, его обычно используют в качестве первого шага в синтезе фруктоза из глюкозы; второй этап - окисление сорбита до фруктозы, катализируемое сорбитолдегидрогеназа. Основной путь от глюкозы до фруктозы (гликолиз ) включает фосфорилирование глюкозы гексокиназа формировать глюкозо-6-фосфат с последующей изомеризацией до фруктозо-6-фосфат и гидролиз фосфата, но путь сорбита полезен, потому что он не требует ввода энергия в виде АТФ:
- Семенные пузырьки: Фруктоза, полученная из сорбита, используется сперматозоиды.
- Печень: Фруктоза, полученная из сорбита, может использоваться в качестве источника энергии для гликолиза и гликонеогенез.
Альдозоредуктаза также присутствует в линза, сетчатка, Шванновские клетки периферических нервов, плацента и красные кровяные тельца.[нужна цитата ]
В Дрозофила, CG6084 кодировал высококонсервативный белок человеческой альдокеторедуктазы 1B. dAKR1B в гемоцитах необходим и достаточен для увеличения содержания сахарных спиртов в плазме после кишечной инфекции. Повышенный уровень сорбита впоследствии активировал металлопротеиназу 2, которая расщепляет PGRP-LC, чтобы активировать системный иммунный ответ в жировых телах. Таким образом, альдозоредуктаза обеспечивает критическую метаболическую контрольную точку в общем воспалительном ответе.[3]
Структура фермента
Альдозоредуктазу можно рассматривать как прототип фермента суперсемейства ферментов альдокеторедуктазы. Фермент состоит из 315 аминокислотных остатков и складывается в структурный мотив β / α-цилиндра, состоящий из восьми параллельных β-цепей.[4] Соседние нити соединены восемью периферийными α-спиральными сегментами, идущими антипараллельно β-листу.[5] Каталитический активный центр расположен в ядре цилиндра.[5][6] Кофактор НАДФН расположен в верхней части бочки β / α, при этом никотинамидное кольцо выступает вниз в центре цилиндра, а пирофосфат охватывает кромку цилиндра.[1]




Ферментный механизм
В механизм реакции альдозоредуктазы в направлении восстановления альдегида следует последовательному упорядоченному пути, по которому связывается НАДФН, за которым следует субстрат. Связывание НАДФН вызывает конформационное изменение (Фермент • НАДФН → Фермент * • НАДФН), которое включает шарнирное движение поверхностной петли (остатки 213-217), чтобы покрыть часть НАДФН аналогично тому, как это происходит у ремень безопасности. Спиртовой продукт образуется в результате переноса про-R гидрида НАДФН на поверхность карбонильного углерода субстрата. После выпуска спиртового продукта происходит другое изменение конформации (E * • NADP+ → E • НАДФ+), чтобы выпустить НАДП+.[8] Кинетические исследования показали, что переориентация этой петли для высвобождения НАДФ+ По-видимому, представляет собой стадию, ограничивающую скорость в направлении восстановления альдегида.[9][10][11] Поскольку скорость высвобождения кофермента ограничивает каталитическую скорость, можно видеть, что нарушение взаимодействий, стабилизирующих связывание кофермента, может иметь драматические эффекты на максимальную скорость (Vmax).[11]
Гидрид, который переносится из НАДФ+ в глюкозу поступает из C-4 никотинамид кольцо в основании гидрофобной полости. Таким образом, положение этого углерода определяет активный центр фермента. В ферменте существуют три остатка на подходящем расстоянии от C-4, которые могут быть потенциальными донорами протонов: Tyr-48, His-110 и Cys-298. Данные эволюционного, термодинамического и молекулярного моделирования предсказывают, что Tyr-48 является донором протонов. Это предсказание подтвердили результаты исследований мутагенеза.[5][12][13] Таким образом, считается, что взаимодействие [водородной связи] между фенольной гидроксильной группой Tyr-48 и боковой цепью аммония Lys-77 способствует облегчению переноса гидрида.[5]
Роль в диабете
Сахарный диабет считается ведущей причиной новых случаев слепоты и ассоциируется с повышенным риском болезненной невропатии, сердечных заболеваний и почечной недостаточности. Было выдвинуто множество теорий, объясняющих механизмы, приводящие к диабетическим осложнениям, включая стимуляцию метаболизма глюкозы полиольным путем. Дополнительно фермент находится в глазу (роговица, сетчатка, линза ), почка, а миелиновой оболочки - ткани, которые часто вызывают диабетические осложнения.[14] В нормальных гликемических условиях только небольшая часть глюкозы метаболизируется через полиоловый путь, так как большая часть фосфорилируется гексокиназой, и полученный продукт, глюкозо-6-фосфат, используется в качестве субстрата для гликолиза или метаболизма пентозофосфата.[15][16] Однако в ответ на хроническое гипергликемия обнаруженный у диабетиков, поток глюкозы через полиоловый путь значительно увеличивается. До 33% общего использования глюкозы в некоторых тканях может происходить через полиоловый путь.[17]Концентрация глюкозы часто повышается в диабетики долгое время считалось, что альдозоредуктаза ответственна за диабетические осложнения, затрагивающие ряд органов. Много ингибиторы альдозоредуктазы были разработаны как кандидаты в лекарства, но практически все они потерпели неудачу, хотя некоторые эпалрестат коммерчески доступны в нескольких странах. Дополнительные ингибиторы редуктазы, такие как ранирестат, Поналрестат, риналрестат, ризарестат, сорбинил, и берберин[18] в настоящее время проходят клинические испытания.[19]
Смотрите также
Рекомендации
- ^ а б c Петраш Дж. М. (апрель 2004 г.). «Все в семье: альдозоредуктаза и близкородственные альдокеторедуктазы». Клетка. Мол. Life Sci. 61 (7–8): 737–49. Дои:10.1007 / s00018-003-3402-3. PMID 15094999. S2CID 25983505.
- ^ Jedziniak JA, Yates EM, Kinoshita JH (июнь 1973). «Линзовая полиолдегидрогеназа». Exp. Eye Res. 16 (2): 95–104. Дои:10.1016/0014-4835(73)90304-7. PMID 4352688.
- ^ Ян С., Чжао И, Ю Дж, Фан З, Гонг СТ, Тан Х, Пан Л. (август 2019 г.). «Сахарные спирты полиолового пути служат в качестве аларминов, опосредующих локально-системную врожденную иммунную коммуникацию у дрозофилы». Клеточный хозяин и микроб. 26 (2): 240–251. Дои:10.1016 / j.chom.2019.07.001. PMID 31350199.
- ^ Барски О.А., Габбай К.Х., Борен К.М. (сентябрь 1999 г.). «Характеристика гена и промотора альдегидредуктазы человека». Геномика. 60 (2): 188–98. Дои:10.1006 / geno.1999.5915. PMID 10486210.
- ^ а б c d Уилсон Д.К., Борен К.М., Габбай К.Х., Киочо Ф.А. (июль 1992 г.). «Маловероятный сайт сахарного субстрата в структуре 1,65 A человеческого холофермента альдозоредуктазы, вовлеченный в диабетические осложнения». Наука. 257 (5066): 81–4. Дои:10.1126 / science.1621098. PMID 1621098.
- ^ Rondeau JM, Tête-Favier F, Podjarny A, et al. (Январь 1992 г.). «Новый НАДФН-связывающий домен, выявленный кристаллической структурой альдозоредуктазы». Природа. 355 (6359): 469–72. Bibcode:1992Натура.355..469р. Дои:10.1038 / 355469a0. PMID 1734286. S2CID 4260654.
- ^ а б Рисунок 11-4 в: Жезл Цветок; Хамфри П. Рэнг; Морин М. Дейл; Риттер, Джеймс М. (2007). Фармакология Рэнга и Дейла. Эдинбург: Черчилль Ливингстон. ISBN 978-0-443-06911-6.
- ^ Накано Т., Петраш Дж. М. (август 1996 г.). «Кинетические и спектроскопические доказательства ингибирования активного центра альдозоредуктазы человека». Биохимия. 35 (34): 11196–202. Дои:10.1021 / bi9608121. PMID 8780524.
- ^ Гримшоу CE, Шахбаз М., Путни К.Г. (октябрь 1990 г.). «Механические основы нелинейной кинетики восстановления альдегида, катализируемого альдозоредуктазой». Биохимия. 29 (42): 9947–55. Дои:10.1021 / bi00494a027. PMID 2125486.
- ^ Кубически TJ, Hyndman DJ, Morjana NA, Flynn TG (апрель 1992 г.). «Исследования альдозоредуктазы в мышцах свиней. Кинетический механизм и доказательства медленного конформационного изменения при связывании кофермента». J. Biol. Chem. 267 (10): 6510–7. PMID 1551865. Получено 2010-05-18.
- ^ а б Гримшоу CE, Борен К.М., Лай С.Дж., Габбай К.Х. (ноябрь 1995 г.). «Человеческая альдозоредуктаза: константы скорости механизма, включающего взаимное превращение тройных комплексов рекомбинантным ферментом дикого типа». Биохимия. 34 (44): 14356–65. Дои:10.1021 / bi00044a012. PMID 7578039.
- ^ Tarle I, Borhani DW, Wilson DK, Quiocho FA, Petrash JM (декабрь 1993 г.). «Исследование активного сайта альдозоредуктазы человека. Сайт-направленный мутагенез Asp-43, Tyr-48, Lys-77 и His-110». J. Biol. Chem. 268 (34): 25687–93. PMID 8245005. Получено 2010-05-18.
- ^ Борен К.М., Гримшоу К.Э., Лай С.Дж. и др. (Март 1994). «Тирозин-48 является донором протонов, а гистидин-110 управляет стереохимической селективностью субстрата в реакции восстановления альдозоредуктазы человека: кинетика фермента и кристаллическая структура мутантного фермента Y48H». Биохимия. 33 (8): 2021–32. Дои:10.1021 / bi00174a007. PMID 8117659.
- ^ Schrijvers BF, De Vriese AS, Flyvbjerg A (декабрь 2004 г.). «От гипергликемии до диабетической болезни почек: роль метаболических, гемодинамических, внутриклеточных факторов и факторов / цитокинов роста». Endocr. Ред. 25 (6): 971–1010. Дои:10.1210 / er.2003-0018. PMID 15583025. Получено 2010-05-18.
- ^ Габбай К.Х., Мерола Л.О., Филд РА (январь 1966 г.). «Путь сорбита: присутствие в нерве и пуповине с накоплением субстрата при диабете». Наука. 151 (3707): 209–10. Bibcode:1966Научный ... 151..209Г. Дои:10.1126 / science.151.3707.209. PMID 5907911. S2CID 31291584.
- ^ Линдстад Р.И., МакКинли-Макки Дж.С. (сентябрь 1993 г.). «Метилглиоксаль и путь полиола. Трехуглеродные соединения являются субстратами для сорбитолдегидрогеназы печени овцы». FEBS Lett. 330 (1): 31–5. Дои:10.1016 / 0014-5793 (93) 80913-Ф. PMID 8370454. S2CID 39393722.
- ^ Ченг Х.М., Гонсалес Р.Г. (апрель 1986 г.). «Влияние высокого уровня глюкозы и окислительного стресса на метаболизм хрусталика, альдозоредуктазу и старческий катарактогенез». Метаб. Clin. Exp. 35 (4 Дополнение 1): 10–4. Дои:10.1016/0026-0495(86)90180-0. PMID 3083198.
- ^ Wu LY, Ma ZM, Fan XL, Zhao T, Liu ZH, Huang X, Li MM, Xiong L, Zhang K, Zhu LL, Fan M (ноябрь 2009 г.). «Анти-некрозная роль гипоксического прекондиционирования после острой аноксии опосредована альдозоредуктазным и сорбитольным путями в клетках PC12». Шапероны клеточного стресса. 15 (4): 387–94. Дои:10.1007 / s12192-009-0153-6. ЧВК 3082650. PMID 19902381.
- ^ Schemmel KE, Padiyara RS, D'Souza JJ (сентябрь 2009 г.). «Ингибиторы альдозоредуктазы в лечении диабетической периферической нейропатии: обзор». J. Осложненный диабет. 24 (5): 354–60. Дои:10.1016 / j.jdiacomp.2009.07.005. PMID 19748287.
дальнейшее чтение
- Дениз Р., доктор философии. Феррье (2005). Иллюстрированные обзоры Липпинкотта: биохимия (Иллюстрированные обзоры Липпинкотта). Хагерстаун, Мэриленд: Липпинкотт Уильямс и Уилкинс. п. 319. ISBN 0-7817-2265-9.
- Attwood MA, Doughty CC (декабрь 1974 г.). «Очистка и свойства альдозоредуктазы печени теленка». Биохим. Биофиз. Acta. 370 (2): 358–68. Дои:10.1016/0005-2744(74)90097-7. PMID 4216364.
- Богосян Р.А., МакГиннесс ET (апрель 1979 г.). «Аффинная очистка и свойства альдозоредуктазы свиного мозга». Биохим. Биофиз. Acta. 567 (2): 278–86. Дои:10.1016 / 0005-2744 (79) 90113-х. PMID 36151.

