Лактатдегидрогеназа - Lactate dehydrogenase
| Лактатдегидрогеназа | |||||||||
|---|---|---|---|---|---|---|---|---|---|
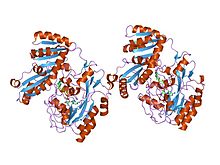
 Тетрамер лактатдегидрогеназы M (LDH5), человек | |||||||||
| Идентификаторы | |||||||||
| Номер ЕС | 1.1.1.27 | ||||||||
| Количество CAS | 9001-60-9 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| БРЕНДА | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | AmiGO / QuickGO | ||||||||
| |||||||||
Лактатдегидрогеназа (LDH или же LD) является фермент найдены почти во всех живых клетках. ЛДГ катализирует превращение лактат к пируват и обратно, поскольку он преобразует NAD+ к НАДН и назад. А дегидрогеназа это фермент, который переносит гидрид от одной молекулы к другой.
ЛДГ существует в четырех различных классах ферментов. Эта статья специально о НАД (P) -зависимый L-лактатдегидрогеназа. Другие LDH действуют на D-лактат и / или зависят от цитохром с: D-лактатдегидрогеназа (цитохром) и L-лактатдегидрогеназа (цитохром).
ЛДГ широко экспрессируется в тканях организма, таких как клетки крови и сердечная мышца. Поскольку он выделяется при повреждении тканей, он является маркером распространенных травм и заболеваний, таких как сердечная недостаточность.
Реакция

Лактатдегидрогеназа катализирует взаимное превращение пируват и лактат с сопутствующим взаимным превращением НАДН и НАД+. Он превращает пируват, конечный продукт гликолиз, чтобы лактат, когда кислород отсутствует или в дефиците, и он выполняет обратную реакцию во время Цикл Кори в печень. При высоких концентрациях лактата фермент ингибирует обратную связь, и скорость превращения пирувата в лактат снижается. Он также катализирует дегидрирование 2-гидроксибутират, но это гораздо более бедный субстрат, чем лактат.
Активный сайт

LDH у людей использует Его (193) в качестве донора протонов и работает в унисон с кофермент (Arg 99 и Asn 138) и субстрат (Arg106; Arg169; Thr 248) связывающие остатки.[1][2] Активный сайт His (193) обнаружен не только в человеческой форме ЛДГ, но и у многих различных животных, что свидетельствует о конвергентной эволюции ЛДГ. Две разные субъединицы LDH (LDHA, также известная как субъединица M LDH, и LDHB, также известная как субъединица H LDH) сохраняют один и тот же активный сайт и одни и те же аминокислоты, участвующие в реакции. Заметная разница между двумя субъединицами, составляющими третичную структуру ЛДГ, заключается в замене аланин (в цепочке M) с глутамин (в цепочке H). Это крошечное, но заметное изменение, как полагают, является причиной того, что субъединица H может связываться быстрее, и каталитическая активность субъединицы M не снижается при воздействии тех же условий, что и субъединица H, тогда как активность субъединицы H снижается в пять раз.[3]
Изоферменты
Лактатдегидрогеназа состоит из четырех субъединиц (тетрамера). Двумя наиболее распространенными субъединицами являются белок LDH-M и LDH-H, кодируемый LDHA и LDHB гены соответственно. Эти две субъединицы могут образовывать пять возможных тетрамеров (изоферментов): 4H, 4M и три смешанных тетрамера (3H1M, 2H2M, 1H3M). Эти пять изоформ ферментативно схожи, но имеют разное тканевое распределение: основные изоферменты скелетных мышц и печени, M4, имеет четыре мышечные (M) субъединицы, а H4 является основным изоферментом сердечной мышцы у большинства видов животных, содержащим четыре субъединицы сердца (H).
- ЛДГ-1 (4H) - в сердце и в РБК (красные кровяные тельца ), так же хорошо как мозг[4]
- ЛДГ-2 (3H1M) - в ретикулоэндотелиальной системы
- ЛДГ-3 (2H2M) - в легкие
- ЛДГ-4 (1H3M) - в почки, плацента, и поджелудочная железа
- ЛДГ-5 (4М) - в печень и поперечно-полосатые мышцы,[5] также присутствует в мозг[4]
ЛДГ-2 обычно является преобладающей формой в сыворотка. Уровень ЛДГ-1 выше уровня ЛДГ-2 («перевернутая модель») предполагает инфаркт миокарда (повреждение сердечных тканей высвобождает сердечную ЛДГ, богатую ЛДГ-1, в кровоток). Использование этого явления для диагностики инфаркта в значительной степени заменено использованием Тропонин Измерение I или T.[нужна цитата ]
Есть еще две субъединицы LDH млекопитающих, которые могут быть включены в тетрамеры LDH: LDHC и LDHBx. LDHC - это белок LDH, специфичный для семенников, который кодируется геном LDHC. LDHBx - это пероксисома -специфический белок ЛДГ. LDHBx - это форма чтения LDHB. LDHBx создается перевод LDHB мРНК, но стоп-кодон интерпретируется как аминокислота -кодирование кодон. В результате, перевод продолжается до следующего стоп-кодона. Это приводит к добавлению семи аминокислотных остатков к нормальному белку LDH-H. Расширение содержит пероксисомальный целевой сигнал, так что LDHBx импортируется в пероксисому.[6]
|
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Семейства белков
|
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Семейство также содержит L-лактатдегидрогеназы, которые катализируют превращение L-лактат к пируват, последний этап анаэробного гликолиза. Малатдегидрогеназы, которые катализируют взаимное превращение малата в оксалоацетат и участвуют в цикле лимонной кислоты, и L-2-гидроксиизокапроатдегидрогеназы также являются членами семьи. В N-конец это Rossmann NAD-связывающая складка и C-конец - необычная складка альфа + бета.[7][8]
Интерактивная карта проезда
Нажмите на гены, белки и метаболиты ниже, чтобы ссылки на соответствующие статьи.[§ 1]
- ^ Интерактивную карту путей можно редактировать на WikiPathways: «ГликолизГлюконеогенез_WP534».
Ферментативная регуляция
Этот белок может использовать морфеин модель аллостерическая регуляция.[9]
Гипогликемия, вызванная этанолом
Этанол дегидрируется до ацетальдегида с помощью алкогольдегидрогеназы, а затем до уксусной кислоты с помощью ацетальдегиддегидрогеназы. Во время этой реакции образуется 2 НАДН. Если присутствует большое количество этанола, вырабатывается большое количество НАДН, что приводит к истощению НАД.+. Таким образом, превращение пирувата в лактат увеличивается из-за связанной с ним регенерации НАД.+. Следовательно, при отравлении этанолом может развиться анион-щелевой метаболический ацидоз (лактоацидоз).
Повышенное соотношение НАДН / НАД + также может вызвать гипогликемию у (в противном случае) голодного человека, который пил и зависит от глюконеогенеза для поддержания уровня глюкозы в крови. Аланин и лактат являются основными глюконеогенными предшественниками, которые вступают в глюконеогенез в виде пирувата. Высокое соотношение НАДН / НАД + сдвигает равновесие лактатдегидрогеназы в сторону лактата, так что может образовываться меньше пирувата и, следовательно, нарушается глюконеогенез.
Регулировка субстрата
ЛДГ также регулируется относительными концентрациями его субстратов. ЛДГ становится более активным в периоды экстремальной мышечной нагрузки из-за увеличения количества субстратов для реакции ЛДГ. Когда скелетные мышцы заставляют производить высокие уровни мощности, потребность в АТФ для обеспечения аэробного АТФ приводит к накоплению свободных АДФ, АМФ и Pi. Последующий гликолитический поток, особенно производство пирувата, превышает способность пируватдегидрогеназы и других ферментов-челноков метаболизировать пируват. Поток через ЛДГ увеличивается в ответ на повышенные уровни пирувата и НАДН для метаболизма пирувата в лактат.[10]
Транскрипционная регуляция
ЛДГ подвергается транскрипционной регуляции с помощью PGC-1α. PGC-1α регулирует ЛДГ за счет снижения транскрипции мРНК ЛДГ-А и ферментативной активности преобразования пирувата в лактат.[11]
Генетика
Субъединицы M и H кодируются двумя разными гены:
- Субъединица M кодируется LDHA, расположен на хромосома 11p 15.4 (Онлайн-менделевское наследование в человеке (OMIM): 150000 ).
- Субъединица H кодируется LDHB, расположен на хромосоме 12p12.2-p12.1 (Онлайн-менделевское наследование в человеке (OMIM): 150100 ).
- Третья изоформа, LDHC или же LDHX, выражается только в яички (Онлайн-менделевское наследование в человеке (OMIM): 150150 ); его ген, вероятно, является дубликатом LDHA и также находится на одиннадцатой хромосоме (11p15.5-p15.3).
- Четвертая изоформа локализована в пероксисома. Это тетрамер, содержащий одну субъединицу LDHBx, которая также кодируется LDHB ген. Белок LDHBx на семь аминокислот длиннее, чем белок LDHB (LDH-H). Это удлинение аминокислоты генерируется функциональным трансляционным считыванием.[6]
Мутации субъединицы M связаны с редким заболеванием. напряженный миоглобинурия (см. статью OMIM), и описаны мутации субъединицы H, но, по-видимому, не приводят к заболеванию.
Мутации
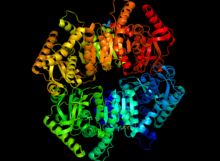
В редких случаях мутация в генах, контролирующих выработку лактатдегидрогеназы, приводит к заболеванию, известному как дефицит лактатдегидрогеназы. В зависимости от того, какой ген несет мутацию, возникает один из двух типов: либо дефицит лактатдегидрогеназы-A (также известный как болезнь накопления гликогена XI), либо дефицит лактатдегидрогеназы-B. Оба эти состояния влияют на то, как организм расщепляет сахар, в первую очередь в определенных мышечных клетках. Дефицит лактатдегидрогеназы-А вызван мутацией LDHA ген, в то время как дефицит лактатдегидрогеназы-B вызван мутацией гена LDHB.[12]
Это состояние наследуется по аутосомно-рецессивному паттерну, а это означает, что оба родителя должны внести мутировавший ген, чтобы это состояние проявилось.[13]
Полный фермент лактатдегидрогеназы состоит из четырех белковые субъединицы.[14] Поскольку две наиболее распространенные субъединицы, обнаруживаемые в лактатдегидрогеназе, кодируются LDHA и гены LDHB, любая разновидность этого заболевания вызывает аномалии многих ферментов лактатдегидрогеназы, обнаруженных в организме. В случае недостаточности лактатдегидрогеназы-A мутации гена LDHA приводят к выработке аномальной субъединицы лактатдегидрогеназы-A, которая не может связываться с другими субъединицами, чтобы сформировать полную фермент. Отсутствие функциональной субъединицы снижает количество образующегося фермента, что приводит к общему снижению активности. Во время анаэробной фазы гликолиз (в Цикл Кори ) мутировавший фермент не может преобразовывать пируват в лактат для производства дополнительной энергии, необходимой клеткам. Поскольку эта субъединица имеет самую высокую концентрацию ферментов ЛДГ, обнаруженных в скелетных мышцах (которые являются основными мышцами, ответственными за движение), физическая активность высокой интенсивности приведет к недостаточному количеству энергии, производимой во время этой анаэробной фазы.[15] Это, в свою очередь, приведет к ослаблению мышечной ткани и, в конечном итоге, к ее разрушению, состояние, известное как рабдомиолиз. Процесс рабдомиолиза также высвобождает миоглобин в кровь, которая в конечном итоге попадет в мочу и заставит ее стать красной или коричневой: еще одно состояние, известное как миоглобинурия.[16] Среди других распространенных симптомов - непереносимость физических упражнений, которая состоит из усталости, мышечной боли и судорог во время упражнений, а также кожной сыпи.[17][18] В тяжелых случаях миоглобинурия может повредить почки и привести к опасной для жизни почечной недостаточности.[19] Чтобы получить окончательный диагноз, может быть проведена биопсия мышцы, чтобы подтвердить низкую активность ЛДГ или ее отсутствие. В настоящее время нет специального лечения этого состояния.
В случае дефицита лактатдегидрогеназы-B мутации гена LDHB приводят к выработке аномальной субъединицы лактатдегидрогеназы-B, которая не может связываться с другими субъединицами с образованием полного фермента. Как и в случае недостаточности лактатдегидрогеназы-А, эта мутация снижает общую эффективность фермента.[20] Однако между этими двумя случаями есть некоторые существенные различия. Первое - это место, где проявляется заболевание. При дефиците лактатдегидрогеназы-B самая высокая концентрация субъединиц B может быть обнаружена в сердечной мышце или сердце. Внутри сердца лактатдегидрогеназа играет роль преобразования лактата обратно в пируват, так что пируват можно снова использовать для выработки большего количества энергии.[21] С мутированным ферментом общая скорость этого превращения снижается. Однако, в отличие от дефицита лактатдегидрогеназы-A, эта мутация, по-видимому, не вызывает никаких симптомов или проблем со здоровьем, связанных с этим состоянием.[18][22] В настоящий момент неясно, почему это так. Пострадавшие люди обычно обнаруживаются только тогда, когда обычные анализы крови показывают низкий уровень ЛДГ в крови.
Роль в мышечной усталости
Возникновение ацидоза в периоды интенсивных упражнений обычно связывают с накоплением водорода, диссоциированного от лактата. Раньше считалось, что молочная кислота вызывает усталость. Исходя из этого, идея о том, что производство лактата является основной причиной мышечной усталости во время упражнений, получила широкое распространение. Более тщательный, механистический анализ продукции лактата в «анаэробных» условиях показывает, что нет биохимических доказательств того, что продукция лактата через ЛДГ способствует ацидозу. Хотя активность ЛДГ связана с мышечной усталостью,[23] Производство лактата с помощью комплекса ЛДГ работает как система, замедляющая наступление мышечной усталости. Джордж Брукс и его коллеги из Калифорнийского университета в Беркли, где был обнаружен лактатный челнок, показали, что лактат на самом деле является метаболическим топливом, а не продуктом жизнедеятельности или причиной усталости.
ЛДГ помогает предотвратить мышечную недостаточность и усталость несколькими способами. Реакция образования лактата генерирует цитозольный НАД +, который попадает в глицеральдегид-3-фосфатдегидрогеназа реакции, чтобы помочь поддерживать цитозольный окислительно-восстановительный потенциал и способствовать потоку субстрата через вторая фаза гликолиза для содействия генерации АТФ. Это, по сути, дает больше энергии сокращающимся мышцам при тяжелых нагрузках. Производство и удаление лактата из клетки также выбрасывает протон, потребляемый в реакции ЛДГ - удаление избыточных протонов, образующихся в результате эта реакция брожения служит буферной системой для мышечного ацидоза.[нужна цитата ] Как только накопление протонов превышает скорость поглощения при производстве и удалении лактата через симпорт LDH,[24] возникает мышечный ацидоз.
Анализ крови
| Нижний предел | Верхний предел | Единица измерения | Комментарии |
|---|---|---|---|
| 50[25] | 150[25] | Ед / л | |
| 0.4[26] | 1.7[26] | мкмоль / л | |
| 1.8[27] | 3.4[27] | µКат / Л | <70 лет[27] |
На анализы крови, повышенный уровень лактатдегидрогеназы обычно указывает на повреждение тканей, которое имеет несколько потенциальных причин, отражающих его широкое распространение в тканях:
- Гемолитическая анемия[28]
- Анемия, вызванная недостаточностью витамина B12[28]
- Инфекции Такие как инфекционный мононуклеоз, менингит, энцефалит, ВИЧ / СПИД. Заметно увеличивается в сепсис.[28]
- Инфаркт, Такие как инфаркт кишечника, инфаркт миокарда и инфаркт легкого[28]
- Острая болезнь почек[28]
- Острое заболевание печени[28]
- Рабдомиолиз[29]
- Панкреатит[28]
- Переломы костей[28]
- Рак, особенно Рак яичек и лимфома. Высокий ЛДГ после химиотерапия указывает на более слабый ответ и худшую выживаемость.[28]
- Суровый шок[28]
- Гипоксия[28]
Низкий и нормальный уровни ЛДГ обычно не указывают на какую-либо патологию.[28] Низкий уровень может быть вызван большим потреблением Витамин С.
ЛДГ - это белок, который обычно появляется во всем организме в маленькое количество.
Тестирование на рак

Многие виды рака могут повышать уровень ЛДГ, поэтому ЛДГ можно использовать в качестве онкомаркер, но в то же время он бесполезен для выявления конкретного вида рака. Измерение уровня ЛДГ может быть полезным при мониторинге лечения рака. К доброкачественным состояниям, которые могут повышать уровень ЛДГ, относятся сердечная недостаточность, гипотиреоз, анемия, преэклампсия, менингит, энцефалит, острый панкреатит, ВИЧ и заболевания легких или печени.[30]
Распад тканей высвобождает ЛДГ, и, следовательно, ЛДГ можно измерить как заменитель разрушения ткани (например, гемолиз ). ЛДГ измеряется с помощью теста на лактатдегидрогеназу (ЛДГ) (также известного как тест на ЛДГ или тест на дегидрогеназу молочной кислоты). Сравнение измеренных значений ЛДГ с нормальным диапазоном помогает в диагностике.[31]
Гемолиз
В лекарство, ЛДГ часто используется в качестве маркера разрушения тканей, поскольку ЛДГ в большом количестве красные кровяные тельца и может служить маркером для гемолиз. Неправильно обработанный образец крови может показать ложноположительный высокий уровень ЛДГ из-за эритроцит повреждать.
Его также можно использовать как маркер инфаркт миокарда. После инфаркта миокарда уровни ЛДГ достигают максимума через 3–4 дня и остаются повышенными до 10 дней. Таким образом, повышенные уровни ЛДГ (где уровень ЛДГ1 выше, чем ЛДГ2, т. Е. Переворот ЛДГ, как обычно, в сыворотке, ЛДГ2 выше, чем ЛДГ1) могут быть полезны для определения наличия у пациента миокардиальных нарушений. инфаркт, если они обратятся к врачу через несколько дней после приступа боли в груди.
Оборот тканей
Другое использование - оценка разрушение тканей в целом; это возможно при отсутствии других индикаторов гемолиз. Он используется для отслеживания рак (особенно лимфома ) пациентов, как раковые клетки имеют высокую скорость обмена с разрушенными клетками, что приводит к повышенной активности ЛДГ.
ВИЧ
ЛДГ часто измеряется у ВИЧ-инфицированных как неспецифический маркер для пневмония из-за Pneumocystis jirovecii (PCP). Повышенный уровень ЛДГ на фоне симптомов со стороны верхних дыхательных путей у пациента с ВИЧ предполагает, но не является диагностическим признаком PCP. Однако у ВИЧ-инфицированных пациентов с респираторными симптомами очень высокий уровень ЛДГ (> 600 МЕ / л) указывал на гистоплазмоз (Вероятность в 9,33 раза выше) при исследовании 120 пациентов с PCP и 30 пациентов с гистоплазмозом.[32]
Тестирование в других жидкостях организма
Экссудаты и транссудаты
Измерение ЛДГ в жидкости, отсасываемой из плевральный выпот (или же перикардиальный выпот ) может помочь в различении экссудаты (активно секретируемая жидкость, например, из-за воспаление ) или же транссудаты (пассивно секретируемая жидкость из-за высокого гидростатическое давление или низкий онкотическое давление ). Обычный критерий (входит в Критерии света ) заключается в том, что отношение жидкой ЛДГ к верхнему пределу нормальной сывороточной ЛДГ более 0,6[33] или же 2⁄3[34] указывает на экссудат, а меньшее соотношение указывает на транссудат. В разных лабораториях есть разные значения верхнего предела сывороточного ЛДГ, но примеры включают 200[35] и 300[35] IU / L.[36] В эмпиема уровень ЛДГ в целом будет превышать 1000 МЕ / л.
Менингит и энцефалит
Высокий уровень лактатдегидрогеназы в спинномозговой жидкости часто связан с бактериальный менингит.[37] В случае популярный менингит, высокий уровень ЛДГ, в целом, указывает на наличие энцефалит и бедный прогноз.
В лечении рака
ЛДГ участвует в инициации опухоли и метаболизме. Раковые клетки полагаются на усиленный гликолиз, приводящий к увеличению производства лактата в дополнение к аэробному дыханию в митохондриях, даже в условиях достаточного количества кислорода (процесс, известный как Эффект варбурга[38]). Это состояние ферментативного гликолиза катализируется А-формой ЛДГ. Этот механизм позволяет опухолевым клеткам преобразовывать большую часть своих запасов глюкозы в лактат независимо от наличия кислорода, переводя использование метаболитов глюкозы с простого производства энергии на стимулирование ускоренного роста и репликации клеток.
LDH A и возможность ингибирования его активности были определены как многообещающая мишень для лечения рака, направленная на предотвращение пролиферации канцерогенных клеток. Химическое ингибирование LDH A продемонстрировало заметные изменения в метаболических процессах и общей выживаемости клеток карциномы. Оксамат является цитозольным ингибитором ЛДГ А, который значительно снижает выработку АТФ в опухолевых клетках, а также увеличивает выработку активные формы кислорода (ROS). Эти АФК стимулируют пролиферацию раковых клеток, активируя киназы, которые управляют факторами роста прогрессии клеточного цикла при низких концентрациях,[39] но может повредить ДНК из-за окислительного стресса при более высоких концентрациях. Вторичные продукты окисления липидов также могут инактивировать ЛДГ и влиять на его способность регенерировать НАДН,[40] прямое нарушение способности ферментов превращать лактат в пируват.
Хотя недавние исследования показали, что активность ЛДГ не обязательно является индикатором метастатического риска,[41] Экспрессия ЛДГ может выступать в качестве общего маркера в прогнозе рака. Было обнаружено, что экспрессия LDH5 и VEGF в опухолях и строме является сильным прогностическим фактором диффузного или смешанного рака желудка.[42]
Прокариоты
Кепкамембрана переплет домен находится в прокариотический лактатдегидрогеназа. Он состоит из большого семинитевого антипараллельный бета-лист с обеих сторон окружен альфа-спирали. Это позволяет мембрана ассоциация.[43]
Смотрите также
Рекомендации
- ^ Холмс RS, Голдберг E (октябрь 2009 г.). «Компьютерный анализ лактатдегидрогеназ млекопитающих: ЛДГ человека, мыши, опоссума и утконоса». Вычислительная биология и химия. 33 (5): 379–85. Дои:10.1016 / j.compbiolchem.2009.07.006. ЧВК 2777655. PMID 19679512.
- ^ Уилкс HM, Холбрук JJ (декабрь 1988 г.). «Специфическая, высокоактивная малатдегидрогеназа путем изменения структуры лактатдегидрогеназы». Наука. 242 (4885): 1541–44. Bibcode:1988Sci ... 242.1541W. Дои:10.1126 / science.3201242. PMID 3201242.
- ^ Ивентофф В., Россманн М.Г., Тейлор С.С., Торфф Х.Дж., Мейер Х., Кейл В., Кильц Х.Х. (июль 1977 г.). «Структурные адаптации изоферментов лактатдегидрогеназы». Труды Национальной академии наук Соединенных Штатов Америки. 74 (7): 2677–81. Bibcode:1977PNAS ... 74.2677E. Дои:10.1073 / pnas.74.7.2677. ЧВК 431242. PMID 197516.
- ^ а б Чжан Ю., Чен К., Слоан С.А., Беннетт М.Л., Шольце А.Р., О'Киф С. и др. (Сентябрь 2014 г.). «База данных транскриптомов для секвенирования РНК и сплайсинга глии, нейронов и сосудистых клеток коры головного мозга». Журнал неврологии. 34 (36): 11929–47. Дои:10.1523 / JNEUROSCI.1860-14.2014. ЧВК 4152602. PMID 25186741.
- ^ Ван Эрд Дж. П., Крейцер Е. К. (1996). Клиническая химия для анализа 2. С. 138–139. ISBN 978-90-313-2003-5.
- ^ а б Шуерен Ф., Лингнер Т., Джордж Р., Хофхейс Дж., Гартнер Дж., Томс С. (2014). «Пероксисомальная лактатдегидрогеназа вырабатывается путем считывания трансляции у млекопитающих». eLife. 3: e03640. Дои:10.7554 / eLife.03640. ЧВК 4359377. PMID 25247702.
- ^ Чепмен А.Д., Кортес А., Даффорн Т.Р., Кларк А.Р., Брэди Р.Л. (1999). «Структурные основы субстратной специфичности в малатдегидрогеназах: кристаллическая структура тройного комплекса цитоплазматической малатдегидрогеназы свиней, альфа-кетомалоната и тетрагидоната». Дж Мол Биол. 285 (2): 703–12. Дои:10.1006 / jmbi.1998.2357. PMID 10075524.
- ^ Мадерн Д. (2002). «Молекулярная эволюция в суперсемействе L-малат и L-лактатдегидрогеназа». Дж Мол Эвол. 54 (6): 825–40. Bibcode:2002JMolE..54..825M. Дои:10.1007 / s00239-001-0088-8. PMID 12029364. S2CID 469660.
- ^ Селвуд Т., Джаффе Е.К. (март 2012 г.). «Динамические диссоциирующие гомоолигомеры и контроль функции белка». Arch. Biochem. Биофизы. 519 (2): 131–43. Дои:10.1016 / j.abb.2011.11.020. ЧВК 3298769. PMID 22182754.
- ^ Сприт Л.Л., Хоулетт Р.А., Хейгенхаузер Г.Дж. (2000). «Ферментативный подход к производству лактата в скелетных мышцах человека во время упражнений». Медико-спортивные упражнения. 32 (4): 756–63. Дои:10.1097/00005768-200004000-00007. PMID 10776894.
- ^ Саммерматтер С, Сантос Дж, Перес-Шиндлер Дж, Хандшин С. (2013). «Скелетная мышца PGC-1α контролирует гомеостаз лактата всего тела посредством зависимой от рецептора эстрогена α-зависимой активации ЛДГ В и подавления ЛДГ А.» Proc Natl Acad Sci U S A. 110 (21): 8738–43. Bibcode:2013ПНАС..110.8738С. Дои:10.1073 / pnas.1212976110. ЧВК 3666691. PMID 23650363.
- ^ «Дефицит лактатдегидрогеназы». Домашний справочник по генетике. 29 февраля 2016 г.. Получено 2 марта 2016.
- ^ «Заболевания - Заболевания обмена веществ - Причины / Наследование». Ассоциация мышечной дистрофии. Получено 2 марта 2016.
- ^ Миллар Д. Б., Фраттали V, Уиллик Г. Е. (июнь 1969 г.). «Четвертичная структура лактатдегидрогеназы. I. Молекулярная масса субъединицы и обратимая ассоциация при кислом pH». Биохимия. 8 (6): 2416–21. Дои:10.1021 / bi00834a025. PMID 5816379.
- ^ Канно Т., Судо К., Маэкава М., Нисимура Ю., Укита М., Фукутаке К. (март 1988 г.). «Дефицит М-субъединицы лактатдегидрогеназы: новый тип наследственной миопатии напряжения». Clinica Chimica Acta; Международный журнал клинической химии. 173 (1): 89–98. Дои:10.1016/0009-8981(88)90359-2. PMID 3383424.
- ^ «Миоглобинурия; рабдомиолиз». нервно-мышечный.wustl.edu. Получено 2 марта 2016.
- ^ Хоффманн Г.Ф. (1 января 2002 г.). Наследственные метаболические заболевания. Липпинкотт Уильямс и Уилкинс. ISBN 9780781729000.
- ^ а б «Гликогенозы». нервно-мышечный.wustl.edu. Получено 2 марта 2016.
- ^ «Гликогеновая болезнь накопления XI - Условия - GTR - NCBI». www.ncbi.nlm.nih.gov. Получено 2 марта 2016.
- ^ «Ген LDHB». Домашний справочник по генетике. 29 февраля 2016 г.. Получено 2 марта 2016.
- ^ «Лактатдегидрогеназа - Руководство по ферментам Уортингтона». www.worthington-biochem.com. Получено 2 марта 2016.
- ^ "Запись OMIM № 614128 - ДЕФИЦИТ ЛАКТАТДЕГИДРОГЕНАЗЫ B; LDHBD". www.omim.org. Получено 2 марта 2016.
- ^ Теш П., Сьёдин Б., Торстенссон А., Карлссон Дж. (1978).«Мышечная усталость и ее связь с накоплением лактата и активностью ЛДГ у человека». Acta Physiol Scand. 103 (4): 413–20. Дои:10.1111 / j.1748-1716.1978.tb06235.x. PMID 716962.
- ^ Джуэл С., Кларсков С., Нильсен Дж. Дж., Круструп П., Мор М., Бангсбо Дж. (2004). «Влияние интервальных тренировок высокой интенсивности на высвобождение лактата и H + из скелетных мышц человека». Am J Physiol Endocrinol Metab. 286 (2): E245-51. Дои:10.1152 / ajpendo.00303.2003. PMID 14559724.
- ^ а б Результаты анализа крови - нормальные диапазоны В архиве 2012-11-02 в Wayback Machine Bloodbook.Com
- ^ а б Fachwörterbuch Kompakt Medizin E-D / D-E. Автор: Фриц-Юрген Нёринг. Издание 2. Издательство: Elsevier, Urban & FischerVerlag, 2004. ISBN 3-437-15120-7, ISBN 978-3-437-15120-0. Длина: 1288 страницы
- ^ а б c Список референтных диапазонов из Университетской больницы Упсалы («Лабораторслисты»). Artnr 40284 Sj74a. Выдан 22 апреля 2008 г.
- ^ а б c d е ж грамм час я j k л «Лактатдегидрогеназа (ЛД)». Лабораторные тесты онлайн. Последнее обновление: 22 июня 2018 г.}}
- ^ Кельц Э., Хан Ф.Ю., Манн Г. (2019). «Рабдомиолиз. Роль диагностических и прогностических факторов». Мышцы Связки Сухожилия J. 3 (4): 303–12. Дои:10.32098 / mltj.04.2013.11. ЧВК 3940504. PMID 24596694.CS1 maint: несколько имен: список авторов (связь)
- ^ Стэнфордский онкологический центр. «Диагностика рака - понимание рака». Понимание рака. Стэнфордская медицина.
- ^ «Тест на лактатдегидрогеназу: Медицинская энциклопедия MedlinePlus». MedlinePlus. Национальная медицинская библиотека США.
- ^ Батт А.А., Майклс С., Грир Д., Кларк Р., Киссинджер П., Мартин Д.Х. (июль 2002 г.). «Уровень ЛДГ в сыворотке как ключ к диагностике гистоплазмоза». СПИД Читать. 12 (7): 317–21. PMID 12161854.
- ^ Хеффнер Дж. Э., Браун Л. К., Барбьери, Калифорния (апрель 1997 г.). «Диагностическая ценность тестов, которые различают экссудативный и транссудативный плевральный выпот. Основные исследователи исследования». Грудь. 111 (4): 970–80. Дои:10.1378 / сундук.111.4.970. PMID 9106577.
- ^ Light RW, Macgregor MI, Luchsinger PC, Ball WC (октябрь 1972 г.). «Плевральный выпот: диагностическое разделение транссудатов и экссудатов». Анна. Междунар. Med. 77 (4): 507–13. Дои:10.7326/0003-4819-77-4-507. PMID 4642731.
- ^ а б Джозеф Дж., Бадринатх П., Басран Г.С., Сан С.А. (ноябрь 2001 г.). «Плевральная жидкость - транссудат или экссудат? Пересмотр диагностических критериев». Грудная клетка. 56 (11): 867–70. Дои:10.1136 / торакс.56.11.867. ЧВК 1745948. PMID 11641512.
- ^ Джозеф Дж., Бадринатх П., Басран Г.С., Сан С.А. (март 2002 г.). «Является ли градиент альбумина или соотношение жидкости и сывороточного альбумина лучше, чем лактатдегидрогиназа плевральной жидкости в диагностике отделения плеврального выпота?». BMC Pulm Med. 2: 1. Дои:10.1186/1471-2466-2-1. ЧВК 101409. PMID 11914151.
- ^ Штейн Дж. Х. (1998). Медицина внутренних органов. Elsevier Health Sciences. С. 1408–. ISBN 978-0-8151-8698-4. Получено 12 августа 2013.
- ^ Варбург О (1956). «О происхождении раковых клеток». Наука. 123 (3191): 309–14. Bibcode:1956Научный ... 123..309Вт. Дои:10.1126 / science.123.3191.309. PMID 13298683.
- ^ Ирани К., Ся Й, Цвейер Дж. Л., Соллотт С.Дж., Дер С.Дж., Ферон Э.Р., Сундаресан М., Финкель Т., Гольдшмидт-Клермонт П.Дж. (1997). «Митогенная передача сигналов, опосредованная оксидантами в Ras-трансформированных фибробластах». Наука. 275 (5306): 1649–52. Дои:10.1126 / science.275.5306.1649. PMID 9054359. S2CID 19733670.
- ^ Раманатан Р., Манчини Р.А., Суман С.П., Пляж К.М. (2014). «Ковалентное связывание 4-гидрокси-2-ноненаля с лактатдегидрогеназой снижает образование NADH и снижает активность метмиоглобина». J Agric Food Chem. 62 (9): 2112–7. Дои:10.1021 / jf404900y. PMID 24552270.
- ^ Сюй Х.Н., Кадлечек С., Профка Х, Гликсон Дж.Д., Ризи Р., Ли Л.З. (2014). «Является ли более высокий уровень лактата индикатором метастатического риска опухоли? Пилотное исследование MRS с использованием гиперполяризованного (13) C-пирувата». Акад. Радиол. 21 (2): 223–31. Дои:10.1016 / j.acra.2013.11.014. ЧВК 4169113. PMID 24439336.
- ^ Ким Х.С., Ли ХЭ, Ян Х.К., Ким У.Х. (2014). «Высокая экспрессия лактатдегидрогеназы 5 коррелирует с высокой экспрессией фактора роста эндотелия опухолей и стромальных сосудов при раке желудка». Патобиология. 81 (2): 78–85. Дои:10.1159/000357017. PMID 24401755.
- ^ Дим О., Пратт Э.А., Хо Ц., Айзенберг Д. (август 2000 г.). «Кристаллическая структура D-лактатдегидрогеназы, дыхательного фермента периферической мембраны». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 97 (17): 9413–8. Bibcode:2000PNAS ... 97.9413D. Дои:10.1073 / пнас.97.17.9413. ЧВК 16878. PMID 10944213.
дальнейшее чтение
- Джонсон В. Т., Кэнфилд В. К. (1985). «Кишечная абсорбция и выведение цинка у стрептозотоциновых диабетических крыс под влиянием пищевого цинка и белка». J Nutr. 115 (9): 1217–27. Дои:10.1093 / jn / 115.9.1217. PMID 3897486.
- Эйн С.Х., Мансер К., Адейеми С.Д. (1985). «Злокачественная тератома крестцово-копчиковой кишки - энтодермальный синус, опухоль желточного мешка - у младенцев и детей: обзор за 32 года». J Pediatr Surg. 20 (5): 473–7. Дои:10.1016 / с0022-3468 (85) 80468-1. PMID 3903096.
- Адзума М., Ши М., Даненберг К.Д., Гарднер Х., Барретт С., Жак С.Дж., Шерод А., Икбал С., Эль-Хуэйри А., Ян Д., Чжан В., Даненберг П.В., Ленц Х.Д. (2007). «Уровни лактатдегидрогеназы в сыворотке и гликолиз значительно коррелируют с экспрессией VEGFA и VEGFR в опухоли у пациентов с метастатическим CRC». Фармакогеномика. 8 (12): 1705–13. Дои:10.2217/14622416.8.12.1705. PMID 18086000.
- Masepohl B, Klipp W, Pühler A (1988). «Генетическая характеристика и анализ последовательности дублированной области гена nifA / nifB Rhodobacter capsulatus». Мол Джен Генет. 212 (1): 27–37. Дои:10.1007 / bf00322441. PMID 2836706. S2CID 21009965.
- Галардо М.Н., Регейра М., Риера М.Ф., Пеллиццари Э.Х., Цигоррага С.Б., Мерони С.Б. (2014). «Лактат регулирует функцию половых клеток самцов крыс с помощью активных форм кислорода». PLOS ONE. 9 (1): e88024. Bibcode:2014PLoSO ... 988024G. Дои:10.1371 / journal.pone.0088024. ЧВК 3909278. PMID 24498241.
- Теш П., Сьёдин Б., Торстенссон А., Карлссон Дж. (1978). «Мышечная усталость и ее связь с накоплением лактата и активностью ЛДГ у человека». Acta Physiol Scand. 103 (4): 413–20. Дои:10.1111 / j.1748-1716.1978.tb06235.x. PMID 716962.
- Бек О., Йернстрем Б., Мартинес М., Репке Д. Б. (1988). «Изучение ароматического гидроксилирования 1-метилтетрагидро-бета-карболина (меттриптолина) на крысах in vitro». Chem Biol Взаимодействие. 65 (1): 97–106. Дои:10.1016/0009-2797(88)90034-8. PMID 3345575.
- Саммерматтер С, Сантос Дж, Перес-Шиндлер Дж, Хандшин С. (2013). «Скелетная мышца PGC-1α контролирует гомеостаз лактата всего тела посредством зависимой от рецептора эстрогена α-зависимой активации ЛДГ В и подавления ЛДГ А.» Proc Natl Acad Sci U S A. 110 (21): 8738–43. Bibcode:2013ПНАС..110.8738С. Дои:10.1073 / pnas.1212976110. ЧВК 3666691. PMID 23650363.
- Робергс Р.А., Гиасванд Ф., Паркер Д. (2004). «Биохимия метаболического ацидоза, вызванного физической нагрузкой». Am J Physiol Regul Integr Comp Physiol. 287 (3): R502-16. Дои:10.1152 / ajpregu.00114.2004. PMID 15308499.
- Кресдж Н., Симони Р.Д., Хилл Р.Л. (2005). «Отто Фриц Мейерхоф и выяснение гликолитического пути». J Biol Chem. 280 (4): e3. PMID 15665335.
внешняя ссылка
 СМИ, связанные с Лактатдегидрогеназа в Wikimedia Commons
СМИ, связанные с Лактатдегидрогеназа в Wikimedia Commons