Лактопероксидаза - Википедия - Lactoperoxidase
Лактопероксидаза это пероксидаза фермент секретируется из молочных, слюнных и других слизистых желез[5] который действует как естественный антибактериальный агент.[6] Лактопероксидаза входит в состав гем пероксидаза семейство ферментов. У человека лактопероксидаза кодируется LPO ген.[7][8]
Лактопероксидаза катализирует окисление ряда неорганических и органических субстраты к пероксид водорода.[9] Эти субстраты включают бромид и йодид и поэтому лактопероксидазу можно отнести к категории галопероксидаза. Другой важный субстрат - это тиоцианат. Окисленные продукты, образующиеся под действием этого фермента, обладают мощным бактерицидный виды деятельности. Лактопероксидаза вместе со своими неорганическими ионными субстратами, перекисью водорода и окисленными продуктами известна как лактопероксидазная система.[10]
Система лактопероксидазы играет важную роль в врожденная иммунная система убивая бактерии в молоке и слизистая оболочка (выстилки преимущественно энтодермального происхождения, покрытые эпителием, которые участвуют в абсорбции и секреции), следовательно, увеличение лактопероксидазной системы может иметь терапевтическое применение. Кроме того, добавление или увеличение лактопероксидазной системы имеет потенциальные применения для борьбы с бактериями в пищевых продуктах и потребительских товарах для здоровья. Система лактопероксидазы не атакует ДНК и не обладает мутагенными свойствами.[11] Однако при определенных условиях система лактопероксидазы может способствовать окислительному стрессу.[12] Кроме того, лактопероксидаза может способствовать инициации рак молочной железы, благодаря своей способности окислять эстрогенные гормоны, производящие свободный радикал промежуточные звенья.[13]
Структура
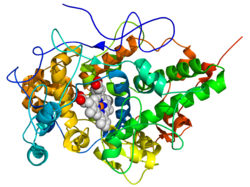
В состав лактопероксидазы в основном входят альфа-спирали плюс два коротких антипараллельных бета-нити.[14] Лактопероксидаза относится к семейство пероксидазы гема ферментов млекопитающих, которые также включают миелопероксидаза (MPO), эозинофильная пероксидаза (EPO), пероксидаза щитовидной железы (TPO) и простагландин H-синтаза (PGHS). А гем кофактор связан около центра белка.[15]
Функция
Лактопероксидаза катализирует пероксид водорода (ЧАС2О2) окисление нескольких акцепторных молекул:[16]
- восстановленный акцептор + H2О2 → окисленный акцептор + H2О
Конкретные примеры включают:
- тиоцианат (SCN−) → гипотиоцианит (OSCN−)[17][18]
- бромид (Br−) → гипобромит (Братан−)
- йодид (Я−) → гипойодит (IO−)
Источник пероксид водорода (ЧАС2О2) обычно является реакцией глюкоза с кислород в присутствии фермента глюкозооксидаза (EC 1.1.3.4 ), что также имеет место в слюна. Глюкоза, в свою очередь, может образовываться из крахмал в присутствии фермента слюны амилоглюкозидаза (EC 3.2.1.3 ).
Эти относительно короткоживущие окисленные промежуточные соединения обладают мощным бактерицидный эффекты, следовательно, лактопероксидаза является частью системы антимикробной защиты в тканях, которые экспрессируют лактопероксидазу.[10] Система лактопероксидазы эффективна в уничтожении ряда аэробный[19] и некоторые анаэробный микроорганизмы.[20] Исследование (1984 г.): «Действие смесей лактопероксидазы, тиоцианата и пероксида водорода на бактерии зависит от экспериментальных условий. Если бактерии культивируются после воздействия лактопероксидазы, тиоцианата и перекиси водорода на питательный агар в аэробных условиях, они могут не расти. , тогда как они легко растут на кровяном агаре в анаэробных условиях ».[21] По своей антимикробной способности лактопероксидаза, по-видимому, действует синергетически с лактоферрин[22] и лизоцим.[23]
Приложения
Лактопероксидаза - эффективное противомикробное средство. Следовательно, применение лактопероксидазы находят в консервировании продуктов питания, косметики и офтальмологических растворов. Кроме того, лактопероксидаза нашла применение при лечении зубов и ран. Наконец, лактопероксидаза может найти применение в качестве противоопухолевых и противовирусных агентов.[24]
Молочные продукты
Лактопероксидаза является эффективным противомикробным средством и используется в качестве антибактериального средства для уменьшения бактериальной микрофлоры в молоке и молочных продуктах.[25] Активация лактопероксидазной системы добавлением перекиси водорода и тиоцианата увеличивает срок хранения охлажденного сырого молока.[16][26][27][28] Он достаточно термостойкий и используется как индикатор чрезмерной пастеризации молока.[29]
Забота о полости рта
Система лактопероксидазы считается подходящей для лечения гингивит и парадентоз.[30] Лактопероксидаза использовалась в зубной пасте или ополаскивателе для рта для уменьшения количества бактерий в полости рта и, следовательно, кислоты, производимой этими бактериями.[31]
Косметика
Комбинация лактопероксидазы, глюкозы, глюкозооксидаза (БОГ), йодид и тиоцианат считаются эффективными при консервировании косметики.[32]
Рак и вирусные инфекции
Было обнаружено, что конъюгаты антител глюкозооксидазы и лактопероксидазы эффективны в уничтожении опухолевых клеток in vitro.[33] Кроме того, макрофаги, подвергающиеся воздействию лактопероксидазы, стимулируются к уничтожению раковых клеток.[34]
Гипотиоцианит, вырабатываемый пероксидазой, подавляет Вирус простого герпеса[35] и Вирус иммунодефицита человека.[36]
Клиническое значение
Врожденная иммунная система
Антибактериальная активность лактопероксидазы играет важную роль в системе иммунной защиты.[37][38][39]
Гипотиоцианит является одним из реактивных промежуточных продуктов, продуцируемых действием лактопероксидазы на тиоцианат и перекись водорода, производимая двойная оксидаза 2 белки, также известные как Duox2.[40][41] Секреция тиоцианата[42] в кистозный фиброз пациентов уменьшается, что приводит к снижению выработки противомикробного гипотиоцианита и, следовательно, способствует увеличению риска инфекции дыхательных путей.[43][44]
Система лактопероксидазы эффективно ингибирует Helicobacter pylori в буфере; однако в цельной человеческой слюне он имеет более слабый антибактериальный эффект.[45] Система лактопероксидазы не атакует ДНК и не обладает мутагенными свойствами.[11] Однако при определенных условиях система лактопероксидазы может способствовать окислительному стрессу.[12] Было показано, что лактопероксидаза в присутствии тиоцианата может вызывать бактерицидные и цитотоксические эффекты перекиси водорода в определенных условиях, например, когда перекись водорода присутствует в реакционных смесях в избытке тиоцианата.[21]
Рак молочной железы
Окисление эстрадиол лактопероксидазой является возможным источником окислительный стресс в рак молочной железы.[12][13] Способность лактопероксидазы распространять цепную реакцию, приводящую к потреблению кислорода и накоплению внутриклеточного перекиси водорода, может объяснить вызванные гидроксильным радикалом повреждения оснований ДНК, недавно обнаруженные в ткани рака груди у женщин.[12] Лактопероксидаза может участвовать в канцерогенезе молочной железы из-за ее способности взаимодействовать с эстрогенными гормонами и окислять их посредством двух стадий одноэлектронной реакции.[13] Лактопероксидаза реагирует с фенольный Кольцо эстрогены производить реактивный свободные радикалы.[46] Кроме того, лактопероксидаза может активировать канцерогенные ароматические и гетероциклические амины и повышать уровни связывания активированных продуктов с ДНК, что предполагает потенциальную роль катализированной лактопероксидазой активации канцерогенов в возникновении рака груди.[47]
Забота о полости рта
В течение последних десятилетий было опубликовано несколько клинических исследований, описывающих клиническую эффективность системы лактопероксидазы в различных продуктах для ухода за полостью рта (зубные пасты, полоскания для рта). Показав косвенно, путем измерения экспериментальных гингивит и кариес параметры, которыми полоскает рот[48][49] содержащие амилоглюкозидазу (γ-амилаза ) и глюкозооксидаза активируют лактопероксидазную систему, частично выяснен защитный механизм ферментов в продуктах по уходу за полостью рта. Ферменты, такие как лизоцим, лактопероксидаза и глюкозооксидаза переносятся из зубных паст в пленка. Эти ферменты, входящие в состав пленки, обладают высокой каталитической активностью.[50][51] Кроме того, в составе зубных паст система лактопероксидазы оказывает благотворное влияние на предотвращение кариеса в раннем детстве.[52] за счет уменьшения количества колоний, образованных кариесогенной микрофлорой, при одновременном увеличении концентрации тиоцианата. С ксеростомия пациентам зубные пасты с лактопероксидазной системой, по-видимому, превосходят фторид -содержащие зубные пасты в отношении бляшка образования и гингивита.[53] Требуются дополнительные исследования[54] для дальнейшего изучения защитных механизмов.[55]
Применение лактопероксидазы не ограничивается кариесом, гингивитом и т. Д. пародонтит.[56] Комбинация лизоцима и лактопероксидазы может применяться для поддержки лечения синдрома жжения во рту (глоссодия ). В сочетании с лактоферрином лактопероксидаза борется с галитоз;[57] В сочетании с лактоферрином и лизоцимом лактопероксидаза помогает улучшить симптомы ксеростомии.[58] Кроме того, гели с лактопероксидазой помогают улучшить симптомы рака полости рта, когда выработка слюны нарушена из-за облучения. В этом случае также оральные бактериальные Флора находятся под благоприятным влиянием.[59][60][61]
Смотрите также
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000167419 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000009356 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Tenovuo JO (1985). «Пероксидазная система в секретах человека». В Tenovuo JO, Pruitt KM (ред.). Система лактопероксидазы: химия и биологическое значение. Нью-Йорк: Деккер. п. 272. ISBN 978-0-8247-7298-7.
- ^ Прюитт К.М., Рейтер Б. (1985). «Биохимия пероксидазных систем: антимикробное действие». В Tenovuo JO, Pruitt KM (ред.). Система лактопероксидазы: химия и биологическое значение. Нью-Йорк: Деккер. п. 272. ISBN 978-0-8247-7298-7.
- ^ Dull TJ, Uyeda C, Strosberg AD, Nedwin G, Seilhamer JJ (сентябрь 1990 г.). «Молекулярное клонирование кДНК, кодирующих лактопероксидазу крупного рогатого скота и человека». ДНК клетки биол. 9 (7): 499–509. Дои:10.1089 / dna.1990.9.499. PMID 2222811.
- ^ Кисер С., Катерина С.К., Энглер Дж. А., Рахемтулла Б., Рахемтулла Ф. (сентябрь 1996 г.). «Клонирование и анализ последовательности кДНК, кодирующей пероксидазу слюны человека». Ген. 173 (2): 261–4. Дои:10.1016/0378-1119(96)00078-9. PMID 8964511.
- ^ Колер Х, Дженцер Х (1989). «Взаимодействие лактопероксидазы с перекисью водорода. Образование промежуточных продуктов фермента и образование свободных радикалов». Свободный Радич. Биол. Med. 6 (3): 323–39. Дои:10.1016/0891-5849(89)90059-2. PMID 2545551.
- ^ а б Теновуо Дж.О., Прюитт К.М., ред. (1985). Система лактопероксидазы: химия и биологическое значение. Нью-Йорк: Деккер. п. 272. ISBN 978-0-8247-7298-7.
- ^ а б White WE, Pruitt KM, Mansson-Rahemtulla B (февраль 1983 г.). «Антибактериальная система пероксидаза-тиоцианат-пероксид не повреждает ДНК». Антимикробный. Агенты Chemother. 23 (2): 267–72. Дои:10.1128 / aac.23.2.267. ЧВК 186035. PMID 6340603.
- ^ а б c d Сайпе Х.Дж., Джордан С.Дж., Ханна П.М., Мейсон Р.П. (ноябрь 1994 г.). «Метаболизм 17-бета-эстрадиола лактопероксидазой: возможный источник окислительного стресса при раке груди». Канцерогенез. 15 (11): 2637–43. Дои:10.1093 / carcin / 15.11.2637. PMID 7955118.
- ^ а б c Гибауди Э.М., Лауренти Э, Бельтрамо П, Феррари РП (2000). «Могут ли эстрогенные радикалы, генерируемые лактопероксидазой, участвовать в молекулярном механизме канцерогенеза груди?». Редокс Rep. 5 (4): 229–35. Дои:10.1179/135100000101535672. PMID 10994878. S2CID 24253204.
- ^ Сингх А.К., Смит М.Л., Ямини С., Олссон П.И., Синха М., Каур П., Шарма С., Пол Дж.А., Сингх Т.П., Пол К.Г. (октябрь 2012 г.). «Структура бычьей карбонил лактопероксидазы при разрешении 2,0 Å и инфракрасные спектры как функция pH». Белковый журнал. 31 (7): 598–608. Дои:10.1007 / s10930-012-9436-3. PMID 22886082. S2CID 22945713.
- ^ PDB: 2р5л; Сингх А.К., Сингх Н., Шарма С., Сингх С.Б., Каур П., Бхушан А., Шринивасан А., Сингх Т.П. (февраль 2008 г.). «Кристаллическая структура лактопероксидазы при разрешении 2,4 А». Журнал молекулярной биологии. 376 (4): 1060–75. Дои:10.1016 / j.jmb.2007.12.012. PMID 18191143.
- ^ а б де Вит Дж. Н., ван Хойдонк А. С. (1996). «Структура, функции и применение лактопероксидазы в естественных противомикробных системах». Нидерландский журнал молока и молочных продуктов. 50: 227–244.
- ^ Вевер Р., Каст В. М., Касиноедин Дж. Х., Боеленс Р. (декабрь 1982 г.). «Перекисное окисление тиоцианата, катализируемое миелопероксидазой и лактопероксидазой». Биохим. Биофиз. Acta. 709 (2): 212–9. Дои:10.1016/0167-4838(82)90463-0. PMID 6295491.
- ^ Прюитт К.М., Теновуо Дж., Эндрюс Р.В., Маккейн Т. (февраль 1982 г.). «Катализируемое лактопероксидазой окисление тиоцианата: полярографические исследования продуктов окисления». Биохимия. 21 (3): 562–7. Дои:10.1021 / bi00532a023. PMID 7066307.
- ^ Фвейя Л.В., Льюис М.Дж., Грандисон А.С. (июль 2008 г.). «Задача тестирования системы лактопероксидазы против ряда бактерий с использованием различных агентов активации». J. Dairy Sci. 91 (7): 2566–74. Дои:10.3168 / jds.2007-0322. PMID 18565914.
- ^ Куртуа П., Майерус П., Лаббе М., Ванден Аббеле А., Юрасовски Е., Пуртуа М. (сентябрь 1992 г.). «Восприимчивость анаэробных микроорганизмов к гипотиоцианиту, продуцируемому лактопероксидазой». Acta Stomatol Belg. 89 (3): 155–62. PMID 1481764.
- ^ а б Карлссон Дж., Эдлунд М.Б., Хенстрём Л. (июнь 1984 г.). «Бактерицидное и цитотоксическое действие смесей гипотиоцианит-перекись водорода». Заразить иммунную. 44 (3): 581–6. Дои:10.1128 / IAI.44.3.581-586.1984. ЧВК 263633. PMID 6724690.
- ^ Райтер Б. (1983). «Биологическое значение лактоферрина». Int J Tissue React. 5 (1): 87–96. PMID 6345430.
- ^ Роджер В., Теновуо Дж., Ленандер-Лумикари М., Сёдерлинг Э., Вилья П. (1994). «Лизоцим и лактопероксидаза ингибируют адгезию Streptococcus mutans NCTC 10449 (серотип c) к обработанному слюной гидроксиапатиту in vitro». Кариес Res. 28 (6): 421–8. Дои:10.1159/000262015. PMID 7850845.
- ^ Харпер, У. Джеймс (2000). Обзор биологических свойств компонентов сыворотки. Чикаго, Иллинойс: Американский институт молочных продуктов. п. 54.
- ^ Reiter B .; Härnulv BG. «Сохранение охлажденного и неохлажденного молока с помощью его естественной лактопероксидазной системы». Dairy Ind. Int. 47 (5): 13–19.
- ^ Zajac M, Glandys J, Skarzynska M, Härnulv G, Eilertsen K (1983). «Сохранение качества молока путем тепловой обработки или активации лактопероксидазной системы в сочетании с хранением в холодильнике». Milchwissenschaft. 38 (11).
- ^ Zajac M, Glandys J, Skarzynska M, Härnulv G, Björck L (1983). «Изменения бактериологического качества сырого молока, стабилизированные активацией его лактопероксидазной системы и хранящиеся при различных температурах». J. Food Prot. 46 (12): 1065–1068. Дои:10.4315 / 0362-028x-46.12.1065. PMID 30921865.
- ^ Корхонен Х (1980). «Новый метод консервирования сырого молока: антибактериальная система лактопероксидазы». World Anim. Rev. 35: 23–29.
- ^ Маркс Н.Э., Грандисон А.С., Льюис М.Дж. (2008). «Использование полосок обнаружения перекиси водорода для определения степени пастеризации цельного молока». Международный журнал молочных технологий. 54 (1): 20–22. Дои:10.1111 / j.0134-727X.2001.00008.x (неактивно 09.09.2020).CS1 maint: DOI неактивен по состоянию на сентябрь 2020 г. (связь)
- ^ Заявка WO WO1988002600, Poulson OM, "Ферментосодержащая бактерицидная композиция и препараты для лечения зубов и ран, содержащие эту композицию", опубликовано 1988-04-21.
- ^ Hoogedoorn H (1985). «Активация пероксидазной системы слюны: клинические исследования». В Tenovuo JO, Pruitt KM (ред.). Система лактопероксидазы: химия и биологическое значение. Нью-Йорк: Деккер. С. 217–228. ISBN 978-0-8247-7298-7.
- ^ США 5607681, Galley E, Godfrey DC, Guthrie WG, Hodgkinson DM, Linnington HL, "Антимикробные композиции, содержащие йодид, тиоцианат, глюкозу и оксидазу глюкозы", опубликовано 4 марта 1997 г., передано The Boots Company PLC.
- ^ Станиславский М., Руссо В., Гоавец М., Ито Н. (октябрь 1989 г.). «Иммунотоксины, содержащие глюкозооксидазу и лактопероксидазу с опухолевыми свойствами: эффективность уничтожения in vitro на модели клеток плазмоцитомы мыши». Рак Res. 49 (20): 5497–504. PMID 2790777.
- ^ Лефковиц Д.Л., Сие Т.С., Миллс К., Кастро А. (1990). «Индукция фактора некроза опухоли и цитотоксичности макрофагами, подвергшимися воздействию лактопероксидазы и микропероксидазы». Life Sci. 47 (8): 703–9. Дои:10.1016/0024-3205(90)90625-2. PMID 2402192.
- ^ Микола Х, Варис М., Теновуо Дж. (Март 1995 г.). «Ингибирование вируса простого герпеса типа 1, респираторно-синцитиального вируса и эховируса типа 11 с помощью гипотиоцианита, генерируемого пероксидазой». Противовирусный Res. 26 (2): 161–71. Дои:10.1016 / 0166-3542 (94) 00073-H. PMID 7605114.
- ^ Pourtois M, Binet C., Van Tieghem N, Courtois PR, Vandenabbeele A, Thirty L (май 1991 г.). «Слюна может способствовать быстрому подавлению инфицирования ВИЧ». СПИД. 5 (5): 598–600. Дои:10.1097/00002030-199105000-00022. PMID 1650564.
- ^ Wijkstrom-Frei C, El-Chemaly S., Ali-Rachedi R, Gerson C, Cobas MA, Forteza R, Salathe M, Conner GE (август 2003 г.). «Лактопероксидаза и защита дыхательных путей человека». Являюсь. J. Respir. Cell Mol. Биол. 29 (2): 206–12. CiteSeerX 10.1.1.325.1962. Дои:10.1165 / rcmb.2002-0152OC. PMID 12626341.
- ^ Коннер Г.Е., Салате М., Фортеза Р. (декабрь 2002 г.). «Лактопероксидаза и метаболизм перекиси водорода в дыхательных путях». Являюсь. J. Respir. Крит. Care Med. 166 (12, часть 2): S57–61. Дои:10.1164 / rccm.2206018. PMID 12471090.
- ^ Conner GE, Wijkstrom-Frei C, Randell SH, Fernandez VE, Salathe M (январь 2007 г.). «Система лактопероксидазы связывает транспорт анионов с защитой организма при муковисцидозе». FEBS Lett. 581 (2): 271–8. Дои:10.1016 / j.febslet.2006.12.025. ЧВК 1851694. PMID 17204267.
- ^ Томас Э.Л., Бейтс КП, Джефферсон М.М. (сентябрь 1980 г.). «Ион гипотиоцианита: обнаружение антимикробного агента в слюне человека». J. Dent. Res. 59 (9): 1466–72. Дои:10.1177/00220345800590090201. PMID 6931123. S2CID 7717994.
- ^ Томас Э.Л., Ауне TM (май 1978 г.). «Лактопероксидаза, пероксид, тиоцианатная противомикробная система: корреляция окисления сульфгидрила с антимикробным действием». Заразить. Иммунная. 20 (2): 456–63. Дои:10.1128 / IAI.20.2.456-463.1978. ЧВК 421877. PMID 352945.
- ^ Xu Y, Szép S, Lu Z (декабрь 2009 г.). «Антиоксидантная роль тиоцианата в патогенезе муковисцидоза и других заболеваний, связанных с воспалением». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 106 (48): 20515–9. Дои:10.1073 / pnas.0911412106. ЧВК 2777967. PMID 19918082.
- ^ Moskwa P, Lorentzen D, Excoffon KJ, Zabner J, McCray PB, Nauseef WM, Dupuy C, Bánfi B (январь 2007 г.). «Новая система защиты дыхательных путей хозяина неисправна при кистозном фиброзе». Являюсь. J. Respir. Крит. Care Med. 175 (2): 174–83. Дои:10.1164 / rccm.200607-1029OC. ЧВК 2720149. PMID 17082494.
- ^ Minarowski Ł, Sands D, Minarowska A, Karwowska A, Sulewska A, Gacko M, Chyczewska E (2008). «Концентрация тиоцианата в слюне больных муковисцидозом». Folia Histochem. Цитобиол. 46 (2): 245–6. Дои:10.2478 / v10042-008-0037-0. PMID 18519245.
- ^ Хаукиоджа А., Ихалин Р., Лоймаранта В., Ленандер М., Теновуо Дж. (Сентябрь 2004 г.). «Чувствительность Helicobacter pylori к врожденному защитному механизму, системе лактопероксидазы, в буфере и в цельной слюне человека». Журнал медицинской микробиологии. 53 (Pt 9): 855–60. Дои:10.1099 / jmm.0.45548-0. PMID 15314191.
- ^ Левстад, РА (декабрь 2006 г.). «Кинетическое исследование окисления эстрогенов, катализируемого лактопероксидазой». Биометаллы. 19 (6): 587–92. Дои:10.1007 / s10534-006-0002-3. PMID 16944280. S2CID 19254664.
- ^ Горлевска-Робертс KM, Teitel CH, Lay JO, Roberts DW, Kadlubar FF (декабрь 2004 г.). «Катализируемая лактопероксидазой активация канцерогенных ароматических и гетероциклических аминов». Chem. Res. Токсикол. 17 (12): 1659–66. Дои:10.1021 / tx049787n. PMID 15606142.
- ^ Hugoson A, Koch G, Thilander H, Hoogendorn H (1974). «Лактопероксидаза в профилактике образования зубного налета, гингивита и кариеса (III)». Одонт Реви. 25 (1): 69–80. PMID 4522423.
- ^ Мидда М, Кукси М.В. (1986). «Клиническое использование средства для ухода за зубами, содержащего ферменты». J Clin Periodontol. 13 (10): 950–6. Дои:10.1111 / j.1600-051x.1986.tb01433.x. PMID 3098804.
- ^ Ханниг К., Шпицмюллер Б., Люкс ХК, Альтенбургер М., Аль-Ахмад А., Ханниг М. (2010). «Эффективность ферментативных зубных паст для иммобилизации защитных ферментов в пленке in situ». Arch Oral Biol. 55 (7): 463–469. Дои:10.1016 / j.archoralbio.2010.03.020. PMID 20417500.
- ^ Ханниг С., Ханниг М., Аттин Т. (2005). «Ферменты в приобретенной пленке эмали». Eur J Oral Sci. 113 (1): 2–13. Дои:10.1111 / j.1600-0722.2004.00180.x. PMID 15693823.
- ^ Джиоти С., Шасикиран Н.Д., Редди В.В. (2009). «Влияние зубной пасты, содержащей лактопероксидазную систему, на кариесогенные бактерии у детей с кариесом в раннем детстве». J Clin Педиатр Дент. 33 (4): 299–303. Дои:10.17796 / jcpd.33.4.83331867x68w120n. PMID 19725235.
- ^ ван Стинберге Д., Ван ден Эйнде Э., Якобс Р., Квиринен М. (1994). «Эффект зубной пасты, содержащей лактопероксидазу, при радиационно-индуцированной ксеростомии». Int Dent J. 44 (2): 133–138. PMID 8063434.
- ^ Ханниг, Кристиан; Ханниг, Матиас; Аттин, Томас (2005). «Ферменты в приобретенной пленке эмали». Европейский журнал оральных наук. 113 (1): 2–13. Дои:10.1111 / j.1600-0722.2004.00180.x. ISSN 0909-8836. PMID 15693823.
- ^ Кирстиля В., Ленандер-Лумикари М., Тенуово Дж. (1994). «Действие зубной пасты, содержащей лактопероксидазную систему, на зубной налет и всю слюну in vivo». Акта Одонтол Сканд. 52 (6): 346–353. Дои:10.3109/00016359409029032. PMID 7887144.
- ^ Марино Р., Торретта С., Капаччио П., Пигнатаро Л., Спадари Ф (2010). «Различные терапевтические стратегии при синдроме жжения во рту: предварительные данные». J Oral Pathol Med. 39 (8): 611–616. Дои:10.1111 / j.1600-0714.2010.00922.x. PMID 20701667.
- ^ Шин К., Яэгаки К., Мурата Т., Ии Х, Танака Т., Аояма И., Ямаути К., Тойда Т., Ивацуки К. (2011). «Влияние композиции, содержащей лактоферрин и лактопероксидазу, на неприятный запах изо рта и бактерии слюны: рандомизированное, двойное слепое, перекрестное, плацебо-контролируемое клиническое испытание». Clin Oral Investigation. 15 (4): 485–493. Дои:10.1007 / s00784-010-0422-х. PMID 20512389. S2CID 21991883.
- ^ Хиль-Монтойя Дж. А., Гуардия-Лопес I, Гонсалес-Молес М. А. (2008). «Оценка клинической эффективности жидкости для полоскания рта и геля для полости рта, содержащего антимикробные белки лактопероксидазу, лизоцим и лактоферрин, у пожилых пациентов с сухостью во рту - пилотное исследование». Геродонтология. 25 (1): 3–9. Дои:10.1111 / j.1741-2358.2007.00197.x. PMID 18194332.
- ^ Надь К., Урбан Е., Фазвкас О., Турзо Л., Надь Е. (2007). «Контролируемое исследование геля лактопероксидазы на флору полости рта и слюну у облученных пациентов с раком полости рта». J Craniofac Surg. 18 (5): 1157–1164. Дои:10.1097 / scs.0b013e3180de6311. PMID 17912104. S2CID 1253647.
- ^ Шахдад С.А., Тейлор С., Барклай С.К., Стиб И.Н., Прешоу П.М. (2005). «Двойное слепое перекрестное исследование систем Biotène Oralbalance и BioXtra в качестве заменителей слюны у пациентов с ксеростомией после лучевой терапии». Eur J Cancer Care (англ.). 14 (4): 319–326. Дои:10.1111 / j.1365-2354.2005.00587.x. PMID 16098116.
- ^ Матеар Д.В., Барбаро Дж. (2005). «Эффективность заменителей слюны при лечении сухости во рту у пожилых людей: пилотное исследование». J R Soc продвижение здоровья. 125 (1): 35–41. Дои:10.1177/146642400512500113. PMID 15712851. S2CID 36508570.
дальнейшее чтение
- Галиясевич С., Саед GM, Diamond MP, Abu-Soud HM (сентябрь 2004 г.). «Высокая константа скорости диссоциации комплекса двухвалентного железа с диоксигруппой связана с каталазоподобной активностью лактопероксидазы». J. Biol. Chem. 279 (38): 39465–70. Дои:10.1074 / jbc.M406003200. PMID 15258136. S2CID 30280587.
- Экстранд Б (1994). «Лактопероксидаза и лактоферрин». В Beuchat LR, Dillon VM, Board RG (ред.). Природные антимикробные системы и консервирование продуктов питания. Oxon: CAB International. ISBN 978-0-85198-878-8.
- де Вит Дж. Н., ван Хойдонк А. С. (2000). «Лактопероксидаза: физико-химические свойства, возникновение, механизм действия и применение». Британский журнал питания. 84 (Приложение 1): S19 – S25. Дои:10.1017 / S0007114500002208. PMID 11242442.
- Томас Э.Л., Пера К.А., Смит К.В., Чван А.К. (февраль 1983 г.). «Ингибирование Streptococcus mutans антимикробной системой лактопероксидазы». Заразить. Иммунная. 39 (2): 767–78. Дои:10.1128 / IAI.39.2.767-778.1983. ЧВК 348016. PMID 6832819.
- Корхонен Х., Мериляйнен В., Антила М., Кувалайнен К. (1980). «[Антимикробные факторы в молоке и устойчивость к инфекциям у младенцев]». Duodecim (на финском). 96 (3): 184–99. PMID 7192622.
- Орам Дж. Д., Рейтер Б. (август 1966 г.). «Ингибирование стрептококков лактопероксидазой, тиоцианатом и перекисью водорода. Влияние ингибиторной системы на чувствительные и устойчивые штаммы стрептококков группы N». Biochem. J. 100 (2): 373–81. Дои:10.1042 / bj1000373. ЧВК 1265145. PMID 4290983.
- Орам Дж. Д., Рейтер Б. (август 1966 г.). «Ингибирование стрептококков лактопероксидазой, тиоцианатом и перекисью водорода. Окисление тиоцианата и природа ингибирующего соединения». Biochem. J. 100 (2): 382–8. Дои:10.1042 / bj1000382. ЧВК 1265146. PMID 5338806.
- Ханнуксела С., Теновуо Дж., Роджер В., Ленандер-Лумикари М., Экстранд Дж. (1994). «Фторид подавляет антимикробные пероксидазные системы в цельной слюне человека». Кариес Res. 28 (6): 429–34. Дои:10.1159/000262016. PMID 7850846.
- Ауне TM, Томас Э.Л. (март 1978 г.). «Окисление белковых сульфгидрилов продуктами окисления тиоцианат-иона, катализируемого пероксидазой». Биохимия. 17 (6): 1005–10. Дои:10.1021 / bi00599a010. PMID 204336.
- Экстранд Б., Муллан В.М., Уотерхаус А (1985). «Ингибирование антибактериальной системы лактопероксидаза-тиоцианат-пероксид водорода термически обработанным молоком». J. Food Prot. 48 (6): 494–498. Дои:10.4315 / 0362-028X-48.6.494. PMID 30943594.
- Райтер Б., Хярнулв Г. (1984). «Антибактериальная система лактопероксидазы: естественное происхождение, биологические функции и практическое применение». J. Food Prot. 47 (9): 724–732. Дои:10.4315 / 0362-028X-47.9.724. PMID 30934451.
внешняя ссылка
- Лактопероксидаза в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)