Опухоль Вильмса - Википедия - Wilms tumor
| Опухоль Вильмса | |
|---|---|
| Другие имена | Опухоль Вильмса |
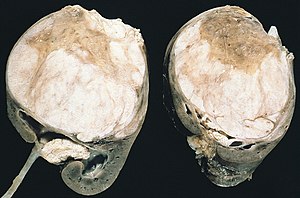 | |
| Разрез на разрезе, показывающий две половины образца нефробластомы. Обратите внимание на выступающие перегородки, разделяющие поверхность среза, и выступ опухоли в почечной лоханке, напоминающий ботриоидную рабдомиосаркому. | |
| Произношение | |
| Специальность | Онкология, урология, нефрология |
Опухоль Вильмса, также известный как нефробластома, это рак из почки что обычно происходит в дети, редко в взрослые люди.[1] Он назван в честь Макс Вильмс, немецкий хирург (1867–1918), который первым его описал.[2]
Ежегодно в США диагностируется около 650 случаев.[3] Большинство случаев встречается у детей без ассоциированных генетических синдромов; однако меньшинство детей с опухолью Вильмса имеют врожденные аномалии.[3] Он очень хорошо поддается лечению, вылечилось около 9/10 детей.[3]
Признаки и симптомы
Типичные признаки и симптомы опухоли Вильмса включают следующее:
- безболезненное пальпируемое образование в брюшной полости
- потеря аппетита
- боль в животе
- высокая температура
- тошнота и рвота
- кровь в моче (примерно в 20% случаев)
- высокое кровяное давление в некоторых случаях (особенно при синхронном или метахронном двустороннем поражении почек)
- Редко как варикоцеле[4]
Патогенез
Опухоль Вильмса имеет множество причин, которые в широком смысле можно разделить на синдромные и несиндромальные. Синдромные причины опухоли Вильмса возникают в результате изменений генов, таких как Опухоль Вильмса 1 (WT1) или опухоли Вильмса 2 (WT2), и опухоль проявляется с группой других признаков и симптомов.[5] Несиндромальная опухоль Вильмса не связана с другими симптомами или патологиями.[5] Многие, но не все случаи опухоли Вильмса развиваются из нефрогенных остатков, которые представляют собой фрагменты ткани в почке или вокруг нее, которые развиваются до рождения и становятся злокачественными после рождения. В частности, случаи двусторонней опухоли Вильмса, а также случаи опухоли Вильмса, происходящие от определенных генетических синдромов, таких как Синдром Дениса-Драша, прочно связаны с нефрогенными остатками.[5] Большинство нефробластом находятся только на одной стороне тела и встречаются с обеих сторон менее чем в 5% случаев, хотя у людей с синдромом Дениса-Драша чаще всего встречаются двусторонние или множественные опухоли.[6] Они, как правило, представляют собой инкапсулированные и васкуляризованные опухоли, которые не пересекают среднюю линию живота. В случаях метастаз обычно это легкое. Разрыв опухоли Вильмса подвергает пациента риску кровотечение и перитонеальное распространение опухоли. В таких случаях необходимо хирургическое вмешательство хирурга, имеющего опыт удаления столь хрупкой опухоли.[нужна цитата ]
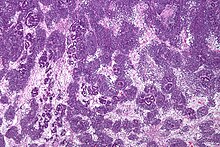
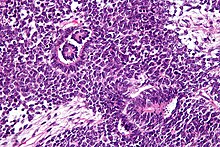
Патологически трехфазная нефробластома состоит из трех элементов:
Опухоль Вильмса - злокачественная опухоль, содержащая метанефрическая бластема, стромальные и эпителиальные производные. Характерно наличие абортивных канальцев и клубочков, окруженных веретенообразной клеточной стромой. Строма может включать поперечно-полосатую мышца, хрящ, кость, жировая ткань и фиброзная ткань. Дисфункция возникает, когда опухоль сдавливает нормальную паренхиму почек.
Мезенхимальный компонент может включать клетки, демонстрирующие дифференцировку рабдомиоидов или злокачественные новообразования (рабдомиосаркоматозный Вильмс).
Опухоли Вильмса можно разделить на две прогностические группы на основе патологических характеристик:
- Благоприятный - Содержит хорошо проработанные компоненты, упомянутые выше
- Анапластический - Содержит диффузную анаплазию (плохо развитые клетки)
Мутации WT1 ген, расположенный на коротком плече хромосома 11 (11p13) наблюдаются примерно в 20% опухолей Вильмса.[7][8] По крайней мере, половина опухолей Вильмса с мутациями в WT1 также несут мутации в CTNNB1, ген, кодирующий протоонкоген бета-катенин.[9] Этот последний ген находится на коротком плече хромосома 3 (3p22.1).
В большинстве случаев мутации ни в одном из этих генов отсутствуют.[10]
| Название синдрома | Связанный генетический вариант | Риск опухоли Вильмса | Описание синдрома |
| Синдром WAGR (Опухоль Вильмса, аниридия, аномалии половых органов, задержка развития) | Удаление гена, которое включает оба WT1 и PAX6 | 45–60% | Характеризуется опухолью Вильмса, аниридия (отсутствие радужки), гемигипертрофия (одна сторона тела больше другой), аномалии мочеполовой системы, неоднозначные гениталии, умственная отсталость.[11] |
| Синдром Дениса-Драша (DDS) | WT1 (экзон 8 и 9) | 74% | Характерны заболевания почек с рождения, приводящие к ранней почечной недостаточности, неоднозначности гениталий (интерсексуальные расстройства).[11] |
| Синдром Беквита-Видемана | Аномальная регуляция хромосомы 11p15.5 | 7% | Характеризуется макросмией (большой размер при рождении), макроглоссия (большой язык), гемигипертрофия (одна сторона тела больше), другие опухоли в теле, омфалоцеле (открытая брюшная стенка) и висцеромегалия (увеличение внутренних органов брюшной полости).[11] |
Ассоциация с H19 было сообщено.[12] H19 - это длинная некодирующая РНК расположен на коротком плече хромосома 11 (11п15.5).
Диагностика
Большинство людей с опухолью Вильмса имеют бессимптомное новообразование в брюшной полости, которое замечает член семьи или медицинский работник.[13] Опухоли почек также могут быть обнаружены во время планового скрининга у детей, у которых были известны предрасполагающие клинические синдромы.[13] Диагностический процесс включает сбор анамнеза, медицинский осмотр и серию анализов, включая анализы крови, мочи и визуализации.[14]
При подозрении на опухоль Вильмса обычно сначала проводят ультразвуковое исследование, чтобы подтвердить наличие внутрипочечного образования.[14] А компьютерная томография или же МРТ также можно использовать для получения более детального изображения. Наконец, диагноз опухоли Вильмса подтверждается образцом ткани.[15] В большинстве случаев биопсия не делается в первую очередь, потому что есть риск распространения раковых клеток во время процедуры. Лечение в Северной Америке нефрэктомия или в Европе химиотерапия с последующей нефрэктомией. Окончательный диагноз ставится при патологическом исследовании образца нефрэктомии.[15]
Постановка
Стадия - это стандартный способ описания степени распространения опухоли Вильмса.[16] и определить прогноз и лечение. Постановка основана на анатомический находки и патология опухолевых клеток.[17][18] В зависимости от степени опухолевой ткани на момент постановки диагноза рассматриваются пять стадий.
При опухоли Вильмса I стадии (43% случаев) должны выполняться все следующие критерии:
- Опухоль ограничена почка и полностью вырезан.
- Поверхность почечная капсула цела.
- Перед удалением опухоль не разрывается и не проводится биопсия (открытая или игла).
- Отсутствие поражения лимфо-сосудистых пространств экстраренальных или почечных синусов
- За пределами иссечения остаточной опухоли не видно.
- Метастазов опухоли в лимфатические узлы не выявлено.
На стадии II (23% случаев) должны выполняться 1 или несколько из следующих критериев:
- Опухоль выходит за пределы почки, но полностью иссекается.
- Никаких остаточных опухолей на границах иссечения или за ними.
- Также может существовать любое из следующих условий:
- Опухолевое поражение кровеносных сосудов почечного синуса и / или вне паренхимы почек.
- Обширное опухолевое поражение мягких тканей почечного синуса.
На стадии III (20% случаев) должны выполняться 1 или несколько из следующих критериев:
- Неоперабельная первичная опухоль.
- Метастазы в лимфатические узлы.
- Опухоль присутствует на хирургических краях.
- Распространение опухоли на поверхность брюшины до или во время операции или рассечение тромба опухоли.
- Перед удалением опухоли была сделана биопсия, или во время операции наблюдается локальное разливание опухоли, ограниченное боку.
Стадия IV (10% случаев) Опухоль Вильмса определяется наличием гематогенных метастазов (легкие, печень, кости или мозг) или метастазов в лимфатические узлы за пределами брюшно-тазовой области.
V стадия (5% случаев) Опухоль Вильмса определяется двусторонним поражением почек на момент постановки первичного диагноза. Для пациентов с двусторонним поражением следует попытаться[согласно кому? ] провести стадию каждой стороны в соответствии с вышеуказанными критериями (стадия от I до III) на основе степени заболевания до биопсии.
Лечение / прогноз
Общая 5-летняя выживаемость оценивается примерно в 90%,[19][20] но для людей прогноз во многом зависит от индивидуальных постановка и лечение. Раннее удаление обычно способствует положительным результатам.
Опухоль-специфическая потеря гетерозиготности (LOH) для хромосом 1p и 16q определяет подмножество пациентов с опухолью Вильмса, у которых значительно повышен риск рецидива и смерти. LOH для этих хромосомных областей теперь может использоваться как независимый прогностический фактор вместе со стадией заболевания, чтобы нацелить интенсивность лечения на риск неудачи лечения.[21][22] Число копий в масштабе всего генома и статус LOH можно оценить с помощью виртуальное кариотипирование опухолевых клеток (свежих или залитых парафином).
Статистика может иногда показывать более благоприятные результаты для более агрессивных стадий, чем для менее агрессивных стадий, что может быть вызвано более агрессивным лечением и / или случайная изменчивость в учебных группах. Кроме того, опухоль V стадии не обязательно хуже опухоли стадии IV.
| Этап[23] | Гистопатология[23] | 4 года безрецидивная выживаемость (RFS) или выживание без событий (EFS)[23] | 4 года Общая выживаемость (ОПЕРАЦИОННЫЕ СИСТЕМЫ)[23] | Уход[23] |
|---|---|---|---|---|
| I этап[23] | Благоприятное гистологическое исследование у детей младше 24 месяцев или вес опухоли менее 550 г | 85% | 98% | Только хирургическое вмешательство (должно выполняться только в рамках клинического исследования) |
| Благоприятная гистология у детей старше 24 месяцев или вес опухоли более 550 г | 94% RFS | 98% | Нефрэктомия + забор лимфатических узлов с соблюдением режима EE-4A | |
| Размытый анапластический | 68% EFS | 80% | Нефрэктомия + забор лимфатических узлов с последующим лечением EE-4A и лучевая терапия | |
| II этап[23] | Благоприятная гистология | 86% RFS | 98% | Нефрэктомия + забор лимфатических узлов с последующей схемой EE-4A |
| Фокальный анапластический | 80% EFS | 80% | Нефрэктомия + забор лимфатических узлов с последующей лучевой терапией брюшной полости и режимом ДД-4А | |
| Диффузный анапластик | 83% EFS | 82% | Нефрэктомия + забор лимфатических узлов с последующей лучевой терапией брюшной полости и режим I | |
| III стадия[23] | Благоприятная гистология | 87% RFS | 94% | Нефрэктомия + забор лимфатических узлов с последующей лучевой терапией брюшной полости и режимом ДД-4А |
| Фокальный анапластический | 88% RFS | 100% (8 человек в исследовании) | Нефрэктомия + забор лимфатических узлов с последующей лучевой терапией брюшной полости и режимом DD-4A | |
| Очаговая анапластика (предоперационное лечение) | 71% RFS | 71% | Предоперационное лечение по схеме DD-4A с последующей нефрэктомией + забор лимфатических узлов и абдоминальная лучевая терапия | |
| Диффузный анапластик | 46% EFS | 53% | Предоперационное лечение по схеме I с последующей нефрэктомией + забор лимфатических узлов и лучевая терапия брюшной полости | |
| Диффузный анапластик | 65% EFS | 67% | Немедленная нефрэктомия + забор лимфатических узлов с последующей лучевой терапией брюшной полости и режимом I | |
| IV этап[23] | Благоприятная гистология | 76% RFS | 86% | Нефрэктомия + забор лимфатических узлов с последующей лучевой терапией брюшной полости, двусторонней лучевой терапией легких и режимом DD-4A |
| Фокальный анапластический | 61% EFS | 72% | Нефрэктомия + забор лимфатических узлов с последующей лучевой терапией брюшной полости, двусторонней лучевой терапией легких и режимом DD-4A | |
| Диффузный анапластик | 33% EFS | 33% | Немедленная нефрэктомия + забор лимфатических узлов с последующей лучевой терапией брюшной полости, лучевой терапией всего легкого и режимом I | |
| Диффузный анапластик (предоперационное лечение) | 31% EFS | 44% | Предоперационное лечение по схеме I с последующей нефрэктомией + забор лимфатических узлов с последующей лучевой терапией брюшной полости, лучевой терапией всего легкого | |
| V этап[23] | Общий | 61% EFS | 80% | |
| Благоприятная гистология | 65% | 87% | Предоперационное лечение по схеме ДД-4А с последующей нефроносохраняющей операцией или нефрекомией, стадированием опухолей и химиотерапией и / или лучевой терапией в зависимости от патологии и стадии | |
| Фокальный анапластический | 76% | 88% | Предоперационное лечение по схеме ДД-4А с последующей нефроносохраняющей операцией или нефрекомией, стадированием опухолей и химиотерапией и / или лучевой терапией в зависимости от патологии и стадии | |
| Диффузный анапластик | 25% | 42% | Предоперационное лечение по схеме ДД-4А с последующей нефроносохраняющей операцией или нефрекомией, стадированием опухолей и химиотерапией и / или лучевой терапией в зависимости от патологии и стадии |
В случае рецидива опухоли Вильмса 4-летняя выживаемость детей со стандартным риском оценивается в 80%.[24]
Эпидемиология
Опухоль Вильмса - самая распространенная злокачественная опухоль почек у детей.[25] Существует ряд редких генетических синдромов, которые связаны с повышенным риском развития опухоли Вильмса.[26] Правила скрининга различаются в зависимости от страны; однако специалисты в области здравоохранения рекомендуют регулярное ультразвуковое обследование людей со связанными генетическими синдромами.[26]
Опухоль Вильмса поражает примерно одного человека на 10000 во всем мире в возрасте до 15 лет.[27] Люди африканского происхождения могут иметь немного более высокие показатели опухоли Вильмса.[27] Пиковый возраст опухоли Вильмса составляет от 3 до 4 лет, и большинство случаев возникает в возрасте до 10 лет.[28] Генетическая предрасположенность к опухоли Вильмса у лиц с аниридия было установлено, из-за делеций в полосе p13 на хромосоме 11.[29]
История
Доктор Сидни Фарбер, основатель Института рака Дана-Фарбер, и его коллеги достигли первых ремиссий при опухоли Вильмса в 1950-х годах. Используя антибиотик актиномицин D в дополнение к хирургическому вмешательству и лучевой терапии, они повысили процент излечения с 40 до 89 процентов.[нужна цитата ]
Использование компьютерная томография к диагностике опухоли Вильмса началась в начале 1970-х годов благодаря интуиции доктора Марио Костичи, итальянский врач. Он обнаружил, что на прямых рентгенограммах и на урографических изображениях можно идентифицировать определяющие элементы для дифференциального диагноза с опухолью Вильмса. Эта возможность была предпосылкой для начала лечения.[30]
Известные случаи
Эта секция содержит информацию неясного или сомнительного характера важность или же актуальность к теме статьи. (Узнайте, как и когда удалить этот шаблон сообщения) |
Винс Нил Дочь Скайлар умерла от рака в августе 1995 года, за месяц до того, как он выпустил свой альбом. Вырезанный в камне, который включает трибьют-трек "Skylar's Song".
Смотрите также
- Гемигипертрофия
- Национальная группа исследования опухолей Вильмса (NWTS)
- Синдром Перлмана
- Виртуальный кариотип для 1p и 16q LOH
Рекомендации
- ^ База данных EBSCO проверено URAC; доступ из Больница Маунт-Синай, Нью-Йорк
- ^ WhoNamedIt.com: Макс Вильмс
- ^ а б c «Лечение опухолей Вильмса и других детских опухолей почек». Национальный институт рака. Получено 2018-11-12.
- ^ Эргинель Б., Вурал С., Акын М., Карадаг К.А., Север Н., Йылдыз А. и др. (2014) Опухоль Вильмса: 24-летнее ретроспективное исследование из одного центра. Педиатр Hematol Oncol 31: 409–414
- ^ а б c Редакционная коллегия PDQ по педиатрическому лечению (2002), «Лечение опухолей Вильмса и других детских опухолей почек (PDQ®): версия для специалистов в области здравоохранения», Информационные сводки PDQ по раку, Национальный институт рака (США), PMID 26389282, получено 2018-11-26
- ^ Гуарагна М.С., Соарди ФК, Ассумпсао Дж. Г., Замбальди Л., Кардиналли И. А., Юнес Дж. А., де Мелло М. П., Брандалис С. Р., Агияр С. (август 2010 г.). «Новая мутация гена WT1 p.H377N, связанная с синдромом Дениса-Драша». Журнал детской гематологии / онкологии. 32 (6): 486–8. Дои:10.1097 / MPH.0b013e3181e5e20d. PMID 20562648. S2CID 205860918.
- ^ Call KM, Glaser T, Ito CY, Buckler AJ, Pelletier J, Haber DA, Rose EA, Kral A, Yeger H, Lewis WH (февраль 1990 г.). «Выделение и характеристика гена полипептида цинкового пальца в опухолевом локусе Вильмса 11 хромосомы человека». Клетка. 60 (3): 509–20. Дои:10.1016 / 0092-8674 (90) 90601-А. PMID 2154335. S2CID 29092372.
- ^ Хафф V (октябрь 1998 г.). «Генетика опухоли Вильмса». Американский журнал медицинской генетики. 79 (4): 260–7. Дои:10.1002 / (SICI) 1096-8628 (19981002) 79: 4 <260 :: AID-AJMG6> 3.0.CO; 2-Q. PMID 9781905.
- ^ Маити С., Алам Р., Амос С. И., Хафф В. (ноябрь 2000 г.). «Частая ассоциация мутаций бета-катенина и WT1 в опухолях Вильмса». Исследования рака. 60 (22): 6288–92. PMID 11103785.
- ^ Рутесхаузер Е.К., Робинсон С.М., Хафф В. (июнь 2008 г.) «Генетика опухоли Вильмса: мутации в WT1, WTX и CTNNB1 составляют лишь около одной трети опухолей». Гены, хромосомы и рак. 47 (6): 461–70. Дои:10.1002 / gcc.20553. ЧВК 4332772. PMID 18311776.
- ^ а б c Dome JS, Graf N, Geller JI, Fernandez CV, Mullen EA, Spreafico F, Van den Heuvel-Eibrink M, Pritchard-Jones K (сентябрь 2015 г.). "Достижения в области лечения и биологии опухолей Вильмса: прогресс благодаря международному сотрудничеству". Журнал клинической онкологии. 33 (27): 2999–3007. Дои:10.1200 / JCO.2015.62.1888. ЧВК 4567702. PMID 26304882.
- ^ Coorens THH, Treger TD, Al-Saadi R, Moore L, Tran MGB, Mitchell TJ, Tugnait S, Thevanesan C, Young MD, Oliver TRW, Oostveen M, Collord G, Tarpey PS, Cagan A, Hooks Y, Bestive M, Reynolds BC, Barone G, Anderson J, Jorgensen M, Burke GAA, Visser J, Nicholson JC, Smeulders N, Mushtaq I, Stewart GD, Campbell PJ, Wedge DC, Martincorena I, Rampling D, Hook L, Warren AY, Coleman N , Chowdhury T, Sebire N, Drost J, Saeb-Parsy K, Stratton MR, Straathof K, Pritchard-Jones K, Behjati S (2019) Эмбриональные предшественники опухоли Вильмса. Наука 366 (6470): 1247-1251
- ^ а б Редакционная коллегия PDQ по педиатрическому лечению (2002). Лечение опухолей Вильмса и других детских опухолей почек (PDQ®): версия для специалистов в области здравоохранения. Информационные сводки PDQ по раку. Национальный институт рака (США). PMID 26389282. Получено 2018-11-12.
- ^ а б «Представление, диагностика и стадирование опухоли Вильмса».
- ^ а б Szychot E, Apps J, Pritchard-Jones K (январь 2014 г.). «Опухоль Вильмса: биология, диагностика и лечение». Переводческая педиатрия. 3 (1): 12–24. Дои:10.3978 / j.issn.2224-4336.2014.01.09. ЧВК 4728859. PMID 26835318.
- ^ "Как ставится опухоль Вильмса?". www.cancer.org. Получено 2015-11-15.
- ^ "Опухоль Вильмса - Детство - Этапы". Cancer.Net. Получено 2015-11-15.
- ^ «Лечение по типу и стадии опухоли Вильмса». www.cancer.org. Получено 2015-11-13.
- ^ Stewénius Y, Jin Y, Øra I, de Kraker J, Bras J, Frigyesi A, Alumets J, Sandstedt B, Meeker AK, Gisselsson D (ноябрь 2007 г.). «Нарушение сегрегации хромосом и дисфункция теломер в агрессивных опухолях Вильмса». Клинические исследования рака. 13 (22, п. 1): 6593–602. Дои:10.1158 / 1078-0432.CCR-07-1081. PMID 18006759.
- ^ Tournade MF, Com-Nougué C, de Kraker J, Ludwig R, Rey A, Burgers JM, Sandstedt B, Godzinski J, Carli M, Potter R, Zucker JM (январь 2001 г.). «Оптимальная продолжительность предоперационной терапии односторонней и неметастатической опухоли Вильмса у детей старше 6 месяцев: результаты испытаний и исследования опухолей Вильмса Девятого международного общества педиатрической онкологии». Журнал клинической онкологии. 19 (2): 488–500. Дои:10.1200 / jco.2001.19.2.488. PMID 11208843.
- ^ Мессахель Б., Уильямс Р., Ридольфи А., А'херн Р., Уоррен В., Тинворт Л., Хобсон Р., Аль-Саади Р., Уайман Г., Брандлер М.А., Келси А., Себир Н., Джонс С., Вуянич Г., Притчард-Джонс К. (Март 2009 г.). «Потеря аллелей при 16q определяет худший прогноз опухоли Вильмса независимо от подхода к лечению в клинических испытаниях UKW1-3: исследование детской группы рака и лейкемии (CCLG)». Европейский журнал рака. 45 (5): 819–26. Дои:10.1016 / j.ejca.2009.01.005. PMID 19231157.
- ^ Гранди П.Е., Бреслоу Н.Э., Ли С., Перлман Э., Беквит Дж. Б., Ричи М.Л., Шамбергер Р.С., Хаасе Г.М., Д'Анджио Дж. Дж., Дональдсон М., Коппс М.Дж., Малоголовкин М., Ширер П., Томас П.Р., Маклис Р., Томлинсон Г. Хафф В., Грин DM (октябрь 2005 г.). «Потеря гетерозиготности по хромосомам 1p и 16q является неблагоприятным прогностическим фактором при благоприятной гистологии опухоли Вильмса: отчет Национальной группы изучения опухолей Вильмса». Журнал клинической онкологии. 23 (29): 7312–21. Дои:10.1200 / JCO.2005.01.2799. PMID 16129848.
- ^ а б c d е ж грамм час я j Если в полях не указано иное, то ссылка: Лечение опухоли Вильмса в Национальный институт рака. Последнее изменение: 29.03.2012
- ^ Спреафико Ф, Причард Джонс К., Малоголовкин М. Х., Бержерон С., Хейл Дж., Де Кракер Дж., Даллорсо С., Ача Т, де Камарго Б., Дом Дж. С., Граф Н. (декабрь 2009 г.). «Лечение рецидивов опухолей Вильмса: извлеченные уроки». Экспертный обзор противоопухолевой терапии. 9 (12): 1807–15. Дои:10.1586 / эра.09.159. PMID 19954292. S2CID 207212698.
- ^ Sonn G, Shortliffe LM (октябрь 2008 г.). «Лечение опухоли Вильмса: современные стандарты лечения». Природа Клиническая практика. Урология. 5 (10): 551–60. Дои:10.1038 / ncpuro1218. PMID 18836464. S2CID 23599363.
- ^ а б Kalish JM, Doros L, Helman LJ, Hennekam RC, Kuiper RP, Maas SM, Maher ER, Nichols KE, Plon SE, Porter CC, Rednam S, Schultz KA, States LJ, Tomlinson GE, Zelley K, Druley TE (июль 2017 г. ). «Рекомендации по надзору за детьми с синдромами избыточного роста и предрасположенностью к опухолям Вильмса и гепатобластоме». Клинические исследования рака. 23 (13): e115 – e122. Дои:10.1158 / 1078-0432.CCR-17-0710. ЧВК 5538793. PMID 28674120.
- ^ а б Бреслоу Н., Ольшан А., Беквит Дж. Б., Грин Д.М. (1993). «Эпидемиология опухоли Вильмса». Медицинская и детская онкология. 21 (3): 172–81. Дои:10.1002 / МПО.2950210305. PMID 7680412.
- ^ Бреслоу, NE, Беквит Дж. Б., Перлман Э. Дж., Рив А. Э. (сентябрь 2006 г.). «Распределение по возрасту, весу при рождении, нефрогенному отдыху и гетерогенности в патогенезе опухоли Вильмса». Детская кровь и рак. 47 (3): 260–7. Дои:10.1002 / pbc.20891. ЧВК 1543666. PMID 16700047.
- ^ Причард-Джонс К., Флеминг С., Дэвидсон Д., Бикмор В., Портеус Д., Госден К., Бард Дж., Баклер А., Пеллетье Дж., Хаусман Д. (июль 1990 г.). «Ген опухоли кандидата Вильмса участвует в развитии мочеполовой системы». Природа. 346 (6280): 194–7. Bibcode:1990Натура.346..194P. Дои:10.1038 / 346194a0. PMID 2164159. S2CID 4350729.
- ^ Нефробластома в детстве: современные возможности для ранней рентгенологической диагностики, итальянский журнал хирургии, 1969 г.
внешняя ссылка
| Классификация | |
|---|---|
| Внешние ресурсы |