Тирозинкиназа рецептора AXL - AXL receptor tyrosine kinase
Рецептор тирозин-протеинкиназы UFO является фермент что у людей кодируется AXL ген.[5][6] Первоначально ген был обозначен как UFO в связи с неустановленной функцией этого белка.[7] Однако за годы, прошедшие с момента его открытия, исследование профиля и механизма экспрессии AXL сделало его все более привлекательной целью, особенно для лечения рака. В последние годы AXL превратился в ключевой фактор, способствующий избавлению от иммунитета и устойчивости раковых клеток к лекарствам, что приводит к агрессивному и метастатическому раку.[8]
AXL - это клеточная поверхность рецептор тирозинкиназа, часть семейства киназ ТАМ, включая TYRO3 и MERTK.[нужна цитата ]
Структура генов и белков
Ген Axl эволюционно консервативен у позвоночных. Этот ген имеет два различных варианта транскрипта с альтернативным сплайсингом.[6]
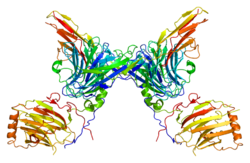
Белок, кодируемый этим геном, является членом рецепторная тирозинкиназа подсемейство. Хотя он похож на другие рецепторные тирозинкиназы, белок Axl представляет собой уникальную структуру внеклеточной области, которая сопоставляет IgL и FNIII повторяется.[6]
Белок AXL характеризуется внеклеточной структурой, состоящей из двух повторов, подобных фибронектину типа 3, и двух иммуноглобулиноподобных повторов, а также его внутриклеточного тирозинкиназного домена.
AXL находится в непосредственной близости от BCL3 онкоген, который находится на уровне 19q13.1-q13.2.[6]
Функция
Рецептор AXL преобразует сигналы от внеклеточный матрикс в цитоплазма путем связывания факторов роста, таких как витамин К-зависимый белок, специфичный для остановки роста белка, ген 6 (ГАЗ6 ). Он участвует в стимуляции пролиферация и выживание клеток. Протеолитическое расщепление внеклеточного домена AXL металлопротеиназы ADAM10 и ADAM17 может подавлять эту сигнальную активность.[9]
Сигнальные пути, активируемые ниже AXL, включают PI3K-AKT-mTOR, MEKERK, NF-κB и JAK / STAT.[10]
Этот рецептор также может опосредовать агрегацию клеток путем гомофильного связывания.[6]
Белок AXL экспрессируется в нормальных тканях, особенно в строме костного мозга и миелоидных клетках, а также в опухолевых клетках и сосудистой сети опухоли.[11][12] При раке AXL экспрессируется на опухолевых клетках, а также на соседних иммунных клетках, включая дендритные клетки, макрофаги, и NK-клетки.
Axl - ингибитор врожденный иммунный ответ. Функция активированного AXL в нормальных тканях включает эффективный клиренс апоптотического материала и подавление TLR-зависимых воспалительных реакций и активности естественных клеток-киллеров.[13]
AXL является предполагаемой движущей силой разнообразных клеточных процессов, которые имеют решающее значение для развития, роста и распространения опухолей, включая пролиферацию, инвазивность и миграцию, эпителиально-мезенхимальный переход, стволовость, ангиогенез и иммунная модуляция.[10] AXL считается драйвером рака и коррелирует с плохой выживаемостью при многочисленных агрессивных опухолях, включая тройной отрицательный рак груди (TNBC), острый миелоидный лейкоз (AML), немелкоклеточный рак легкого (NSCLC), рак поджелудочной железы и рак яичников. , среди прочего.[14]
Клиническое значение
Axl был впервые выделен в 1988 году и идентифицирован как онкоген при скрининге трансформирующих генов у пациентов с хронический миелолейкоз - что переросло в «взрывной кризис».[15] С тех пор повышенная экспрессия AXL была связана с многочисленными видами рака, включая рак легких, рак молочной железы, панкреатический рак, рак яичников, рак толстой кишки и меланома среди прочего, и было показано, что они имеют сильную корреляцию с плохими результатами выживания.[12]
Было показано, что AXL является ключевым фактором лекарственной устойчивости к таргетной терапии, иммунотерапии и химиотерапии на различных моделях животных. Основываясь на текущих знаниях о роли AXL в устойчивости к терапии, будущие исследования помогут определить, имеет ли AXL трансляционное применение в качестве биомаркера для прогнозирования терапевтического ответа на известные лекарства.
В последнее время AXL был вовлечен в хронические фиброзные заболевания нескольких органов, включая печень.[16]
AXL также может играть важную роль в Вирус Зика инфекция, позволяющая проникнуть вирусу в клетки-хозяева.[17]
Как мишень для наркотиков
Исследования показали, что нокдаун AXL приводит к подавлению транскрипционных факторов, необходимых для ЕМТ, включая Slug, Twist и Zeb1, а также к повышенной экспрессии E-кадгерина.[18]
Клинические исследования
Рак
Несколько препаратов, классифицируемых как «ингибиторы AXL», вступили в клинические испытания; однако многие нацелены на множественные рецепторы киназ в дополнение к AXL. Самый продвинутый AXL селективный ингибитор бемчентиниб (BGB324 или R428), небольшая молекула для перорального применения, которая в настоящее время проходит несколько клинических испытаний фазы II для лечения НМРЛ, TNBC, AML и меланомы. Бемчентиниб используется в качестве монотерапии и в качестве комбинированной терапии с существующими и новыми видами таргетной терапии, иммунотерапией и химиотерапией.
Моноклональные антитела, нацеленные на AXL (YW327.6S2) и рецептор-ловушку AXL (GL2I.T), в настоящее время находятся в стадии доклинической разработки. Кроме того, ожидается, что пероральный ингибитор AXL (TP-0903) войдет в фазу 1 клинических испытаний в ноябре 2016 года (для запущенных солидных опухолей: NCT02729298).
Астеллас Фарма в настоящее время тестирует гильтеритиниб (ASP2215), сдвоенный FLT3 -AXL ингибитор тирозинкиназы в острый миелоидный лейкоз (AML). В 2017 году гильтеритиниб получил одобрение FDA. статус орфанных препаратов для AML.[19]
Эти одобренные препараты, а также текущие и ожидаемые клинические испытания подчеркивают потенциально широкую безопасность и эффективность ингибирования AXL.[10]
Взаимодействия
Было показано, что тирозинкиназа рецептора AXL взаимодействовать с участием TENC1.[20]
использованная литература
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000167601 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000002602 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ О'Брайан Дж. П., Фрай Р. А., Когсуэлл П. К., Нойбауэр А., Китч Б., Прокоп С., Эспиноза Р., Ле Бо М. М., Эрп Г. С., Лю Е. Т. (октябрь 1991 г.). «axl, трансформирующий ген, выделенный из первичных клеток миелоидного лейкоза человека, кодирует новую рецепторную тирозинкиназу». Молекулярная и клеточная биология. 11 (10): 5016–31. Дои:10.1128 / mcb.11.10.5016. ЧВК 361494. PMID 1656220.
- ^ а б c d е «Ген Entrez: тирозинкиназа рецептора AXL AXL».
- ^ Янссен Дж. В., Шульц А. С., Стеенвоорден А. С., Шмидбергер М., Штрел С., Амброс П. Ф., Бартрам С. Р. (1991). «Новый предполагаемый рецептор тирозинкиназы с онкогенным потенциалом». Онкоген. 6 (11): 2113–20. PMID 1834974.
- ^ Davidsen, Kjersti T .; Haaland, Gry S .; Ложь, Мария К .; Лоренс, Джеймс Б. (2017). Роль тирозинкиназы рецептора Axl в пластичности опухолевых клеток и устойчивости к терапии. В: Акслен Л., Уотник Р. (ред.) Биомаркеры микросреды опухоли.. Спрингер, Чам. С. 351–376. ISBN 978-3-319-39147-2.
- ^ Миллер М.А., Удин М.Дж., Салливан Р.Дж., Ван С.Дж., Мейер А.С., Им Х, Фредерик Д.Т., Тадрос Дж., Гриффит Л.Г., Ли Х., Вайследер Р., Флаэрти К.Т., Гертлер Ф.Б., Лауффенбургер Д.А. (2016). «Снижение протеолитического шеддинга рецепторных тирозинкиназ является посттрансляционным механизмом устойчивости к ингибиторам киназ». Открытие рака. 6 (4): 382–99. Дои:10.1158 / 2159-8290.CD-15-0933. ЧВК 5087317. PMID 26984351.
- ^ а б c Гей, Карл М; Баладжи, Кавита; Байерс, Лорен Аверетт (2017). «Преодоление AXL: нацеливание на AXL при злокачественных новообразованиях человека». Британский журнал рака. 116 (4): 415–423. Дои:10.1038 / bjc.2016.428. ISSN 0007-0920. ЧВК 5318970. PMID 28072762.
- ^ Neubauer A, Fiebeler A, Graham DK, O'Bryan JP, Schmidt CA, Barckow P, Serke S, Siegert W., Snodgrass HR, Huhn D (1994). «Экспрессия axl, трансформирующей рецепторной тирозинкиназы, при нормальном и злокачественном гематопоэзе». Кровь. 84 (6): 1931–41. Дои:10.1182 / кровь.V84.6.1931.1931. PMID 7521695.
- ^ а б Шие Ю.С., Лай С.Й., Као Ю.Р., Шайа С.Г., Чу Ю.В., Ли Х.С., Ву К.В. (2005). «Экспрессия axl в аденокарциноме легкого и корреляция с прогрессированием опухоли». Неоплазия. 7 (12): 1058–64. Дои:10.1593 / neo.05640. ЧВК 1501169. PMID 16354588.
- ^ Rothlin CV, Ghosh S, Zuniga EI, Oldstone MB, Lemke G (2007). «Рецепторы ТАМ являются плейотропными ингибиторами врожденного иммунного ответа». Ячейка. 131 (6): 1124–36. Дои:10.1016 / j.cell.2007.10.034. PMID 18083102. S2CID 12908403.
- ^ Вайкоци П., Князев П., Кункель А., Капелле Х. Х., Берндт С., фон Тенг-Коблигк Х., Кисслинг Ф., Эйхельсбахер Ю., Эссиг М., Рид Т.А., Эрбер Р., Ульрих А. (апрель 2006 г.). «Доминантно-отрицательное ингибирование тирозинкиназы рецептора Axl подавляет рост и инвазию опухолевых клеток мозга и продлевает выживаемость». Труды Национальной академии наук Соединенных Штатов Америки. 103 (15): 5799–804. Дои:10.1073 / pnas.0510923103. ЧВК 1458653. PMID 16585512.
- ^ Лю Э., Хьелле Б., Епископ Дж. М. (1988). «Трансформирующие гены при хроническом миелолейкозе». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 85 (6): 1952–6. Дои:10.1073 / пнас.85.6.1952. ЧВК 279899. PMID 3279421.
- ^ Барсена С., Стефанович М., Тутусаус А., Хоаннас Л., Менендес А., Гарсиа-Руис С., Санчо-Бру П., Мари М., Кабальерия Дж., Ротлин К.В., Фернандес-Чека Дж. С., де Фрутос П. Г., Моралес А. (2015). «Путь Gas6 / Axl активируется при хроническом заболевании печени, и его нацеливание снижает фиброз за счет инактивации звездчатых клеток печени». Журнал гепатологии. 63 (3): 670–678. Дои:10.1016 / j.jhep.2015.04.013. ISSN 1934-5909. ЧВК 4543529. PMID 25908269.
- ^ Новаковски Т.Дж., Пыльца А.А., Ди Лулло Э., Сандовал-Эспиноза С., Берштейн М., Кригштейн А.Р. (2016). «Анализ экспрессии подчеркивает, что AXL является кандидатом рецептора входа вируса Зика в нервные стволовые клетки». Стволовая клетка. 18 (5): 591–596. Дои:10.1016 / j.stem.2016.03.012. ISSN 1934-5909. ЧВК 4860115. PMID 27038591.
- ^ Asiedu MK, Beauchamp-Perez FD, Ingle JN, Behrens MD, Radisky DC, Knutson KL (2014). «AXL индуцирует переход эпителия в мезенхиму и регулирует функцию стволовых клеток рака груди». Онкоген. 33 (10): 1316–24. Дои:10.1038 / onc.2013.57. ЧВК 3994701. PMID 23474758.
- ^ Нам, Джеймс (20 июля 2017 г.). «Гильтеритиниб получил статус орфанного препарата для лечения острого миелоидного лейкоза». Советник по терапии рака. Haymarket Media Inc.
- ^ Хафизи С., Алиндри Ф., Карлссон Р., Дальбек Б. (декабрь 2002 г.). «Взаимодействие тирозинкиназы рецептора Axl с C1-TEN, новым белком, содержащим домен C1, гомологичным тензину». Сообщения о биохимических и биофизических исследованиях. 299 (5): 793–800. Дои:10.1016 / S0006-291X (02) 02718-3. PMID 12470648.
дальнейшее чтение
- Нойбауэр А., Бурхерт А., Майвальд С., Грусс Х. Дж., Серке С., Хун Д., Виттиг Б., Лю Э. (март 1997 г.). «Недавний прогресс в изучении роли Axl, рецепторной тирозинкиназы, в злокачественной трансформации миелоидных лейкозов». Лейкемия и лимфома. 25 (1–2): 91–6. Дои:10.3109/10428199709042499. PMID 9130617.
- Бергсагель П.Л., Виктор-Кобрин С., Тимблин С.Р., Трепель Дж., Кюль В.М. (январь 1992 г.). «КДНК мыши кодирует панэпителиальный гликопротеин, который также экспрессируется на плазматических клетках». Журнал иммунологии. 148 (2): 590–6. PMID 1729376.
- Партанен Дж., Мякеля Т.П., Алитало Р., Лехваслайхо Х., Алитало К. (ноябрь 1990 г.). «Предполагаемые тирозинкиназы, экспрессируемые в клетках лейкемии человека К-562». Труды Национальной академии наук Соединенных Штатов Америки. 87 (22): 8913–7. Дои:10.1073 / pnas.87.22.8913. ЧВК 55070. PMID 2247464.
- О'Брайан Дж. П., Фриделл Ю. В., Коски Р., Варнум Б., Лю ET (январь 1995 г.). «Трансформирующая рецепторная тирозинкиназа, Axl, посттрансляционно регулируется протеолитическим расщеплением». Журнал биологической химии. 270 (2): 551–7. Дои:10.1074 / jbc.270.2.551. PMID 7822279.
- Ли С.Т., Странк К.М., Spritz RA (декабрь 1993 г.). «Обзор мРНК протеинтирозинкиназы, экспрессируемых в нормальных меланоцитах человека». Онкоген. 8 (12): 3403–10. PMID 8247543.
- Schulz AS, Schleithoff L, Faust M, Bartram CR, Janssen JW (февраль 1993 г.). «Геномная структура рецептора НЛО человека». Онкоген. 8 (2): 509–13. PMID 8381225.
- О'Брайан Дж. П., Сонъян З., Кэнтли Л., Дер С. Дж., Поусон Т. (апрель 1996 г.). «Адаптерный белок млекопитающих с консервативной гомологией 2 Src и фосфотирозин-связывающими доменами родственен Shc и специфически экспрессируется в головном мозге». Труды Национальной академии наук Соединенных Штатов Америки. 93 (7): 2729–34. Дои:10.1073 / pnas.93.7.2729. ЧВК 39699. PMID 8610109.
- Марк М.Р., Чен Дж., Хаммондс Р.Г., Садик М., Годовск П.Дж. (апрель 1996 г.). «Характеристика Gas6, члена суперсемейства белков, содержащих домен G, в качестве лиганда для Rse и Axl». Журнал биологической химии. 271 (16): 9785–9. Дои:10.1074 / jbc.271.16.9785. PMID 8621659.
- Браунгер Дж., Шлейтофф Л., Шульц А.С., Кесслер Х., Ламмерс Р., Ульрих А., Бартрам С.Р., Янссен Дж. В. (июнь 1997 г.). «Внутриклеточная передача сигналов тирозинкиназы рецептора Ufo / Axl опосредуется главным образом через сайт стыковки с несколькими субстратами». Онкоген. 14 (22): 2619–31. Дои:10.1038 / sj.onc.1201123. PMID 9178760.
- Танака К., Нагаяма И., Накано Т., Такамура Н., Намба Х., Фукада С., Кума К., Ямасита С., Нива М. (март 1998 г.). «Профиль экспрессии генов протеинтирозинкиназ рецепторного типа в щитовидной железе человека». Эндокринология. 139 (3): 852–8. Дои:10.1210 / en.139.3.852. PMID 9492013.
- Янагита М., Араи Х., Исии К., Накано Т., Охаши К., Мизуно К., Варнум Б., Фукацу А., Дои Т., Кита Т. (апрель 2001 г.). «Gas6 регулирует пролиферацию мезангиальных клеток через Axl при экспериментальном гломерулонефрите». Американский журнал патологии. 158 (4): 1423–32. Дои:10.1016 / S0002-9440 (10) 64093-X. ЧВК 1891897. PMID 11290560.
- Сан В.С., Мисао Р., Ивагаки С., Фудзимото Дж., Тамая Т. (июнь 2002 г.). «Совместная экспрессия гена 6, специфичного для остановки роста, и рецепторных тирозинкиназ, Axl и Sky, в эндометрите матки человека и эндометриозе яичников». Молекулярная репродукция человека. 8 (6): 552–8. Дои:10,1093 / моль · ч / 8,6,552. PMID 12029073.
- D'Arcangelo D, Gaetano C, Capogrossi MC (октябрь 2002 г.). «Подкисление предотвращает апоптоз эндотелиальных клеток за счет активации Axl». Циркуляционные исследования. 91 (7): e4-12. Дои:10.1161 / 01.RES.0000036753.50601.E9. PMID 12364394.
- Ито М., Накашима М., Накаяма Т., Оцуру А., Нагаяма Й., Такамура Н., Демедчик Е.П., Секин И., Ямасита С. (ноябрь 2002 г.). «Экспрессия тирозинкиназы рецепторного типа Axl и ее лиганда Gas6 в детских карциномах щитовидной железы вокруг Чернобыля». Щитовидная железа. 12 (11): 971–5. Дои:10.1089/105072502320908303. PMID 12490074.