ERBB3 - Википедия - ERBB3
Рецепторная тирозин-протеинкиназа erbB-3, также известный как HER3 (рецептор эпидермального фактора роста человека 3), является мембраносвязанной белок что у людей кодируется ERBB3 ген.
ErbB3 является членом семейство рецепторов эпидермального фактора роста (EGFR / ERBB) рецепторных тирозинкиназ. ErbB3 с нарушенной киназой, как известно, образует активные гетеродимеры с другими членами семейства ErbB, в первую очередь с лиганд с нарушенным связыванием ErbB2.
Ген и экспрессия
Человек ERBB3 Ген расположен на длинном плече хромосомы 12 (12q13). Он кодируется 23 651 пар оснований и переводится в 1342 аминокислоты.[5]
Во время человеческого развития ERBB3 выражается в коже, костях, мышцах, нервной системе, сердце, легких и кишечном эпителии.[6] ERBB3 экспрессируется в желудочно-кишечном тракте, репродуктивной системе, коже, нервной системе, мочевыводящих путях и эндокринной системе взрослого человека.[7]
Структура
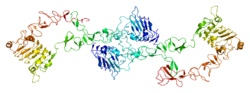
ErbB3, как и другие члены семейства тирозинкиназ рецептора ErbB, состоит из внеклеточного домена, трансмембранного домена и внутриклеточного домена. Внеклеточный домен содержит четыре субдомена (I-IV). Субдомены I и III богаты лейцином и в первую очередь участвуют в связывании лиганда. Поддомены II и IV богаты цистеином и, скорее всего, способствуют конформации и стабильности белка за счет образования дисульфидных связей. Субдомен II также содержит петлю димеризации, необходимую для образования димера.[8] Цитоплазматический домен содержит юкстамембранный сегмент, киназный домен и С-концевой домен.[9]
Нелигандированный рецептор принимает конформацию, которая ингибирует димеризацию. Связывание нейрегулина с лиганд-связывающими субдоменами (I и III) вызывает конформационные изменения в ErbB3, которые вызывают выступание петли димеризации в субдомене II, активируя белок для димеризации.[9]
Функция
Было показано, что ErbB3 связывает лиганды Херегулин[10] и NRG-2.[11] Связывание лиганда вызывает изменение конформации, которое делает возможной димеризацию, фосфорилирование и активацию передачи сигнала. ErbB3 может гетеродимеризоваться с любым из трех других членов семейства ErbB. Теоретический гомодимер ErbB3 будет нефункциональным, потому что белок с нарушенной киназой требует трансфосфорилирования его партнером по связыванию, чтобы быть активным.[9]
В отличие от других членов семейства тирозинкиназ рецептора ErbB, которые активируются посредством аутофосфорилирования при связывании лиганда, было обнаружено, что киназа ErbB3 нарушена, имея только 1/1000 активности аутофосфорилирования EGFR и неспособность фосфорилировать другие белки.[12] Следовательно, ErbB3 должен действовать как аллостерический активатор.
Взаимодействие с ErbB2
Димер ErbB2-ErbB3 считается наиболее активным из возможных димеров ErbB, отчасти потому, что ErbB2 является предпочтительным партнером по димеризации для всех членов семейства ErbB, а ErbB3 является предпочтительным партнером ErbB2.[13] Эта конформация гетеродимера позволяет сигнальному комплексу активировать несколько путей, включая MAPK, PI3K / Akt и PLCγ.[14] Также есть доказательства того, что гетеродимер ErbB2-ErbB3 может связываться и активироваться EGF-подобными лигандами.[15][16]
Активация Путь PI3K / Akt
Внутриклеточный домен ErbB3 содержит 6 сайтов узнавания для домена SH2 субъединицы p85 PI3K.[17] Связывание ErbB3 вызывает аллостерическую активацию p110α, субъединица липидкиназы PI3K,[14] функция не найдена ни в EGFR или ErbB2.
Роль в раке
Хотя не было обнаружено доказательств того, что сверхэкспрессия, конститутивная активация или мутация ErbB3 являются онкогенными,[18] белок как партнер гетеродимеризации, наиболее критично с ErbB2, вовлечен в рост, пролиферацию, химиотерапевтическую резистентность и способствует инвазии и метастазированию.[19][20]
ErbB3 связан с направленной терапевтической резистентностью при многих видах рака, включая резистентность к:
- Ингибиторы HER2 при раке молочной железы HER2 +[21]
- антиэстрогеновая терапия в ER+ рак груди[22][23]
- Ингибиторы EGFR при раке легких, головы и шеи[24][25]
- гормоны при раке простаты[26]
- Ингибиторы IGF1R при гепатомах[27]
- BRAF ингибиторы в меланоме[28]
Сверхэкспрессия ErbB2 может способствовать образованию активных гетеродимеров с ErbB3 и другими членами семейства ErbB без необходимости связывания лиганда, что приводит к слабой, но конститутивной сигнальной активности.[14]
Роль в нормальном развитии
ERBB3 выражается в мезенхима эндокардиальной подушки, которая позже разовьется в клапаны сердца. ErbB3 нулевые эмбрионы мышей обнаруживают сильно недоразвитые атриовентрикулярные клапаны, что приводит к гибели на 13,5-й день эмбриона. Хотя эта функция ErbB3 зависит от нейрегулина, она, по-видимому, не требует ErbB2, который не экспрессируется в ткани.[29]
ErbB3 также, по-видимому, необходим для дифференцировки нервного гребня и развития симпатической нервной системы.[30] и производные нервного гребня, такие как Шванновские клетки.[31]
Смотрите также
- Семейство рецепторов эпидермального фактора роста
- Рецептор эпидермального фактора роста
- Рецепторные тирозинкиназы
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000065361 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000018166 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ген ERBB3 - Генные карты | Белок ERBB3".
- ^ Кусенс Л., Ян-Фэн Т.Л., Ляо Ю.К., Чен Э, Грей А., МакГрат Дж., Зеебург П.Х., Либерманн Т.А., Шлессингер Дж., Франк У. (1985). «Рецептор тирозинкиназы с обширной гомологией с рецептором EGF разделяет хромосомное положение с онкогеном neu». Наука. 230 (4730): 1132–9. Дои:10.1126 / science.2999974. PMID 2999974.
- ^ Прижент С.А., Лемуан Н.Р., Хьюз С.М., Пахарь Г.Д., Селден С., Гуллик В.Дж. (1992). «Экспрессия белка c-erbB-3 в нормальных тканях взрослого человека и плода». Онкоген. 7 (7): 1273–8. PMID 1377811.
- ^ Чо HS, Leahy DJ (2002). «Структура внеклеточной области HER3 обнаруживает междоменную связь». Наука. 297 (5585): 1330–3. Дои:10.1126 / science.1074611. PMID 12154198. S2CID 23069349.
- ^ а б c Роскоски Р. (2014). «Семейство протеин-тирозинкиназ и рака ErbB / HER». Pharmacol. Res. 79: 34–74. Дои:10.1016 / j.phrs.2013.11.002. PMID 24269963.
- ^ Carraway KL, Sliwkowski MX, Akita R, Platko JV, Guy PM, Nuijens A, Diamonti AJ, Vandlen RL, Cantley LC, Cerione RA (1994). «Продукт гена erbB3 является рецептором херегулина». J. Biol. Chem. 269 (19): 14303–6. PMID 8188716.
- ^ Каррауэй К.Л., Вебер Дж.Л., Унгер М.Дж., Ледесма Дж., Ю.Н., Гассманн М., Лай К. (1997). «Нейрегулин-2, новый лиганд тирозинкиназ рецептора ErbB3 / ErbB4». Природа. 387 (6632): 512–6. Дои:10.1038 / 387512a0. PMID 9168115. S2CID 4310136.
- ^ Ши Ф., Telesco SE, Лю Й., Радхакришнан Р., Леммон М.А. (2010). «Внутриклеточный домен ErbB3 / HER3 компетентен связывать АТФ и катализировать аутофосфорилирование». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 107 (17): 7692–7. Дои:10.1073 / pnas.1002753107. ЧВК 2867849. PMID 20351256.
- ^ Цахар Э., Уотерман Х., Чен Х, Левковиц Г., Карунагаран Д., Лави С., Рацкин Б.Дж., Ярден Й. (1996). «Иерархическая сеть межрецепторных взаимодействий определяет передачу сигнала с помощью фактора дифференцировки Neu / нейрегулина и эпидермального фактора роста». Мол. Клетка. Биол. 16 (10): 5276–87. Дои:10.1128 / MCB.16.10.5276. ЧВК 231527. PMID 8816440.
- ^ а б c Citri A, Skaria KB, Yarden Y (2003). «Глухонемым: биология ErbB-2 и ErbB-3». Exp. Cell Res. 284 (1): 54–65. Дои:10.1016 / с0014-4827 (02) 00101-5. PMID 12648465.
- ^ Пинкас-Крамарски Р., Ленферинк А.Е., Бакус С.С., Лясс Л., ван де Полл М.Л., Клаппер Л.Н., Цахар Э., Села М., ван Зоелен Е.Дж., Ярден Ю. (1998). «Онкогенный гетеродимер ErbB-2 / ErbB-3 является суррогатным рецептором эпидермального фактора роста и бетацеллюлина». Онкоген. 16 (10): 1249–58. Дои:10.1038 / sj.onc.1201642. PMID 9546426. S2CID 25652800.
- ^ Алиманди М., Ван Л. М., Боттаро Д., Ли С. К., Куо А., Франкель М., Феди П., Тан С., Липпман М., Пирс Дж. Х. (1997). «Эпидермальный фактор роста и бетацеллулин опосредуют передачу сигнала через совместно экспрессируемые рецепторы ErbB2 и ErbB3». EMBO J. 16 (18): 5608–17. Дои:10.1093 / emboj / 16.18.5608. ЧВК 1170193. PMID 9312020.
- ^ Приджент С.А., Гуллик В.Дж. (1994). «Идентификация сайтов связывания c-erbB-3 для фосфатидилинозитол 3'-киназы и SHC с использованием рецептора EGF / химеры c-erbB-3». EMBO J. 13 (12): 2831–41. Дои:10.1002 / j.1460-2075.1994.tb06577.x. ЧВК 395164. PMID 8026468.
- ^ Чжан К., Сунь Дж., Лю Н, Вэнь Д., Чанг Д., Томасон А., Йошинага С.К. (1996). «Трансформация клеток NIH 3T3 рецепторами HER3 или HER4 требует присутствия HER1 или HER2». J. Biol. Chem. 271 (7): 3884–90. Дои:10.1074 / jbc.271.7.3884. PMID 8632008. S2CID 7190224.
- ^ Холбро Т., Бирли Р.Р., Маурер Ф., Козичак М., Барбас К.Ф., Хайнс Н.Э. (2003). «Гетеродимер ErbB2 / ErbB3 функционирует как онкогенная единица: ErbB2 требует ErbB3, чтобы управлять пролиферацией клеток опухоли груди». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 100 (15): 8933–8. Дои:10.1073 / pnas.1537685100. ЧВК 166416. PMID 12853564.
- ^ Ван С., Хуанг Х, Ли СК, Лю Б. (2010). «Повышенная экспрессия erbB3 придает устойчивость к паклитакселу в клетках рака молочной железы, сверхэкспрессирующих erbB2, посредством позитивной регуляции сурвивина». Онкоген. 29 (29): 4225–36. Дои:10.1038 / onc.2010.180. PMID 20498641. S2CID 22169790.
- ^ Сергина Н.В., Рауш М., Ван Д., Блэр Дж., Ханн Б., Шокат К.М., Моассер М.М. (2007). «Избавление от терапии ингибиторами тирозинкиназы семейства HER с помощью неактивного киназы HER3». Природа. 445 (7126): 437–41. Дои:10.1038 / природа05474. ЧВК 3025857. PMID 17206155.
- ^ Осипо К., Мике К., Ченг Д., Вейхель А., Бертуччи А., Лю Х., Джордан В. К. (2007). «Роль HER2 / neu и HER3 в устойчивом к фулвестранту раке молочной железы». Int. Дж. Онкол. 30 (2): 509–20. Дои:10.3892 / ijo.30.2.509 (неактивно 12.10.2020). PMID 17203234.CS1 maint: DOI неактивен по состоянию на октябрь 2020 г. (связь)
- ^ Миллер Т.В., Перес-Торрес М., Нарасанна А., Гикс М., Стол О, Перес-Тенорио Г., Гонсалес-Ангуло А.М., Хеннесси Б.Т., Миллс ГБ, Кеннеди Дж.П., Линдсли К.В., Артеага К.Л. (2009). «Потеря гомолога фосфатазы и тензина, удаленного на хромосоме 10, вовлекает ErbB3 и передачу сигналов рецептора инсулиноподобного фактора роста-I, способствуя устойчивости к антиэстрогенам при раке груди». Рак Res. 69 (10): 4192–201. Дои:10.1158 / 0008-5472.CAN-09-0042. ЧВК 2724871. PMID 19435893.
- ^ Энгельман Дж. А., Зейнуллаху К., Мицудоми Т., Сонг Y, Хайленд К., Парк Дж. О., Линдеман Н., Гейл С. М., Чжао Х, Кристенсен Дж., Косака Т., Холмс А. Дж., Роджерс А. М., Каппуццо Ф., Мок Т., Ли К., Джонсон Б. Э. , Cantley LC, Jänne PA (2007). «Амплификация МЕТ приводит к устойчивости к гефитинибу при раке легких за счет активации передачи сигналов ERBB3». Наука. 316 (5827): 1039–43. Дои:10.1126 / science.1141478. PMID 17463250. S2CID 23254145.
- ^ Erjala K, Sundvall M, Junttila TT, Zhang N, Savisalo M, Mali P, Kulmala J, Pulkkinen J, Grenman R, Elenius K (2006). «Передача сигналов через ErbB2 и ErbB3 связана с резистентностью и амплификацией рецептора эпидермального фактора роста (EGFR) с чувствительностью к ингибитору EGFR гефитинибу в клетках плоскоклеточного рака головы и шеи». Clin. Рак Res. 12 (13): 4103–11. Дои:10.1158 / 1078-0432.CCR-05-2404. PMID 16818711. S2CID 5571305.
- ^ Чжан Ю., Линн Д., Лю З., Меламед Дж., Тавора Ф., Янг С.Й., Burger AM, Hamburger AW (2008). «EBP1, белок, связывающий ErbB3, снижается при раке простаты и участвует в резистентности к гормонам». Мол. Рак Ther. 7 (10): 3176–86. Дои:10.1158 / 1535-7163.MCT-08-0526. ЧВК 2629587. PMID 18852121.
- ^ Desbois-Mouthon C, Baron A, Blivet-Van Eggelpoël MJ, Fartoux L, Venot C, Bladt F, Housset C, Rosmorduc O (2009). «Ингибирование рецептора инсулиноподобного фактора роста-1 вызывает механизм резистентности через рецептор эпидермального фактора роста / путь передачи сигналов HER3 / AKT: рациональная основа для нацеливания на рецептор инсулиноподобного фактора роста-1 и рецептор эпидермального фактора роста при гепатоцеллюлярной карциноме». Clin. Рак Res. 15 (17): 5445–56. Дои:10.1158 / 1078-0432.CCR-08-2980. PMID 19706799. S2CID 207699374.
- ^ Kugel, C.H .; Hartsough, E.J .; Дэвис, М. А .; Сетиады, Ю.Ю .; Аплин, А. Э. (17 июля 2014 г.). «Функционально-блокирующие антитела ERBB3 ингибируют адаптивный ответ на ингибитор RAF». Журнал исследований рака. 74 (15): 4122–4132. Дои:10.1158 / 0008-5472.CAN-14-0464. ЧВК 4120074. PMID 25035390.
- ^ Ритмахер Д., Зонненберг-Ритмахер Э., Бринкманн В., Ямаи Т., Левин Г. Р., Берчмайер С. (1997). «Тяжелые невропатии у мышей с целевыми мутациями в рецепторе ErbB3». Природа. 389 (6652): 725–30. Дои:10.1038/39593. PMID 9338783. S2CID 28741273.
- ^ Britsch, S; Ли, Л; Кирхгоф, S; Тьюринг, F; Бринкманн, В; Берчмайер, С; Ритмахер, Д. (1998). «Рецепторы ErbB2 и ErbB3 и их лиганд, нейрегулин-1, необходимы для развития симпатической нервной системы». Гены и развитие. 12 (12): 1825–36. Дои:10.1101 / gad.12.12.1825. ЧВК 316903. PMID 9637684.
- ^ Дэвис AM (1998). «Выживание нейронов: ранняя зависимость от шванновских клеток». Curr. Биол. 8 (1): R15–8. Дои:10.1016 / s0960-9822 (98) 70009-0. PMID 9427620. S2CID 2745201.
дальнейшее чтение
- Корфас Дж., Рой К., Буксбаум Дж. Д. (2004). «Передача сигналов Neuregulin 1-erbB и молекулярные / клеточные основы шизофрении». Nat. Неврологи. 7 (6): 575–80. Дои:10.1038 / nn1258. PMID 15162166. S2CID 10692780.
- Пахарь Г.Д., Уитни Г.С., Нойбауэр М.Г. и др. (1990). «Молекулярное клонирование и экспрессия дополнительного гена, связанного с рецептором эпидермального фактора роста». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 87 (13): 4905–9. Дои:10.1073 / pnas.87.13.4905. ЧВК 54229. PMID 2164210.
- Краус М.Х., Иссинг В., Мики Т. и др. (1990). «Выделение и характеристика ERBB3, третьего члена семейства рецепторов ERBB / эпидермального фактора роста: доказательства сверхэкспрессии в подмножестве опухолей молочной железы человека». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 86 (23): 9193–7. Дои:10.1073 / пнас.86.23.9193. ЧВК 298460. PMID 2687875.
- Алиманди М., Романо А., Курия М.С. и др. (1995). «Кооперативная передача сигналов ErbB3 и ErbB2 при неопластической трансформации и карциномах молочной железы человека». Онкоген. 10 (9): 1813–21. PMID 7538656.
- Wallasch C, Weiss FU, Niederfellner G, et al. (1995). «Херегулин-зависимая регуляция онкогенной передачи сигналов HER2 / neu путем гетеродимеризации с HER3». EMBO J. 14 (17): 4267–75. Дои:10.1002 / j.1460-2075.1995.tb00101.x. ЧВК 394510. PMID 7556068.
- Хоран Т., Вен Дж., Аракава Т. и др. (1995). «Связывание фактора дифференцировки Neu с внеклеточным доменом Her2 и Her3». J. Biol. Chem. 270 (41): 24604–8. Дои:10.1074 / jbc.270.41.24604. PMID 7592681. S2CID 23576318.
- Shintani S, Funayama T, Yoshihama Y и др. (1995). «Прогностическое значение избыточной экспрессии ERBB3 при плоскоклеточном раке полости рта». Рак Lett. 95 (1–2): 79–83. Дои:10.1016 / 0304-3835 (95) 03866-У. PMID 7656248.
- Като М., Язаки Ю., Сугимура Т., Терада М. (1993). «Ген c-erbB3 кодирует секретируемую, а также трансмембранную рецепторную тирозинкиназу». Biochem. Биофиз. Res. Сообщество. 192 (3): 1189–97. Дои:10.1006 / bbrc.1993.1542. PMID 7685162.
- Кулуску Дж. М., Пахарь Г. Д., Карлтон Г. В. и др. (1993). «Характеристика фактора дифференцировки клеток рака груди, который специфически активирует рецептор HER4 / p180erbB4». J. Biol. Chem. 268 (25): 18407–10. PMID 7689552.
- Зелада-Хедман М., Верер Г., Коллинз П. и др. (1995). «Высокая экспрессия EGFR в фиброаденомах по сравнению с карциномами груди». Противораковый Res. 14 (5A): 1679–88. PMID 7847801.
- Shintani S, Funayama T, Yoshihama Y, et al. (1996). «Экспрессия продуктов гена семейства c-erbB при аденоидно-кистозной карциноме слюнных желез: иммуногистохимическое исследование». Противораковый Res. 15 (6B): 2623–6. PMID 8669836.
- Чанг Х., Ризе Д. Д., Гилберт В. и др. (1997). «Лиганды для рецепторов семейства ErbB, кодируемые нейрегулиноподобным геном». Природа. 387 (6632): 509–12. Дои:10.1038 / 387509a0. PMID 9168114. S2CID 4359654.
- Фиддес Р.Дж., Кэмпбелл Д.Х., Джейн П.В. и др. (1998). «Анализ рекрутирования Grb7 с помощью рецепторов erbB, активируемых герегулином, показывает новую селективность в отношении erbB3». J. Biol. Chem. 273 (13): 7717–24. Дои:10.1074 / jbc.273.13.7717. PMID 9516479. S2CID 22017882.
- Джонс Дж. Т., Баллинджер М. Д., Писакан П. И. и др. (1998). «Связывающее взаимодействие домена egf герегулин-бета с рецепторами ErbB3 и ErbB4, оцениваемое с помощью мутагенеза аланинового сканирования». J. Biol. Chem. 273 (19): 11667–74. Дои:10.1074 / jbc.273.19.11667. PMID 9565587. S2CID 42404398.
- Ли Х, Майл Нью-Джерси (1998). «Выделение и характеристика четырех альтернативных транскриптов c-erbB3, экспрессированных в клеточных линиях, происходящих от карциномы яичников, и в нормальных тканях человека». Онкоген. 16 (25): 3243–52. Дои:10.1038 / sj.onc.1201866. PMID 9681822. S2CID 9785761.
- Виджапуркар У, Ченг К., Коланд Дж. Г. (1998). «Мутация тирозинового остатка сайта связывания Shc в ErbB3 / HER3 блокирует херегулин-зависимую активацию митоген-активируемой протеинкиназы». J. Biol. Chem. 273 (33): 20996–1002. Дои:10.1074 / jbc.273.33.20996. PMID 9694850. S2CID 9469356.
- Ю Джи, Гамбург А.В. (1999). «Взаимодействие белка p23 / p198 с ErbB-3». Ген. 229 (1–2): 215–21. Дои:10.1016 / S0378-1119 (98) 00604-0. PMID 10095121.
- Лин Дж., Адам Р.М., Сантистеван Э., Фриман М.Р. (1999). «Путь фосфатидилинозитол-3'-киназы представляет собой путь выживания клеток, активируемых доминирующим фактором роста, в клетках карциномы предстательной железы человека LNCaP». Рак Res. 59 (12): 2891–7. PMID 10383151.