Сигнальный путь ежа - Hedgehog signaling pathway
| Белковый ёжик | |||||||
|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||
| Организм | |||||||
| Символ | чч | ||||||
| UniProt | Q02936 | ||||||
| |||||||
| Сигнал Hedge N-terminal | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| Символ | HH_signal | ||||||||
| Pfam | PF01085 | ||||||||
| ИнтерПро | IPR000320 | ||||||||
| CATH | 3д1м | ||||||||
| SCOP2 | 3д1м / Объем / СУПФАМ | ||||||||
| |||||||||
| Смотрите также ИнтерПро: IPR001657. | |||||||||
В Сигнальный путь ежа это сигнальный путь который передает информацию эмбриональный ячейки, необходимые для правильного дифференциация клеток. Различные части эмбриона имеют разные концентрации сигнальных белков hedgehog. Путь также играет роль у взрослого. Заболевания, связанные с нарушением работы этого пути, включают: базально-клеточная карцинома.[1]
Сигнальный путь Hedgehog является одним из ключевых регуляторов развития животных и присутствует во всех билатерии.[2] Путь получил свое название от полипептид лиганд, внутриклеточная сигнальная молекула под названием Hedgehog (Чч) обнаружен у плодовых мушек рода Дрозофила; личинка плодовой мухи, лишенная Чч Говорят, что ген похож на ежики. Чч один из дрозофилов ген сегментной полярности продукты, участвующие в создании основы мухи план тела. Личинки без Чч короткие и колючие, напоминающие ежа. Молекула остается важной на более поздних стадиях эмбриогенез и метаморфоза.
У млекопитающих есть три гомолога Hedgehog, Пустыня (DHH), Индийский (IHH), и Соник (SHH), из которых Соник изучен лучше всего. Этот путь не менее важен во время эмбрионального развития позвоночных и поэтому представляет интерес для эволюционная биология развития. В нокаутные мыши без компонентов пути, мозг, скелет, мускулатура, желудочно-кишечный тракт и легкие не развиваются правильно. Недавние исследования указывают на роль передачи сигналов Hedgehog в регуляции взрослые стволовые клетки участвует в поддержании и восстановлении взрослых ткани. Этот путь также участвовал в развитии некоторых раки. Лекарства, которые специально нацелены на передачу сигналов Hedgehog для борьбы с этим заболеванием, активно разрабатываются рядом ученых. Фармацевтические компании.
Открытие

В 1970-х годах фундаментальная проблема в биология развития было понять, как относительно простое яйцо может привести к сложному сегментированный план тела. В конце 1970-х Кристиан Нюсслейн-Фольхард и Эрик Вишаус изолированные мутации в генах, контролирующих развитие сегментированной передне-задней оси тела мухи;[3] их метод «насыщающего мутагенеза» привел к открытию группы генов, участвующих в развитии сегментация тела, помогая основать сферу эволюционная биология развития.[4] В 1995 году они разделили Нобелевская премия с Эдвард Б. Льюис за их работу по изучению генетических мутаций в Дрозофила эмбриогенез.[5]
В Дрозофила Ежик (чч) был идентифицирован как один из нескольких генов, важных для создания различий между передней и задней частями отдельных сегментов тела. Муха чч ген был независимо клонирован в 1992 году лабораториями Джима Молера, Филип Бичи, Томас Б. Корнберг и Сайго Каору. Некоторые мутанты ежа приводят к появлению эмбрионов аномальной формы, которые необычно короткие и короткие по сравнению с дикого типа эмбрионы. Функция гена полярности сегментов ежа изучалась с точки зрения его влияния на нормально поляризованное распределение кутикулы личинок. зубчики а также особенности на придатках взрослых, таких как ноги и усики.[6] Мутантные личинки ежа имеют тенденцию к "твердым лужайкам" зубчиков, а не к нормальному типу зубчиков (рис. 1). Появление коротеньких и «волосатых» личинок вдохновило на название 'Ежик '.
Плодовая муха


Механизм
Клетки насекомых выражают полный размер цинковый палец фактор транскрипции Кубитус прерывистый (Ci), который образует комплекс с кинезин -подобный белок Costal-2 (Cos2) и локализуется в цитоплазме, связанном с клеточными микротрубочки (Фигура 2). В СКФ комплекс нацелен на белок Ci полной длины 155 кДа для протеосома -зависимое расщепление, которое генерирует фрагмент 75 кДа (CiR). CiR накапливается в клетке и распространяется в ядро, где он действует как со-репрессор для Ежика (Чч) гены-мишени.[7] Шаги, ведущие к белку Ci протеолиз включают фосфорилирование белка Ci несколькими протеинкиназы; PKA, GSK3β и CK1 (Фигура 2).[8] В Дрозофила протеин Slimb является частью СКФ комплекс который нацелен на белки для убиквитилирование. Slimb связывается с фосфорилированный Ci-белок.
В отсутствие Hh (рис. 3) трансмембранный белок клеточной поверхности, называемый Исправлено (PTCH) предотвращает высокую экспрессию и активность 7 мембранный рецептор[9] называется Сглаженный (SMO). Patched имеет сходство последовательности с известными белками мембранного транспорта. Когда присутствует внеклеточный Hh (рис. 3), он связывается с Patched и ингибирует его, позволяя Smoothened накапливать и ингибировать протеолитическое расщепление белка Ci. Этот процесс, скорее всего, включает прямое взаимодействие Smoothened и Costal-2 и может включать секвестрацию комплекса, содержащего белок Ci, в микродомен, где нарушаются этапы, ведущие к протеолизу белка Ci.[7] Механизм, с помощью которого связывание Hh с Patched приводит к увеличению уровней Smoothened, неясен (шаг 1 на рисунке 3). После связывания Hh с Patched уровни Smoothened значительно увеличиваются по сравнению с уровнем, поддерживаемым в клетках, когда Patched не связан с Hh.[10] Было высказано предположение, что фосфорилирование Smoothened играет роль в Hh-зависимой регуляции уровней Smoothened.[11]
В клетках с Hh-активированным патчем (рис. 3) интактный белок Ci накапливается в цитоплазме клетки, и уровни CiR снижаются, что позволяет транскрипции некоторых генов, таких как декапентаплегический (dpp, член BMP семейство факторов роста). Для других Hh-регулируемых генов экспрессия требует не только потери CiR, но также положительного действия нерасщепленного Ci, чтобы действовать как активатор транскрипции.[8] Costal-2 обычно важен для удержания Ci-белка в цитоплазме, но взаимодействие Smoothened с Costal-2 позволяет некоторому интактному Ci-белку попасть в ядро. В Дрозофила Слитый белок (Fu на рисунке 3) представляет собой протеинкиназу, которая связывается с Costal-2. Fused может ингибировать Suppressor of Fused (SUFU), который, в свою очередь, взаимодействует с Ci для регулирования транскрипции гена в некоторых типах клеток.[12]
Роль
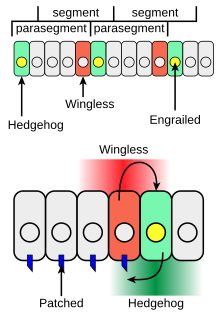
Еж играет роль в развитии сегмента тела личинки и в формировании взрослых придатков. При формировании сегментов тела в развивающихся Дрозофила эмбрион, полосы клеток, которые синтезируют фактор транскрипции закрепленный может также экспрессировать межклеточный сигнальный белок Hedgehog (зеленый на рисунке 4). Еж не может свободно перемещаться очень далеко от клеток, которые его образуют, поэтому он активирует только тонкую полоску клеток, прилегающих к клеткам, экспрессирующим заживление. Действуя в этой местной манере, ёжик работает как паракринный фактор. Только клетки с одной стороны от клеток, экспрессирующих engrailed, компетентны отвечать на Hedgehog после взаимодействия Hh с рецепторным белком Patched (синий на фиг. 4).
Клетки с Hh-активированным Patched рецептором синтезируют Бескрылый белок (красный на рисунке 4). Если Дрозофила эмбрион изменяется так, чтобы продуцировать Hh во всех клетках, все компетентные клетки отвечают и образуют более широкую полосу экспрессирующих Wingless клеток в каждом сегменте. В бескрылый ген имеет вышележащую регуляторную область транскрипции, которая связывает фактор транскрипции Ci Hh-зависимым образом, что приводит к увеличению бескрылый транскрипция (взаимодействие 2 на фиг. 3) в полосе клеток, прилегающих к полосе продуцирующих Hh клеток.[13]
Белок Wingless действует как внеклеточный сигнал и формирует структуру соседних рядов клеток, активируя свой рецептор на клеточной поверхности. Завитые. Wingless действует на клетки, экспрессирующие engrailed, для стабилизации полосок экспрессии engrailed. Бескрылый является членом Wnt семейство сигнальных белков от клетки к клетке. Взаимная передача сигналов с помощью Hedgehog и Wingless стабилизирует границу между парасегментами (Рис. 4, вверху). Воздействие Wingless и Hedgehog на другие полосы клеток в каждом сегменте устанавливает позиционный код, который учитывает различные анатомические особенности вдоль передне-задней оси сегментов.[14]
Белок Wingless называют «бескрылым» из-за фенотип некоторых бескрылый летают мутанты. Бескрылый и Ежик действуют вместе во время метаморфоза координировать формирование крыла. Ёжик выражен в задней части развивающейся Дрозофила конечности. Ежик также участвует в координации развития глаз, мозга, гонад, кишечника и трахеи. Подавление активности hedgehog приводит к снижению развития глаз у амфипод. Гаммарус минус.[15]
Аннелиды
Ежик также участвует в сегментации кольчатых червей; потому что параллельная эволюция кажется маловероятным, это предполагает общее происхождение сегментации между двумя типами.[16] Хотя Hh не вызывает образования сегментов, он, по-видимому, стабилизирует сегментированные поля после их появления.[16]
Позвоночные
Механизм

Соник ежик (SHH) является наиболее изученным лигандом пути позвоночных. Большая часть того, что известно о передаче сигналов hedgehog, было установлено путем изучения SHH. это переведено в качестве предшественника ~ 45 кДа и подвергается автокаталитический обработки (процесс "1" на рисунке 5) для получения ~ 20 кДа N-концевой сигнальный домен (называемый SHH-N) и ~ 25 кДа C-терминал домен без известной сигнальной роли. Во время спайности холестерин молекула добавляется к карбоксил конец N-концевого домена,[17] который участвует в передаче, секреции и рецепторном взаимодействии лиганда. SHH может сигнализировать в автокринный мода, влияя на клетки, в которых он производится. Секреция и как следствие паракринный Передача сигналов hedgehog требует участия белка Dispatched (DISP) (процесс «2» на фиг. 5).
Когда SHH достигает своей целевой ячейки, он связывается с Исправлено-1 (PTCH1) рецептор (процесс «3» на фиг. 5, синяя молекула). В отсутствие лиганда PTCH1 ингибирует Сглаженный (SMO), нижестоящий белок в пути (процесс «4»). Было высказано предположение, что SMO регулируется небольшой молекулой, клеточная локализация которой контролируется PTCH.[18] ПТЧ1 имеет гомология к Ниманн-Пик заболевание, тип С1 (NPC1 ), который, как известно, транспортирует липофильный молекулы через мембрану.[19] PTCH1 имеет стерол Sensing domain (SSD), который, как было показано, необходим для подавления активности SMO.[20] Текущая теория предполагает, что PTCH регулирует SMO, удаляя оксистерины от СМО. PTCH действует как стериновый насос и удаляет оксистерины, которые были созданы 7-дегидрохолестерин редуктаза.[21] После связывания белка Hh или мутации в SSD PTCH насос выключается, позволяя оксистеринам накапливаться вокруг SMO.

Такое накопление стеролов позволяет SMO активизироваться или оставаться на мембране в течение более длительного периода времени. Эта гипотеза подтверждается существованием ряда небольших молекул. агонисты и антагонисты пути, которые действуют на SMO. Связывание SHH снимает ингибирование SMO, что приводит к активации GLI. факторы транскрипции (Процесс «5»): активаторы Gli1 и Gli2 и репрессор Gli3. Последовательность молекулярных событий, которые связывают SMO с GLI, плохо изучена. Активированный GLI накапливается в ядре (процесс «6») и контролирует транскрипцию генов-мишеней hedgehog (процесс «7»). Недавно сообщалось, что PTCH1 подавляет транскрипцию генов-мишеней hedgehog посредством механизма, независимого от Сглаженный.[22]
Помимо PTCH1, у млекопитающих есть еще один рецептор hedgehog, PTCH2, который идентичность последовательности с ПТЧ1 - 54%.[23] Все три ежа млекопитающих связывают оба рецептора одинаково. близость, поэтому PTCH1 и PTCH2 не могут различать лиганды. Однако они различаются по своим образцам экспрессии. PTCH2 экспрессируется на гораздо более высоких уровнях в яички и передает там сигналы ежа пустыни.[23] По-видимому, он играет отличную от PTCH1 роль передачи сигналов ниже по течению. В отсутствие лиганд Связывание PTCH2 имеет пониженную способность подавлять активность SMO.[24] Более того, чрезмерное выражение PTCH2 не заменяет мутировавший PTCH1 в базально-клеточная карцинома.[25]
У беспозвоночных, как и у Дрозофила, связывание Hedgehog с PTCH приводит к интернализация и секвестрация лиганда.[26] Как следствие, in vivo прохождение ежа над восприимчивым полем, которое экспрессирует рецептор, приводит к ослаблению сигнала, эффект, называемый лиганд-зависимым антагонизм (LDA). В отличие от Дрозофила, позвоночные обладают другим уровнем регуляции hedgehog посредством LDA, опосредованного Hh-взаимодействующим белком 1 (HHIP1). HHIP1 также изолирует лиганды hedgehog, но, в отличие от PTCH, он не влияет на активность SMO.[27]
Роль

Члены семейства ежей играют ключевую роль в самых разных процессах развития.[14] Один из наиболее изученных примеров - действие Соник ежик во время развития конечности позвоночного. Классические эксперименты Сондерса и Гасселинга в 1968 году по развитию зачатка куриных конечностей легли в основу морфоген концепция. Они показали, что идентичность пальцев на конечности цыпленка определялась диффузный фактор, произведенный зона поляризующей активности (ZPA), небольшой участок ткани на задний край конечности. Оказалось, что развитие млекопитающих происходит по той же схеме. Позднее было показано, что этот фактор диффузии Соник ежик. Однако до недавнего времени оставалось неясным, как SHH определяет цифровую идентичность. Текущая модель, предложенная Харфом и другие.,[28] утверждает, что как концентрация, так и время воздействия SHH определяют, в какой палец будет развиваться ткань в мышь эмбрион (рисунок 6).
Цифры V, IV и часть III возникают непосредственно из клеток, которые экспрессируют SHH во время эмбриогенез. В этих клетках сигналы SHH в автокринный моды, и эти пальцы развиваются правильно в отсутствие DISP, который необходим для внеклеточной диффузии лиганда. Эти цифры различаются продолжительностью времени, в течение которого SHH продолжает отображаться. Самый задний палец V развивается из клеток, которые экспрессируют лиганд в течение самого длительного периода времени. Клетки IV пальца экспрессируют SHH в течение более короткого времени, а клетки III пальца еще короче. Цифра II развивается из клеток, которые подвергаются умеренным концентрациям внеклеточного SHH. Наконец, для разработки Digit I не требуется SHH. В каком-то смысле это стандартная программа для клеток зачатка конечностей.
Передача сигналов Hedgehog остается важной для взрослых. Соник ежик было показано, что способствует распространению взрослые стволовые клетки из различных тканей, в том числе примитивных кроветворный клетки[29] молочная железа[30] и нейронные[31] стволовые клетки. Активация ежового пути необходима для перехода волосяной фолликул от состояния покоя до фазы роста.[32]Это не удалось из-за токсичности, обнаруженной на животных моделях.[33]
Болезнь человека
Нарушение передачи сигналов hedgehog во время эмбрионального развития из-за вредной мутации или потребления тератогены беременной матерью, может привести к серьезным отклонениям в развитии. Голопрозэнцефалия, отказ эмбрионального передний мозг делиться с образованием полушарий головного мозга, происходит примерно у 1 из 8000 живорождений и примерно у 1 из 200 самопроизвольных абортов у людей и обычно связано с мутациями в генах, участвующих в пути ежа, включая SHH и ПТЧ.[34] Циклопия, один из самых серьезных дефектов голопрозэнцефалия, возникает, если ингибитор пути циклопамин потребляется беременными млекопитающими.[35]
Активация пути hedgehog вовлечена в развитие раки в различных органах, в том числе мозг, легкое, молочная железа, предстательная железа и кожа. Базально-клеточная карцинома, наиболее распространенная форма рака злокачественная опухоль, имеет наиболее тесную связь с передачей сигналов hedgehog. Мутации с потерей функции в Исправлено и активируя мутации в Сглаженный были выявлены у пациентов с этим заболеванием.[36] Аномальная активация пути, вероятно, приводит к развитию болезни через трансформацию взрослые стволовые клетки в раковые стволовые клетки которые вызывают опухоль. Исследователи рака надеются, что специфические ингибиторы передачи сигналов hedgehog обеспечат эффективное лечение широкого спектра злокачественных новообразований.[37] Связь между сигнальным путем hedgehog и развитием рака очень сложна. Тем не менее ясно, что аберрантная активация передачи сигналов hedgehog ведет к росту, пролиферации и инвазии опухолевых клеток.[38]
Ориентация на путь ежа
Наиболее распространенный способ воздействия на этот путь - модулирование SMO. Антагонист и агонист SMO, как уже было показано, влияют на регуляцию пути ниже по течению. Для лечения рака доступно несколько ингибиторов сигнального пути hedgehog, таких как висмодегиб и сонидегиб. Эти препараты считаются многообещающими методами лечения рака, особенно для пациентов с резистентным / запущенным раком. Ингибиторы SMO представляют собой потенциальное средство лечения некоторых видов рака. Однако из-за вредных и потенциально токсичных побочных эффектов ингибиторов SMO ингибиторов SMO, неопределенной безопасности у детей и доказательств того, что у некоторых пациентов развивается устойчивость к ингибиторам SMO, необходимы новые классы лекарств.[38]Наиболее клинически продвинутыми агентами таргетинга SMO являются: циклопамин -конкурентный. Итраконазол (Sporanox ) также было показано, как воздействовать на SMO с помощью механизма, отличного от циклопамин и висмодегиб.[39] Итраконазол (ITZ) ингибирует SMO при наличии мутаций, придающих устойчивость к висмодегиб и другие циклопамин -конкурентные антагонисты, например IPI-926 и LDE-225 компании Novartis.[40] ПТЧ[41] и Gli3 (5E1)[42] антитела также являются способом регулирования этого пути. Нижестоящий эффектор и сильный активатор транскрипции siRNA Gli1 использовались для подавления роста клеток и стимулирования апоптоза.[43] Триоксид мышьяка (Trisenox ) также было показано, что ингибирует передачу сигналов hedgehog, нарушая функцию и транскрипцию Gli.[44][45]
Было идентифицировано несколько экологических модификаторов передачи сигналов Hedgehog, которые представляют потенциальную опасность для здоровья или развития. Диетические алкалоиды, содержащиеся в помидорах (томатодин),[46] картофель (соланидин),[46] пасленовые, такие как перец и баклажаны (соласодин).[46] и куркума (куркумин)[47] было показано, что они противодействуют SMO и нарушают передачу сигналов Hedgehog. Кроме того, некоторые токсиканты окружающей среды могут блокировать передачу сигналов Hedgehog. Пиперонил бутоксид (PBO) - это полусинтетическая пестицидная добавка, разработанная в 1940-х годах, которую можно найти в тысячах домашних и сельскохозяйственных продуктов.[48] Несмотря на его широкое использование, способность PBO ингибировать передачу сигналов hedgehog и действовать как мощный тератоген развития не была признана до недавнего времени.[49][50]
Метастаз
Активация пути Hedgehog приводит к увеличению экспрессии белка Snail и снижению E-кадгерин и узкие стыки.[51]
Регулирование опухоли
Активация пути Hedgehog приводит к увеличению ангиогенных факторов (ангиопоэтин-1 и ангиопоэтин-2),[52] Циклины (циклин D1 и B1),[53] антиапоптотические гены и снижение апоптотических генов (Fas).[54]
Клинические испытания
- Висмодегиб[55] FDA одобрило (январь 2012 г.) для базально-клеточная карцинома.
- Sonidegib Одобрено FDA (июль 2015 г.) для базально-клеточная карцинома.
- Итраконазол[56]
Эволюция

Ланцетник, которые примитивны хордовые, обладают только одним гомологом Дрозофила Чч (рисунок 7). У позвоночных, с другой стороны, есть несколько лигандов Hedgehog, которые попадают в три подгруппы: Пустыня, Индийский и Соник, каждый из которых представлен одним геном млекопитающего. Это следствие двух раундов дупликации всего генома, которые произошли на ранних этапах эволюции позвоночных.[57] Два таких события дали бы четыре гомологичных гена, один из которых, должно быть, был утерян. Пустынные ежи наиболее близки к Дрозофила Чч. Дополнительные дупликации генов произошли у некоторых видов[14] такой как данио Данио Рерио, который имеет дополнительный ежик ген в звуковой группа. Различные линии позвоночных адаптировали ежей к уникальным процессам развития. Например, гомолог X.laevis полосатый ёжик участвует в регенерации саламандра конечность.[58]
тсс претерпела ускоренную эволюцию в линии приматов, ведущей к человеку.[59] Дорус и другие. Предполагается, что это позволило более комплексно регулировать белок и, возможно, сыграло роль в увеличении объема и сложности человеческого мозга.
Кудрявая семья WNT рецепторы имеют некоторое сходство последовательности с Сглаженный.[60] Сглаженный, кажется, функционально расходящийся член Рецептор, связанный с G-белком (GPCR) суперсемейство. Были рассмотрены другие сходства между сигнальными путями WNT и Hh.[61] Нусс заметил, что «сигнальная система, основанная на липидно-модифицированных белках и специфических мембранных транслокаторах, является древней и, возможно, была основателем сигнальных систем Wnt и Hh».
Было высказано предположение, что передача сигналов беспозвоночных и позвоночных ниже по течению от Smoothened значительно разошлась.[62] Роль супрессора слияния (SUFU) у позвоночных повышена по сравнению с Дрозофила где его роль относительно невелика. Costal-2 особенно важен в Дрозофила. Слитая протеинкиназа является регулятором SUFU в Дрозофила, но может не играть роли в пути Hh позвоночных.[63] У позвоночных передача сигналов Hh в значительной степени вовлечена в развитие реснички.[64]
В семействе белков Hedgehog наблюдается поразительная эволюция на уровне домена, N-концевой домен (Hedge) и C-концевой домен (Hog), которые позже были объединены в единую транскрипционную единицу.[65][66] Домен Hog содержит последовательность, называемую Hint (Hedgehog INTein), которая по последовательности и функциям аналогична бактериальной и грибковой. интеины.[67] Домен Hog присутствует во многих эукариотических ветвях, то есть красных водорослях, мхах, динофлагеллятах, якобидах и других одноклеточных эуркариотах.[68] Хоанофлагелляты содержат ген под названием hoglet, который также кодирует Hog-домен C-концевого домена hedgehog. Однако у Choanoflagellates и низших эукариот нет регионов, подобных хедж-домену, что позволяет предположить, что свиньи эволюционировали первыми.[67][68] Poriferans имеют как хедж-подобные белки (называемые хеджирующими), так и свиноподобные белки, но они существуют как две полностью отдельные транскрипционные единицы.[65][66] Книдарианцы содержат гены hedgling и hog, но также имеют полный ген hedgehog, что указывает на то, что hedge и hog были соединены в hedgehog после последнего общего предка poriferans и cnidarians.[66]
Bilaterians не содержат гены хеджирования, что позволяет предположить, что они были потеряны в результате делеции до того, как эта ветвь отделилась от других многоклеточных животных.[2] Однако гены, содержащие домен Hog, без домена Hedge присутствуют в нескольких билатериальных клонах. Они находятся в Лофотрохозоа и Нематода.[69] Hedgehog-подобные гены, 2 патченных гомолога и патч-родственные гены существуют у червя C. elegans.[70][71] Было показано, что эти гены кодируют белки, которые играют роль в C. elegans разработка.[70][71] Пока Enoplea нематоды сохранили настоящего Ежика, Хромадорейцы потеряли архетипического Hedgehog и вместо этого развили расширенный репертуар из 61 дивергентного полуортологичного гена с новыми N-концевыми доменами, ассоциированными с Hog.[68][69] Эти N-концевые домены, ассоциированные с Hog в C. elegans впоследствии были классифицированы, сначала бородавочник (WRT) и сурок (GRD), затем наземный (GRL) и куахог (QUA).[70][71] C. elegansвместе с другими видами нематод потеряли GPCR Smoothened.[70][71]
Смотрите также
- Соник ежик, наиболее изученный лиганд позвоночного пути
- Сглаженный консервированные GPCR компонент пути
- Netpath - Кураторский ресурс путей передачи сигналов у людей
- Ингибиторы передачи сигналов Hh
- Циклопамин, встречающаяся в природе небольшая молекула
- Sonidegib
- Висмодегиб, утвержден для базально-клеточная карцинома.
Рекомендации
- ^ Страницы биологии Кимбалла В архиве 26 июня 2008 г. Wayback Machine, Сигнальный путь ежа[самостоятельно опубликованный источник? ]
- ^ а б Ингам П. У., Накано Ю., Сегер С. (июнь 2011 г.). «Механизмы и функции передачи сигналов Hedgehog через метазоа». Природа Обзоры Генетика. 12 (6): 393–406. Дои:10.1038 / nrg2984. PMID 21502959.
- ^ Нюсслейн-Фольхард C, Wieschaus E (октябрь 1980 г.). «Мутации, влияющие на количество сегментов и полярность у дрозофилы». Природа. 287 (5785): 795–801. Дои:10.1038 / 287795a0. PMID 6776413.
- ^ Артур В (февраль 2002 г.). «Новые концептуальные основы эволюционной биологии развития». Природа. 415 (6873): 757–64. Дои:10.1038 / 415757a. PMID 11845200.
- ^ Нобелевская премия 1995 г. за открытие генетический контроль раннего эмбрионального развития
- ^ Молер Дж (декабрь 1988 г.). «Требования к гену сегментарной полярности hedgehog в формировании паттерна кутикулы личинок и взрослых особей дрозофилы». Генетика. 120 (4): 1061–72. ЧВК 1203569. PMID 3147217.
- ^ а б Коллинз Р.Т., Коэн С.М. (май 2005 г.). «Генетический скрининг дрозофилы для выявления новых компонентов сигнального пути hedgehog». Генетика. 170 (1): 173–84. Дои:10.1534 / генетика.104.039420. ЧВК 1449730. PMID 15744048.
- ^ а б Лум Л., Бичи, штат Пенсильвания (июнь 2004 г.). «Сеть ответа Hedgehog: датчики, коммутаторы, маршрутизаторы». Наука. 304 (5678): 1755–9. CiteSeerX 10.1.1.476.3902. Дои:10.1126 / science.1098020. PMID 15205520.
- ^ Чен В., Рен XR, Нельсон С.Д., Барак Л.С., Чен Дж.К., Бичи П.А., де Соваж Ф., Лефковиц Р.Дж. (декабрь 2004 г.). «Зависимая от активности интернализация сглаженного, опосредованная бета-аррестином 2 и GRK2». Наука. 306 (5705): 2257–60. Дои:10.1126 / science.1104135. PMID 15618519.
- ^ Альседо Дж., Цзоу Й., Нолл М. (август 2000 г.). «Посттранскрипционная регуляция сглаживания является частью механизма самокоррекции в сигнальной системе Hedgehog». Молекулярная клетка. 6 (2): 457–65. Дои:10.1016 / S1097-2765 (00) 00044-7. PMID 10983991.
- ^ Апионишев С., Катанаева Н.М., Маркс С.А., Кальдерон Д., Томлинсон А. (январь 2005 г.).«Drosophila сглаживает сайты фосфорилирования, необходимые для передачи сигнала Hedgehog». Природа клеточной биологии. 7 (1): 86–92. Дои:10.1038 / ncb1210. PMID 15592457.
- ^ Хо К.С., Суяма К., Фиш М., Скотт М.П. (март 2005 г.). «Дифференциальная регуляция транскрипции гена-мишени Hedgehog с помощью Costal2 и супрессора Fused». Разработка. 132 (6): 1401–12. Дои:10.1242 / dev.01689. PMID 15750186.
- ^ Фон Олен Т., Лессинг Д., Нусс Р., Хупер Дж. Э. (март 1997 г.). «Передача сигналов Hedgehog регулирует транскрипцию через cubitus interruptus, специфичный для последовательности ДНК-связывающий белок». Труды Национальной академии наук Соединенных Штатов Америки. 94 (6): 2404–9. Дои:10.1073 / пнас.94.6.2404. ЧВК 20100. PMID 9122207.
- ^ а б c Ingham PW, McMahon AP (декабрь 2001 г.). «Передача сигналов ежа в развитии животных: парадигмы и принципы». Гены и развитие. 15 (23): 3059–87. Дои:10.1101 / gad.938601. PMID 11731473.
- ^ Aspiras AC, Prasad R, Fong DW, Carlini DB, Angelini DR (май 2012 г.). «Параллельное снижение экспрессии гена развития глаз hedgehog в отдельно взятых пещерных популяциях амфиподы Gammarus minus». Журнал эволюционной биологии. 25 (5): 995–1001. Дои:10.1111 / j.1420-9101.2012.02481.x. PMID 22462461.
- ^ а б Dray N, Tessmar-Raible K, Le Gouar M, Vibert L, Christodoulou F, Schipany K, Guillou A, Zantke J, Snyman H, Béhague J, Vervoort M, Arendt D, Balavoine G (июль 2010 г.). «Передача сигналов Hedgehog регулирует формирование сегментов у кольчатых червей Platynereis». Наука. 329 (5989): 339–42. Дои:10.1126 / science.1188913. ЧВК 3182550. PMID 20647470.
- ^ Банавали Н.К. (ноябрь 2019 г.). «Механизм модификации холестерина лиганда Hedgehog». Журнал вычислительной химии. 41: 520–527. Дои:10.1002 / jcc.26097.
- ^ Тайпале Дж., Купер М.К., Маити Т., Бичи, Пенсильвания (август 2002 г.). «Patched действует каталитически, подавляя активность Smoothened». Природа. 418 (6900): 892–7. Дои:10.1038 / природа00989. PMID 12192414.
- ^ Дэвис Дж. П., Чен Ф. В., Иоанну Ю. А. (декабрь 2000 г.). «Трансмембранная молекулярная насосная активность белка Ниманна-Пика C1». Наука. 290 (5500): 2295–8. Дои:10.1126 / science.290.5500.2295. PMID 11125140.
- ^ Стратт Х., Томас С., Накано Й., Старк Д., Нив Б., Тейлор А.М., Ингхэм П.В. (апрель 2001 г.). «Мутации в чувствительном к стеролам домене Patched предполагают роль везикулярного транспорта в регуляции Smoothened». Текущая биология. 11 (8): 608–13. Дои:10.1016 / S0960-9822 (01) 00179-8. PMID 11369206.
- ^ Коркоран РБ, Скотт депутат (май 2006 г.). «Оксистерины стимулируют передачу сигнала Sonic hedgehog и пролиферацию клеток медуллобластомы». Труды Национальной академии наук Соединенных Штатов Америки. 103 (22): 8408–13. Дои:10.1073 / pnas.0602852103. ЧВК 1462959. PMID 16707575.
- ^ Рахнама Ф., Симокава Т., Лаут М., Финта С., Когерман П., Теглунд С., Тофтгард Р., Зафиропулос П. Г. (февраль 2006 г.). «Ингибирование активации гена GLI1 с помощью Patched1». Биохимический журнал. 394 (Pt 1): 19–26. Дои:10.1042 / BJ20050941. ЧВК 1385998. PMID 16229683.
- ^ а б Карпентер Д., Стоун Д.М., Кисть Дж., Райан А., Арманини М., Франц Г., Розенталь А., де Соваж Ф.Дж. (ноябрь 1998 г.). «Характеристика двух запатентованных рецепторов семейства белков hedgehog позвоночных». Труды Национальной академии наук Соединенных Штатов Америки. 95 (23): 13630–4. Дои:10.1073 / пнас.95.23.13630. ЧВК 24870. PMID 9811851.
- ^ Рахнама Ф., Тофтгорд Р., Зафиропулос П. Г. (март 2004 г.). «Отличительные роли вариантов сплайсинга PTCH2 в передаче сигналов Hedgehog». Биохимический журнал. 378 (Pt 2): 325–34. Дои:10.1042 / BJ20031200. ЧВК 1223965. PMID 14613484.
- ^ Зафиропулос П.Г., Унден А.Б., Рахнама Ф., Холлингсворт Р.Э., Тофтгорд Р. (февраль 1999 г.). «PTCH2, новый человеческий патчированный ген, который подвергается альтернативному сплайсингу и активируется в базально-клеточных карциномах». Исследования рака. 59 (4): 787–92. PMID 10029063.
- ^ Инкардона Дж. П., Ли Дж. Х., Робертсон С. П., Энга К., Капур Р. П., Ролинк Х. (октябрь 2000 г.). «Рецептор-опосредованный эндоцитоз растворимого и связанного с мембраной Sonic hedgehog by Patched-1». Труды Национальной академии наук Соединенных Штатов Америки. 97 (22): 12044–9. Дои:10.1073 / pnas.220251997. ЧВК 17291. PMID 11027307.
- ^ Jeong J, McMahon AP (январь 2005 г.). «Рост и структура нервной трубки млекопитающих регулируются частично перекрывающейся обратной связью антагонистов hedgehog patchched 1 и Hhip1». Разработка. 132 (1): 143–54. Дои:10.1242 / dev.01566. PMID 15576403.
- ^ Harfe BD, Scherz PJ, Nissim S, Tian H, McMahon AP, Tabin CJ (август 2004 г.). «Доказательства наличия временного градиента Shh, основанного на расширении, при определении идентичности пальцев позвоночных». Клетка. 118 (4): 517–28. Дои:10.1016 / j.cell.2004.07.024. PMID 15315763.
- ^ Бхардвадж Г., Мердок Б., Ву Д., Бейкер Д. П., Уильямс К. П., Чедвик К., Линг Л. Э., Карану Ф. Н., Бхатия М. (февраль 2001 г.). «Sonic hedgehog индуцирует пролиферацию примитивных гемопоэтических клеток человека посредством регуляции BMP». Иммунология природы. 2 (2): 172–80. Дои:10.1038/84282. PMID 11175816.
- ^ Лю С., Донту Г., Mantle ID, Патель С., Ан Н.С., Джексон К.В., Сури П., Вича М.С. (июнь 2006 г.). «Передача сигналов Hedgehog и Bmi-1 регулируют самообновление нормальных и злокачественных стволовых клеток молочной железы человека». Исследования рака. 66 (12): 6063–71. Дои:10.1158 / 0008-5472.CAN-06-0054. ЧВК 4386278. PMID 16778178.
- ^ Ан С., Джойнер А.Л. (октябрь 2005 г.). «Анализ in vivo покоящихся взрослых нервных стволовых клеток, отвечающих на Sonic hedgehog». Природа. 437 (7060): 894–7. Дои:10.1038 / природа03994. PMID 16208373.
- ^ Паладини Р.Д., Салех Дж., Цянь С., Сюй Г.Х., Рубин Л.Л. (октябрь 2005 г.). «Модуляция роста волос с помощью низкомолекулярных агонистов сигнального пути hedgehog». Журнал следственной дерматологии. 125 (4): 638–46. Дои:10.1111 / j.0022-202X.2005.23867.x. PMID 16185261.
- ^ http://phx.corporate-ir.net/phoenix.zhtml?c=123198&p=irol-newsArticle&ID=997941&highlight=[требуется полная цитата ]
- ^ Онлайн-менделевское наследование в человеке (OMIM): Голопрозэнцефалия - 236100
- ^ Киллер РФ (октябрь 1978 г.). «Циклопамин и родственные стероидные алкалоидные тератогены: их возникновение, структурные отношения и биологические эффекты». Липиды. 13 (10): 708–15. Дои:10.1007 / BF02533750. PMID 723484.
- ^ Xie J, Murone M, Luoh SM, Ryan A, Gu Q, Zhang C, Bonifas JM, Lam CW, Hynes M, Goddard A, Rosenthal A, Epstein EH, de Sauvage FJ (январь 1998 г.). «Активация сглаженных мутаций при спорадической базальноклеточной карциноме». Природа. 391 (6662): 90–2. Дои:10.1038/34201. PMID 9422511.
- ^ Чен Дж. К., Тайпале Дж., Янг К. Э., Маити Т., Бичи, Пенсильвания (октябрь 2002 г.). «Модуляция сглаженной активности низкими молекулами». Труды Национальной академии наук Соединенных Штатов Америки. 99 (22): 14071–6. Дои:10.1073 / pnas.182542899. ЧВК 137838. PMID 12391318.
- ^ а б Шкода AM, Симович Д., Карин В., Кардум В., Вранич С., Серман Л. (февраль 2018 г.). «Роль сигнального пути Hedgehog при раке: всесторонний обзор». Боснийский журнал фундаментальных медицинских наук. 18 (1): 8–20. Дои:10.17305 / bjbms.2018.2756. ЧВК 5826678. PMID 29274272.
- ^ Ким Дж., Тан Дж. Й., Гонг Р., Ким Дж., Ли Дж. Дж., Клемонс К. В., Чонг С. Р., Чанг К. С., Ферештех М., Гарднер Д., Рейя Т., Лю Джо, Эпштейн Е. Х., Стивенс Д. А., Бичи ПА (апрель 2010 г.). «Итраконазол, широко используемый противогрибковый препарат, который подавляет активность пути Hedgehog и рост рака». Раковая клетка. 17 (4): 388–99. Дои:10.1016 / j.ccr.2010.02.027. ЧВК 4039177. PMID 20385363.
- ^ Ким Дж., Афтаб Б.Т., Тан Дж.Й., Ким Д., Ли А.Х., Резаи М., Ким Дж., Чен Б., Кинг Е.М., Бородовский А., Риггинс Г.Дж., Эпштейн Е.Н., Бичи П.А., Рудин С.М. (январь 2013 г.). «Итраконазол и триоксид мышьяка ингибируют активацию пути Hedgehog и рост опухоли, связанный с приобретенной устойчивостью к сглаженным антагонистам». Раковая клетка. 23 (1): 23–34. Дои:10.1016 / j.ccr.2012.11.017. ЧВК 3548977. PMID 23291299.
- ^ Накамура М., Кубо М., Янаи К., Миками Ю., Икебе М., Нагаи С., Ямагути К., Танака М., Катано М. (2007). «Антитела Anti-patched-1 подавляют сигнальный путь hedgehog и пролиферацию рака поджелудочной железы». Противораковые исследования. 27 (6A): 3743–7. PMID 17970037.
- ^ Хант Р., Брагина О., Дрюс М., Касак Л., Тиммуск С., Валкна А., Когерман П., Ярвекюльг Л. (август 2007 г.). «Создание и характеристика мышиных моноклональных антител 5E1 против человеческого фактора транскрипции GLI3». Гибридома. 26 (4): 231–40. Дои:10.1089 / hyb.2007.0507. PMID 17725385.
- ^ Stecca B, Mas C, Ruiz i Altaba A (май 2005 г.). «Вмешательство в передачу сигналов HH-GLI подавляет рак простаты». Тенденции в молекулярной медицине. 11 (5): 199–203. Дои:10.1016 / j.molmed.2005.03.004. PMID 15882606.
- ^ Beauchamp EM, Ringer L, Bulut G, Sajwan KP, Hall MD, Lee YC, Peaceman D, Ozdemirli M, Rodriguez O, Macdonald TJ, Albanese C, Toretsky JA, Uren A (январь 2011 г.). «Триоксид мышьяка подавляет рост раковых клеток человека и развитие опухолей у мышей, блокируя путь Hedgehog / GLI». Журнал клинических исследований. 121 (1): 148–60. Дои:10.1172 / JCI42874. ЧВК 3007144. PMID 21183792.
- ^ Ким Дж., Ли Дж. Дж., Ким Дж., Гарднер Д., Бичи, Пенсильвания (июль 2010 г.). «Мышьяк противодействует пути Hedgehog, предотвращая накопление ресничек и снижая стабильность транскрипционного эффектора Gli2». Труды Национальной академии наук Соединенных Штатов Америки. 107 (30): 13432–7. Дои:10.1073 / pnas.1006822107. ЧВК 2922148. PMID 20624968.
- ^ а б c Липинский Р.Дж., Бушман В. (август 2010 г.). «Идентификация ингибиторов передачи сигналов Hedgehog с релевантным воздействием на человека путем скрининга малых молекул». Токсикология in vitro. Toxicol In Vitro. 24 (5): 1404–9. Дои:10.1016 / j.tiv.2010.04.011. ЧВК 2891024. PMID 20434536.
- ^ Эламин М.Х., Шинвари З., Хендраяни С.Ф., Аль-Хинди Х., Аль-Шаил Э., Хафага Ю. и др. (Март 2010 г.). «Куркумин подавляет сигнальный путь Sonic Hedgehog и запускает апоптоз в клетках медуллобластомы». Молекулярный канцерогенез. 49 (3): 302–14. Дои:10.1002 / mc.20604. PMID 20025076.
- ^ «Решение о перерегистрации пиперонилбутоксида» (PDF). USEPA.
- ^ Ван Дж., Лу Дж., Мук Р.А., Чжан М., Чжао С., Барак Л.С. и др. (Август 2012 г.). «Инсектицидный синергист пиперонилбутоксид подавляет передачу сигналов ежей: оценка химических рисков». Токсикологические науки. 128 (2): 517–23. Дои:10.1093 / toxsci / kfs165. ЧВК 3493191. PMID 22552772.
- ^ Эверсон JL, Sun MR, Финк DM, Heyne GW, Melberg CG, Nelson KF, Doroodchi P, Colopy LJ, Ulschmid CM, Martin AA, McLaughlin MT, Lipinski RJ (октябрь 2019 г.). «Оценка токсичности для развития воздействия пиперонилбутоксида, нацеленного на передачу сигналов Sonic Hedgehog, морфогенез переднего мозга и лица у мышей: исследование in vitro и in vivo». Перспективы гигиены окружающей среды. 127 (10): 107006. Дои:10.1289 / EHP5260. ЧВК 6867268. PMID 31642701.
- ^ Ли X, Дэн В., Гвоздь CD, Бейли С.К., Краус М.Х., Рупперт Дж.М., Лобо-Рупперт С.М. (январь 2006 г.). «Улитка индукция - это ранний ответ на Gli1, который определяет эффективность эпителиальной трансформации». Онкоген. 25 (4): 609–21. Дои:10.1038 / sj.onc.1209077. ЧВК 1361531. PMID 16158046.
- ^ Ли С.В., Московиц М.А., Симс-младший (март 2007 г.). «Sonic hedgehog обратно пропорционально регулирует экспрессию ангиопоэтина-1 и ангиопоэтина-2 в фибробластах». Международный журнал молекулярной медицины. 19 (3): 445–51. Дои:10.3892 / ijmm.19.3.445. PMID 17273793.
- ^ Адольф С., Хетерингтон Р., Эллис Т., Уэйнрайт Б. (февраль 2006 г.). «Patched1 действует как привратник, способствуя развитию клеточного цикла». Исследования рака. 66 (4): 2081–8. Дои:10.1158 / 0008-5472.CAN-05-2146. PMID 16489008.
- ^ Атхар М., Ли С, Тан Х, Чи С., Чжан Х, Ким А.Л., Тайринг С.К., Копелович Л., Хеберт Дж., Эпштейн Э.Х., Бикерс Д.Р., Се Дж. (Октябрь 2004 г.). «Ингибирование сглаженной передачи сигналов предотвращает индуцированную ультрафиолетом B карциному базальных клеток за счет регуляции экспрессии Fas и апоптоза». Исследования рака. 64 (20): 7545–52. Дои:10.1158 / 0008-5472.CAN-04-1393. PMID 15492281.
- ^ Номер клинического исследования NCT00636610 для "Исследование GDC-0449 (ингибитор пути ежа) с одновременной химиотерапией и бевацизумабом в качестве терапии первой линии для метастатического колоректального рака" в ClinicalTrials.gov
- ^ Номер клинического исследования NCT01108094 для «Пилотного исследования биомаркеров для оценки эффективности итраконазола у пациентов с базально-клеточными карциномами» в ClinicalTrials.gov
- ^ Вада Х, Макабе К. (2006). «Дублирование генома ранних позвоночных как возможная хроника эволюционной истории нервного гребня». Международный журнал биологических наук. 2 (3): 133–41. Дои:10.7150 / ijbs.2.133. ЧВК 1474148. PMID 16763673.
- ^ Старк Д. Р., Гейтс ПБ, Брокес Дж. П., Ферретти П. (июль 1998 г.). «Член семьи Ёжиков выражается во всех регенерирующих и развивающихся конечностях». Динамика развития. 212 (3): 352–63. Дои:10.1002 / (SICI) 1097-0177 (199807) 212: 3 <352 :: AID-AJA3> 3.0.CO; 2-G. PMID 9671939.
- ^ Дорус С., Андерсон Дж. Р., Валлендер Э. Дж., Гилберт С. Л., Чжан Л., Хемник Л. Г., Райдер О. А., Ли В., Лан Б. Т. (июль 2006 г.). «Sonic Hedgehog, ключевой ген развития, претерпел интенсивную молекулярную эволюцию у приматов». Молекулярная генетика человека. 15 (13): 2031–7. Дои:10.1093 / hmg / ddl123. PMID 16687440.
- ^ Грауль Р.С., Сэде В. (2001). «Эволюционные отношения между рецепторами, связанными с G-белком, с использованием подхода с кластерной базой данных». AAPS PharmSci. 3 (2): 25–42. Дои:10.1208 / пс030212. ЧВК 2779559. PMID 11741263.
- ^ Nusse R (ноябрь 2003 г.). «Wnts и Hedgehogs: модифицированные липидами белки и сходство сигнальных механизмов на поверхности клетки». Разработка. 130 (22): 5297–305. Дои:10.1242 / dev.00821. PMID 14530294.
- ^ Varjosalo M, Li SP, Taipale J (февраль 2006 г.). «Дивергенция механизма передачи сигнала hedgehog между дрозофилой и млекопитающими». Клетка развития. 10 (2): 177–86. Дои:10.1016 / j.devcel.2005.12.014. PMID 16459297.
- ^ Чен М.Х., Гао Н., Каваками Т., Чуанг П.Т. (август 2005 г.). «Мыши с дефицитом слитого гомолога не проявляют фенотипов, указывающих на нарушение передачи сигналов hedgehog во время эмбрионального развития». Молекулярная и клеточная биология. 25 (16): 7042–53. Дои:10.1128 / MCB.25.16.7042-7053.2005. ЧВК 1190231. PMID 16055716.
- ^ Хуанфу Д., Андерсон К.В. (январь 2006 г.). «Передача сигналов от Smo к Ci / Gli: сохранение и расхождение путей Hedgehog от дрозофилы к позвоночным». Разработка. 133 (1): 3–14. Дои:10.1242 / dev.02169. PMID 16339192.
- ^ а б Matus DQ, Magie CR, Pang K, Martindale MQ, Thomsen GH (январь 2008 г.). «Семейство генов Hedgehog книдарий, Nematostella vectensis, и значение для понимания эволюции пути Hedgehog у многоклеточных животных». Биология развития. 313 (2): 501–18. Дои:10.1016 / j.ydbio.2007.09.032. ЧВК 2288667. PMID 18068698.
- ^ а б c Адамска М., Матус Д.К., Адамски М., Грин К., Рохсар Д.С., Мартиндейл М.К., Дегнан Б.М. (октябрь 2007 г.). «Эволюционное происхождение белков ежа». Текущая биология. 17 (19): R836-7. Дои:10.1016 / j.cub.2007.08.010. PMID 17925209.
- ^ а б Снелл Е.А., Брук Н.М., Тейлор В.Р., Казан Д., Филипп Х., Голландия П.В. (февраль 2006 г.). «Необычный белок хоанофлагеллят, выпущенный автокаталитической обработкой Hedgehog». Ход работы. Биологические науки. 273 (1585): 401–7. Дои:10.1098 / rspb.2005.3263. ЧВК 1560198. PMID 16615205.
- ^ а б c Bürglin TR (март 2008 г.). «Эволюция генов hedgehog и связанных с ним генов, их происхождение от белков Hog у предков эукариот и открытие нового мотива Hint». BMC Genomics. 9 (127): 127. Дои:10.1186/1471-2164-9-127. ЧВК 2362128. PMID 18334026.
- ^ а б Бюрглин TR (2008). «Семейство белков Hedgehog». Геномная биология. 9 (11): 241. Дои:10.1186 / gb-2008-9-11-241. ЧВК 2614485. PMID 19040769.
- ^ а б c d Зугасти О., Раджан Дж., Кувабара ЧП (октябрь 2005 г.). «Функция и распространение гомологов, связанных с Patched- и Hedgehog, у C. elegans». Геномные исследования. 15 (10): 1402–10. Дои:10.1101 / гр.3935405. ЧВК 1240083. PMID 16204193.
- ^ а б c d Bürglin TR, Kuwabara PE (январь 2006 г.). «Гомологи сигнальной сети Hh у C. elegans». WormBook: 1–14. Дои:10.1895 / wormbook.1.76.1. ЧВК 4781598. PMID 18050469.
внешняя ссылка
- https://web.archive.org/web/20060716083827/http://hedgehog.sfsu.edu/ (База данных Hedgehog Pathway)
- http://www.novusbio.com/hedgehogpathway.html (Схема сигнального пути ежа)
