ABL (ген) - ABL (gene)
Тирозин-протеинкиназа ABL1 также известный как ABL1 это белок что у людей кодируется ABL1 ген (предыдущий символ ABL) расположен на хромосома 9.[5] c-Abl иногда используется для обозначения версии гена, обнаруженного в геноме млекопитающих, в то время как v-Abl относится к вирусному гену, который первоначально был выделен из Вирус лейкемии мышей Абельсона.[6]
Функция
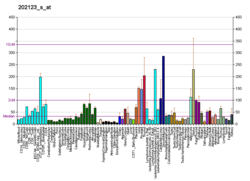
В ABL1 протоонкоген кодирует цитоплазматический и ядерный белок тирозинкиназа который участвует в процессах дифференцировки клеток, деление клеток, клеточная адгезия и стрессовая реакция.[7] Активность белка ABL1 негативно регулируется его SH3 домен, а удаление домена SH3 превращает ABL1 в онкоген. В t (9; 22) транслокация приводит к тому, что голова к хвосту слияние из BCR и ABL1 гены, приводящие к ген слияния присутствует во многих случаях хронического миелогенный лейкоз. ДНК-связывающая активность повсеместно экспрессируемой тирозинкиназы ABL1 регулируется CDC2 -опосредованный фосфорилирование, предполагая функцию клеточного цикла для ABL1. В ABL1 Ген экспрессируется в виде транскрипта мРНК размером 6 или 7 т.п.н. с альтернативно сплайсированными первыми экзонами, сплайсированными с общими экзонами 2-11.[8]
Клиническое значение

Мутации в ABL1 ген связаны с хронический миелолейкоз (CML). При ХМЛ ген активируется перемещенный внутри BCR (область кластера точек останова) ген на хромосоме 22. Этот новый ген слияния, BCR-ABL, кодирует нерегулируемую тирозинкиназу, нацеленную на цитоплазму, которая позволяет клеткам пролиферировать без регулирования цитокины. Это, в свою очередь, позволяет клетке стать раковый.
Этот ген является партнером гена слияния с BCR ген в Филадельфийская хромосома, характерная аномалия при хроническом миелогенный лейкоз (CML) и редко в некоторых других лейкемия формы. Транскрипт BCR-ABL кодирует тирозинкиназа, который активирует медиаторов клеточный цикл система регуляции, приводящая к клональному миелопролиферативное заболевание. Белок BCR-ABL может ингибироваться различными небольшими молекулами. Одним из таких ингибиторов является мезилат иматиниба, который занимает домен тирозинкиназы и ингибирует влияние BCR-ABL на клеточный цикл. Второе поколение Ингибиторы тирозинкиназы BCR-ABL также находятся в стадии разработки для ингибирования мутантов BCR-ABL, устойчивых к иматинибу.
Взаимодействия
ABL ген был показан взаимодействовать с:
- ABI1,[9][10][11]
- ABI2,[12][13]
- ABL2,[12]
- Банкомат,[14][15][16]
- BCAR1,[17][18]
- BCR,[19][20][21]
- BRCA1,[22]
- КОТ,[23]
- CBL,[24][25]
- CRKL,[26][27][28]
- DOK1,[29][30]
- EPHB2,[31]
- GPX1,[32]
- GRB10,[33][34]
- MTOR,[35]
- GRB2,[26][36]
- MDM2,[37]
- NCK1,[24][26]
- NEDD9,[38][39]
- НТРК1,[40][41]
- P73,[42][43]
- PAG1,[44]
- PAK2,[45]
- PSTPIP1,[46]
- RAD9A,[47]
- RAD51,[14]
- RB1,[48][49]
- RFX1,[50]
- RYBP,[51]
- SHC1,[19][52]
- СОРБС2,[25][53]
- ЗИП1,[54]
- SPTAN1,[54]
- TERF1,[16]
- VAV1,[55] и
- YTHDC1.[56]
Регулирование
Есть некоторые свидетельства того, что экспрессия Abl регулируется микроРНК. miR-203.[57]
Смотрите также
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000097007 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000026842 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Щилик С., Скорски Т., Николаидес Н.С., Манцелла Л., Малагуарнера Л., Вентурелли Д., Гевиртц А.М., Калабретта Б. (август 1991 г.). «Селективное ингибирование пролиферации лейкозных клеток антисмысловыми олигодезоксинуклеотидами BCR-ABL». Наука. 253 (5019): 562–5. Дои:10.1126 / science.1857987. PMID 1857987.
- ^ Абельсон Х.Т., Рабштейн Л.С. (август 1970 г.). «Лимфосаркома: вирус-индуцированное заболевание, независимое от тимуса, у мышей». Исследования рака. 30 (8): 2213–22. PMID 4318922.
- ^ "UniProtKB - P00519 (ABL1_HUMAN)". Uniprot. Получено 18 мая 2020.
- ^ "Ген Entrez: ABL1 v-abl Гомолог 1 вирусного онкогена мышиного лейкоза Абельсона".
- ^ Тани К., Сато С., Сукэдзане Т., Кодзима Х., Хиросе Х., Ханафуса Х., Шишидо Т. (июнь 2003 г.). «Интерфактор Abl 1 способствует фосфорилированию тирозина 296 млекопитающих, активируемых (Mena) с-Abl киназой». J. Biol. Chem. 278 (24): 21685–92. Дои:10.1074 / jbc.M301447200. PMID 12672821.
- ^ Биесова З., Пикколи С., Вонг В.Т. (январь 1997 г.). «Выделение и характеристика e3B1, белка, связывающего eps8, который регулирует рост клеток». Онкоген. 14 (2): 233–41. Дои:10.1038 / sj.onc.1200822. PMID 9010225.
- ^ Ямамото А., Сузуки Т., Сакаки Ю. (июнь 2001 г.). «Выделение hNap1BP, который взаимодействует с человеческим Nap1 (NCKAP1), экспрессия которого подавляется при болезни Альцгеймера». Ген. 271 (2): 159–69. Дои:10.1016 / S0378-1119 (01) 00521-2. PMID 11418237.
- ^ а б Цао Ц., Ленг Й., Ли Ц., Куфе Д. (апрель 2003 г.). «Функциональное взаимодействие протеин-тирозинкиназ c-Abl и Arg в ответе на окислительный стресс». J. Biol. Chem. 278 (15): 12961–7. Дои:10.1074 / jbc.M300058200. PMID 12569093.
- ^ Дай З., Пендергаст AM (ноябрь 1995 г.). «Abi-2, новый SH3-содержащий белок, взаимодействует с тирозинкиназой c-Abl и модулирует трансформирующую активность c-Abl». Genes Dev. 9 (21): 2569–82. Дои:10.1101 / gad.9.21.2569. PMID 7590236.
- ^ а б Чен Г., Юань С.С., Лю В., Сюй И, Трухильо К., Сонг Б., Конг Ф, Гофф С.П., Ву Ю., Арлингхаус Р., Балтимор Д., Гассер П.Дж., Пак М.С., Сун П., Ли Е.Ю. (апрель 1999 г.). «Радиационно-индуцированная сборка рекомбинационного комплекса Rad51 и Rad52 требует ATM и c-Abl». J. Biol. Chem. 274 (18): 12748–52. Дои:10.1074 / jbc.274.18.12748. PMID 10212258.
- ^ Шафман Т., Ханна К.К., Кедар П., Спринг К., Козлов С., Йен Т., Хобсон К., Гатеи М., Чжан Н., Уоттерс Д., Эгертон М., Шайло И., Харбанда С., Куфе Д., Лавин М.Ф. (май 1997 г.). «Взаимодействие между белком ATM и c-Abl в ответ на повреждение ДНК». Природа. 387 (6632): 520–3. Дои:10.1038 / 387520a0. PMID 9168117. S2CID 4334242.
- ^ а б Киши С., Чжоу XZ, Зив Й., Кху К., Хилл Д.Е., Шайло Й., Лу КП (август 2001 г.). «Теломерный белок Pin2 / TRF1 как важная мишень ATM в ответ на двухцепочечные разрывы ДНК». J. Biol. Chem. 276 (31): 29282–91. Дои:10.1074 / jbc.M011534200. PMID 11375976.
- ^ Салгия Р., Писик Е., Саттлер М., Ли Дж. Л., Уэмура Н., Вонг В. К., Бурки С. А., Хираи Х., Чен Л. Б., Гриффин Дж. Д. (октябрь 1996 г.). «p130CAS образует сигнальный комплекс с адаптерным белком CRKL в гемопоэтических клетках, трансформированных онкогеном BCR / ABL». J. Biol. Chem. 271 (41): 25198–203. Дои:10.1074 / jbc.271.41.25198. PMID 8810278.
- ^ Майер Б.Дж., Хираи Х., Сакаи Р. (март 1995 г.). «Доказательства того, что домены SH2 способствуют процессуальному фосфорилированию протеин-тирозинкиназами». Curr. Биол. 5 (3): 296–305. Дои:10.1016 / S0960-9822 (95) 00060-1. PMID 7780740. S2CID 16957239.
- ^ а б Пуил Л., Лю Дж., Гиш Дж., Мбамалу Дж., Боутелл Д., Пеликчи П. Г., Арлингхаус Р., Поусон Т. (февраль 1994 г.). «Онкобелки Bcr-Abl связываются непосредственно с активаторами сигнального пути Ras». EMBO J. 13 (4): 764–73. Дои:10.1002 / j.1460-2075.1994.tb06319.x. ЧВК 394874. PMID 8112292.
- ^ Лин Х, Ма Г, Сун Т, Лю Дж, Арлингхаус РБ (январь 2003 г.). «Взаимодействие Bcr и Abl: онкогенная активация c-Abl путем секвестрации Bcr». Рак Res. 63 (2): 298–303. PMID 12543778.
- ^ Пендергаст А.М., Мюллер А.Дж., Хавлик М.Х., Мару Й., Витте О.Н. (июль 1991 г.). «Последовательности BCR, необходимые для трансформации онкогеном BCR-ABL, связываются с регуляторным доменом SH2 ABL нефосфотирозин-зависимым образом». Клетка. 66 (1): 161–71. Дои:10.1016 / 0092-8674 (91) 90148-П. PMID 1712671. S2CID 9933891.
- ^ Foray N, Marot D, Randrianarison V, Venezia ND, Picard D, Perricaudet M, Favaudon V, Jeggo P (июнь 2002 г.). «Конститутивная ассоциация BRCA1 и c-Abl и его ATM-зависимое разрушение после облучения». Мол. Клетка. Биол. 22 (12): 4020–32. Дои:10.1128 / MCB.22.12.4020-4032.2002. ЧВК 133860. PMID 12024016.
- ^ Цао Ц., Ленг Й., Куфе Д. (август 2003 г.). «Активность каталазы регулируется c-Abl и Arg в ответ на окислительный стресс». J. Biol. Chem. 278 (32): 29667–75. Дои:10.1074 / jbc.M301292200. PMID 12777400.
- ^ а б Миёси-Акияма Т., Алеман Л.М., Смит Дж. М., Адлер К.Э., Майер Б.Дж. (июль 2001 г.). «Регулирование фосфорилирования Cbl с помощью тирозинкиназы Abl и адаптера Nck SH2 / SH3». Онкоген. 20 (30): 4058–69. Дои:10.1038 / sj.onc.1204528. PMID 11494134.
- ^ а б Субейран П., Барак А., Шимкевич И., Дикич И. (февраль 2003 г.). «Комплекс Cbl-ArgBP2 опосредует убиквитинирование и деградацию c-Abl». Biochem. J. 370 (Pt 1): 29–34. Дои:10.1042 / BJ20021539. ЧВК 1223168. PMID 12475393.
- ^ а б c Рен Р., Йе З.С., Балтимор Д. (апрель 1994 г.). «Протеин-тирозинкиназа Abl выбирает адаптер Crk в качестве субстрата, используя сайты связывания SH3». Genes Dev. 8 (7): 783–95. Дои:10.1101 / gad.8.7.783. PMID 7926767.
- ^ Хини С., Колибаба К., Бхат А., Ода Т., Оно С., Фаннинг С., Друкер Б.Дж. (январь 1997 г.). «Прямое связывание CRKL с BCR-ABL не требуется для трансформации BCR-ABL». Кровь. 89 (1): 297–306. Дои:10.1182 / blood.V89.1.297. PMID 8978305.
- ^ Кионо В.Т., де Йонг Р., Пак Р.К., Лю Й., Хейстеркамп Н., Гроффен Дж., Дерден Д.Л. (ноябрь 1998 г.). «Дифференциальное взаимодействие Crkl с Cbl или C3G, Hef-1 и мотивом активации на основе тирозина иммунорецептора гамма-субъединицы в передаче сигналов миелоидного высокоаффинного рецептора Fc для IgG (Fc гамма RI)». J. Immunol. 161 (10): 5555–63. PMID 9820532.
- ^ ван Дейк Т.Б., ван Ден Аккер Э., Амельсвоорт депутат, Мано Х., Левенберг Б., фон Линдерн М. (ноябрь 2000 г.). «Фактор стволовых клеток индуцирует фосфатидилинозитол-3'-киназозависимое образование комплекса Lyn / Tec / Dok-1 в гемопоэтических клетках». Кровь. 96 (10): 3406–13. Дои:10.1182 / кровь.V96.10.3406. PMID 11071635.
- ^ Яманаши Ю., Балтимор Д. (январь 1997 г.). «Идентификация Abl- и rasGAP-ассоциированного белка 62 кДа в качестве стыковочного белка, Док». Клетка. 88 (2): 205–11. Дои:10.1016 / S0092-8674 (00) 81841-3. PMID 9008161. S2CID 14205526.
- ^ Ю. Х. Х., Зиш А. Х., Доделет В. К., Паскуале Э. Б. (июль 2001 г.). «Множественные сигнальные взаимодействия киназ Abl и Arg с рецептором EphB2». Онкоген. 20 (30): 3995–4006. Дои:10.1038 / sj.onc.1204524. PMID 11494128.
- ^ Цао Ц., Ленг Й., Хуанг В., Лю Х, Куфе Д. (октябрь 2003 г.). «Глутатионпероксидаза 1 регулируется тирозинкиназами c-Abl и Arg». J. Biol. Chem. 278 (41): 39609–14. Дои:10.1074 / jbc.M305770200. PMID 12893824.
- ^ Бай Р. Я., Ян Т., Шрем С., Мюнцерт Г., Вайднер К. М., Ван Дж. Ю., Дуйстер Дж. (Август 1998 г.). «SH2-содержащий адаптерный белок GRB10 взаимодействует с BCR-ABL». Онкоген. 17 (8): 941–8. Дои:10.1038 / sj.onc.1202024. PMID 9747873.
- ^ Франц Дж. Д., Джорджетти-Перальди С., Оттингер Э. А., Шелсон С. Е. (январь 1997 г.). "Человеческий GRB-IRbeta / GRB10. Варианты сплайсинга белка, связывающего рецептор инсулина и фактора роста, с доменами PH и SH2". J. Biol. Chem. 272 (5): 2659–67. Дои:10.1074 / jbc.272.5.2659. PMID 9006901.
- ^ Кумар В., Сабатини Д., Пандей П., Гинграс А.С., Маджумдер П.К., Кумар М., Юань З.М., Кармайкл Г., Вайксельбаум Р., Зоненберг Н., Куфе Д., Харбанда С. (апрель 2000 г.). «Регулирование рапамицина и FKBP-мишени 1 / млекопитающее-мишень рапамицина и кэп-зависимая инициация трансляции протеин-тирозинкиназой c-Abl». J. Biol. Chem. 275 (15): 10779–87. Дои:10.1074 / jbc.275.15.10779. PMID 10753870.
- ^ Warmuth M, Bergmann M, Priess A, Häuslmann K, Emmerich B, Hallek M (декабрь 1997 г.). «Киназа Hck семейства Src взаимодействует с Bcr-Abl по киназно-независимому механизму и фосфорилирует Grb2-связывающий сайт Bcr». J. Biol. Chem. 272 (52): 33260–70. Дои:10.1074 / jbc.272.52.33260. PMID 9407116.
- ^ Goldberg Z, Vogt Sionov R, Berger M, Zwang Y, Perets R, Van Etten RA, Oren M, Taya Y, Haupt Y (июль 2002 г.). «Фосфорилирование тирозина Mdm2 с помощью c-Abl: последствия для регуляции p53». EMBO J. 21 (14): 3715–27. Дои:10.1093 / emboj / cdf384. ЧВК 125401. PMID 12110584.
- ^ Минегиси М., Татибана К., Сато Т., Ивата С., Нодзима Ю., Моримото С. (октябрь 1996 г.). «Структура и функция Cas-L, связанного с субстратом белка с Crk 105 кДа, который участвует в передаче сигналов бета-1 интегрином в лимфоцитах». J. Exp. Med. 184 (4): 1365–75. Дои:10.1084 / jem.184.4.1365. ЧВК 2192828. PMID 8879209.
- ^ Law SF, Estojak J, Wang B, Mysliwiec T., Kruh G, Golemis EA (июль 1996 г.). «Человеческий усилитель филаментации 1, новый p130cas-подобный стыковочный белок, связывается с киназой фокальной адгезии и индуцирует рост псевдогифала в Saccharomyces cerevisiae». Мол. Клетка. Биол. 16 (7): 3327–37. Дои:10.1128 / mcb.16.7.3327. ЧВК 231327. PMID 8668148.
- ^ Кох А., Манчини А., Стефан М., Ниденталь Р., Ниманн Х., Тамура Т. (март 2000 г.). «Прямое взаимодействие рецептора фактора роста нервов, TrkA, с нерецепторной тирозинкиназой, c-Abl, через петлю активации». FEBS Lett. 469 (1): 72–6. Дои:10.1016 / S0014-5793 (00) 01242-4. PMID 10708759.
- ^ Яно Х., Конг Ф., Бирге Р. Б., Гофф С. П., Чао М. В. (февраль 2000 г.). «Ассоциация тирозинкиназы Abl с рецептором фактора роста нервов Trk». J. Neurosci. Res. 59 (3): 356–64. Дои:10.1002 / (SICI) 1097-4547 (20000201) 59: 3 <356 :: AID-JNR9> 3.0.CO; 2-G. PMID 10679771.
- ^ Юань З.М., Шиоя Х., Ишико Т., Сунь Х, Гу Дж., Хуанг Й.Й., Лу Х., Харбанда С., Вейксельбаум Р., Куфе Д. (июнь 1999 г.). «p73 регулируется тирозинкиназой c-Abl в апоптотическом ответе на повреждение ДНК». Природа. 399 (6738): 814–7. Дои:10.1038/21704. PMID 10391251. S2CID 4421613.
- ^ Агами Р., Бландино Г., Орен М., Шауль Ю. (июнь 1999 г.). «Взаимодействие c-Abl и p73alpha и их сотрудничество для индукции апоптоза». Природа. 399 (6738): 809–13. Дои:10.1038/21697. PMID 10391250. S2CID 4394015.
- ^ Вен С.Т., Ван Эттен Р.А. (октябрь 1997 г.). «Продукт гена PAG, стресс-индуцированный белок с антиоксидантными свойствами, представляет собой Abl SH3-связывающий белок и физиологический ингибитор активности тирозинкиназы c-Abl». Genes Dev. 11 (19): 2456–67. Дои:10.1101 / gad.11.19.2456. ЧВК 316562. PMID 9334312.
- ^ Roig J, Tuazon PT, Zipfel PA, Pendergast AM, Traugh JA (декабрь 2000 г.). «Функциональное взаимодействие между c-Abl и p21-активированной протеинкиназой гамма-PAK». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 97 (26): 14346–51. Дои:10.1073 / pnas.97.26.14346. ЧВК 18921. PMID 11121037.
- ^ Конг Ф., Спенсер С., Коте Дж. Ф., Ву И, Тремблей М.Л., Ласки Л.А., Гофф С.П. (декабрь 2000 г.). «Цитоскелетный белок PSTPIP1 направляет протеинтирозинфосфатазу PEST-типа к киназе c-Abl, чтобы опосредовать дефосфорилирование Abl». Мол. Клетка. 6 (6): 1413–23. Дои:10.1016 / S1097-2765 (00) 00138-6. PMID 11163214.
- ^ Йошида К., Комацу К., Ван Х. Г., Куфе Д. (май 2002 г.). «c-Abl тирозинкиназа регулирует белок контрольной точки Rad9 человека в ответ на повреждение ДНК». Мол. Клетка. Биол. 22 (10): 3292–300. Дои:10.1128 / MCB.22.10.3292-3300.2002. ЧВК 133797. PMID 11971963.
- ^ Миямура Т., Нисимура Дж., Юфу Ю., Навата Х. (февраль 1997 г.). «Взаимодействие BCR-ABL с белком ретинобластомы в хромосомно-позитивных линиях Филадельфии». Int. J. Hematol. 65 (2): 115–21. Дои:10.1016 / S0925-5710 (96) 00539-7. PMID 9071815.
- ^ Велч П.Дж., Ван Дж.Й. (ноябрь 1993 г.). «С-концевой белок-связывающий домен в белке ретинобластомы регулирует ядерную тирозинкиназу c-Abl в клеточном цикле». Клетка. 75 (4): 779–90. Дои:10.1016 / 0092-8674 (93) 90497-Е. PMID 8242749.
- ^ Агами Р., Шауль И. (апрель 1998 г.). «Киназная активность c-Abl, но не v-Abl, усиливается прямым взаимодействием с RFXI, белком, который связывает энхансеры нескольких вирусов и генов, регулируемых клеточным циклом». Онкоген. 16 (14): 1779–88. Дои:10.1038 / sj.onc.1201708. PMID 9583676.
- ^ Чжу Дж., Шор СК (декабрь 1996 г.). «Активность тирозинкиназы c-ABL регулируется путем ассоциации с новым белком, связывающим SH3-домен». Мол. Клетка. Биол. 16 (12): 7054–62. Дои:10.1128 / mcb.16.12.7054. ЧВК 231708. PMID 8943360.
- ^ Вишневски Д., Страйф А., Свендеман С., Эрдьюмент-Бромаж Х, Героманос С., Кавано В. М., Темпст П., Кларксон Б. (апрель 1999 г.). «Новая SH2-содержащая фосфатидилинозитол 3,4,5-трифосфат-5-фосфатаза (SHIP2) конститутивно фосфорилируется по тирозину и связана с гомологичным src геном коллагена (SHC) в клетках-предшественниках хронического миелогенного лейкоза». Кровь. 93 (8): 2707–20. Дои:10.1182 / кровь.V93.8.2707. PMID 10194451.
- ^ Ван Б., Големис Е.А., Крух Г.Д. (июль 1997 г.). «ArgBP2, Arg / Abl-взаимодействующий белок, содержащий домен с множественной гомологией Src 3, фосфорилируется в v-Abl-трансформированных клетках и локализуется в стрессовых волокнах и Z-дисках кардиоцитов». J. Biol. Chem. 272 (28): 17542–50. Дои:10.1074 / jbc.272.28.17542. PMID 9211900.
- ^ а б Ziemnicka-Kotula D, Xu J, Gu H, Potempska A, Kim KS, Jenkins EC, Trenkner E, Kotula L (май 1998 г.). «Идентификация кандидатного человеческого белка, связывающего домен с гомологией 3 Src спектрина, предполагает общий механизм ассоциации тирозинкиназ с основанным на спектрине скелетом мембраны». J. Biol. Chem. 273 (22): 13681–92. Дои:10.1074 / jbc.273.22.13681. PMID 9593709.
- ^ Bassermann F, Jahn T, Miething C, Seipel P, Bai RY, Coutinho S, Tybulewicz VL, Peschel C, Duyster J (апрель 2002 г.). «Ассоциация Bcr-Abl с протоонкогеном Vav участвует в активации пути Rac-1». J. Biol. Chem. 277 (14): 12437–45. Дои:10.1074 / jbc.M112397200. PMID 11790798.
- ^ Рафальска И., Чжан З., Бендерска Н., Вольф Х., Хартманн А.М., Брак-Вернер Р., Штамм С. (август 2004 г.). «Внутриядерная локализация и функция YT521-B регулируются фосфорилированием тирозина». Гм. Мол. Genet. 13 (15): 1535–49. Дои:10,1093 / hmg / ddh167. PMID 15175272.
- ^ Буэно М.Дж., Перес де Кастро I, Гомес де Седрон М., Сантос Дж., Калин Г.А., Сигудоса Дж. К., Кроче С.М., Фернандес-Пикерас Дж., Малумбрес М. (июнь 2008 г.). «Генетическое и эпигенетическое подавление микроРНК-203 усиливает экспрессию онкогенов ABL1 и BCR-ABL1». Раковая клетка. 13 (6): 496–506. Дои:10.1016 / j.ccr.2008.04.018. HDL:10261/7369. PMID 18538733.
дальнейшее чтение
- Shore SK, Tantravahi RV, Reddy EP (декабрь 2002 г.). «Пути трансформации, активируемые тирозинкиназой v-Abl». Онкоген. 21 (56): 8568–76. Дои:10.1038 / sj.onc.1206084. PMID 12476303.
- Шауль Y (2000). «c-Abl: активация и ядерные мишени». Разница в гибели клеток. 7 (1): 10–6. Дои:10.1038 / sj.cdd.4400626. PMID 10713716.
- Эра Т (2002). «Bcr-Abl - это« молекулярный переключатель »для принятия решения о росте и дифференцировке гемопоэтических стволовых клеток». Int. J. Hematol. 76 (1): 35–43. Дои:10.1007 / BF02982716. PMID 12138893. S2CID 10269867.
- Пендергаст AM (2002). «Киназы семейства Abl: механизмы регуляции и передачи сигналов». Достижения в области исследования рака, том 85. Adv. Рак Res. Достижения в исследованиях рака. 85. С. 51–100. Дои:10.1016 / S0065-230X (02) 85003-5. ISBN 978-0120066858. PMID 12374288.
- Кеунг Ю.К., Бити М., Стюард В., Джекл Б., Петнати М. (2002). «Хронический миелоцитарный лейкоз с эозинофилией, t (9; 12) (q34; p13) и перестройка гена ETV6-ABL: отчет о болезни и обзор литературы». Рак Генет. Цитогенет. 138 (2): 139–42. Дои:10.1016 / S0165-4608 (02) 00609-X. PMID 12505259.
- Сальо Дж., Чиллони Д. (2004).«Abl: прототип онкогенных слитых белков». Клетка. Мол. Life Sci. 61 (23): 2897–911. Дои:10.1007 / s00018-004-4271-0. PMID 15583852. S2CID 35998018.
- Шауль Й, Бен-Иехояда М (2005). «Роль c-Abl в реакции стресса на повреждение ДНК». Cell Res. 15 (1): 33–5. Дои:10.1038 / sj.cr.7290261. PMID 15686624.
- Йошида К. (2007). «Регулирование ядерного нацеливания тирозинкиназы Abl в ответ на повреждение ДНК». Достижения в молекулярной онкологии. Adv. Exp. Med. Биол. Успехи экспериментальной медицины и биологии. 604. стр.155–65. Дои:10.1007/978-0-387-69116-9_15. ISBN 978-0-387-69114-5. PMID 17695727.
внешняя ссылка
- Гены, + abl в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Онлайн-менделевское наследование в человеке (OMIM): 189980 (ABL)
- Абельсон + лейкемия + вирус в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Дрозофила Abl тирозинкиназа - Интерактивная муха
- ABL1 Информация со ссылками в Шлюз миграции ячеек
- ABL1 на Атлас генетики и онкологии
- Человек ABL1 расположение генома и ABL1 страница сведений о гене в Браузер генома UCSC.
- Обзор всей структурной информации, доступной в PDB за UniProt: P00519 (Человеческая тирозин-протеинкиназа ABL1) на PDBe-KB.
- Обзор всей структурной информации, доступной в PDB за UniProt: P00520 (Тирозин-протеинкиназа мыши ABL1) на PDBe-KB.