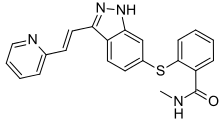
Акситиниб - Axitinib
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Инлита, Аксиникс |
| AHFS /Drugs.com | Монография |
| MedlinePlus | a612017 |
| Данные лицензии | |
| Беременность категория |
|
| Маршруты администрация | Устный |
| Код УВД | |
| Легальное положение | |
| Легальное положение | |
| Фармакокинетический данные | |
| Биодоступность | 58%[1] |
| Связывание с белками | >99%[1] |
| Метаболизм | Печеночный (главным образом CYP3A4 /CYP3A5 -опосредованно, но с некоторым участием CYP1A2, CYP2C19, UGT1A1 )[1] |
| Устранение период полураспада | 2,5-6,1 часов[1] |
| Экскреция | Фекалии (41%; 12% в неизмененном виде), моча (23%)[1] |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Лиганд PDB | |
| Панель управления CompTox (EPA) | |
| ECHA InfoCard | 100.166.384 |
| Химические и физические данные | |
| Формула | C22ЧАС18N4ОS |
| Молярная масса | 386.47 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
| | |
Акситиниб (AG013736; торговое наименование Инлита) представляет собой небольшую молекулу ингибитор тирозинкиназы разработан Pfizer. Было показано, что он значительно подавляет рост рака груди у животных (ксенотрансплантат ) модели[2] и показал частичные ответы в клинических испытаниях с карцинома почек (RCC)[3] и несколько других типов опухолей.[4]
Он был одобрен для ПКР Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США после небольшого увеличения выживаемость без прогрессирования,[5] хотя были сообщения о смертельных побочных эффектах.[6]
Допуски и показания
Карцинома почек
Он получил одобрение для использования в качестве лечения почечно-клеточного рака от США FDA (27 января 2012 г.), EMA (13 сентября 2012 г.), UK MHRA (3 сентября 2012 г.) и Австралийский TGA (26 июля 2012 г.).[7][8][9][10]
Клинические испытания
Фаза II клиническое испытание показали хороший ответ на комбинированную химиотерапию с гемцитабин для продвинутых панкреатический рак.[11] Однако 30 января 2009 г. компания Pfizer сообщила, что на этапе III клинические испытания Применение препарата в комбинации с гемцитабином не показало улучшенных показателей выживаемости по сравнению с лечением с использованием одного гемцитабина при распространенном раке поджелудочной железы, и испытание было остановлено.[12]
В 2010 г. было проведено исследование III фазы ранее леченных метастазов. карцинома почек (мПКР) показали значительно более длительную выживаемость без прогрессирования по сравнению с сорафениб.[13] В декабре 2011 г. Консультативный комитет по онкологическим препаратам (ODAC) единогласно проголосовали за то, чтобы рекомендовать США FDA одобрить акситиниб в качестве второй линии лечения пациентов с прогрессирующей почечно-клеточной карциномой (ПКР) на основании результатов исследования фазы III, в котором сравнивали акситиниб и сорафениб.[14]
Он также был изучен в сочетании с Ингибитор ALK1 далантерцепт.[15]
Исследование, опубликованное в 2015 году[16] показали, что акситиниб эффективно ингибирует мутированный ген (BCR-ABL1 [T315I]), что часто встречается в хронические миелоидные лейкозы и острый лимфобластный лейкоз у взрослых которые стали устойчивыми к другим ингибиторы тирозинкиназы любить иматиниб. Это один из первых примеров обнаружения нового показания к существующему лекарству путем скрининга известных лекарств с использованием собственных клеток пациента.
Противопоказания
Единственное противопоказание к акситинибу - повышенная чувствительность к акситинибу.[10]
Предостережения включают:[1]
- Гипертония
- Тромбоэмболические (венозные и артериальные) события
- Геморрагические события (включая кровоизлияние в мозг)
- Перфорация желудочно-кишечного тракта и свищ
- Функция щитовидной железы, рекомендуется сначала измерять функцию щитовидной железы, а затем периодически во время лечения акситинибом.
- Прекратите лечение за 24 часа до операции из-за возможных изменений свертывания крови.
- Протеинурия, рекомендуется сначала контролировать протеинурию, а затем периодически во время терапии.
- Сообщается о повышении уровня ферментов печени, рекомендуется регулярно контролировать АСТ, АЛТ и билирубин во время лечения акситинибом.
- Умеренная печеночная недостаточность требует снижения дозы
Побочные эффекты
Диарея, гипертония, повышенная утомляемость, снижение аппетита, тошнота, дисфония, синдром ладони-стопы, снижение веса, рвота, астения и запор являются наиболее частыми побочными эффектами, возникающими у более чем 20% пациентов.[17]
Взаимодействия
Совместное администрирование с сильными CYP3A4 /CYP3A5 По возможности следует избегать применения ингибиторов, поскольку они могут снизить плазменный клиренс акситиниба.[1]
Механизм действия
Считается, что его основным механизмом действия является рецептор фактора роста эндотелия сосудов 1-3, c-KIT и PDGFR торможение, это, в свою очередь, позволяет ему подавлять ангиогенез (образование новых кровеносных сосудов опухолями).[18]
Было также предложено, чтобы он мог действовать, побуждая аутофагия, как и некоторые другие ингибиторы тирозинкиназы, такие как сорафениб.[19]
Также было показано[16] связываться (в конформации, отличной от связывания VEGF) с BCR-ABL слитый белок, специфически ингибирующий лекарственно-устойчивую мутантную изоформу T315I.
| Протеин | IC50 (нМ) |
|---|---|
| VEGFR1 | 0.1 |
| VEGFR2 | 0.2 |
| VEGFR3 | 0.1-0.3 |
| PDGFR | 1.6 |
| c-KIT | 1.7 |
Фармакокинетика
| Биодоступность | ТМаксимум | CМаксимум | AUC | Vd | Связывание с белками плазмы | Ферменты метаболизма | т1/2 | Пути выведения |
|---|---|---|---|---|---|---|---|---|
| 58% | 2,5-4,1 часа | 27,8 нг / мл | 265 нг • ч / мл | 160 л | >99% | Главным образом CYP3A4 и CYP3A5. Меньший вклад от CYP1A2, CYP2C19, UGT1A1 | 2,5-6,1 часов | Фекалии (41%), моча (23%) |
Фирменные наименования
В Бангладеш он находится под торговой маркой Axinix.
В Германия, Швейцария и в других странах Европы он доступен под торговой маркой Inlyta.
использованная литература
- ^ а б c d е ж г час «Дозирование инлита (акситиниба), показания, взаимодействия, побочные эффекты и многое другое». Ссылка на Medscape. WebMD. Получено 25 января 2014.
- ^ Вилмес Л.Дж., Паллавичини М.Г., Флеминг Л.М., Гиббс Дж., Ван Д., Ли К.Л. и др. (Апрель 2007 г.). «AG-013736, новый ингибитор тирозинкиназ рецептора VEGF, подавляет рост рака груди и снижает проницаемость сосудов, что обнаруживается с помощью динамической магнитно-резонансной томографии с контрастированием». Магнитно-резонансная томография. 25 (3): 319–27. Дои:10.1016 / j.mri.2006.09.041. PMID 17371720.
- ^ Рини Б., Рикс О., Буковски Р., Майклсон М.Д., Уилдинг Дж., Худес Дж. И др. (Июнь 2005 г.). «AG-013736, многоцелевой ингибитор рецептора тирозинкиназы, демонстрирует противоопухолевую активность в исследовании фазы 2 цитокинорезистентного метастатического почечно-клеточного рака (ПКР)». Журнал клинической онкологии, Материалы ежегодного собрания ASCO. 23 (16S): 4509. Архивировано с оригинал на 2014-01-26.
- ^ Руго Х.С., Хербст Р.С., Лю Дж., Парк Дж. В., Кис М.С., Штайнфельдт Х.М. и др. (Август 2005 г.). «Испытание фазы I перорального антиангиогенеза AG-013736 у пациентов с запущенными солидными опухолями: фармакокинетические и клинические результаты». Журнал клинической онкологии. 23 (24): 5474–83. Дои:10.1200 / JCO.2005.04.192. PMID 16027439.
- ^ «FDA одобряет Inlyta для лечения прогрессирующей почечно-клеточной карциномы». Drugs.com. 27 января 2012 г.
- ^ Фаубер Дж., Чу Е. (27 октября 2014 г.). «Скользкий спуск: является ли суррогатная конечная точка доказательства эффективности?». MedPage сегодня.
- ^ «INLYTA (акситиниб) таблетка, покрытая пленкой [Pfizer Laboratories Div Pfizer Inc]». DailyMed. Pfizer Laboratories Div Pfizer Inc. Сентябрь 2013 г.. Получено 25 января 2014.
- ^ «Inlyta: EPAR - Информация о продукте» (PDF). Европейское агентство по лекарствам. Pfizer Ltd. 17 декабря 2013 г.. Получено 25 января 2014.
- ^ «Inlyta 1 мг, 3 мг, 5 мг и 7 мг таблетки, покрытые пленочной оболочкой - Сводка характеристик продукта (SPC)». электронный сборник лекарств. Pfizer Limited. 5 декабря 2013. Архивировано с оригинал на 2014-02-22. Получено 25 января 2014.
- ^ а б «ИНФОРМАЦИЯ О ПРОДУКТЕ ИНЛИТА (акситиниб)» (PDF). Услуги электронного бизнеса TGA. Pfizer Australia Pty Ltd. 5 июля 2013 г.. Получено 25 января 2014.
- ^ Spano JP, Chodkiewicz C, Maurel J, Wong R, Wasan H, Barone C и др. (Июнь 2008 г.). «Эффективность гемцитабина плюс акситиниба по сравнению с одним гемцитабином у пациентов с распространенным раком поджелудочной железы: открытое рандомизированное исследование фазы II». Ланцет. 371 (9630): 2101–8. Дои:10.1016 / S0140-6736 (08) 60661-3. PMID 18514303. S2CID 11062859.
- ^ «Лекарство от рака поджелудочной железы Pfizer не работает, испытания остановлены». Рейтер. 30 января 2009 г.
- ^ «Исследование фазы III Pfizer по мПКР дало положительные результаты». 19 ноя 2010.
- ^ «ODAC единодушно поддерживает акситиниб при почечно-клеточной карциноме». 7 декабря 2011 г.
- ^ Комбинация ALK1 / VEGF активна в Advanced RCC. Янв 2017
- ^ а б Пемовска Т., Джонсон Э., Контро М., Репаски Г.А., Чен Дж., Уэллс П. и др. (Март 2015 г.). «Акситиниб эффективно ингибирует BCR-ABL1 (T315I) с четко выраженной конформацией связывания». Природа. 519 (7541): 102–5. Bibcode:2015Натура.519..102П. Дои:10.1038 / природа14119. PMID 25686603. S2CID 4389086.
- ^ «Информация, предписывающая FDA» (PDF). 30 января 2012 г.
- ^ Эскудье Б, Гор М (2011). «Акситиниб для лечения метастатической почечно-клеточной карциномы». Лекарства в исследованиях и разработках. 11 (2): 113–26. Дои:10.2165/11591240-000000000-00000. ЧВК 3585900. PMID 21679004.
- ^ Чжан И, Сюэ Д., Ван Х, Лу М, Гао Б., Цяо Х (январь 2014 г.). «Скрининг ингибиторов киназ, направленных на BRAF, для регулирования аутофагии на основе киназных путей». Отчеты по молекулярной медицине. 9 (1): 83–90. Дои:10.3892 / mmr.2013.1781. PMID 24213221.
