Ритуксимаб - Rituximab
 | |
| Моноклональные антитела | |
|---|---|
| Тип | Целое антитело |
| Источник | Химерный (мышь /человек ) |
| Цель | CD20 |
| Клинические данные | |
| Торговые наименования | Ритуксан, Мабтера, Труксима и др.[1] |
| Другие имена | ритуксимаб-аббс, ритуксимаб-пввр |
| AHFS /Drugs.com | Монография |
| MedlinePlus | a607038 |
| Данные лицензии |
|
| Беременность категория | |
| Маршруты администрация | Внутривенное вливание |
| Класс препарата | Моноклональные антитела |
| Код УВД | |
| Легальное положение | |
| Легальное положение | |
| Фармакокинетический данные | |
| Биодоступность | 100% (IV) |
| Устранение период полураспада | От 30 до 400 часов (зависит от дозы и продолжительности лечения) |
| Экскреция | Неопределенный: при РЭС может происходить фагоцитоз и катаболизм. |
| Идентификаторы | |
| Количество CAS | |
| DrugBank | |
| ChemSpider |
|
| UNII | |
| КЕГГ | |
| ЧЭМБЛ | |
| Панель управления CompTox (EPA) | |
| ECHA InfoCard | 100.224.382 |
| Химические и физические данные | |
| Формула | C6416ЧАС9874N1688О1987S44 |
| Молярная масса | 143860.04 г · моль−1 |
| | |
Ритуксимаб, продается под торговой маркой Ритуксан среди прочего, это лекарство, используемое для лечения некоторых аутоиммунные заболевания и виды рак.[3] Он используется для неходжкинская лимфома, хронический лимфолейкоз, ревматоидный артрит, гранулематоз Вегенера, идиопатическая тромбоцитопеническая пурпура, пузырчатка обыкновенная, миастения и Вирус Эпштейна-Барра -положительный кожно-слизистые язвы.[3][4][5][6] Это дается медленное введение в вену.[3]
Общие побочные эффекты, которые часто возникают в течение двух часов после приема лекарства, включают сыпь, зуд, низкое кровяное давление и одышка.[3] Другие серьезные побочные эффекты включают реактивацию гепатит Б у ранее инфицированных, прогрессирующая мультифокальная лейкоэнцефалопатия, и токсический эпидермальный некролиз.[3][7] Неясно, используется ли во время беременность безопасен для развивающегося плода или новорожденного ребенка.[3][2]
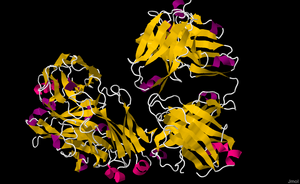
Ритуксимаб - это химерный моноклональное антитело против белка CD20, который в первую очередь находится на поверхности иммунной системы В-клетки.[8] Когда он связывается с этим белком, он вызывает гибель клеток.[3]
Ритуксимаб был одобрен для медицинского применения в 1997 году.[8] Это на Список основных лекарственных средств Всемирной организации здравоохранения.[9] Срок действия патента истек в 2016 году, и ряд биоаналоги были запущены.[10]
Медицинское использование
Ритуксимаб уничтожает как нормальные, так и злокачественные В-клетки которые имеют CD20 на своей поверхности и поэтому используются для лечения заболеваний, которые характеризуются наличием слишком большого количества B-клеток, сверхактивных B-клеток или дисфункциональных B-клеток.[требуется медицинская цитата ]
Ритуксимаб применяется в сочетании с флударабин и циклофосфамид для лечения ранее нелеченого и ранее леченного CD20-положительного хронического лимфолейкоза.[11] Ритуксимаб применяется в сочетании с метотрексат для лечения активного ревматоидного артрита от умеренной до тяжелой степени с неадекватным ответом на один или несколько видов терапии антагонистами TNF.[11] Ритуксимаб применяется в сочетании с глюкокортикоиды для лечения гранулематоза с полиангиитом и микроскопический полиангиит.[11]
Ритуксимаб в комбинации с гиалуронидаза человек, продается под торговыми марками Мабтера СК и Ритуксан Хицела,[12] используется для лечения фолликулярная лимфома, диффузная В-клеточная лимфома большого размера и хронический лимфолейкоз.[13]
Рак крови
Ритуксимаб используется для лечения рак системы белой крови Такие как лейкемии и лимфомы, включая неходжкинскую лимфому, хронический лимфолейкоз и подтип лимфомы Ходжкина с преобладанием лимфоцитов.[14] Это также включает Макроглобулинемия Вальденстрема, разновидность НХЛ.[3]
Аутоиммунные заболевания
Ритуксимаб оказался эффективным ревматоидный артрит лечение в трех рандомизированных контролируемых испытаниях и в настоящее время лицензировано для использования при рефрактерном ревматоидном заболевании.[15] В США он был одобрен FDA для использования в сочетании с метотрексат (MTX) для уменьшения признаков и симптомов у взрослых пациентов с умеренно или сильно активным ревматоидным артритом (РА), у которых был неадекватный ответ на один или несколько анти-TNF-альфа терапия. В Европе лицензия несколько более строгая: она разрешена для использования в комбинации с метотрексатом у пациентов с тяжелым активным РА, у которых неадекватный ответ на одну или несколько анти-TNF терапий.[16]
Есть некоторые доказательства эффективности, но не обязательно безопасность, при ряде других аутоиммунных заболеваний, а ритуксимаб широко используется не по назначению лечить сложные случаи рассеянный склероз,[17][18] системная красная волчанка, хроническая воспалительная демиелинизирующая полинейропатия и аутоиммунный анемии.[19] Наиболее опасным, но одним из самых редких побочных эффектов является: прогрессирующая мультифокальная лейкоэнцефалопатия (ПМЛ) инфекция, которая обычно заканчивается летальным исходом; однако зарегистрировано лишь очень небольшое количество случаев аутоиммунных заболеваний.[19][20]
Другие аутоиммунные заболевания, которые лечили ритуксимабом, включают: аутоиммунная гемолитическая анемия, чистая аплазия эритроцитов, тромботическая тромбоцитопеническая пурпура (ТТП),[21] идиопатическая тромбоцитопеническая пурпура (ИТП),[22][23] Синдром Эванса,[24] васкулит (например, гранулематоз Вегенера ), буллезные кожные заболевания (например, пузырчатка, пемфигоид - с очень обнадеживающими результатами примерно 85% быстрого выздоровления при пузырчатке, согласно исследованию 2006 г.),[25] Тип 1 сахарный диабет, Синдром Шегрена, энцефалит против рецепторов NMDA и Болезнь Девича,[26] Офтальмопатия Грейвса,[27] аутоиммунный панкреатит,[28] Синдром Opsoclonus myoclonus (OMS),[29] и Заболевание, связанное с IgG4.[30] Есть некоторые свидетельства того, что он неэффективен при лечении IgA-опосредованных аутоиммунных заболеваний.[31]
Пересадка органов
Ритуксимаб используется не по прямому назначению при лечении трансплантацияпочки получатели. Этот препарат может быть полезен при трансплантации несовместимых групп крови. Он также используется в качестве индукционной терапии у высокочувствительных пациентов, которым предстоит трансплантация почки. Эффективность ритуксимаба в этой ситуации не доказана, и, как и все истощающие агенты, существует риск инфицирования.[нужна цитата ]
Неблагоприятные события
К серьезным нежелательным явлениям, которые могут привести к смерти или инвалидности, относятся:[11][3]
- Суровый инфузионная реакция.
- Остановка сердца
- Синдром высвобождения цитокинов
- Синдром лизиса опухоли, вызывая острая травма почек
- Инфекции
- Гепатит Б реактивация
- Другие вирусные инфекции
- Прогрессирующая мультифокальная лейкоэнцефалопатия (PML) вызвано JC вирус реактивация[32]
- Иммунная токсичность с истощением В-клеток от 70% до 80% лимфома пациенты
- Легочный токсичность[33]
- Непроходимость кишечника и перфорация[34]
Два пациента с системная красная волчанка умер от прогрессирующая мультифокальная лейкоэнцефалопатия (ПМЛ) после лечения ритуксимабом. PML вызывается активацией JC вирус, распространенный вирус в головном мозге, который обычно скрыт. Реактивация вируса JC обычно приводит к смерти или серьезному повреждению мозга.[35]
По крайней мере, один пациент с ревматоидный артрит развился ПМЛ после лечения ритуксимабом.[36]
Сообщалось, что ритуксимаб является возможным кофактором хронического Гепатит E инфекция у человека с лимфомой. Инфекция гепатита Е обычно острый инфекция, предполагающая, что лекарство в сочетании с лимфомой могло ослабить иммунный ответ организма на вирус.[37]
Механизмы действия
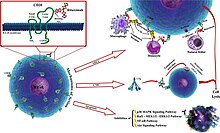

Антитело связывается с белком клеточной поверхности. CD20. CD20 широко экспрессируется на В-клетках, от ранних пре-В-клеток до более поздних дифференциация, но отсутствует на терминально дифференцированных плазматические клетки. Хотя функция CD20 неизвестна, он может играть роль в Ca2+ приток через плазматические мембраны, поддерживая внутриклеточный Ca2+ концентрация и активация B-клеток.
Ритуксимаб относительно неэффективен для уничтожения клеток с низким уровнем CD20 на клеточной поверхности. Он имеет тенденцию прилипать к одной стороне В-клеток, где находится CD20, образуя крышку и притягивая белки на эту сторону. Присутствие кэпа изменяет эффективность естественных киллеров (NK) в разрушении этих B-клеток. Когда NK-клетка защелкивалась на крышке, ее успешное уничтожение составляло 80%. Напротив, когда В-клетке не хватало этого асимметричного белкового кластера, она погибала только в 40% случаев.[39][40]
Обнаружены следующие эффекты:[41]
- В Fc порция ритуксимаба посредников антителозависимая клеточная цитотоксичность (ADCC) и комплемент-зависимая цитотоксичность (CDC).
- Ритуксимаб оказывает общее регулирующее действие на клеточный цикл.
- Предпочтительное удаление злокачественных В-клеток с высоким уровнем CD20 и высокой склонностью к передаче сигналов BCR, особенно при хроническом лимфолейкозе (ХЛЛ).
- Это увеличивается MHC II и молекулы адгезии LFA-1 и LFA-3 (антиген, связанный с функцией лимфоцитов).
- Это вызывает потерю CD23.
- Он подавляет Рецептор В-клеток.
- Это побуждает апоптоз CD20 + клеток.
Комбинированный эффект приводит к элиминации В-клеток (включая раковые) из организма, что позволяет новой популяции здоровых В-клеток развиваться из лимфоидных. стволовые клетки.
Ритуксимаб связывается с аминокислоты 170-173 и 182-185 на CD20, которые физически близки друг к другу в результате дисульфидная связь между аминокислотами 167 и 183.[42]
История
Ритуксимаб был разработан исследователями Набилом Ханной, Митчеллом Реффом и сотрудниками компании IDEC Pharmaceuticals под названием IDEC-C2B8. Патент на лекарство в США был выдан в 1998 году и истек в 2015 году.[43]
На основании его безопасности и эффективности в клинические испытания,[44] ритуксимаб был одобрен США. Управление по контролю за продуктами и лекарствами в 1997 году для лечения B-клеток неходжкинские лимфомы устойчив к другим химиотерапия режимы.[45] Ритуксимаб в сочетании с НАРЕЗАТЬ химиотерапия, превосходит только CHOP в лечении диффузная В-клеточная лимфома большого размера и многие другие В-клеточные лимфомы.[46] В 2010 году он был одобрен Европейская комиссия для поддерживающего лечения после первоначального лечения фолликулярная лимфома.[47]
Ритуксимаб в настоящее время реализуется совместно с Биоген и Genentech в США Hoffmann-La Roche в Канаде и Европейском Союзе, Chugai Pharmaceuticals, Zenyaku Kogyo в Японии и AryoGen в Иране.[нужна цитата ]
Это на Список основных лекарственных средств Всемирной организации здравоохранения.[9]
В 2014 году Genentech реклассифицировала ритуксан как специальный препарат, класс препаратов, которые можно приобрести только у специализированных дистрибьюторов в США.[48] Поскольку скидки и скидки оптовиков больше не действуют, больницы будут платить больше.[48]
Первоначально доступный для внутривенных инъекций (например, более 2,5 часов), в 2016 году он получил одобрение ЕС в составе для подкожных инъекций для CLL.[49]
Срок действия патентов на препарат истек в Европе в феврале 2013 года и в США в сентябре 2016 года.[50] К ноябрю 2018 г.[Обновить], несколько биоаналоги был одобрен в США, Индии, Европейском Союзе, Швейцарии, Японии и Австралии.[51][50][52]
Исследование
Синдром хронической усталости
Ритуксимаб не улучшил симптомы у пациентов с Синдром хронической усталости в испытании, опубликованном в 2019 году.[53][54] У 22% участников были серьезные события.[53] Это потенциальное использование было исследовано после того, как улучшение синдрома хронической усталости было замечено у двух онкологических больных, получавших ритуксимаб.[55]
Интратекальный
При заболеваниях ЦНС можно назначать ритуксимаб. интратекально и эта возможность изучается.[56]
Другие моноклональные препараты против CD20
Эффективность и успех Ритуксимаба привели к разработке некоторых других моноклональных антител против CD20:
- окрелизумаб, гуманизированный (90% -95% человеческий) агент, истощающий В-клетки.
- офатумумаб (HuMax-CD20) агент, полностью разрушающий В-клетки человека.[57]
- Анти-CD20 третьего поколения, такие как обинутузумаб имеют гликоинженерный Fc-фрагмент (Fc)[58] с усиленным связыванием с гамма-рецепторами Fc, которые увеличивают ADCC (антителозависимая клеточная цитотоксичность ).[59] Эта стратегия повышения способности моноклонального антитела индуцировать ADCC использует преимущество того факта, что отображаемый гликан Fc контролирует сродство антитела к рецепторам Fc.[60]
Рекомендации
- ^ Drugs.com Международные торговые марки ритуксимаба В архиве 2016-04-22 в Wayback Machine Доступ к странице 1 апреля 2016 г.
- ^ а б c «Применение ритуксимаба во время беременности». Drugs.com. 16 декабря 2019 г.. Получено 2 февраля 2020.
- ^ а б c d е ж грамм час я «Ритуксимаб». Американское общество фармацевтов систем здравоохранения. В архиве из оригинала 27 марта 2016 г.. Получено 8 декабря 2016.
- ^ Тандан, Руп; Хехир, Майкл К .; Вахид, Вакар; Ховард, Дианта Б. (август 2017 г.). «Лечение ритуксимабом миастении гравис: систематический обзор». Мышцы и нервы. 56 (2): 185–196. Дои:10.1002 / mus.25597. ISSN 1097-4598. PMID 28164324. S2CID 19504332.
- ^ Певица, O; МакКьюн, WJ (май 2017 г.). «Новости поддерживающей терапии гранулематоза с полиангиитом и микроскопическим полиангиитом». Текущее мнение в ревматологии. 29 (3): 248–253. Дои:10.1097 / BOR.0000000000000382. PMID 28306595. S2CID 35805200.
- ^ Дойчинов С.Д., Фенд Ф, Кинтанилья-Мартинес Л. (март 2018 г.). "ВЭБ-положительные лимфопролиферации производных B-T- и NK-клеток в хозяевах без иммунодефицита". Патогены (Базель, Швейцария). 7 (1): 28. Дои:10.3390 / pathogens7010028. ЧВК 5874754. PMID 29518976.
- ^ «Предупреждение в штучной упаковке и новые рекомендации по снижению риска гепатита B». НАС. Управление по контролю за продуктами и лекарствами (FDA). 13 января 2017 г.. Получено 2 февраля 2020.
- ^ а б Босх, Ксавьер; Рамуш-Казальс, Мануэль; Хамашта, Мунтер А. (2013). Лекарства, нацеленные на В-клетки при аутоиммунных заболеваниях. Springer Science & Business Media. С. 1–4. ISBN 9783034807067. В архиве из оригинала от 5 ноября 2017 года.
- ^ а б Всемирная организация здоровья (2019). Типовой список основных лекарственных средств Всемирной организации здравоохранения: 21-й список 2019 г.. Женева: Всемирная организация здравоохранения. HDL:10665/325771. WHO / MVP / EMP / IAU / 2019.06. Лицензия: CC BY-NC-SA 3.0 IGO.
- ^ «Биосимиляры ритуксимаба доказали свою безопасность и эффективность». www.medscape.com. Архивировано из оригинал 15 марта 2018 г.. Получено 29 ноябрь 2017.
- ^ а б c d «Ритуксан-ритуксимаб для инъекций, раствор». DailyMed. 6 ноября 2019 г.. Получено 2 февраля 2020.
- ^ «Мабтера СК / Ритуксан Хицела (ритуксимаб гиалуронидаза)». Рош. Получено 9 августа 2020.
- ^ «Ритуксан, гицеларитуксимаб и гиалуронидаза для инъекций, раствор». DailyMed. 3 декабря 2019 г.. Получено 2 февраля 2020.
- ^ Сайни К.С., Азим Х.А. мл., Кокороччио Э., Ванацци А., Сайни М.Л., Равьеле ПР, Прунери Дж., Пеккатори Ф.А. (2011). «Ритуксимаб при лимфоме Ходжкина: всегда ли цель поражена?». Лечение рака Rev. 37 (5): 385–90. Дои:10.1016 / j.ctrv.2010.11.005. PMID 21183282.
- ^ Эдвардс Дж., Щепански Л., Сечински Дж., Филипович-Сосновска А., Эмери П., Клоуз Д., Стивенс Р., Шоу Т. (2004). «Эффективность В-клеточной терапии ритуксимабом у пациентов с ревматоидным артритом». N Engl J Med. 350 (25): 2572–81. Дои:10.1056 / NEJMoa032534. PMID 15201414.
- ^ Так PP, Kalden JR (2011). «Достижения ревматологии: новая таргетная терапия». Исследования и лечение артрита. 13 (Приложение 1): S5. Дои:10.1186 / 1478-6354-13-S1-S5. ЧВК 3123966. PMID 21624184.
- ^ Макгинли, член парламента; Мосс, БП; Коэн, Дж. А. (январь 2017 г.). «Безопасность моноклональных антител для лечения рассеянного склероза». Экспертное заключение о безопасности лекарственных средств. 16 (1): 89–100. Дои:10.1080/14740338.2017.1250881. PMID 27756172. S2CID 36762194.
- ^ Он, Дайан; Го, Руи; Чжан, Фубо; Чжан, Чао; Донг, Шуай; Чжоу, Хунъюй (6 декабря 2013 г.). «Ритуксимаб при ремиттирующем рассеянном склерозе». Кокрановская база данных систематических обзоров (12): CD009130. Дои:10.1002 / 14651858.CD009130.pub3. ISSN 1469-493X. PMID 24310855.
- ^ а б Пол, Марла (20 мая 2009 г.). «Популярное лекарство от рака, связанное с часто смертельным вирусом, поедающим мозг». Новости и информация Северо-Западного университета. В архиве из оригинала 29 мая 2010 г.. Получено 22 мая 2009.
- ^ «FDA предупреждает об опасениях по поводу безопасности применения ритуксана у новых пациентов». НАС. Управление по контролю за продуктами и лекарствами (FDA) (Пресс-релиз). 18 декабря 2006 г. Архивировано с оригинал 13 мая 2009 г.. Получено 29 апреля 2013.
- ^ Фруассар А., Вейрадье А., Хиэ М., Бенхаму И., Коппо П. (август 2015 г.). «Ритуксимаб при аутоиммунной тромботической тромбоцитопенической пурпуре: история успеха». Eur J Intern Med. 26 (9): 659–65. Дои:10.1016 / j.ejim.2015.07.021. PMID 26293834.
- ^ Брэндструп П., Бьеррум О.В., Нильсен О.Дж. и др. (Апрель 2005 г.). «Лечение химерными моноклональными антителами к CD20 ритуксимабом для лечения рефрактерной идиопатической тромбоцитопенической пурпуры у взрослых». Являюсь. J. Hematol. 78 (4): 275–80. Дои:10.1002 / ajh.20276. PMID 15795920. S2CID 42218074.
- ^ Патель В., Михатов Н., Купер Н., Стаси Р., Каннингем-Рандлс С., Бассел Дж. Б. (2007). «Долгосрочные ответы, наблюдаемые при применении ритуксимаба у пациентов с ИТП» (PDF). Сообщество онкологии. 4 (2): 107. Дои:10.1016 / с 1548-5315 (11) 70061-4. Архивировано из оригинал (PDF) 29 сентября 2007 г.. Получено 18 апреля 2007.
- ^ Shanafelt TD, Madueme HL, Wold RC, Tefferi A (2003). «Ритуксимаб для иммунной цитопении у взрослых: идиопатическая тромбоцитопеническая пурпура, аутоиммунная гемолитическая анемия и синдром Эванса» (PDF). Труды клиники Мэйо. 78 (11): 1340–1346. Дои:10.4065/78.11.1340. PMID 14601692. Архивировано из оригинал (PDF) 13 марта 2006 г.
- ^ A. Razzaque Ahmed, M.D .; Захари Спигельман, доктор медицины; Лиза А. Кавачини, доктор философии; Маршалл Р. Познер, доктор медицины (26 октября 2006 г.). «Лечение обыкновенной пузырчатки ритуксимабом и внутривенным иммуноглобулином». N Engl J Med. 355 (17): 1772–1779. Дои:10.1056 / nejmoa062930. PMID 17065638.
- ^ Джейкоб А., Вайншенкер Б.Г., Виолич I, Маклински Н., Крупп Л., Фокс Р.Дж., Вингерчук Д.М., Боггилд М., Константинеску К.С., Миллер А., Де Анжелис Т., Матиелло М., Кри Б.А. (2008). «Лечение оптического нейромиелита ритуксимабом: ретроспективный анализ 25 пациентов». Arch Neurol. 65 (11): 1443–1448. Дои:10.1001 / archneur.65.11.noc80069. PMID 18779415.
- ^ «Лечение ритуксимабом пациентов с тяжелой кортикостероидной резистентной тироид-ассоциированной офтальмопатией». В архиве с оригинала 22 августа 2017 г.. Получено 19 октября 2011.
- ^ «Иммуномодуляторы и ритуксимаб в лечении аутоиммунного панкреатита». Дои:10.3998 / panc.2013.20. В архиве из оригинала 2 мая 2014 г.. Получено 30 апреля 2014. Цитировать журнал требует
| журнал =(помощь) - ^ Пранзателли, М. Р. (2004). «Иммунологические и клинические реакции на ритуксимаб у ребенка с синдромом опсоклонуса-миоклонуса». Педиатрия. 115 (1): e115–9. Дои:10.1542 / педс.2004-0845. PMID 15601813.
- ^ Хосрошахи, А .; Уоллес, З. С .; Crowe, J. L .; Akamizu, T .; Азуми, А .; Carruthers, M.N .; Chari, S.T .; Della-Torre, E .; Frulloni, L .; Goto, H .; Hart, P.A .; Kamisawa, T .; Kawa, S .; Кавано, М .; Kim, M. H .; Kodama, Y .; Кубота, К .; Lerch, M. M .; Löhr, M .; Masaki, Y .; Matsui, S .; Mimori, T .; Накамура, S .; Nakazawa, T .; Ohara, H .; Окадзаки, К .; Ryu, J.H .; Saeki, T .; Schleinitz, N .; и другие. (2015). «Международное согласованное руководство по ведению и лечению заболеваний, связанных с IgG4». Артрит и ревматология. 67 (7): 1688–1699. Дои:10.1002 / арт.39132. PMID 25809420. S2CID 39750214.
- ^ Хе Й, Шимода М., Оно Й, Вильялобос И.Б., Митра А, Кония Т, Грандо С.А., Зона JJ, Маверакис Э. (2015). «Сохранение аутореактивных IgA-секретирующих В-клеток, несмотря на многочисленные иммунодепрессанты, включая ритуксимаб». JAMA Dermatol. 151 (6): 646–50. Дои:10.1001 / jamadermatol.2015.59. PMID 25901938.
- ^ Molloy, Eamonn S .; Калабрезе, Леонард Х. (2012). «Прогрессирующая мультифокальная лейкоэнцефалопатия, связанная с иммуносупрессивной терапией при ревматических заболеваниях: возрастающая роль биологических методов лечения». Артрит и ревматизм. 64 (9): 3043–3051. Дои:10.1002 / арт.34468. PMID 22422012.
- ^ Бертон С., Качмарски Р., Ян-Мохамед Р. (2003). «Интерстициальный пневмонит, связанный с терапией ритуксимабом». N Engl J Med. 348 (26): 2690–1, обсуждение 2690–1. Дои:10.1056 / NEJM200306263482619. PMID 12826649.
- ^ «Сообщения об непроходимости и перфорации кишечника при применении РИТУКСАНА (ритуксимаб)» (PDF). Рош Канада. 10 ноября 2006 г. Архивировано с оригинал (PDF) 27 марта 2014 г.
- ^ «Ритуксимаб (продается как Ритуксан) Информация». НАС. Управление по контролю за продуктами и лекарствами (FDA). 23 июля 2015 г. В архиве из оригинала 15 ноября 2009 г.. Получено 15 ноября 2009.
- ^ «Ритуксимаб, РА и ПМЛ» (PDF). НАС. Управление по контролю за продуктами и лекарствами (FDA). Архивировано из оригинал (PDF) 16 сентября 2008 г.. Получено 14 сентября 2008.
- ^ Кристон, Левенте (2009). «Проблемы отчетности метаанализа диагностических исследований точности». Анналы внутренней медицины. 150 (6): 430. Дои:10.7326/0003-4819-150-6-200903170-00025. PMID 19293085.
- ^ Сейфизаде, Наргес; Сейфизаде, Найер; Hasenkamp, J; Уэрта-Йепез, S (2016). «Молекулярный взгляд на ритуксимаб: моноклональные антитела против В-клеточной неходжкинской лимфомы и других заболеваний». Crit Rev Oncol Hematol. 97: 275–290. Дои:10.1016 / j.critrevonc.2015.09.001. PMID 26443686.
- ^ Рудницкая, Д .; Oszmiana, A .; Финч, Д. К .; Стрикленд, I .; Schofield, D. J .; Lowe, D.C .; Слиман, М. А .; Дэвис, Д. М. (2013). «Ученые выясняют, почему определенное лекарство от рака так эффективно». Кровь. 121 (23): 4694–4702. Дои:10.1182 / кровь-2013-02-482570. PMID 23613524. В архиве из оригинала 3 мая 2013 г.. Получено 29 апреля 2013.
- ^ Рудницкая, Д .; Oszmiana, A .; Финч, Д. К .; Стрикленд, I .; Schofield, D. J .; Lowe, D.C .; Слиман, М. А .; Дэвис, Д. М. (2013). «Ритуксимаб вызывает поляризацию В-клеток, которая усиливает его терапевтическую функцию при опосредованной NK-клетками антителозависимой клеточной цитотоксичности». Кровь. 121 (23): 4694–4702. Дои:10.1182 / кровь-2013-02-482570. PMID 23613524.
- ^ Шоу, Т. (2003). «В-клеточная терапия ревматоидного артрита: опыт ритуксимаба (анти-CD20)». Анналы ревматических болезней. 62 (90002): 55ii – 59. Дои:10.1136 / ard.62.suppl_2.ii55. ЧВК 1766758. PMID 14532151.
- ^ Связующее М, Отто Ф, Mertelsmann R, Велкен Х., Трепель М. (2006). «Эпитоп, распознаваемый ритуксимабом». Кровь. 108 (6): 1975–1978. Дои:10.1182 / кровь-2006-04-014639. PMID 16705086.CS1 maint: несколько имен: список авторов (связь)
- ^ DrugBank DB00073 В архиве 2014-01-05 в Wayback Machine
- ^ Мэлони Д.Г., Грилло-Лопес А.Дж., Уайт К.А. и др. (Сентябрь 1997 г.). «Терапия моноклональными антителами IDEC-C2B8 (ритуксимаб) к CD20 у пациентов с рецидивирующей неходжкинской лимфомой низкой степени злокачественности». Кровь. 90 (6): 2188–95. Дои:10.1182 / кровь.V90.6.2188. PMID 9310469.
- ^ Скотт, Шейн Д. (1998). «Ритуксимаб: новое терапевтическое моноклональное антитело для неходжкинской лимфомы». Онкологическая практика. 6 (3): 195–197. Дои:10.1046 / j.1523-5394.1998.006003195.x. PMID 9652253.
- ^ Принципы внутренней медицины Харрисона, Лонго и др. McGraw Hill Medical 2011 стр.931
- ^ «Рош получает разрешение ЕС на поддерживающую терапию фолликулярной лимфомы». 29 октября 2010 г. В архиве из оригинала 31 октября 2010 г.
- ^ а б Сапорито, Билл (27 октября 2014 г.). "Больницы в ярости из-за повышения цен на лекарства от рака". Время. В архиве из оригинала 20 октября 2015 г.. Получено 26 октября 2015.
- ^ «ЕС одобрил второе показание для подкожной формы ритуксимаба Рош». В архиве из оригинала 7 июня 2016 г.. Получено 9 июн 2016.
- ^ а б «Биосимиляры Ритуксимаба». Инициатива по дженерикам и биосимилярам. 14 апреля 2017. В архиве из оригинала 31 марта 2017 г.. Получено 29 апреля 2017.
- ^ «FDA одобрило первый биоаналог для лечения взрослых пациентов с неходжкинской лимфомой». НАС. Управление по контролю за продуктами и лекарствами (FDA) (Пресс-релиз). 28 ноября 2018 г.. Получено 11 ноября 2019.
- ^ Лахири, Диптенду; Остерман, Синтия (2 ноября 2018 г.). «Новартис отказывается от одобрения в США биоподобного ритуксимаба». Рейтер. Получено 3 ноября 2018.
- ^ а б Флюж, Эйстейн; Rekeland, Ingrid G .; Льен, Катарина; Турмер, Ханне; Borchgrevink, Petter C .; Шефер, Кристоф; Сёрланд, Кари; Асмус, Йорг; Кториду-Вален, Ирини (2 апреля 2019 г.). «Истощение В-лимфоцитов у пациентов с миалгическим энцефаломиелитом / синдромом хронической усталости: рандомизированное, двойное слепое, плацебо-контролируемое исследование». Анналы внутренней медицины. 170 (9): 585–593. Дои:10.7326 / M18-1451. ISSN 0003-4819. PMID 30934066. S2CID 91186383.
- ^ Такер, Мириам Э. (2 апреля 2019 г.). «Ритуксимаб не улучшает симптоматику у пациентов с ME / CFS». Medscape.
- ^ Кастро-Марреро, Иисус; Саес-Франкас, Найя; Сантильо, Дафна; Алегри, Хосе (2017). «Лечение и лечение синдрома хронической усталости / миалгического энцефаломиелита: все дороги ведут в Рим». Британский журнал фармакологии. 174 (5): 345–369. Дои:10.1111 / bph.13702. ЧВК 5301046. PMID 28052319.
- ^ Боннан, М. Феррари, S; Bertandeau, E; Демаслес, S; Krim, E; Микель, М; Баррозу, Б. (2014). «Интратекальная терапия ритуксимабом при рассеянном склерозе: обзор доказательств, подтверждающих необходимость будущих исследований». Текущие цели в отношении лекарств. 15 (13): 1205–14. Дои:10.2174/1389450115666141029234644. PMID 25355180.
- ^ "Genmab.com / HuMax-CD20 (офатумумаб)". Архивировано из оригинал 11 сентября 2007 г.. Получено 3 декабря 2007.
- ^ «ФК-структура». В архиве из оригинала 10 ноября 2007 г.. Получено 3 декабря 2007.
- ^ Экклс, С.А. (2001). «Моноклональные антитела против рака:« волшебные пули »или просто спусковой крючок?». Исследование рака груди. 3 (2): 86–90. Дои:10.1186 / bcr276. ЧВК 138676. PMID 11250751.
- ^ Маверакис Э., Ким К., Шимода М., Гершвин М., Патель Ф., Уилкен Р., Райчаудхури С., Рухак Л. Р., Лебрилла CB (2015). «Гликаны в иммунной системе и измененная теория аутоиммунитета гликанов: критический обзор». J Аутоиммунный. 57 (6): 1–13. Дои:10.1016 / j.jaut.2014.12.002. ЧВК 4340844. PMID 25578468.
внешняя ссылка
- «Ритуксимаб». Портал информации о наркотиках. Национальная медицинская библиотека США.
- «Смесь гиалуронидазы с ритуксимабом». Портал информации о наркотиках. Национальная медицинская библиотека США.
- «Ритуксимаб и гиалуронидаза (профессиональные консультации пациентов)». Drugs.com.
- «Инъекции ритуксимаба и гиалуронидазы для человека». MedlinePlus.
