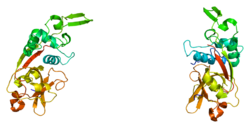Катепсин Z - Википедия - Cathepsin Z
Катепсин Z, также называемый катепсин X или же катепсин Р, это белок что у людей кодируется CTSZ ген.[5][6] Он является членом семейства протеаз цистеин-катепсина, которое состоит из 11 членов.[7] Как один из 11 катепсинов, катепсин Z имеет отличительные черты от других. Сообщалось, что катепсин Z участвует в рак злокачественность и воспаление.
Структура
Ген
В CTSZ ген расположен в 20q13.32 на хромосома 20, состоящий из 6 экзоны. Обнаружено как минимум два варианта транскрипта этого гена, но установлена полноразмерная природа только одного из них.[6]
Протеин
Катепсин Z характеризуется необычным и уникальным 3-аминокислота вставка в высококонсервативную область между глутамин предполагаемой оксинионной дыры и активного центра цистеин. Про-область катепсина Z не имеет существенного сходства с последовательностями других семейств катепсина.[8] Он содержит всего 41 аминокислотный остаток без консервативного мотива ERFNIN или GNFD, обнаруженного в других цистеиновых протеиназах. Кроме того, последовательность прорегиона не содержит остатка лизина.
Функция
Белок, кодируемый этим геном, является лизосомальной цистеиновой протеиназой и членом семейства пептидаз С1. Он проявляет как карбоксимонопептидазную, так и карбоксидипептидазную активности. На сегодняшний день идентифицировано одиннадцать цистеиновых протеиназ человека, в том числе катепсин B, катепсин С, катепсин G, катепсин H, катепсин К, катепсин L, катепсин L2 или V, катепсин О, катепсин S, катепсин Z и катепсин W. Эти цистеиновые протеиназы принадлежат к семейству папаина и представляют собой основной компонент лизосомальной протеолитической системы. Помимо того, что эти протеиназы играют важную роль в деградации и обмене белков, они, по-видимому, играют внеклеточную роль в ряде нормальных и патологических состояний. Катепсин Z человека имеет отличительные черты от других цистеиновых протеаз человека.[9] Это экзопептидаза со строгой карбоксипептидазной активностью, тогда как большинство других катепсинов являются эндопептидазами.[7] Катепсин Z имеет открытую интегрин -связывающий мотив Arg-Gly-Asp в пропептиде фермента, посредством которого катепсин Z, как было показано, взаимодействует с несколькими интегринами во время нормального гомеостаз, иммунные процессы и рак.[10][11][12][13] Также показано, что он связывает клеточную поверхность гепарин сульфатные протеогликаны, указывающие на возможные функции в клеточная адгезия и фагоцитоз.[14]
Клиническое значение
Этот ген повсеместно экспрессируется в линиях раковых клеток и первичных опухолях и, подобно другим членам этого семейства, может участвовать в онкогенезе. Например, катепсин Z способствует инвазии и миграции через некаталитический механизм, предполагая, что несколько способов клеточной инвазии могут быть вовлечены в злокачественное новообразование.[13] Сообщается также, что катепсин Z обладает защитной, но не протеолитической функцией при воспалительном заболевании желудка.[15] В другом исследовании сообщается, что катепсин Z может отвечать за: дофамин гибель нейрона и, таким образом, вовлечена в патогенный каскад.[16] Однонуклеотидный полиморфизм в CTSZ обнаружен связанный с туберкулез восприимчивость, что указывает на то, что пути с участием этого белка могут дать новые методы лечения туберкулеза.[17]
Взаимодействия
Катепсин Z показал взаимодействовать со следующими белками: CEP55, FBXO6, KIFC1, KRT40, КРТАП5-9, КРТАП5-9, LYPLAL1, MID2, MSN, MTUS2, NOTCH2NL, PLK2, PLSCR1, SGOL2, и SPRED2.[18]
Катепсин Z также может взаимодействовать с:
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000101160 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000016256 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Сантамария I, Веласко Дж., Пендас А.М., Фуэйо А., Лопес-Отин С. (июль 1998 г.). «Катепсин Z, новая цистеиновая протеиназа человека с коротким пропептидным доменом и уникальным расположением в хромосоме». Журнал биологической химии. 273 (27): 16816–23. Дои:10.1074 / jbc.273.27.16816. PMID 9642240.
- ^ а б "Entrez Gene: CTSZ катепсин Z".
- ^ а б Turk V, Stoka V, Vasiljeva O, Renko M, Sun T, Turk B, Turk D (январь 2012 г.). «Цистеиновые катепсины: от структуры, функции и регуляции к новым границам». Biochimica et Biophysica Acta (BBA) - Белки и протеомика. 1824 (1): 68–88. Дои:10.1016 / j.bbapap.2011.10.002. ЧВК 7105208. PMID 22024571.
- ^ Нэглер Д.К., Чжан Р., Там В., Сулеа Т., Пурисима Е.О., Менард Р. (сентябрь 1999 г.). «Катепсин X человека: цистеиновая протеаза с уникальной карбоксипептидазной активностью». Биохимия. 38 (39): 12648–54. Дои:10.1021 / bi991371z. PMID 10504234.
- ^ Нэглер Д.К., Менар Р. (август 1998 г.). «Человеческий катепсин X: новая цистеиновая протеаза семейства папаина с очень короткой прорегионом и уникальными вставками». Письма FEBS. 434 (1–2): 135–9. Дои:10.1016 / s0014-5793 (98) 00964-8. PMID 9738465. S2CID 22899822.
- ^ Lechner AM, Assfalg-Machleidt I, Zahler S, Stoeckelhuber M, Machleidt W, Jochum M, Nägler DK (декабрь 2006 г.). «RGD-зависимое связывание прокатепсина X с интегрином alphavbeta3 опосредует клеточно-адгезивные свойства». Журнал биологической химии. 281 (51): 39588–97. Дои:10.1074 / jbc.M513439200. PMID 17065156.
- ^ Кос Дж., Джевникар З., Обермайер Н. (апрель – июнь 2009 г.). «Роль катепсина X в передаче сигналов клеток». Адгезия и миграция клеток. 3 (2): 164–6. Дои:10.4161 / cam.3.2.7403. ЧВК 2679876. PMID 19262176.
- ^ Обермайер Н., Свайгер У., Богио М., Джерас М., Кос Дж. (Ноябрь 2008 г.). «Созревание дендритных клеток зависит от протеолитического расщепления катепсином X». Журнал биологии лейкоцитов. 84 (5): 1306–15. Дои:10.1189 / jlb.0508285. ЧВК 3252843. PMID 18701767.
- ^ а б c Аккари Л., Гочева В., Кестер Дж. К., Хантер К. Э., Квик М. Л., Севенич Л., Ван Х. В., Петерс С., Тан Л. Х., Климстра Д. С., Райнхекель Т., Джойс Дж. А. (октябрь 2014 г.). «Различные функции катепсина Z, полученного из макрофагов и раковых клеток, объединяются, чтобы способствовать злокачественному образованию опухоли через взаимодействия с внеклеточным матриксом». Гены и развитие. 28 (19): 2134–50. Дои:10.1101 / гад.249599.114. ЧВК 4180975. PMID 25274726.
- ^ а б Teller A, Jechorek D, Hartig R, Adolf D, Reißig K, Roessner A, Franke S (январь 2015 г.). «Нарушение регуляции апоптотических сигнальных путей за счет взаимодействия RPLP0 и катепсина X / Z при раке желудка». Патология, исследования и практика. 211 (1): 62–70. Дои:10.1016 / j.prp.2014.09.005. PMID 25433997.
- ^ Крюгер С., Бернхардт А., Калински Т., Бальденспергер М., Зех М., Теллер А., Адольф Д., Райнхекель Т., Ресснер А., Кестер Д. (2013). «Индукция предраковых ответов хозяина за счет дефицита катепсина x / z у мышей, инфицированных Helicobacter pylori». PLOS ONE. 8 (7): e70242. Дои:10.1371 / journal.pone.0070242. ЧВК 3728094. PMID 23936173.
- ^ Пишлар А.Х., Зидар Н., Кикель Д., Кос Дж. (Июль 2014 г.). «Катепсин X способствует апоптозу клеток PC12 и SH-SY5Y, вызванному 6-гидроксидофамином». Нейрофармакология. 82: 121–31. Дои:10.1016 / j.neuropharm.2013.07.040. PMID 23958447. S2CID 22499368.
- ^ Адамс Л.А., Мёллер М., Небель А., Шрайбер С., ван дер Мерве Л., ван Хелден П.Д., Хоал Э.Г. (июнь 2011 г.). «Полиморфизмы промотора MC3R и CTSZ 3'UTR связаны с восприимчивостью к туберкулезу». Европейский журнал генетики человека. 19 (6): 676–81. Дои:10.1038 / ejhg.2011.1. ЧВК 3110050. PMID 21368909.
- ^ «Сеть взаимодействия ЦТСЗ». BioGRID. Получено 6 августа 2016.
- ^ Хафнер А., Главан Г., Обермайер Н., Живин М., Шлибс Р., Кос Дж. (Август 2013 г.). «Нейропротекторная роль γ-енолазы в микроглии на мышиной модели болезни Альцгеймера регулируется катепсином X». Ячейка старения. 12 (4): 604–14. Дои:10.1111 / acel.12093. PMID 23621429. S2CID 23835547.
дальнейшее чтение
- Нэглер Д.К., Менар Р. (август 1998 г.). «Человеческий катепсин X: новая цистеиновая протеаза семейства папаина с очень короткой прорегионом и уникальными вставками». Письма FEBS. 434 (1–2): 135–9. Дои:10.1016 / S0014-5793 (98) 00964-8. PMID 9738465. S2CID 22899822.
- Pungercar J, Ивановский G (2000). «Идентификация и молекулярное клонирование катепсина P, новой предполагаемой цистеиновой протеазы человека семейства папаина». Pflügers Archiv. 439 (3 Прил.): R116–8. Дои:10.1007 / s004240000112. PMID 10653162. S2CID 22775842.
- Пунгеркар Дж., Вийяк А., Ивановски Г., Крижай И. (2000). «Тканевая экспрессия и иммунолокализация нового человеческого катепсина P». Pflügers Archiv. 439 (3 Прил.): R119–21. Дои:10.1007 / s004240000113. PMID 10653163. S2CID 22728027.
- Сивараман Дж., Нэглер Д.К., Чжан Р., Менард Р., Сиглер М. (январь 2000 г.). «Кристаллическая структура прокатепсина X человека: цистеиновая протеаза с прорегионом, ковалентно связанным с активным сайтом цистеина». Журнал молекулярной биологии. 295 (4): 939–51. Дои:10.1006 / jmbi.1999.3410. PMID 10656802.
- Гункар Г., Клеменчич I, Тюрк Б, Тюрк V, Караогланович-Кармона А., Джулиано Л., Тюрк Д. (март 2000 г.). «Кристаллическая структура катепсина X: триггер кольца His23 позволяет карбоксимонопептидазной и карбоксидипептидазной активности протеазы». Структура. 8 (3): 305–13. Дои:10.1016 / S0969-2126 (00) 00108-8. PMID 10745011.
- Deussing J, von Olshausen I, Peters C (апрель 2000 г.). «Мышиный и человеческий катепсин Z: клонирование кДНК, характеристика генов и хромосомная локализация». Biochimica et Biophysica Acta (BBA) - Структура и экспрессия гена. 1491 (1–3): 93–106. Дои:10.1016 / s0167-4781 (00) 00021-x. PMID 10760573.
- Bonthron DT, Hayward BE, Moran V, Strain L (август 2000 г.). «Характеристика TH1 и CTSZ, двух не импринтированных генов ниже GNAS1 в хромосоме 20q13». Генетика человека. 107 (2): 165–75. Дои:10.1007 / s004390000344. PMID 11030415. S2CID 25570066.
- Хартли Дж. Л., Темпл Г. Ф., Браш Массачусетс (ноябрь 2000 г.). «Клонирование ДНК с использованием сайт-специфической рекомбинации in vitro». Геномные исследования. 10 (11): 1788–95. Дои:10.1101 / гр.143000. ЧВК 310948. PMID 11076863.
- Simpson JC, Wellenreuther R, Poustka A, Pepperkok R, Wiemann S (сентябрь 2000 г.). «Систематическая субклеточная локализация новых белков, идентифицированных с помощью крупномасштабного секвенирования кДНК». Отчеты EMBO. 1 (3): 287–92. Дои:10.1093 / embo-reports / kvd058. ЧВК 1083732. PMID 11256614.
- Wiemann S, Arlt D, Huber W., Wellenreuther R, Schleeger S, Mehrle A, Bechtel S, Sauermann M, Korf U, Pepperkok R, Sültmann H, Poustka A (октябрь 2004 г.). «От ORFeome к биологии: конвейер функциональной геномики». Геномные исследования. 14 (10B): 2136–44. Дои:10.1101 / гр.2576704. ЧВК 528930. PMID 15489336.
- Пузер Л., Баррос Н.М., Оливейра В., Джулиано М.А., Лу Г., Хассанейн М., Джулиано Л., Мейсон Р.В., Кармона А.К. (март 2005 г.). «Определение субстратной специфичности катепсина Р мыши». Архивы биохимии и биофизики. 435 (1): 190–6. Дои:10.1016 / j.abb.2004.12.007. PMID 15680921.
- Мехрле А., Розенфельдер Х., Шупп И., дель Валь С., Арльт Д., Хане Ф., Бектель С., Симпсон Дж., Хофманн О., Хиде В., Глаттинг К. Х., Хубер В., Пепперкок Р., Поустка А., Виман С. (январь 2006 г.). «База данных LIFEdb в 2006 году». Исследования нуклеиновых кислот. 34 (Выпуск базы данных): D415–8. Дои:10.1093 / nar / gkj139. ЧВК 1347501. PMID 16381901.
- Lechner AM, Assfalg-Machleidt I, Zahler S, Stoeckelhuber M, Machleidt W, Jochum M, Nägler DK (декабрь 2006 г.). «RGD-зависимое связывание прокатепсина X с интегрином alphavbeta3 опосредует клеточно-адгезивные свойства». Журнал биологической химии. 281 (51): 39588–97. Дои:10.1074 / jbc.M513439200. PMID 17065156.