Лямбда-фаг - Lambda phage
Эта статья поднимает множество проблем. Пожалуйста помоги Улучши это или обсудите эти вопросы на страница обсуждения. (Узнайте, как и когда удалить эти сообщения-шаблоны) (Узнайте, как и когда удалить этот шаблон сообщения)
|
| Вирус эшерихии Лямбда | |
|---|---|
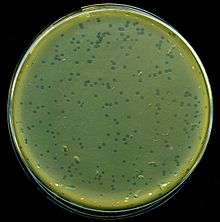 | |
| Бляшки лизиса лямбда-фага на Кишечная палочка бактерии | |
| Классификация вирусов | |
| (без рейтинга): | Вирус |
| Область: | Дуплоднавирия |
| Королевство: | Heunggongvirae |
| Тип: | Уровирикота |
| Учебный класс: | Caudoviricetes |
| Заказ: | Caudovirales |
| Семья: | Siphoviridae |
| Род: | Лямбдавирус |
| Разновидность: | Вирус эшерихии Лямбда |
Фаг энтеробактерий λ (лямбда-фаг, колифаг λ, официально Вирус эшерихии Лямбда) - это бактериальный вирус, или бактериофаг, который заражает виды бактерий кишечная палочка (Кишечная палочка). Это было обнаружено Эстер Ледерберг в 1950 г.[1] Дикий тип этого вируса имеет умеренный жизненный цикл, который позволяет ему либо находиться в пределах геном своего хозяина через лизогения или войти в литический фаза, во время которой он убивает и лизирует клетку, чтобы произвести потомство. Штаммы лямбда, мутировавшие в определенных сайтах, не способны лизогенизировать клетки; вместо этого они растут и вступают в литический цикл после суперинфекции уже лизогенизированной клетки.[2]
Фаговая частица состоит из головы (также известной как капсид ), хвост и волокна хвоста (см. изображение вируса ниже). Головка содержит двухцепочечную линейную ДНК геном. Во время заражения фаговая частица распознает своего хозяина и связывается с ним, Кишечная палочка, в результате чего ДНК в голове фага выбрасывается через хвост в цитоплазму бактериальной клетки. Обычно "литический цикл "следует, где лямбда ДНК реплицируется и в клетке образуются новые фаговые частицы. Затем клетка лизис, высвобождая содержимое клетки, включая собранные вирионы, в окружающую среду. Однако при определенных условиях ДНК фага может интегрироваться в хромосому клетки-хозяина в лизогенный путь. В этом состоянии λ-ДНК называется профаг и проживает в геном без видимого вреда для хозяина. Хост называется лизоген когда присутствует профаг. Этот профаг может войти в литический цикл, когда лизоген входит в стрессовое состояние.
Анатомия

Вирусная частица состоит из головы и хвоста, которые могут иметь хвостовые волокна. Вся частица состоит из 12–14 различных белков, всего более 1000 белковых молекул, и одной молекулы ДНК, расположенной в головке фага. Однако до сих пор не совсем ясно, входят ли белки L и M в состав вириона.[3] Все охарактеризованные лямбдоидные фаги обладают механизмом антитерминации транскрипции, опосредованным N-белком, за исключением фага HK022. [4]

В геном содержит 48 490 пар оснований двухцепочечной линейной ДНК с одноцепочечными сегментами из 12 оснований на обоих 5'-концах.[5] Эти два однонитевых сегмента являются «липкими концами» того, что называется потому что сайт. В потому что сайт циркулирует ДНК в цитоплазме хозяина. Следовательно, в кольцевой форме геном фага имеет длину 48 502 пары оснований.[5] Лямбда-геном можно вставить в Кишечная палочка хромосома и тогда называется профагом. См. Подробности в разделе ниже.
Жизненный цикл
Инфекционное заболевание
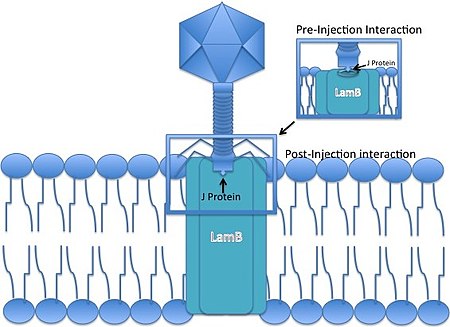
Лямбда-фаг - это фаг с неконтрактильным хвостом, что означает, что во время инфекции он не может «протолкнуть» свою ДНК через мембрану бактериальной клетки. Вместо этого он должен использовать существующий путь для вторжения в клетку-хозяина, развив кончик своего хвоста, чтобы взаимодействовать с определенной порой, чтобы позволить проникнуть своей ДНК в клетку-хозяина.
- Бактериофаг Лямбда связывается с Кишечная палочка клетка с помощью своего белка J в кончике хвоста. Белок J взаимодействует с внешней мембраной мальтозы. порин (продукт ягненок ген) из Кишечная палочка,[6] молекула порина, которая является частью мальтоза оперон.
- Геном линейного фага вводится через внешнюю мембрану.
- ДНК проходит через комплекс пермеазы маннозы во внутренней мембране.[7][8] (кодируется генами manXYZ) и немедленно циркулирует с помощью потому что сайты, 12-основание G-C-богатые слипчивые "липкие концы". Концы одноцепочечной вирусной ДНК лигируются хозяином. ДНК-лигаза. Обычно не принято во внимание, что липкие концы лямбда длиной 12 п.н. были предметом первого прямого нуклеотидного секвенирования биологической ДНК.[9].

- Хозяин ДНК-гираза ставит отрицательный суперспирали в кольцевой хромосоме, заставляя A-T-богатые области раскручиваться и управлять транскрипцией.
- Транскрипция начинается с учредительного пL, пр и пР' промоутеры производство «немедленных» транскриптов. Сначала они выражают N и Cro гены, продуцирующие N, Cro и короткий неактивный белок.
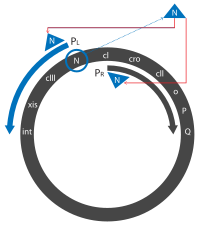
- Кро привязывается к OR3, предотвращая доступ к пRM промотор, предотвращающий экспрессию cI ген. N связывается с двумя Орех (N использования) сайтов, один в N ген в пL рамки считывания и одна в Cro ген в пр рамка чтения.
- Белок N - это антитерминатор, и функции, задействуя транскрибирующий РНК-полимераза в определенных сайтах зарождающейся транскрибируемой мРНК. Когда РНК-полимераза транскрибирует эти области, рекрутирует N и образует комплекс с несколькими белками Nus хозяина. Этот комплекс пропускает большинство терминирующих последовательностей. Расширенные стенограммы ("поздние ранние" стенограммы) включают N и Cro гены вместе с cII и cIII гены и xis, int, О, п и Q гены обсуждаются позже.
- Белок cIII защищает белок cII от протеолиза под действием FtsH (мембраносвязанный незаменимый компонент). E. кишечная палочка протеаза), действуя как конкурентный ингибитор. Это торможение может вызвать бактериостатический состояние, благоприятствующее лизогении. cIII также напрямую стабилизирует белок cII.[10]
При первоначальном заражении стабильность cII определяет образ жизни фага; стабильный cII приведет к лизогенному пути, тогда как если cII распадается, фаг переходит в литический путь. Низкая температура, голодание клеток и высокая множественность заражения (MOI), как известно, способствуют лизогении (см. Обсуждение ниже).
N антитерминация
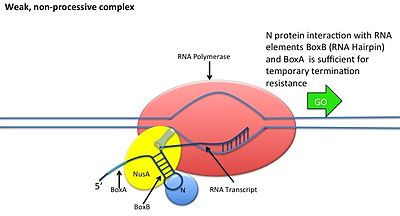
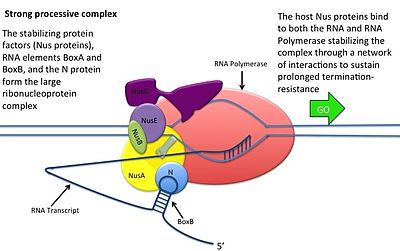
Это происходит без взаимодействия белка N с ДНК; вместо этого белок связывается со свежеотранскрибированной мРНК. Сайты орехов содержат 3 консервативных «ящика», из которых важен только BoxB.
- Последовательности РНК boxB расположены близко к 5'-концу транскриптов pL и pR. При транскрибировании каждая последовательность образует структуру петли шпильки, с которой может связываться белок N.
- Белок N связывается с boxB в каждом транскрипте и связывается с транскрибирующей РНК-полимеразой посредством образования петли РНК. Комплекс N-RNAP стабилизируется за счет последующего связывания нескольких белков Nus хозяина (вещества утилизации N) (которые включают факторы терминации транскрипции / антитерминации и, как ни странно, субъединицу рибосомы).
- Весь комплекс (включая границу Орех сайт на мРНК) продолжает транскрипцию и может пропускать терминирующие последовательности.
Литический жизненный цикл
Это жизненный цикл, которому фаг следует после большинства инфекций, когда белок cII не достигает достаточно высокой концентрации из-за деградации, поэтому не активирует свои промоторы.
- «Поздние ранние» стенограммы продолжают составляться, в том числе xis, int, Q и гены репликации лямбда-генома (OP). Cro доминирует над сайтом репрессора (см. Раздел «Репрессор» ), подавляя синтез из пRM промотор (который является промотором лизогенного цикла).
- Белки O и P инициируют репликацию хромосомы фага (см. «Литическая репликация»).
- Q, другой антитерминатор, привязан к Qut места.
- Транскрипция из пР' промотор теперь может расширяться, чтобы производить мРНК для лизиса, а также белков головы и хвоста.
- Структурные белки и фаговые геномы самоорганизуются в новые фаговые частицы.
- Продукты генов S,р, Rz и Rz1 вызывают лизис клеток. S - это холин, небольшой мембранный белок, который во время, определяемый последовательностью белка, внезапно делает дыры в мембране. R - это эндолизин, фермент, который выходит через S-отверстия и расщепляет клеточную стенку. Rz и Rz1 представляют собой мембранные белки, которые образуют комплекс, который каким-то образом разрушает внешнюю мембрану после того, как эндолизин разрушил клеточную стенку. Для лямбда дикого типа лизис происходит примерно через 50 минут после начала инфекции и высвобождает около 100 вирионов.
Правая транскрипция
Правая транскрипция выражает О, п и Q гены. O и P ответственны за инициацию репликации, а Q - еще один антитерминатор, который позволяет экспрессировать гены головы, хвоста и лизиса из пР'.
Литическая репликация
- В течение первых нескольких циклов репликации лямбда-геном подвергается θ репликация (по кругу).
- Это инициируется в Ори сайт, расположенный в О ген. Белок O связывает Ори сайт, а белок P связывает субъединицу DnaB аппарата репликации хозяина, а также связывает O. Это эффективно управляет ДНК-полимеразой хозяина.
- Вскоре фаг переключается на репликация катящегося круга аналогично тому, что используется фагом M13. ДНК разорвана, и 3 ’конец служит праймером. Обратите внимание, что при этом высвобождаются не отдельные копии генома фага, а одна длинная молекула с множеством копий генома: объединитель.
- Эти конкатемеры расщеплены на своих потому что сайты, как они упакованы. Упаковка не может происходить из кольцевой ДНК фага, только из конкатомерной ДНК.
Q антитерминация



Q похож на N по своему действию: Q связывается с РНК-полимераза в Qut сайты и результирующий комплекс могут игнорировать терминаторы, однако механизм сильно отличается; белок Q сначала связывается с последовательностью ДНК, а не с последовательностью мРНК.[12]
- В Qut сайт находится очень близко к пР' промотор, достаточно близкий, чтобы σ-фактор не высвобождался из холофермента РНК-полимеразы. Часть Qut сайт похож на -10 Прибновый ящик, вызывая приостановку действия холоэнзима.
- Затем белок Q связывает и вытесняет часть σ-фактора, и транскрипция возобновляется.
- Гены головы и хвоста транскрибируются, и соответствующие белки собираются самостоятельно.
Левая транскрипция

Левая транскрипция выражает игра, красный, xis, и int гены. В рекомбинации участвуют гамма- и красный белки. Gam также важен в том смысле, что он ингибирует нуклеазу RecBCD хозяина от разрушения 3 ’концов в репликации по катящемуся кругу. Int и xis являются белками интеграции и удаления, жизненно важными для лизогении.
xis и int регуляция вставки и удаления
- xis и int находятся на одном и том же участке мРНК, поэтому примерно равные концентрации xis и int белки производятся. Это приводит (первоначально) к удалению любых вставленных геномов из генома хозяина.
- МРНК из пL промотор образует стабильную вторичную структуру с стебель-петля в брат раздел мРНК. Это нацелено на 3 '(брат) конец мРНК для деградации РНКазы III, что приводит к более низкой эффективной концентрации int мРНК, чем xis мРНК (как int цистрон ближе к брат последовательность, чем xis цистрон для брат последовательность), поэтому более высокие концентрации xis чем int наблюдается.
- Более высокие концентрации xis чем int не приводят к вставке или удалению фаговых геномов, что является эволюционно благоприятным действием - оставляя любые предварительно вставленные фаговые геномы вставленными (таким образом уменьшая конкуренцию) и предотвращая вставку генома фага в геном обреченного хозяина.
Лизогенный (или лизеногенный) жизненный цикл
Лизогенный жизненный цикл начинается, когда белок cI достигает достаточно высокой концентрации для активации его промоторов после небольшого числа инфекций.
- «Поздние ранние» стенограммы продолжают составляться, в том числе xis, int, Q и гены репликации лямбда-генома.
- Стабилизированный cII способствует транскрипции из пRE, пя и пантиквариат промоутеры.
- В пантиквариат промотор продуцирует антисмысловую мРНК к Q генное послание пр промоторный транскрипт, тем самым отключая продукцию Q. В пRE промотор продуцирует антисмысловую мРНК кро-секции пр стенограмма промотора, отказавшаяся от производства урожая, и есть стенограмма cI ген. Это выражается в включении производства репрессоров КИ. В пя промоутер выражает int ген, что приводит к высоким концентрациям белка Int. Этот белок int интегрирует ДНК фага в хромосому хозяина (см. «Интеграция профага»).
- Отсутствие Q не приводит к расширению пР' рамки считывания промотора, поэтому литические или структурные белки не образуются. Повышенные уровни int (намного выше, чем у xis) приводят к встраиванию лямбда-генома в геном хозяина (см. Диаграмму). Продукция cI приводит к связыванию cI с OR1 и ИЛИ2 сайты в пр промоутер, выключение Cro и экспрессия других ранних генов. cI также связывается с пL промоутер, отключив там транскрипцию.
- Отсутствие кро оставляет OR3 сайт не привязан, поэтому транскрипция с пRM может возникнуть промотор, поддерживая уровни cI.
- Отсутствие транскрипции из пL и пр промоторы не приводят к дальнейшему продуцированию cII и cIII.
- По мере снижения концентраций cII и cIII транскрипция из пантиквариат, пRE и пя перестать продвигаться по службе, так как они больше не нужны.
- Только пRM и пР' промоторы остаются активными, первые продуцируют белок cI, а вторые - короткий неактивный транскрипт. Геном остается встроенным в геном хозяина в неактивном состоянии.
Профаг дублируется при каждом последующем делении клеток хозяина. Фаговые гены, экспрессируемые в этом состоянии покоя, кодируют белки, которые подавляют экспрессию других фаговых генов (таких как структурные гены и гены лизиса), чтобы предотвратить вступление в литический цикл. Эти репрессивные белки расщепляются, когда хозяйская клетка находится в состоянии стресса, что приводит к экспрессии репрессированных фаговых генов. Стресс может быть от голодание, яды (подобно антибиотики ) или другие факторы, которые могут повредить или уничтожить хост. В ответ на стресс активированный профаг вырезается из ДНК клетки-хозяина одним из вновь экспрессированных генных продуктов и вступает в свой литический путь.
Интеграция профага
Интеграция фага λ происходит в особом месте прикрепления в бактериальном и фаговом геномах, которое называется attλ. Последовательность бактериального att-сайта называется attB, между гал и биография оперонов и состоит из частей B-O-B ', в то время как комплементарная последовательность в кольцевом геноме фага называется attP и состоит из частей P-O-P '. Сама интеграция представляет собой последовательный обмен (см. генетическая рекомбинация ) через Холлидей Джанкшн и требует как фагового белка Int, так и бактериального белка IHF (фактор хоста интеграции). И Int, и IHF связываются с attP и образуют интасому, комплекс ДНК-белок, предназначенный для сайт-специфическая рекомбинация ДНК фага и хозяина. Исходная последовательность B-O-B 'заменяется интеграцией в B-O-P'-фаговую ДНК-P-O-B'. ДНК фага теперь является частью генома хозяина.[13]
Поддержание лизогении

- Лизогения поддерживается исключительно cI. cI подавляет транскрипцию из пL и пр одновременно регулируя и контролируя собственное выражение от пRM. Следовательно, это единственный белок, экспрессируемый лизогенным фагом.

- Это координируется пL и пр операторы. У обоих операторов есть три сайта привязки для cI: OL1, OL2, и OL3 за пL, и OR1, ИЛИ2 и OR3 за пр.
- cI наиболее благоприятно связывается с OR1; связывание здесь ингибирует транскрипцию с пр. Поскольку cI легко димеризуется, связывание cI с OR1 значительно увеличивает сродство связывания cI с ИЛИ2, и это происходит почти сразу после OR1 привязка. Это активирует транскрипцию в противоположном направлении от пRM, как N-концевой домен cI на ИЛИ2 усиливает связывание РНК-полимеразы с пRM и, следовательно, cI стимулирует собственную транскрипцию. Когда он присутствует в гораздо более высокой концентрации, он также связывается с OR3, ингибируя транскрипцию с пRM, таким образом регулируя свои собственные уровни в петле отрицательной обратной связи.
- cI привязка к пL Оператор очень похож, за исключением того, что он не имеет прямого воздействия на транскрипцию cI. Однако в качестве дополнительной репрессии собственной экспрессии димеры cI связаны с OR3 и OL3 изогнуть ДНК между ними, чтобы тетрамеризоваться.
- Присутствие cI вызывает иммунитет к суперинфекции другими лямбда-фагами, так как он подавляет их пL и пр промоутеры.
Индукция

Классическая индукция лизогена заключалась в облучении инфицированных клеток УФ-светом. Любая ситуация, когда лизоген подвергается повреждению ДНК или SOS ответ хозяина иначе стимулируется, приводит к индукции.
- Клетка-хозяин, содержащая спящий геном фага, испытывает повреждение ДНК из-за высокой стрессовой среды и начинает подвергаться воздействию SOS ответ.
- RecA (клеточный белок) обнаруживает повреждение ДНК и активируется. Теперь это RecA *, высокоспецифичная ко-протеаза.
- Обычно RecA * связывает LexA (a транскрипция репрессор), активируя активность аутопротеазы LexA, которая разрушает репрессор LexA, позволяя производить Ремонт ДНК белки. В лизогенных клетках этот ответ нарушается, и RecA * стимулирует автодробление cI. Это связано с тем, что cI имитирует структуру LexA на участке авторасщепления.
- Расщепленный cI больше не может димеризоваться и теряет сродство к связыванию ДНК.
- В пр и пL промоторы больше не репрессируются и включаются, и клетка возвращается к литической последовательности событий экспрессии (обратите внимание, что cII нестабилен в клетках, подвергающихся SOS-ответу). Однако есть одно заметное отличие.

Контроль удаления генома фага при индукции
- Геном фага все еще встроен в геном хозяина и нуждается в вырезании для репликации ДНК. В брат раздел за пределы нормального пL Однако транскрипт промотора больше не включается в эту рамку считывания (см. диаграмму).
- Нет брат домен на пL мРНК промотора приводит к отсутствию шпильки на 3'-конце, и транскрипт больше не является мишенью для деградации РНКазы III.
- В новой неповрежденной стенограмме есть по одной копии обоих xis и int, поэтому продуцируются примерно равные концентрации белков xis и int.
- Равные концентрации xis и int приводят к вырезанию встроенного генома из генома хозяина для репликации и более позднего производства фага.
Реактивация множественности и реактивация профага
Реактивация множественности (MR) - это процесс, при котором несколько вирусных геномов, каждый из которых содержит инактивирующее повреждение генома, взаимодействуют внутри инфицированной клетки с образованием жизнеспособного вирусного генома. MR был первоначально обнаружен с фагом T4, но впоследствии был обнаружен в фаге λ (а также во многих других вирусах бактерий и млекопитающих).[14]). MR фага λ, инактивированного УФ-светом, зависит от функции рекомбинации либо хозяина, либо инфицированного фага.[15] Отсутствие обеих систем рекомбинации приводит к потере MR.
Выживаемость УФ-облученного фага λ увеличивается, когда хозяин E. coli является лизогенным для гомологичного профага, это явление называется реактивацией профага.[16] Реактивация профага в фаге λ, по-видимому, происходит за счет рекомбинационного процесса репарации, аналогичного процессу MR.
Репрессор

В репрессор Обнаруженная в фаге лямбда является ярким примером уровня контроля, возможного над экспрессией генов с помощью очень простой системы. Он образует «бинарный переключатель» с двумя генами при взаимоисключающей экспрессии, как обнаружил Барбара Дж. Мейер.[17]
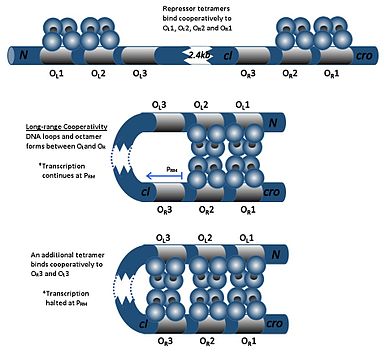
Система генов-репрессоров лямбда состоит из (слева направо на хромосоме):
- cI ген
- Ор3
- Ор2
- Ор1
- Cro ген
Лямбда-репрессор представляет собой самособирающийся димер, также известный как белок cI.[18] Он связывает ДНК в мотиве связывания спираль-поворот-спираль. Он регулирует транскрипцию белка cI и белка Cro.
Жизненный цикл лямбда-фагов контролируется белками cI и Cro. Лямбда-фаг останется в лизогенном состоянии, если преобладают белки cI, но будет преобразован в литический цикл, если преобладают белки кро.
Димер cI может связываться с любым из трех операторов, Oр1, Ор2 и Oр3 в порядке Oр1> Oр2> Oр3. Связывание димера cI с Oр1 усиливает связывание второго димера cI с Oр2, эффект, называемый сотрудничество. Таким образом, Oр1 и Oр2 почти всегда одновременно заняты cI. Однако это не увеличивает сродство между cI и Oр3, которая будет занята только при высокой концентрации ХИ.
При высоких концентрациях cI димеры также связываются с операторами OL1 и OL2 (которые более чем на 2 кб ниже по течению от операторов R). Когда димеры cI связаны с OL1, ОL2, Ор1 и Oр2 в ДНК индуцируется петля, позволяющая этим димерам связываться вместе с образованием октамера. Это явление называется долгосрочное сотрудничество. При образовании октамера димеры cI могут кооперативно связываться с OL3 и Ор3, подавляя транскрипцию cI. Этот автономный регулирование обеспечивает стабильную минимальную концентрацию репрессорной молекулы и, в случае возникновения сигналов SOS, позволяет более эффективную индукцию профага.[19]
- В отсутствие белков cI Cro ген может быть транскрибирован.
- В присутствии белков cI только cI ген может быть транскрибирован.
- При высокой концентрации cI происходит репрессия транскрипции обоих генов.

Некоторые пары оснований выполняют двойную функцию с промотором и оператором для белков cl и cro.
Белок cl включен, при этом репрессор, связанный с полимеразой OR2, увеличивается, и OR1 выключен.
Репрессия лизогена, связанная со всеми тремя сайтами, встречается редко из-за слабой аффинности связывания OR3. Репрессия OR1 увеличивает сродство связывания с OR2 из-за взаимодействия репрессор-репрессор. Повышенные концентрации репрессора усиливают связывание.
Обзор функции белков
| Протеин | Функция в жизненном цикле | Регион промоутера | Описание |
|---|---|---|---|
| cIII | Регуляторный белок CIII. Лизогения, стабильность cII | пL | (Очистить 3) HflB (FtsH) связывающий белок, защищает cII от деградации протеазами. |
| cII | Лизогения, активатор транскрипции | пр | (Очистить 2) Активирует транскрипцию с PAQ, ПRE и Pя промоутеры, транскрибирующие cI и int. Низкая стабильность из-за восприимчивости к клеточному HflB (FtsH) протеазы (особенно в здоровых клетках и клетках, испытывающих SOS-ответ). Высокий уровень cII подтолкнет фаг к интеграции и лизогению, в то время как низкие уровни cII приведет к лизису. |
| cI | Репрессор, поддержание лизогении | пRM, ПRE | (Очистить 1) Ингибитор транскрипции, связывает Oр1, Ор2 и Oр3 (близость Oр1> Oр2 = Oр3, т.е. преимущественно связывает Oр1). При низких концентрациях блокирует Pр промоутер (предотвращающий продукцию Cro). При высоких концентрациях снижает собственное производство за счет Oр3 переплета. Репрессор также подавляет транскрипцию из PL промоутер. Восприимчивы к расщеплению RecA * в ячейках, подвергающихся SOS-ответу. |
| Cro | Лизис, контроль оператора репрессора | пр | Ингибитор транскрипции, связывает Oр3, Ор2 и Oр1 (близость Oр3> Oр2 = Oр1, т.е. преимущественно связывает Oр3). В низких концентрациях блокирует промотор pRM (предотвращая cI производство). При высоких концентрациях снижает собственное производство за счет Oр2 и Oр1 переплет. Нет совместной привязки (см. Ниже для привязки cI) |
| О | Лизис, репликация ДНК | пр | Репликационный белок O. Инициирует репликацию ДНК фага лямбда путем связывания на Ори сайт. |
| п | Лизис, репликация ДНК | пр | Инициирует репликацию ДНК фага лямбда путем связывания с О и DnaB субъединица. Эти связывания обеспечивают контроль над ДНК-полимеразой хозяина. |
| игра | Лизис, репликация ДНК | пL | Тормозит хост RecBCD нуклеаза от разложения 3'-концов - разрешить репликация катящегося круга продолжать. |
| S | Лизис | пР' | Холин, мембранный белок, который перфорирует мембрану во время лизиса. |
| р | Лизис | пР' | Эндолизин, Лизоцим, фермент, который выходит из клетки через отверстия, производимые холином, и расщепляет клеточную стенку. |
| Rz и Rz1 | Лизис | пР' | Образует мембранный белковый комплекс, который разрушает внешнюю клеточную мембрану после разрушения клеточной стенки эндолизином. Спанин, Rz1 (субъединица внешней мембраны) и Rz (субъединица внутренней мембраны). |
| F | Лизис | пР' | Белки капсидной головки фага. |
| D | Лизис | пР' | Белок украшения головы. |
| E | Лизис | пР' | Главный белок головы. |
| C | Лизис | пР' | Незначительный капсидный белок. |
| B | Лизис | пР' | Портальный белок B. |
| А | Лизис | пР' | Белок большой терминазы. |
| J | Лизис | пР' | Белок специфичности хозяина J. |
| М В У Г Л Т Я | Лизис | пР' | Минорный хвостовой белок M. |
| K | Лизис | пР' | Вероятная эндопептидаза. |
| ЧАС | Лизис | пР' | Хвостовая рулетка, белок H. |
| я | Лизис | пР' | Белок сборки хвоста I. |
| FI | Лизис | пР' | ДНК-упаковывающий белок FI. |
| FII | Лизис | пР' | Белок прикрепления хвоста. |
| tfa | Лизис | пР' | Белок сборки волокон хвоста. |
| int | Интеграция генома, эксцизия | пя, ПL | Интеграза, управляет вставкой генома фага в геном хозяина. В условиях низкой int концентрации нет никакого эффекта. Если xis низкая концентрация и int тогда это приводит к вставке генома фага. Если xis и int имеют высокие (и примерно равные) концентрации, что приводит к удалению геномов фагов из генома хозяина. |
| xis | Удаление генома | пя, ПL | Эксцизионаз и int регулятор белка, управляет вырезанием и вставкой генома фага в геном хозяина. |
| N | Антитерминация для транскрипции поздних ранних генов | пL | Антитерминатор, РНК-связывающий белок и кофактор РНК-полимеразы, связывает РНК (в сайтах Nut) и переносится на формирующийся RNApol, который только что транскрибировал сайт ореха. Эта модификация RNApol предотвращает распознавание сайтов терминации, поэтому нормальные сигналы терминации РНК-полимеразы игнорируются, и синтез РНК продолжается в дистальных фаговых генах (cII, cIII, xis, интервал, O, P, Q) |
| Q | Антитерминация для транскрипции поздних литических генов | пр | Антитерминатор, ДНК-связывающий белок и кофактор RNApol, связывает ДНК (в сайтах Qut) и переносится на инициирующую RNApol. Эта модификация RNApol изменяет распознавание терминирующих последовательностей, поэтому нормальные игнорируются; специальные последовательности терминации Q на расстоянии около 20 000 п.н. эффективны. Q-удлиненные транскрипты включают структурные белки фага (A-F, Z-J) и гены лизиса (S, R, Rz и Rz1). Подавляется Pантиквариат антисмысловая мРНК во время лизогении. |
| RecA | SOS ответ | Белок хозяина | Белок репарации ДНК, функционирует как ко-протеаза во время SOS-ответа, авто-расщепление LexA и cI и облегчение лизиса. |
Литический против лизогенного

Важным различием здесь является различие между двумя решениями; лизогения и лизиса при инфицировании, а также продолжение лизогении или лизиса профага. Последнее определяется исключительно активацией RecA в SOS-ответе клетки, как подробно описано в разделе, посвященном индукции. Это также коснется первых; клетка, претерпевающая SOS-ответ, всегда будет лизироваться, поскольку не будет позволено накапливаться белку cI. Однако первоначальное литическое / лизогенное решение об инфекции также зависит от белков cII и cIII.
В клетках с достаточным количеством питательных веществ высока активность протеазы, расщепляющей cII.[20] Это приводит к литическому образу жизни. В клетках с ограниченным количеством питательных веществ активность протеазы низкая, что делает cII стабильным. Это приводит к лизогенному образу жизни. cIII, по-видимому, стабилизирует cII, как напрямую, так и действуя как конкурентный ингибитор соответствующих протеаз. Это означает, что клетка «в беде», то есть при недостатке питательных веществ и в более спящем состоянии, с большей вероятностью подвергнется лизогенизации. Это было бы выбрано, потому что фаг теперь может бездействовать в бактерии, пока не наступят лучшие времена, и поэтому фаг может создавать больше копий себя с дополнительными доступными ресурсами и с более вероятной близостью дальнейших инфицированных клеток.
Полная биофизическая модель для решения lysis-lysogeny лямбда еще предстоит разработать. Компьютерное моделирование и симуляция предполагают, что случайные процессы во время инфекции управляют выбором лизиса или лизогении в отдельных клетках.[21] Однако недавние эксперименты показывают, что физические различия между клетками, существовавшие до инфекции, предопределяют, будет ли клетка лизироваться или станет лизогеном.[22]
Как генетический инструмент
Лямбда-фаг широко использовался как модельный организм, и был богатым источником полезных инструментов в микробная генетика, а позже в молекулярная генетика. Использование включает его применение в качестве вектора для клонирования рекомбинантная ДНК; использование его сайт-специфической рекомбиназы (int) для перетасовки клонированных ДНК посредством метод шлюза; и применение его красного оперон, включая белки Red alpha (также называемые «экзо»), бета и гамма в методе ДНК-инженерии, называемом рекомбинирование. Фрагмент ДНК фага лямбда размером 48 т.п.н. не важен для продуктивной инфекции и может быть заменен чужеродной ДНК. Лямбда-фаг легче проникает в бактерии, чем плазмиды, что делает его полезным вектором, который может разрушать или может стать частью ДНК хозяина. Лямбда-фаг можно манипулировать и использовать в качестве противораковой вакцины, наночастиц, нацеленных на человека. аспартил (аспарагинил) β-гидроксилаза (АСИФ, ха-ха).[23] Лямбда-фаг также сыграл важную роль в изучении специализированная трансдукция.
Смотрите также
- Эстер Ледерберг
- Семья лямбда холина
- Маркер размера молекулярной массы
- Санкар Адхья
- Зиготическая индукция
Рекомендации
- ^ Эстер Ледерберг, "Лизогенность в кишечная палочка штамм К-12, Бюллетень микробной генетики, т.1, стр. 5–8 (январь 1950 г.); с последующим Ледерберг Е.М., Ледерберг Дж. (Январь 1953 г.). «Генетические исследования лизогенности Escherichia Coli». Генетика. 38 (1): 51–64. ЧВК 1209586. PMID 17247421.
- ^ Гриффитс А., Миллер Дж., Сузуки Д., Левонтин Р., Гелбарт В. (2000). Введение в генетический анализ (7-е изд.). Нью-Йорк: У. Х. Фриман. ISBN 978-0-7167-3520-5. Получено 19 мая 2017.
- ^ а б c Раджагопала С.В., Касьенс С., Уетц П. (сентябрь 2011 г.). «Карта взаимодействия белков бактериофага лямбда». BMC Microbiology. 11: 213. Дои:10.1186/1471-2180-11-213. ЧВК 3224144. PMID 21943085.
- ^ Casjens, S. R., & Hendrix, R. W. (2015). Лямбда-бактериофаг: первопроходец и все еще актуален. Вирусология, 479-480, 310–330. DOI: 10.1016 / j.virol.2015.02.010
- ^ а б Кэмпбелл, А. Бактериофаги. В: Neidhardt, FC et al. (1996) кишечная палочка и Сальмонелла тифимуриум: Клеточная и молекулярная биология (ASM Press, Вашингтон, округ Колумбия)
- ^ Вертс С., Мишель В., Хофнунг М., Чарбит А. (февраль 1994 г.). «Адсорбция бактериофага лямбда на белке LamB Escherichia coli K-12: точечные мутации в гене J лямбда, ответственного за расширенный круг хозяев». Журнал бактериологии. 176 (4): 941–7. Дои:10.1128 / jb.176.4.941-947.1994. ЧВК 205142. PMID 8106335.
- ^ Эрни Б., Занолари Б., Кочер HP (апрель 1987 г.). «Маннозная пермеаза Escherichia coli состоит из трех различных белков. Аминокислотная последовательность и функция в транспорте сахара, фосфорилировании сахара и проникновении фаговой лямбда-ДНК». Журнал биологической химии. 262 (11): 5238–47. PMID 2951378.
- ^ Лю, Сюэли; Цзэн, Цзяньвэй; Хуанг, Кай; Ван, Цзявэй (17.06.2019). «Структура переносчика маннозы бактериальной фосфотрансферазной системы». Клеточные исследования. 29 (8): 680–682. Дои:10.1038 / s41422-019-0194-z. ISSN 1748-7838. ЧВК 6796895. PMID 31209249.
- ^ Casjens, S. R., & Hendrix, R. W. (2015). Бактериофаг лямбда: первопроходец и все еще актуален. Вирусология, 479-480, 310–330. DOI: 10.1016 / j.virol.2015.02.010
- ^ Кобилер О., Рокни А., Оппенгейм А.Б. (апрель 2007 г.). «Фаг лямбда CIII: ингибитор протеазы, регулирующий решение о лизисе-лизогении». PLOS One. 2 (4): e363. Bibcode:2007PLoSO ... 2..363K. Дои:10.1371 / journal.pone.0000363. ЧВК 1838920. PMID 17426811.
- ^ а б Сантанджело Т.Дж., Арцимович I (май 2011 г.). «Прерывание и антиттерминация: РНК-полимераза движется по знаку остановки». Обзоры природы. Микробиология. 9 (5): 319–29. Дои:10.1038 / nrmicro2560. ЧВК 3125153. PMID 21478900.
- ^ Дейган П., Хохшильд А. (февраль 2007 г.). «Анти-терминаторный белок бактериофага lambdaQ регулирует экспрессию поздних генов как стабильный компонент комплекса элонгации транскрипции». Молекулярная микробиология. 63 (3): 911–20. Дои:10.1111 / j.1365-2958.2006.05563.x. PMID 17302807.
- ^ Groth AC, Calos MP (январь 2004 г.). «Фаговые интеграции: биология и приложения». Журнал молекулярной биологии. 335 (3): 667–78. Дои:10.1016 / j.jmb.2003.09.082. PMID 14687564.
- ^ Мичод Р.Э., Бернштейн Х., Недельку А.М. (май 2008 г.). «Адаптивное значение секса у микробных патогенов». Инфекция, генетика и эволюция. 8 (3): 267–85. Дои:10.1016 / j.meegid.2008.01.002. PMID 18295550.
- ^ Хаски Р.Дж. (апрель 1969 г.). «Реактивация множественности как тест на функцию рекомбинации». Наука. 164 (3877): 319–20. Bibcode:1969Sci ... 164..319H. Дои:10.1126 / science.164.3877.319. PMID 4887562.
- ^ Бланко М., Деворет Р. (март 1973 г.). «Механизмы восстановления, участвующие в реактивации профага и УФ-реактивации УФ-облученного фага лямбда». Мутационные исследования. 17 (3): 293–305. Дои:10.1016/0027-5107(73)90001-8. PMID 4688367.
- ^ "Барбара Дж. Мейер", HHMI Интерактивный.
- ^ Burz DS, Beckett D, Benson N, Ackers GK (июль 1994). «Самосборка репрессора лямбда-cI бактериофага: влияние односайтовых мутаций на равновесие мономер-димер». Биохимия. 33 (28): 8399–405. Дои:10.1021 / bi00194a003. PMID 8031775.
- ^ Пташное, Марк (2004). Генетический переключатель, п. 112. Лаборатория издательства Колд-Спринг-Харбор, Нью-Йорк. ISBN 978-0879697167.
- ^ Пташне М (1986). "Генетический переключатель. Контроль генов и лямбда фага". Cell Press ISBN 0-86542-315-6
- ^ Аркин А., Росс Дж., Макадамс Х. Х. (август 1998 г.). «Стохастический кинетический анализ бифуркации пути развития в клетках Escherichia coli, инфицированных фагом лямбда». Генетика. 149 (4): 1633–48. ЧВК 1460268. PMID 9691025.
- ^ Сен-Пьер Ф, Энди Д. (декабрь 2008 г.). «Определение клеточной судьбы при инфицировании фагом лямбда». Труды Национальной академии наук Соединенных Штатов Америки. 105 (52): 20705–10. Bibcode:2008ПНАС..10520705С. Дои:10.1073 / pnas.0808831105. ЧВК 2605630. PMID 19098103.
- ^ Sztriha L, Salgó L (апрель 1985 г.). «[Изменения уровня церулоплазмина и цинка в крови у детей, получающих противоэпилептические средства]». Орвози Хетилап. 126 (14): 835–6. Дои:10.1186 / 2051-1426-1-S1-P210. ЧВК 3991175.
дальнейшее чтение
- Джеймс Уотсон, Таня Бейкер, Стивен Белл, Александр Ганн, Майкл Левин, Ричард Лосик «Молекулярная биология гена (международное издание)» - 6-е издание
- Марк Пташне и Нэнси Хопкинс, «Операторы, управляемые репрессором лямбда-фагов», PNAS, v.60, n.4, pp. 1282–1287 (1968).
- Барбара Дж. Мейер, Деннис Г. Клейд и Марк Пташне, «Лямбда-репрессор отключает транскрипцию своего собственного гена», PNAS, v.72, n.12, pp. 4785–4789 (декабрь 1975).
- Брюссов Х., Хендрикс Р.В. (январь 2002 г.). «Геномика фага: маленькое - красиво». Клетка. 108 (1): 13–6. Дои:10.1016 / S0092-8674 (01) 00637-7. PMID 11792317.
- Додд И.Б., Ширвин К.Э., Иган Дж. Б. (апрель 2005 г.). «Пересмотр регуляции гена в лямбда бактериофага». Текущее мнение в области генетики и развития. 15 (2): 145–52. Дои:10.1016 / j.gde.2005.02.001. PMID 15797197.
- Фридман Д.И., Суд DL (апрель 2001 г.). «Бактериофаг лямбда: жив-здоров и продолжает делать свое дело». Текущее мнение в микробиологии. 4 (2): 201–7. Дои:10.1016 / S1369-5274 (00) 00189-2. PMID 11282477.
- Готтесман М., Вайсберг Р.А. 2004 «Маленькая лямбда - кто тебя создал?», Micro и Mol Biol Revs, 68, 796-813 (доступны онлайн по адресу Обзоры микробиологии и молекулярной биологии, Американское общество микробиологии )
- Хендрикс Р.В., Смит М.С., Бернс Р.Н., Форд М.Э., Хатфул Г.Ф. (март 1999 г.). «Эволюционные отношения между различными бактериофагами и профагами: фаг во всем мире». Труды Национальной академии наук Соединенных Штатов Америки. 96 (5): 2192–7. Bibcode:1999PNAS ... 96.2192H. Дои:10.1073 / pnas.96.5.2192. ЧВК 26759. PMID 10051617.
- Китано Х (март 2002 г.). «Системная биология: краткий обзор» (PDF). Наука. 295 (5560): 1662–4. Bibcode:2002Наука ... 295.1662K. Дои:10.1126 / science.1069492. PMID 11872829.
- Пташне, М. «Генетический переключатель: новый взгляд на фаговую лямбду», 3-е издание, 2003 г.
- Пташне М (июнь 2005 г.). «Регуляция транскрипции: от лямбда к эукариотам». Тенденции в биохимических науках. 30 (6): 275–9. Дои:10.1016 / j.tibs.2005.04.003. PMID 15950866.
- Снайдер, Л. и Чампнесс, У. «Молекулярная генетика бактерий», 3-е издание, 2007 г. (содержит информативный и хорошо иллюстрированный обзор лямбда бактериофага)
- Сплашо, Обзор лямбда в Интернете (иллюстрирует гены, активные на всех этапах жизненного цикла)
внешняя ссылка
- Жизненный цикл, Базовая анимация жизненного цикла лямбда (иллюстрирует инфекцию и литические / лизогенные пути с некоторыми деталями белка и транскрипции)
- Видео с покадровой микроскопии из MIT, демонстрирующий как лизис, так и лизогению фагом лямбда
- Жизненный цикл лямбда-фага (базовая наглядная демонстрация жизненного цикла лямбда-бактериофага)
- Геном лямбда-фага в GenBank
- Эталонный протеом лямбда-фага от UniProt
- Структуры белка лямбда-фага в NCBI (Трехмерное отображение белковых структур бактериофага Лямбда)



