Нуклеозид - Nucleoside

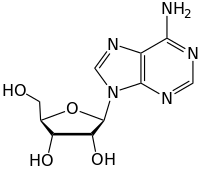
Нуклеозиды находятся гликозиламины это можно рассматривать как нуклеотиды без фосфатная группа. Нуклеозид состоит просто из азотистое основание (также называемый азотистая основа ) и пятиуглеродный сахар (рибоза или 2'-дезоксирибоза), тогда как нуклеотид состоит из азотистого основания, пятиуглеродного сахара и одной или нескольких фосфатных групп. В нуклеозиде аномерный углерод связан через гликозидную связь с N9 пурин или N1 из пиримидин. Примеры нуклеозидов включают: цитидин, уридин, аденозин, гуанозин, тимидин и инозин.[1]
В то время как нуклеозид - это азотистое основание, связанное с сахаром, нуклеотид состоит из нуклеозида. и одна или несколько фосфатных групп. Таким образом, нуклеозиды могут быть фосфорилированный конкретными киназы в ячейке на группу первичного спирта сахара (-CH2-OH) производить нуклеотиды. Нуклеотиды - это молекулярные строительные блоки ДНК и РНК.
Источник
Нуклеозиды могут быть получены из нуклеотидов. de novo, особенно в печени, но в большем количестве они попадают в организм через прием и переваривание нуклеиновых кислот с пищей, в результате чего нуклеотидазы сломать нуклеотиды (такой как тимидинмонофосфат ) в нуклеозиды (такие как тимидин ) и фосфат. Нуклеозиды, в свою очередь, впоследствии расщепляются в просвет пищеварительной системы нуклеозидазы на азотистые основания и рибозу или дезоксирибозу. Кроме того, нуклеотиды могут расщепляться внутри клетки на азотистые основания, и рибозо-1-фосфат или дезоксирибоза-1-фосфат.
Использование в медицине и технике
В медицине несколько аналоги нуклеозидов используются в качестве противовирусных или противораковых средств.[2][3] Вирусная полимераза включает эти соединения с неканоническими основаниями. Эти соединения активируются в клетках, превращаясь в нуклеотиды. Их вводят в виде нуклеозидов, поскольку заряженные нуклеотиды не могут легко проникать через клеточные мембраны.
В молекулярной биологии несколько аналоги сахарной основы существуют. Из-за низкой стабильности РНК, склонной к гидролизу, используются несколько более стабильных альтернативных аналогов нуклеозидов / нуклеотидов, которые правильно связываются с РНК. Это достигается за счет использования другого основного сахара. Эти аналоги включают LNA, морфолино, PNA.
При секвенировании дидезоксинуклеотиды используются. Эти нуклеотиды содержат неканоническую дидезоксирибозу сахара, в которой отсутствует 3'-гидроксильная группа (которая принимает фосфат). Следовательно, он не может связываться со следующим основанием и обрывает цепь, поскольку ДНК-полимеразы не могут отличить его от обычного дезоксирибонуклеотида.
| Азотистая основа | Рибонуклеозид | Дезоксирибонуклеозид |
|---|---|---|
 Аденин А |  Аденозин |  Дезоксиаденозин dA |
 Гуанин г |  Гуанозин | 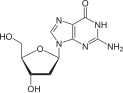 Дезоксигуанозин dG |
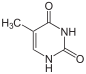 Тимин Т | 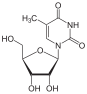 5-Метилуридин м5U |  Тимидин dT |
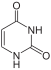 Урацил U |  Уридин |  Дезоксиуридин dU |
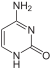 Цитозин C | 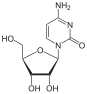 Цитидин | 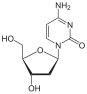 Дезоксицитидин Округ Колумбия |
Смотрите также
использованная литература
- ^ Нельсон, Дэвид Л .; Кокс, Майкл М. (2005). Принципы биохимии (4-е изд.). Нью-Йорк: У. Х. Фриман. ISBN 0-7167-4339-6.
- ^ Гальмарини, Карлос М .; Макки, Джон Р .; Дюмонте, Чарльз (2002). «Аналоги нуклеозидов и азотистые основания в лечении рака». Ланцет онкологии. 3 (7): 415–424. Дои:10.1016 / S1470-2045 (02) 00788-X. PMID 12142171.
- ^ Йордхейм, Ларс Петтер; Дюрантел, Дэвид; Зулим, Фабьен; Дюмонте, Чарльз (2013). «Достижения в разработке аналогов нуклеозидов и нуклеотидов для лечения рака и вирусных заболеваний». Обзоры природы Drug Discovery. 12 (6): 447–464. Дои:10.1038 / nrd4010. PMID 23722347. S2CID 39842610.
