Диффузное повреждение аксонов - Diffuse axonal injury
| Диффузное повреждение аксонов | |
|---|---|
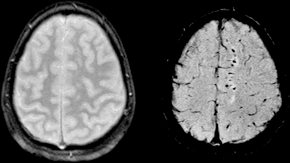 | |
| Два МРТ изображения пациента с диффузным повреждением аксонов в результате травмы, на 1,5 тесла напряженность поля. Слева: обычный градиент вспомнил эхо (GRE). Правильно: Восприимчивость взвешенного изображения (SWI). | |
| Специальность | Неврология |
Диффузное повреждение аксонов (DAI) это Травма головного мозга в котором разбросаны поражения встречаются на обширной территории в белое вещество трактаты, а также серое вещество.[1][2][3][4][5][6][7] DAI - один из самых распространенных и разрушительных типов травматическое повреждение мозга[8] и является основной причиной потери сознания и стойкое вегетативное состояние после тяжелой травмы головы.[9] Это происходит примерно в половине случаев тяжелых травма головы и может быть основным повреждением, возникающим при сотрясении мозга. Результат часто бывает кома, причем более 90% пациентов с тяжелым ДАИ никогда не приходили в сознание.[9] Те, кто действительно просыпается, часто остаются в значительной степени ослабленными.[10]
DAI может возникать по всему спектру тяжести черепно-мозговой травмы (TBI), при которой бремя травмы увеличивается от легкой до тяжелой.[11][12] Сотрясение может быть более легким типом диффузного повреждения аксонов.[12][13]
Механизм
DAI - это результат травматический стрижка силы, возникающие при быстром ускорении или замедлении головы, например, при автомобильных авариях, падениях и нападениях.[14] Автомобильные аварии - самая частая причина DAI; это также может произойти в результате жестокое обращение с ребенком[15] например, в синдром потрясенного ребенка.[16]
Немедленное отключение аксонов может наблюдаться при тяжелой травме головного мозга, но основное повреждение DAI откладывается вторично. аксон разъединения медленно развивались в течение длительного времени.[2] Участки аксонов, которые кажутся белыми из-за миелинизация, называются белое вещество. Поражения как серого, так и белого вещества обнаруживаются в посмертном мозге при КТ и МРТ.[9]
Помимо механического разрушения аксона цитоскелет Патология DAI также включает вторичные физиологические изменения, такие как прерывание аксонального транспорта, прогрессирующие опухоли и дегенерация.[17] Недавние исследования связали эти изменения с перекручиванием и смещением сломанного аксона. микротрубочки, а также тау-белок и белок-предшественник амилоида (APP) осаждение.[17][18]
Характеристики
Поражения обычно существуют в белое вещество мозгов, поврежденных DAI; Эти поражения варьируются по размеру от 1 до 15 мм и распределены характерным образом.[9] DAI чаще всего влияет на белое вещество в областях, включая мозговой ствол, то мозолистое тело, а полушария головного мозга.
В доли мозга Скорее всего, пострадают лобная и височная доли.[19] Другие распространенные места для DAI включают белое вещество в кора головного мозга, высший церебральные ножки,[16] базальный ганглий, таламус и глубокий ядра полушария.[20] Эти области легче повредить из-за разницы в плотности между ними и остальной частью мозга.[20]
Гистологические характеристики
DAI характеризуется разделением аксонов, при котором аксон разрывается в месте растяжения, а часть дистальный до слез деградирует. Хотя когда-то считалось, что основной причиной отделения аксонов был разрыв из-за механических сил во время травмы, теперь стало понятно, что аксоны обычно не разрываются при ударе; скорее вторичный биохимические каскады, которые возникают в ответ на первичная травма (который возникает в результате механических сил в момент травмы) и происходит через несколько часов или дней после первоначальной травмы, в значительной степени ответственны за повреждение аксонов.[21][22][23]
Хотя процессы, вовлеченные во вторичное повреждение головного мозга, все еще плохо изучены, в настоящее время принято считать, что растяжение аксонов во время травмы вызывает физическое нарушение и протеолитический деградация цитоскелет.[24] Он также открывает натриевые каналы в аксолемма, что приводит к потенциалзависимые кальциевые каналы открыть и Ca2+ течь в ячейку.[24] Внутриклеточное присутствие Са2+ запускает несколько различных путей, включая активацию фосфолипазы и протеолитический ферменты, повреждение митохондрии и цитоскелет, и активируя вторичные посланники, что может привести к отрыву аксона и гибели клетки.[21]
Нарушение цитоскелета

Аксоны обычно эластичны, но при быстром растяжении они становятся хрупкими, и аксоны становятся хрупкими. цитоскелет можно сломать. Смещение цитоскелетных элементов после травмы растяжения может привести к разрыву аксона и гибели нейрона. Аксональный транспорт продолжается до точки разрыва цитоскелета, но не дальше, что приводит к накоплению транспортных продуктов и локальному отеку в этой точке.[25] Когда он становится достаточно большим, опухоль может разорвать аксон в месте разрыва цитоскелета, заставляя его отступить к телу клетки и сформировать луковицу.[11] Эта лампочка называется ретракционный шар, признак диффузного повреждения аксонов.[9]
Когда аксон рассечен, Валлеровское вырождение, при котором часть аксона дистальнее разрыва деградирует, происходит в течение одного-двух дней после травмы.[26] Аксолемма распадается,[26] миелин разрушается и начинает отделяться от клеток в антероградном направлении (от тела клетки к концу аксона),[27] и соседние клетки начинаются фагоцитарный активность, поглощение мусора.[28]
Приток кальция
Иногда нарушается только цитоскелет, но часто нарушается аксолемма происходит также, вызывая приток Ca2+ в клетку и развязывая различные процессы разложения.[26][29] Повышение Ca2+ и Na+ уровни и падение K+ уровни обнаруживаются в аксоне сразу после травмы.[21][26] Возможные маршруты Ca2+ запись включает натриевые каналы, поры разрыв мембраны при растяжении, и отказ АТФ-зависимые переносчики из-за механической блокировки или недостатка энергии.[21] Высокий уровень внутриклеточного Ca2+, основная причина посттравматического повреждения клеток,[30] разрушить митохондрии,[11] и вызвать фосфолипазы и протеолитический ферменты которые повреждают каналы Na + и разрушают или изменяют цитоскелет и аксоплазма.[31][26] Избыток Ca2+ также может привести к повреждению гематоэнцефалический барьер и отек мозга.[30]
Один из белки активируется наличием кальций в камере Кальпаин, а Ca2+-зависимый не-лизосомный протеаза.[31] Примерно от 15 минут до получаса после начала травмы начинает происходить процесс, называемый опосредованным кальпаином протеолизом спектрина или CMSP.[32] Кальпаин расщепляет молекулу, называемую спектрин, который удерживает мембрану на цитоскелете, вызывая образование пузыри и разрушение цитоскелета и мембраны и, в конечном итоге, гибель клетки.[31][32] Другие молекулы, которые могут разлагаться кальпаинами: микротрубочка подразделения, белки, связанные с микротрубочками, и нейрофиламенты.[31]
Обычно происходит от одного до шести часов в процессе травмы после растяжения, присутствие кальция в клетке инициирует каспаза каскад, процесс повреждения клеток, который обычно приводит к апоптоз, или «клеточное самоубийство».[32]
Митохондрии, дендриты, и части цитоскелет поврежденные в результате травмы имеют ограниченную способность к заживлению и регенерации, процесс, который происходит в течение 2 или более недель.[33] После травмы астроциты может сжиматься, в результате чего части мозг атрофироваться.[9]
Диагностика

DAI трудно обнаружить, так как он плохо отображается на Компьютерная томография или с помощью других методов макроскопической визуализации, хотя это обнаруживается микроскопически.[9] Однако есть характеристики, типичные для DAI, которые могут или не могут отображаться на компьютерной томографии. Диффузное повреждение имеет больше микроскопических повреждений, чем макроскопическое повреждение, и его трудно обнаружить с помощью КТ и МРТ, но его наличие можно предположить, когда в области видны небольшие кровотечения. мозолистое тело или кора головного мозга.[34] МРТ более полезна, чем КТ, для выявления характеристик диффузного повреждения аксонов в подострых и хронических периодах времени.[35] Новые исследования, такие как Диффузионная тензорная визуализация способны продемонстрировать степень повреждения волоконного тракта белого вещества даже при отрицательном результате стандартной МРТ. Поскольку повреждение аксонов в DAI в значительной степени является результатом вторичного биохимические каскады, он имеет отсроченное начало, поэтому состояние человека с ДАИ, который изначально выглядит здоровым, может ухудшиться позже. Таким образом, травма часто бывает более серьезной, чем предполагалось, и медицинские работники должны подозревать ДАИ у любых пациентов, у которых КТ выглядит нормально, но у которых есть такие симптомы, как бессознательное состояние.[9]
МРТ более чувствительна, чем КТ, но все же подвержена ложные отрицания потому что DAI идентифицируется по признакам отек, который может не всегда присутствовать.[33]
DAI классифицируется по степени тяжести травмы. При степени I присутствует обширное повреждение аксонов, но очаговых аномалий не наблюдается. При степени II повреждения, обнаруженные при степени I, присутствуют в дополнение к очаговым аномалиям, особенно в мозолистом теле. Урон III степени включает в себя как I, так и II степень плюс ростральный мозговой ствол травмы и часто разрывы тканей.[36]
Уход
DAI в настоящее время не имеет специального лечения, помимо этого, для любого типа повреждение головы, который включает стабилизацию пациента и попытки ограничить увеличение внутричерепное давление (ПМС).
История
Идея DAI впервые возникла в результате исследований Сабина Стрих о поражениях белого вещества у людей, перенесших травму головы много лет назад.[37] Стрих впервые предложил идею в 1956 году, назвав ее диффузная дегенерация белого вещества; однако предпочтение было отдано более краткому термину «диффузное повреждение аксонов».[38] Стрих исследовал взаимосвязь между деменцией и травмой головы.[37] и утверждал в 1956 году, что DAI играет неотъемлемую роль в конечном развитии деменции из-за травмы головы.[15] Термин DAI был введен в начале 1980-х годов.[39]
Известные примеры
- Высшая передача ведущий Ричард Хаммонд пострадал от DAI в результате Vampire Dragster Crash в 2006 году.
- Чемпионат мира по автомобилям Водитель Роберто Герреро пострадал DAI в результате сбоя во время тестирования на Автодром Индианаполиса в 1987.[40]
- Формула 1 Водитель Жюль Бьянки пострадал DAI в результате аварии на 2014 Гран-при Японии[41] и умер, не приходя в сознание, через 9 месяцев, 17 июля 2015 г.[42]
- Актер и рассказчик аудиокниги Франк Мюллер, кто читал Стивен Кинг с Темная Башня, пострадал от DAI в 2001 году из-за мотоциклетная авария. Он умер в 2008 году.[43]
- НАСКАР Водитель Адам Петти, внук семикратного чемпиона Кубковой серии Ричард Петти, получил диффузное повреждение аксонов, вызванное смертельным исходом. перелом базилярного черепа в мае 2000 г. Автострада Нью-Гэмпшира во время тренировок к предстоящей гонке.
Смотрите также
Рекомендации
- ^ Стрих SJ (август 1956 г.). «Диффузная дегенерация белого вещества головного мозга при тяжелой деменции после травмы головы». Журнал неврологии, нейрохирургии и психиатрии. 19 (3): 163–85. Дои:10.1136 / jnnp.19.3.163. ЧВК 497203. PMID 13357957.
- ^ а б Повлишок Дж. Т., Беккер Д. П., Ченг К. Л., Воан Г. В. (май 1983 г.). «Аксональное изменение при незначительной травме головы». Журнал невропатологии и экспериментальной неврологии. 42 (3): 225–42. Дои:10.1097/00005072-198305000-00002. PMID 6188807. S2CID 24260379.
- ^ Адамс Дж. Х. (март 1982 г.). «Диффузная травма аксона при неракетной травме головы». Травма, повреждение. 13 (5): 444–5. Дои:10.1016 / 0020-1383 (82) 90105-Х. PMID 7085064.
- ^ Кристман К.В., Грейди М.С., Уокер С.А., Холлоуэй К.Л., Повлишок Д.Т. (апрель 1994 г.). «Ультраструктурные исследования диффузного повреждения аксонов у человека». Журнал нейротравмы. 11 (2): 173–86. Дои:10.1089 / neu.1994.11.173. PMID 7523685.
- ^ Повлишок Дж. Т., Кристман К. В. (август 1995 г.). «Патобиология травматических повреждений аксонов у животных и людей: обзор современных мыслей». Журнал нейротравмы. 12 (4): 555–64. Дои:10.1089 / neu.1995.12.555. PMID 8683606.
- ^ Vascak M, Jin X, Jacobs KM, Povlishock JT (май 2018 г.). «Легкое травматическое повреждение головного мозга вызывает структурное и функциональное отключение локальных тормозных сетей неокортекса через парвальбумин-интернейрон, диффузное аксональное повреждение». Кора головного мозга. 28 (5): 1625–1644. Дои:10.1093 / cercor / bhx058. ЧВК 5907353. PMID 28334184.
- ^ Смит Д.Х., Хикс Р., Повлишок Дж. Т. (март 2013 г.). «Разработка терапии диффузного аксонального повреждения». Журнал нейротравмы. 30 (5): 307–23. Дои:10.1089 / neu.2012.2825. ЧВК 3627407. PMID 23252624.
- ^ Повлишок Дж. Т., Кац Д. И. (январь 2005 г.). «Актуализация невропатологии и неврологического восстановления после черепно-мозговой травмы». Журнал реабилитации после травм головы. 20 (1): 76–94. Дои:10.1097/00001199-200501000-00008. PMID 15668572. S2CID 1094129.
- ^ а б c d е ж грамм час Вассерман Дж., Кенигсберг Р.А. (2007). Диффузное повреждение аксонов. Emedicine.com. Проверено 26 января 2008.
- ^ Футбольный клуб "Винас" и Пилицис Дж. (2006). Проникающая травма головы. Emedicine.com. Проверено 14 января 2008.
- ^ а б c Смит Д.Ф., Мини Д.Ф. (декабрь 2000 г.). «Поражение аксонов при черепно-мозговой травме». Нейробиолог. 6 (6): 483–95. Дои:10.1177/107385840000600611. S2CID 86550146.
- ^ а б Блумбергс ПК, Скотт Дж., Манавис Дж., Уэйнрайт Х., Симпсон Д.А., Маклин А.Дж. (август 1995 г.). «Топография аксонального повреждения, определенная с помощью белка-предшественника амилоида и метода подсчета очков при легкой и тяжелой закрытой травме головы». Журнал нейротравмы. 12 (4): 565–72. Дои:10.1089 / neu.1995.12.565. PMID 8683607.
- ^ Базарян Дж. Дж., Блит Б., Симпелло Л. (февраль 2006 г.). «От скамейки к постели: свидетельства травмы головного мозга после сотрясения мозга - вне рамок компьютерной томографии». Академическая неотложная медицина. 13 (2): 199–214. Дои:10.1197 / j.aem.2005.07.031. PMID 16436787.
- ^ Дженнарелли Т.А. (1993). «Механизмы черепно-мозговой травмы». Журнал неотложной медицины. 11 Дополнение 1: 5–11. PMID 8445204.
- ^ а б Хардман Дж. М., Манукян А. (май 2002 г.). «Патология черепно-мозговой травмы». Клиники нейровизуализации Северной Америки. 12 (2): 175–87, vii. Дои:10.1016 / S1052-5149 (02) 00009-6. PMID 12391630.
- ^ а б Смит Д. и Гринвальд Б. 2003.Ведение и стадирование черепно-мозговой травмы. Emedicine.com. Получено из веб-архива 17 января 2008 г.
- ^ а б Джонсон В.Е., Стюарт В., Смит Д.Х. (август 2013 г.). «Аксональная патология при черепно-мозговой травме». Экспериментальная неврология. Специальный выпуск: дегенерация аксонов. 246: 35–43. Дои:10.1016 / j.expneurol.2012.01.013. ЧВК 3979341. PMID 22285252.
- ^ Тан-Шомер, доктор медицины, Пател А.Р., Баас П.В., Смит Д.Х. (май 2010 г.). «Механическое разрушение микротрубочек в аксонах во время динамического растяжения лежит в основе замедленной эластичности, разборки микротрубочек и дегенерации аксонов». Журнал FASEB. 24 (5): 1401–10. Дои:10.1096 / fj.09-142844. ЧВК 2879950. PMID 20019243.
- ^ Бун Р. и де Монфор Дж. Дж. 2002 г. Травма головного мозга. Обучающие открытия Психологические услуги. Получено из веб-архива 17 января 2008 г.
- ^ а б Сингх Дж. И Сток А. (25 сентября 2006 г.). Травма головы. Emedicine.com. Проверено 17 января 2008.
- ^ а б c d Вольф Дж. А., Стис П. К., Лусарди Т., Мини Д. и Смит Д. Х. (2001). Травматическое повреждение аксонов вызывает приток кальция, модулируемый чувствительными к тетродотоксину натриевыми каналами. Журнал неврологии. 21 (6): 1923–1930
- ^ Арундин М., Аартс М., Лау А., Тимянски М. (сентябрь 2004 г.). «Уязвимость центральных нейронов к вторичным повреждениям после механического растяжения in vitro». J. Neurosci. 24 (37): 8106–23. Дои:10.1523 / JNEUROSCI.1362-04.2004. ЧВК 6729801. PMID 15371512.CS1 maint: несколько имен: список авторов (связь)
- ^ а б Музон Б., Чайтоу Х, Кринен Дж., Бахмайер С., Стюарт Дж., Маллан М., Стюарт В., Кроуфорд Ф. (декабрь 2012 г.). «Повторяющиеся легкие черепно-мозговые травмы на мышиной модели вызывают дефицит обучения и памяти, сопровождающийся гистологическими изменениями» (PDF). Журнал нейротравмы. 29 (18): 2761–73. Дои:10.1089 / neu.2012.2498. PMID 22900595.
- ^ а б Ивата А., Стис П.К., Вольф Дж. А., Чен Х. Х., Тейлор А. Г., Мини Д. Ф. и Смит Д. Х. (2004). Травматическое повреждение аксонов вызывает протеолитическое расщепление потенциал-управляемых натриевых каналов, модулируемое тетродотоксином и ингибиторами протеаз.. Журнал неврологии. 24 (19): 4605—4613.
- ^ Стаал Дж. А., Диксон Т. К., Чанг Р. С., Викерс Дж. К. (2007). «Лечение циклоспорином-A ослабляет отсроченные изменения цитоскелета и вторичную аксотомию после легкого повреждения аксонов». Дев Нейробиол. 67 (14): 1831–42. Дои:10.1002 / dneu.20552. PMID 17702000. S2CID 19415197.CS1 maint: несколько имен: список авторов (связь)
- ^ а б c d е Лопачин Р.М., Ленинг Э.Дж. (1997). «Механизм поступления кальция при повреждении и дегенерации аксонов». Токсикология и прикладная фармакология. 143 (2): 233–244. Дои:10.1006 / taap.1997.8106. PMID 9144441.
- ^ Коуи Р.Дж. и Стэнтон Дж. Б. (2005). Аксоплазматический транспорт и нейрональные реакции на повреждение В архиве 2005-10-29 на Wayback Machine. Медицинский колледж Университета Говарда. Проверено 17 января 2008.
- ^ Хьюз П.М., Уэллс Г.М., Перри В.Х., Браун М.С., Миллер К.М. (2002). «Сравнение экспрессии матриксной металлопротеиназы во время дегенерации Валлера в центральной и периферической нервной системе». Неврология. 113 (2): 273–287. Дои:10.1016 / s0306-4522 (02) 00183-5. PMID 12127085. S2CID 37213275.CS1 maint: несколько имен: список авторов (связь)
- ^ Повлишок Дж. Т., Петтус Э. Х. (1996). «Травматически индуцированное повреждение аксонов: свидетельства стойких изменений проницаемости аксолемм с соответствующими изменениями цитоскелета». Acta Neurochirurgica. 66: 81–86. Дои:10.1007/978-3-7091-9465-2_15. ISBN 978-3-7091-9467-6. PMID 8780803.
- ^ а б Чжоу Ф., Сян З., Фэн В.Х., Чжэнь Л.Х. (2001). "Ca без нейронов2+ проницаемость и ультраструктура ГЭБ при травме головы со вторичным повреждением ». Журнал клинической неврологии. 8 (6): 561–563. Дои:10.1054 / jocn.2001.0980. PMID 11683606. S2CID 43789581.CS1 maint: несколько имен: список авторов (связь)
- ^ а б c d Кастильо М.Р., Бэбсон-младший (1998). "Ca2+-зависимые механизмы повреждения клеток в культивируемых корковых нейронах ». Неврология. 86 (4): 1133–1144. Дои:10.1016 / s0306-4522 (98) 00070-0. PMID 9697120. S2CID 54228571.
- ^ а б c Буки А., Оконкво Д.О., Ван К.К., Повлишок Д.Т. (апрель 2000 г.). «Высвобождение цитохрома с и активация каспазы при травматическом повреждении аксонов». начальный. Журнал неврологии. 20 (8): 2825–34. Дои:10.1523 / JNEUROSCI.20-08-02825.2000. ЧВК 6772193. PMID 10751434.
- ^ а б Корбо Дж., Трипати П. (2004). «Отсроченное представление диффузного аксонального повреждения: отчет о случае». Травма. 44 (1): 57–60. Дои:10.1016 / j.annemergmed.2003.11.010. PMID 15226709.
- ^ Crooks CY, Zumsteg JM, Bell KR (ноябрь 2007 г.). «Черепно-мозговая травма: обзор практики управления и последних достижений». Клиники физической медицины и реабилитации Северной Америки. 18 (4): 681–710, vi. Дои:10.1016 / j.pmr.2007.06.005. PMID 17967360.
- ^ Маас А.И., Стоккетти Н., Баллок Р. (август 2008 г.). «Умеренная и тяжелая черепно-мозговая травма у взрослых». Ланцет. Неврология. 7 (8): 728–41. Дои:10.1016 / S1474-4422 (08) 70164-9. PMID 18635021. S2CID 14071224.
- ^ Лис-Хейли PR, Green P, Rohling ML, Fox DD, Allen LM (август 2003 г.). «Повреждение (я) при черепно-мозговой травме: значение для клинической нейропсихологии». Архив клинической нейропсихологии. 18 (6): 585–94. Дои:10.1016 / S0887-6177 (02) 00155-5. PMID 14591433.
- ^ а б Пирс Дж. М. (2007). «Наблюдения на сотрясение мозга. Обзор». Европейская неврология. 59 (3–4): 113–9. Дои:10.1159/000111872. PMID 18057896. S2CID 10245120.
- ^ Дженнарелли Г.А., Грэм Д.И. (2005). «Невропатология». В Silver JM, McAllister TW, Yudofsky SC (ред.). Учебник по черепно-мозговой травме. Вашингтон, округ Колумбия: Американская психиатрическая ассоциация. п. 34. ISBN 978-1-58562-105-7. Получено 2008-06-10.
- ^ Гранахер Р.П. (2007). Травматическая травма головного мозга: методы клинической и судебно-психиатрической оценки, второе издание. Бока-Ратон: CRC. С. 26–32. ISBN 978-0-8493-8138-6. Получено 2008-07-06.
- ^ «История Роберто Герреро».
- ^ «Жюль Бьянки: Семья подтверждает, что пилот Формулы-1 получил черепно-мозговую травму в результате аварии Гран-при Японии». Получено 8 октября 2014.
- ^ «Пилот Формулы-1 Жюль Бьянки погиб в результате аварии». BBC Sport. BBC. 2015-07-18. Получено 18 июля 2015.
- ^ "Фрэнк Мюллер, борьба его жизни". 2006. Получено 14 декабря, 2017.
внешняя ссылка
| Классификация | |
|---|---|
| Внешние ресурсы |
- Диффузная травма аксонов МРТ и КТ изображения
