Реакция Шапиро - Shapiro reaction
В Реакция Шапиро или же разложение тозилгидразона является органическая реакция в котором кетон или же альдегид преобразуется в алкен через промежуточный гидразон при наличии 2-х эквивалентов литийорганический реагент.[1][2][3] Реакция была обнаружена Роберт Х. Шапиро в 1967 г.[4] Реакция Шапиро была использована в Полный синтез таксола Николау.[5] Эта реакция очень похожа на Реакция Бэмфорда – Стивенса, который также включает основное разложение тозилгидразонов.

Механизм реакции
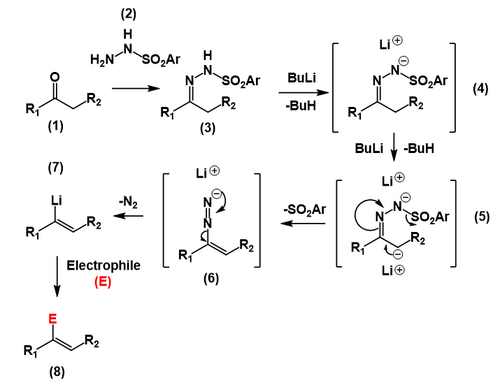
В преддверии реальной реакции Шапиро, кетон или альдегид (1) реагирует с п-толуолсульфонилгидразид[6](2) сформировать п-толуолсульфонилгидразон (или тозилгидразон ) который является гидразон (3). Два эквивалента сильного основание Такие как п-бутиллитий абстрагироваться от протон из гидразона (4) за которым следует меньше кислый протон α к углероду гидразона (5), образуя карбанион. Затем карбанион подвергается реакция элиминации производство углерод-углерод двойная связь и выбросив тозил анион, образующий диазоний анион (6). Этот анион диазония затем теряется как молекулярный азот в результате образуется виниллитий (7), которые затем могут реагировать с различными электрофилы, включая простую нейтрализацию водой или кислотой (8).
Объем
Положение алкена в продукте контролируется местом депротонирования литийорганическим основанием. В общем, кинетически предпочтительный, менее замещенный сайт дифференциально замещенных тозилгидразонов селективно депротонируется, что приводит к менее замещенному виниллитий средний. Хотя для виниллития существует множество вторичных реакций функциональная группа, в реакции Шапиро, в частности воды добавляется, что приводит к протонированию алкен.[7] Другие реакции соединений виниллития включают реакции алкилирования, например, с алкилгалогениды.[8]

Важно отметить, что реакцию Шапиро нельзя использовать для синтеза 1-литиоалкенов (и получаемых в результате функционализированных производных), поскольку сульфонилгидразоны, полученные из альдегидов, подвергаются исключительному присоединению литийорганического основания к атому углерода двойной связи C – N.[9]
Каталитическая реакция Шапиро
Традиционные реакции Шапиро требуют стехиометрического (иногда избыточного) количества основания для образования алкениллитиевых реагентов. Для решения этой проблемы Ямамото и его коллеги разработали эффективный стереоселективный и региоселективный путь к алкенам с использованием комбинации кетон-фенилазиридинилгидразонов в качестве эквивалентов аренсульфонилгидразона с каталитическим количеством амидов лития. Требуемый фенилазиридинилгидразон был получен конденсацией 1-ундекана с 1-ундеканом -амино-2-фенилазиридин. Обработка фенилазиридинилгидразона 0,3 эквивалентами LDA в эфире привела к алкену, показанному ниже, с СНГ:транс соотношение 99,4: 0,6. Это соотношение определяли с помощью капиллярного анализа ГЖХ после преобразования в соответствующие эпоксиды с mCPBA. Загрузка катализатора может быть уменьшена до 0,05 эквивалента в случае реакции в масштабе 30 ммоль.
Высокая стереоселективность достигается за счет преимущественного отщепления α-метиленового водорода син к фенилазиридину, а также объясняется внутренним хелатированием литиированного промежуточного звена.[10]

Комбинированная реакция Шапиро-Судзуки в одном сосуде на месте
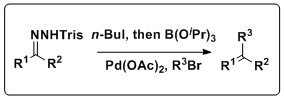
Реакцию Шапиро также можно сочетать с Сузуки реакция для производства различных олефиновых продуктов. Кей и его коллеги разработали методологию, которая объединяет эти реакции в одном процессе, который не требует изоляции бороновая кислота, неудача традиционной муфты Suzuki. Эта реакция имеет широкий диапазон, допускающий множество трисилгидразонов и арилгалогенидов, а также несколько растворителей и источников Pd.[11]
Применение реакции Шапиро в полном синтезе
Реакция Шапиро использовалась для получения олефинов, превращающихся в сложные натуральные продукты. К. Мори с соавторами хотели определить абсолютную конфигурацию группы фитокассана класса натуральных продуктов, называемых фитоалексины. Это было достигнуто путем приготовления встречающегося в природе (-) - фитокассана D из (р)-Кетон Виланда-Мишера. На пути к (-) - фитокассану D трициклический кетон подвергали воздействию условий реакции Шапиро с получением циклического алкенового продукта.[12]

Смотрите также
Рекомендации
- ^ Шапиро, Р. Х.; Lipton, M. F .; Колонко, К. Дж .; Buswell, R.L .; Капуано, Л. А. (1975). «Тозилгидразоны и алкиллитиевые реагенты: Подробнее о региоспецифичности реакции и улавливании трех промежуточных продуктов». Tetrahedron Lett. 16 (22–23): 1811–1814. Дои:10.1016 / S0040-4039 (00) 75263-4.
- ^ Шапиро, Роберт Х. (1976). «Алкены из тозилгидразонов». Органические реакции. Орг. Реагировать. 23. С. 405–507. Дои:10.1002 / 0471264180.or023.03. ISBN 978-0471264187.
- ^ Адлингтон, Роберт М .; Баррет, Энтони Г. М. (1983). «Недавние применения реакции Шапиро». Соотв. Chem. Res. 16 (2): 55–59. Дои:10.1021 / ar00086a004.
- ^ Шапиро, Роберт Х.; Хит, Марша Дж. (1967). «Тозилгидразоны. V. Взаимодействие тозилгидразонов с алкиллитиевыми реагентами. Новый синтез олефинов». Варенье. Chem. Soc. 89 (22): 5734–5735. Дои:10.1021 / ja00998a601.
- ^ Николау, Кириакос К.; Соренсен, Эрик Дж. (1996). Классика в полном синтезе: цели, стратегии, методы. Wiley. ISBN 9783527292318.
- ^ Фридман, Лестер; Литл, Роберт Л .; Райхле, Вальтер Р. (1960). "п-Толуолсульфонилгидразид ". Органический синтез. 40: 93.; Коллективный объем, 5, п. 1055
- ^ Шапиро, Р. Х.; Дункан, Дж. Х. (1971). «2-Борнен (1,7,7-Триметилбицикло [2.2.1] гепт-2-ен)». Органический синтез. 51: 66. Дои:10.15227 / orgsyn.051.0066.; Коллективный объем, 6
- ^ Чемберлин, А. Ричард; Liotta, Ellen L .; Бонд, Ф. Томас (1983). «Получение и реакции алкениллитиевых реагентов: 2-бутилборнена». Органический синтез. 61: 141. Дои:10.15227 / orgsyn.061.0141.; Коллективный объем, 7, п. 77
- ^ Чемберлин, А. Ричард; Блум, Стивен Х. (1990). «Литиоалкены из аренсульфонилгидразонов». Орг. Реагировать. 39 (1): 1–83. Дои:10.1002 / 0471264180.or039.01.
- ^ Маруока, Кейджи; Оиси, Масатака; Ямамото, Хисаши (1991). «Каталитическая реакция Шапиро». Варенье. Chem. Soc. 118 (9): 2289–2290. Дои:10.1021 / ja951422p.
- ^ Passafaro, Marco S .; Кей, Брайан А. (1996). "Один горшок на месте комбинированная реакция Шапиро-Сузуки ». Tetrahedron Lett. 37 (4): 429–432. Дои:10.1016/0040-4039(95)02210-4.
- ^ Ядзима, Арата; Мори, Кенджи (2000). «Синтез и абсолютная конфигурация (-) - фитокассана D, дитерпенового фитоалексина, выделенного из растений риса, Oryza sativa". Евро. J. Org. Chem. 2000 (24): 4079–4091. Дои:10.1002 / 1099-0690 (200012) 2000: 24 <4079 :: AID-EJOC4079> 3.0.CO; 2-R.