Реакция Хорнера – Уодсворта – Эммонса - Horner–Wadsworth–Emmons reaction
| Реакция Хорнера – Уодсворта – Эммонса | |
|---|---|
| Названный в честь | Леопольд Хорнер Уильям С. Уодсворт Уильям Д. Эммонс |
| Тип реакции | Реакция сцепления |
| Идентификаторы | |
| Портал органической химии | Виттиг-Хорнер-реакция |
| RSC ID онтологии | RXNO: 0000056 |
В Реакция Хорнера – Уодсворта – Эммонса (HWE) это химическая реакция используется в органическая химия стабилизированных фосфонат карбанионы с альдегиды (или же кетоны ) производить преимущественно E-алкены.[1]
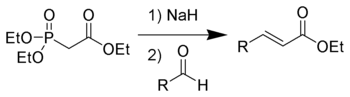

В 1958 г. Леопольд Хорнер опубликовал измененный Реакция Виттига с использованием карбанионов, стабилизированных фосфонатами.[2][3] Уильям С. Уодсворт и Уильям Д. Эммонс далее определил реакцию.[4][5]
В отличие от илиды фосфония используется в Реакция Виттига, карбанионы, стабилизированные фосфонатами, более нуклеофильный но менее простой. Аналогичным образом можно алкилировать карбанионы, стабилизированные фосфонатом. В отличие от илидов фосфония, побочный продукт диалкилфосфатной соли легко удаляется путем водный добыча.
Опубликовано несколько обзоров.[6][7][8][9][10][11]
Механизм реакции
Реакция Хорнера – Уодсворта – Эммонса начинается с депротонирование фосфоната, чтобы получить фосфонат карбанион 1. Нуклеофильное добавление карбаниона на альдегид 2 (или кетон) производство 3а или же 3b это ограничивающий шаг.[12] Если R2 = H, то промежуточные звенья 3а и 4а и промежуточные звенья 3b и 4b могут взаимодействовать друг с другом.[13] Финал устранение из оксафосфетаны 4а и 4b урожай (E) -алкен 5 и (Z) -алкен 6, побочным продуктом которого является диалкил-фосфат.

Соотношение алкена изомеры 5 и 6 зависит от стереохимический результат первоначального добавления карбаниона и способность промежуточных продуктов к уравновешивать.
В электроноакцепторная группа (EWG) альфа к фосфонату необходим для окончательного выведения. В отсутствие электроноакцепторной группы конечным продуктом является α-гидроксифосфонат. 3а и 3b.[14] Однако эти α-гидроксифосфонаты могут быть преобразованы в алкены по реакции с диизопропилкарбодиимид.[15]
Стереоселективность
Реакция Хорнера – Уодсворта – Эммонса способствует образованию (E) -алкены. Как правило, чем больше уравновешивание промежуточных соединений, тем выше селективность для (E) -алкенообразование.
Двузамещенные алкены
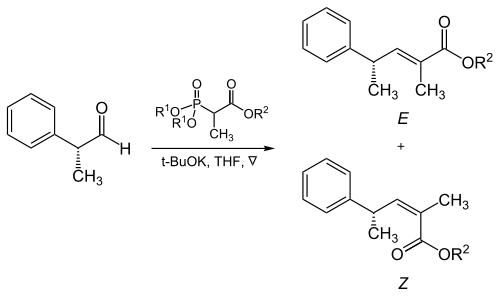
Томпсон и Heathcock провели систематическое исследование реакции метил 2- (диметилфосфоно) ацетата с различными альдегидами.[16] Хотя каждый эффект был небольшим, они имели кумулятивный эффект, позволяющий изменять стереохимический результат без изменения структуры фосфоната. Они нашли большее (E) -стереоселективность при следующих условиях:
- Увеличение стерического объема альдегида
- Более высокие температуры реакции (23 ° C выше −78 ° C)
- Ли > Na > K соли
- Использование растворителя DME над THF
В отдельном исследовании было обнаружено, что объемные фосфонатные и объемные электроноакцепторные группы повышают селективность по Е-алкену.
Тризамещенные алкены
Пространственная масса фосфонатных и электроноакцепторных групп играет решающую роль в реакции α-разветвленных фосфонатов с алифатическими альдегидами.[17]
| р1 | р2 | Соотношение алкенов (E: Z) |
|---|---|---|
| Метил | Метил | 5 : 95 |
| Метил | Этил | 10 : 90 |
| Этил | Этил | 40 : 60 |
| Изопропил | Этил | 90 : 10 |
| Изопропил | Изопропил | 95 : 5 |
Ароматный альдегиды производят почти исключительно (E) -алкены. В случае (Z) -алкены из ароматических альдегидов, можно использовать модификацию Стилла – Дженнари (см. ниже).
Олефинирование кетонов
Стереоселективность реакции Хорнера – Уодсворта – Эммонса кетоны от бедного до скромного.
Вариации
Базовые чувствительные основы
Поскольку многие субстраты нестабильны гидрид натрия, было разработано несколько процедур с использованием более мягких оснований. Масамунэ и Руш развили легкие условия, используя хлорид лития и DBU.[18] Ратке расширил это до литий или же магний галогениды с триэтиламин.[19] Некоторые другие базы оказались эффективными.[20][21][22]
Еще модификация
В. Кларк Стилл и К. Дженнари разработали условия, которые Z-алкены с отличной стереоселективностью.[23] Использование фосфонатов с электроноакцепторными группами (трифторэтил[24]) вместе с сильно диссоциирующими условиями (ХМДС и 18-крон-6 в THF ) может быть достигнуто почти исключительное производство Z-алкена.
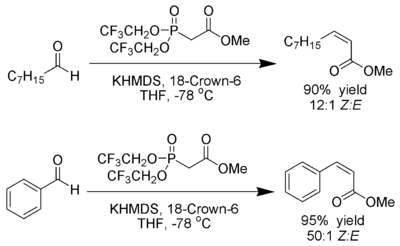
Андо предположил, что использование электронодефицитных фосфонатов ускоряет удаление промежуточных продуктов оксафосфетана.[25]
Смотрите также
- Реакция Виттига
- Реакция Михаэлиса – Арбузова
- Реакция Михаэлиса – Беккера
- Реакция Петерсона
- Теббе олефинирование
Рекомендации
- ^ Уодсворт, У. Орг. Реагировать. 1977, 25, 73. Дои:10.1002 / 0471264180.or025.02
- ^ Леопольд Хорнер; Hoffmann, H.M.R .; Виппель, Х. Бер. 1958, 91, 61–63.
- ^ Хорнер, Л .; Hoffmann, H.M.R .; Wippel, H.G .; Кларе, Г. Бер. 1959, 92, 2499–2505.
- ^ Wadsworth, W. S., Jr .; Эммонс, В. Д. Варенье. Chem. Soc. 1961, 83, 1733. (Дои:10.1021 / ja01468a042 )
- ^ Wadsworth, W. S., Jr .; Эммонс, В. Д. Органический синтез, Сб. Vol. 5, с. 547 (1973); Vol. 45, стр. 44 (1965). (Статья )
- ^ Wadsworth, W. S., Jr. Орг. Реагировать. 1977, 25, 73–253. (Рассмотрение)
- ^ Boutagy, J .; Томас, Р. Chem. Ред. 1974, 74, 87–99. (Рассмотрение, Дои:10.1021 / cr60287a005 )
- ^ Келли, С. Компр. Орг. Synth. 1991, 1, 729–817. (Рассмотрение)
- ^ Б. Э. Марьянов; Рейц, А. Chem. Ред. 1989, 89, 863–927. (Рассмотрение, Дои:10.1021 / cr00094a007 )
- ^ Бискелья, Дж. А., Орелли, Л. Р. Curr. Орг. Chem. 2012, 16, 2206–2230 (Обзор)
- ^ Бискелья, Дж. А., Орелли, Л. Р. Curr. Орг. Chem. 2015, 19, 744–775 (Обзор)
- ^ Larsen, R.O .; Акснес, Г. Фосфор сера 1983, 15, 218–219.
- ^ Lefèbvre, G .; Зейден-Пенне, Дж. J. Chem Soc., Chem. Commun. 1970, 1308–09.
- ^ Кори, Э. Дж.; Квятковский, Г. Т. Варенье. Chem. Soc. 1966, 88, 5654–56. (Дои:10.1021 / ja00975a057 )
- ^ Reichwein, J. F .; Пагенкопф, Б.Л. Варенье. Chem. Soc. 2003, 125, 1821–24. (Дои:10.1021 / ja027658s )
- ^ Томпсон, С.К .; Хиткок, К. Х. J. Org. Chem. 1990, 55, 3386–88. (Дои:10.1021 / jo00297a076 )
- ^ Nagaoka, H .; Киши, Ю. Тетраэдр 1981, 37, 3873–3888.
- ^ Blanchette, M.A .; Чой, В .; Davis, J. T .; Essenfeld, A. P .; Masamune, S .; Roush, W. R .; Сакаи, Т. Буквы Тетраэдра 1984, 25, 2183–2186.
- ^ Rathke, M. W .; Новак, М. J. Org. Chem. 1985, 50, 2624–2626. (Дои:10.1021 / jo00215a004 )
- ^ Патерсон, I .; Юнг, К.-С .; Смэйлл, Дж. Б. Synlett 1993, 774.
- ^ Simoni, D .; Росси, М .; Ронданин, Р .; Mazzali, A .; Baruchello, R .; Малагутти, С .; Роберти, М .; Инвидиата, Ф. П. Орг. Буквы 2000, 2, 3765–3768.
- ^ Blasdel, L.K .; Майерс, А.Г. Орг. Буквы 2005, 7, 4281–4283.
- ^ Тем не менее, W. C .; Дженнари, К. Буквы Тетраэдра 1983, 24, 4405–4408.
- ^ Patois, C .; Savignac, P .; About-Jaudet, E .; Коллиньон, Н. Органический синтез, Сб. Vol. 9, стр.88 (1998); Vol. 73, p.152 (1996). (Статья )
- ^ Андо, К. J. Org. Chem. 1997, 62, 1934–1939. (Дои:10.1021 / jo970057c )
