Биомолекулярная инженерия - Biomolecular engineering
Биомолекулярная инженерия представляет собой применение инженерных принципов и методов для целенаправленного манипулирования молекулами биологического происхождения. Биомолекулярные инженеры объединяют знания о биологические процессы с основными знаниями химическая инженерия чтобы сосредоточиться на решениях на молекулярном уровне вопросов и проблем в науках о жизни, связанных с среда, сельское хозяйство, энергия, промышленность, производство продуктов питания, биотехнология и медицина.
Биомолекулярные инженеры целенаправленно манипулируют углеводы, белки, нуклеиновые кислоты и липиды в рамках соотношения их структуры (см .: структура нуклеиновой кислоты, химия углеводов, структура белка,), функция (см .: функция белка ) и свойств, а также применительно к таким областям, как восстановление окружающей среды, растениеводство и животноводство, биотопливные элементы и биомолекулярная диагностика. Термодинамика и кинетика молекулярного распознавания в ферменты, антитела, Гибридизация ДНК, биоконъюгация / биоиммобилизация и биосепарации. Также уделяется внимание зачаткам инженерных биомолекул в клеточная сигнализация, кинетика роста клеток, инженерия биохимических путей и инженерия биореакторов.
График
История
Во время Второй мировой войны[1] потребность в большом количестве пенициллин приемлемого качества объединила инженеров-химиков и микробиологов, чтобы сосредоточиться на производстве пенициллина. Это создало подходящие условия для запуска цепочки реакций, которые привели к созданию области биомолекулярной инженерии. Биомолекулярная инженерия была впервые определена в 1992 г. Национальные институты здравоохранения США как исследования на стыке химической инженерии и биологии с упором на молекулярном уровне ". Хотя сначала биомолекулярная инженерия была определена как исследование, с тех пор она стала академической дисциплиной и областью инженерной практики. Герцептин гуманизированный Mab для лечения рака груди, стал первым лекарством, разработанным на основе подхода биомолекулярной инженерии и одобренным США FDA. Также, Биомолекулярная инженерия было прежнее название журнала Новая биотехнология.
Будущее
Биотехнологии будущего могут помочь объяснить биомолекулярную инженерию. Глядя на Закон Мура «Предсказание», в будущее квант а процессоры на основе биологии - это «большие» технологии. С помощью биомолекулярной инженерии можно изменять способ работы наших процессоров, чтобы они функционировали в том же смысле, что и работа биологической клетки. Биомолекулярная инженерия может стать одной из наиболее важных научных дисциплин благодаря своим достижениям в анализе паттернов экспрессии генов, а также целенаправленной манипуляции со многими важными биомолекулами для улучшения функциональности. Исследования в этой области могут привести к открытиям новых лекарств, улучшенным методам лечения и развитию новых технологий биопроцессов. С увеличением знаний о биомолекулах скорость обнаружения новых ценных молекул, включая, но не ограничиваясь, антитела, ферменты, вакцина, и терапевтические пептиды будет продолжать ускоряться. Биомолекулярная инженерия создаст новые разработки терапевтических лекарств и ценных биомолекул для лечения или профилактики рака, генетических заболеваний и других типов заболеваний. метаболические заболевания. Также есть ожидание промышленные ферменты которые спроектированы так, чтобы иметь желаемые свойства для улучшения процесса, а также для производства ценных биомолекулярных продуктов при гораздо более низкой стоимости производства. С помощью рекомбинантная технология, будут также производиться новые антибиотики, активные против резистентных штаммов.[2]
Основные биомолекулы
Биомолекулярная инженерия занимается манипуляциями со многими ключевыми биомолекулами. К ним относятся, но не ограничиваются ими, белки, углеводы, нуклеиновые кислоты и липиды. Эти молекулы являются основными строительными блоками жизни, и, контролируя, создавая и манипулируя их формой и функциями, общество получает множество новых возможностей и преимуществ. Поскольку каждый биомолекула отличается, существует ряд методов, используемых для управления каждым из них соответственно.
Белки
Белки полимеры, состоящие из аминокислота цепи, связанные с пептидные связи. У них есть четыре различных уровня структуры: первичный, вторичный, третичный и четвертичный. Первичная структура относится к аминокислотной последовательности основной цепи. Вторичная структура фокусируется на второстепенных конформациях, которые развиваются в результате образования водородных связей между аминокислотной цепью. Если большая часть белка содержит межмолекулярные водородные связи, его называют фибриллярным, и большая часть его вторичной структуры будет бета-листы. Однако, если большая часть ориентации содержит внутримолекулярные водородные связи, то белок называется глобулярным и в основном состоит из альфа спирали. Существуют также конформации, которые состоят из смеси альфа-спиралей и бета-листов, а также бета-спирали с альфа-листы.
Третичная структура белков связана с процессом их складывания и с тем, как устроена молекула в целом. Наконец, четвертичная структура - это группа третичных белков, которые объединяются и связываются. На всех этих уровнях у белков есть множество мест, в которых ими можно манипулировать и регулировать. Используются методы для воздействия на аминокислотную последовательность белка (сайт-направленный мутагенез), укладку и конформацию белка или укладку одного третичного белка в матрице четвертичного белка. Белки, которые являются основным объектом манипуляций, обычно ферменты. Это белки, которые действуют как катализаторы за биохимические реакции. Манипулируя этими катализаторами, можно контролировать скорость реакции, продукты и эффекты. Ферменты и белки важны для области биологии и исследований, в которых существуют определенные подразделения инженерии, сосредоточенные только на белках и ферментах.
Углеводы
Углеводы еще одна важная биомолекула. Это полимеры, называемые полисахариды, которые состоят из цепочек простых сахаров, связанных через гликозидные связи. Эти моносахариды состоят из пяти-шести углеродных колец, содержащих углерод, водород и кислород - обычно в соотношении 1: 2: 1 соответственно. Общие моносахариды глюкоза, фруктоза и рибоза. При соединении вместе моносахариды могут образовывать дисахариды, олигосахариды, и полисахариды: номенклатура зависит от количества моносахаридов, связанных вместе. Общие дисахариды, два моносахарида, соединенные вместе, являются сахароза, мальтоза, и лактоза. Важные полисахариды, звенья многих моносахаридов, являются целлюлоза, крахмал, и хитин.
Целлюлоза представляет собой полисахарид, состоящий из бета-1-4-связей между повторяющимися мономерами глюкозы. Это самый распространенный источник сахара в природе и основная часть бумажной промышленности. Крахмал также является полисахаридом, состоящим из мономеров глюкозы; однако они связаны через связь альфа 1-4 вместо бета. Крахмалы, особенно амилаза, важны во многих отраслях промышленности, включая бумажную, косметическую и пищевую. Хитин является производным целлюлозы, обладающим ацетамид группа вместо –OH на одном из атомов углерода. Ацетимидная группа деацетилируется, тогда полимерная цепь называется хитозан. Оба этих производных целлюлозы являются основным источником исследований в области биомедицины и медицины. пищевая промышленность. Было показано, что они помогают с свертывание крови, обладают антимикробными свойствами и применяются в диетических целях. Много инженерных и исследовательских работ сосредоточено на степени деацетилирование что обеспечивает наиболее эффективный результат для конкретных приложений.
Нуклеиновые кислоты
Нуклеиновые кислоты макромолекулы, которые состоят из ДНК и РНК, которые представляют собой биополимеры, состоящие из цепочек биомолекул. Эти две молекулы являются генетическим кодом и шаблоном, делающим жизнь возможной. Манипуляции с этими молекулами и структурами вызывают серьезные изменения в функциях и экспрессии других макромолекул. Нуклеозиды представляют собой гликозиламины, содержащие азотистые основания, связанные либо с рибоза или сахар дезоксирибозы через бета-гликозидную связь. Последовательность оснований определяет генетический код. Нуклеотиды представляют собой нуклеозиды, которые фосфорилируются специфическими киназы через фосфодиэфирная связь.[3] Нуклеотиды - это повторяющиеся структурные единицы нуклеиновых кислот. Нуклеотиды состоят из азотистого основания, пентозы (рибоза для РНК или дезоксирибозы для ДНК) и трех фосфатных групп. Видеть, Сайт-направленный мутагенез, рекомбинантная ДНК, и ELISA.
Липиды
Липиды биомолекулы, состоящие из глицерин производные инструменты, связанные с жирная кислота цепи. Глицерин это простой полиол имеющий формулу C3H5 (OH) 3. Жирные кислоты - это длинные углеродные цепи, которые имеют карбоновая кислота группа в конце. В углерод цепи могут быть насыщенными водородом; каждая углеродная связь занята атомом водорода или одинарной связью с другим углеродом в углеродной цепи, или они могут быть ненасыщенными; а именно, между атомами углерода в цепи существуют двойные связи. Общие жирные кислоты включают: лауриновая кислота, стеариновая кислота, и олеиновая кислота. Изучение и разработка липидов обычно фокусируется на манипуляциях с липидными мембранами и инкапсуляции. Клеточные мембраны и другие биологические мембраны обычно состоят из фосфолипидный бислой мембрана или ее производное. Наряду с изучением клеточных мембран липиды также являются важными молекулами для хранения энергии. Используя свойства инкапсуляции и термодинамический характеристики, липиды становятся значительными активами в структуре и энергия контроль при конструировании молекул.
Молекул
Рекомбинантная ДНК
Рекомбинантная ДНК представляют собой биомолекулы ДНК, содержащие генетические последовательности, не являющиеся естественными для генома организма. Используя рекомбинантные методы, можно точно вставлять, удалять или изменять последовательность ДНК, вне зависимости от расположения сайтов рестрикции. Рекомбинантная ДНК используется в широком спектре приложений.
Метод

Традиционный метод создания рекомбинантной ДНК обычно включает использование плазмиды в бактериях-хозяевах. Плазмида содержит генетическую последовательность, соответствующую сайту узнавания эндонуклеазы рестрикции, такой как EcoR1. После того, как фрагменты чужеродной ДНК, которые также были разрезаны той же эндонуклеазой рестрикции, были вставлены в клетку-хозяин, ген эндонуклеазы рестрикции экспрессируется путем нагревания,[4] или путем введения биомолекулы, такой как арабиноза.[5] После экспрессии фермент будет расщеплять плазмиду в соответствующем сайте узнавания, создавая липкие концы на плазмиде. Лигазы затем присоединяет липкие концы к соответствующим липким концам фрагментов чужеродной ДНК, создавая плазмиду рекомбинантной ДНК.
Достижения в генная инженерия сделали модификацию генов у микробов достаточно эффективной, что позволило создавать конструкции примерно за несколько недель. Это также позволило изменить сам геном организма. В частности, использование генов из бактериофаг лямбда используются в рекомбинации.[6] Этот механизм, известный как рекомбинирование, использует три белка Exo, Beta и Gam, которые создаются генами exo, bet и gam соответственно. Exo - это двухцепочечная ДНК экзонуклеаза с активностью от 5 до 3 футов. Он разрезает двухцепочечную ДНК, оставляя 3 'выступа. Бета - это белок, который связывается с одноцепочечной ДНК и помогает гомологичная рекомбинация за счет отжига между областями гомологии встроенной ДНК и хромосомной ДНК. Gam-функции для защиты вставки ДНК от разрушения естественными нуклеазы внутри клетки.
Приложения
Рекомбинантная ДНК может быть сконструирована для самых разных целей. Используемые методы позволяют специфическую модификацию генов, позволяя модифицировать любую биомолекулу. Он может быть разработан для лабораторных целей, где он может использоваться для анализа генов в данном организме. В фармацевтической промышленности белки можно модифицировать с помощью методов рекомбинации. Некоторые из этих белков включают человеческий инсулин. Рекомбинантный инсулин синтезируется путем вставки гена человеческого инсулина в Кишечная палочка, который затем производит инсулин для использования человеком.[7][8] Другие белки, такие как гормон роста человека,[9] фактор VIII, и вакцина против гепатита B производится с использованием аналогичных средств. Рекомбинантная ДНК также может использоваться для диагностических методов, включающих использование ELISA метод. Это позволяет конструировать антигены, а также присоединенные ферменты, чтобы распознавать различные субстраты или быть модифицированными для биоиммобилизации. Рекомбинантная ДНК также отвечает за многие продукты, используемые в сельскохозяйственной промышленности. Генетически модифицированная пища, Такие как золотой рис,[10] был разработан, чтобы увеличить производство витамин А для использования в обществах и культурах, где витамин А в пище недостаточно. Другие свойства, которые были созданы в сельскохозяйственных культурах, включают устойчивость к гербицидам.[11] и устойчивость к насекомым.[12]
Сайт-направленный мутагенез
Сайт-направленный мутагенез это техника, которая существует с 1970-х годов. Первые дни исследований в этой области привели к открытиям о потенциале некоторых химических веществ, таких как бисульфит и аминопурин изменить определенные базы в гене. Эти исследования были продолжены, и были разработаны другие процессы для создания определенных нуклеотидных последовательностей в гене, такие как использование рестрикционных ферментов для фрагментации определенных вирусных цепей и их использования в качестве праймеров для бактериальных плазмид. В современном методе, разработанном Майклом Смитом в 1978 г., используется олигонуклеотид, комплементарный бактериальной плазмиде с несоответствием одной пары оснований или серией несовпадений.[13]
Общая процедура
Сайт-направленный мутагенез это ценный метод, позволяющий заменять одно основание в олигонуклеотиде или гене. Основы этой методики включают подготовку праймера, который будет комплементарной цепью бактериальной плазмиды дикого типа. Этот праймер будет иметь несовпадение пар оснований на сайте, где требуется замена. Праймер также должен быть достаточно длинным, чтобы праймер отжигался с плазмидой дикого типа. После отжига праймера ДНК-полимераза завершит праймер. Когда бактериальная плазмида реплицируется, мутированная цепь также будет реплицироваться. Тот же метод можно использовать для создания вставки или удаления гена. Часто ген устойчивости к антибиотикам вставляют вместе с интересующей модификацией, и бактерии культивируют на среде с антибиотиком. Бактерии, которые не были успешно мутированы, не выживут в этой среде, и мутировавшие бактерии можно легко культивировать.

Приложения
Сайт-направленный мутагенез может быть полезен по разным причинам. Замена одной пары оснований может изменить кодон, и таким образом заменить аминокислота в протеине. Это полезно для изучения поведения определенных белков. Это также полезно, потому что ферментами можно целенаправленно манипулировать, изменяя определенные аминокислоты. При изменении аминокислоты, которая находится в непосредственной близости от активного сайта, кинетические параметры могут резко измениться, или фермент может вести себя иначе. Еще одно применение сайт-направленного мутагенеза - замена аминокислотного остатка вдали от активного сайта на лизин остаток или цистеин остаток. Эти аминокислоты облегчают ковалентное связывание фермента с твердой поверхностью, что позволяет повторно использовать ферменты и использовать ферменты в непрерывных процессах. Иногда к белкам добавляют аминокислоты с неприродными функциональными группами (например, кетоны и азиды).[14] Эти добавления могут быть предназначены для облегчения биоконъюгирования или для изучения влияния аминокислотных изменений на форму и функцию белков. Сочетание сайт-направленного мутагенеза и ПЦР используется для снижения активности интерлейкина-6 в раковых клетках.[15] Бактерии bacillus subtilis часто используется в сайт-направленном мутагенезе.[16] Бактерии выделяют через клеточную стенку фермент субтилизин. Биомолекулярные инженеры могут целенаправленно манипулировать этим геном, чтобы, по сути, превратить клетку в фабрику по производству любого белка, который вставлен в коды генов.
Биоиммобилизация и биоконъюгация
Биоиммобилизация и биоконъюгация - это целенаправленное манипулирование подвижностью биомолекулы химическими или физическими средствами для получения желаемого свойства. Иммобилизация биомолекул позволяет использовать характеристики молекулы в контролируемой среде. Например[17]иммобилизацию глюкозооксидазы на гранулах геля альгината кальция можно использовать в биореакторе. Полученный продукт не нуждается в очистке для удаления фермента, поскольку он останется связанным с шариками в колонке. Примерами типов иммобилизованных биомолекул являются ферменты, органеллы и полные клетки. Биомолекулы можно иммобилизовать с помощью ряда методов. Наиболее популярны физический улавливание, адсорбция и ковалентная модификация.
- Физическая ловушка[18] - использование полимера для содержания биомолекулы в матрице без химической модификации. Захват может происходить между решетками полимера, известным как улавливание геля, или внутри микрополостей синтетических волокон, так называемым улавливанием волокон. Примеры включают улавливание ферментов, таких как глюкозооксидаза, в гелевой колонке для использования в качестве биореактор. Важной характеристикой захвата является то, что биокатализатор остается структурно без изменений, но создает большие диффузионные барьеры для субстратов.
- Адсорбция - иммобилизация биомолекул за счет взаимодействия биомолекулы с группами на опоре. Это может быть физическая адсорбция, ионная связь или хелатирование связывания металла. Такие методы могут быть выполнены в мягких условиях и относительно просты, хотя связи сильно зависят от pH, растворителя и температуры. Примеры включают твердофазные иммуноферментные анализы.
- Ковалентная модификация - включает химические реакции между определенными функциональными группами и матрицей. Этот метод образует стабильный комплекс между биомолекулой и матрицей и подходит для массового производства. Из-за образования химической связи с функциональными группами может произойти потеря активности. Примеры используемых химических соединений: соединение DCC.[19] Соединение PDC и связывание EDC / NHS, все из которых используют преимущества реакционноспособных аминов на поверхности биомолекулы.
Поскольку иммобилизация ограничивает биомолекулу, необходимо следить за тем, чтобы функциональность не была полностью потеряна. Рассматриваемые переменные: pH,[20] температура, выбор растворителя, ионная сила, ориентация активных центров за счет конъюгации. Для ферментов конъюгация снижает кинетическую скорость из-за изменения трехмерной структуры, поэтому необходимо следить за тем, чтобы функциональность не была потеряна. Биоиммобилизация используется в таких технологиях, как диагностические биоанализы, биосенсоры, ELISA, и биоразделения. Интерлейкин (IL-6) также может быть биоиммобилизован на биосенсорах. Возможность наблюдать эти изменения в уровнях IL-6 важна при диагностике болезни. У больного раком будет повышенный уровень IL-6, и мониторинг этих уровней позволит врачу наблюдать за развитием болезни. Прямая иммобилизация IL-6 на поверхности биосенсора предлагает быструю альтернативу ELISA.[21]
Полимеразной цепной реакции

В полимеразной цепной реакции (ПЦР) - это научный метод, который используется для воспроизведения фрагмента ДНК молекулы на несколько порядков. ПЦР реализует цикл повторного нагрева и охлаждения, известный как термоциклирование вместе с добавлением Праймеры ДНК и ДНК-полимеразы выборочно воспроизвести ДНК интересующий фрагмент. Методика была разработана Кэри Маллис в 1983 г. во время работы в Cetus Corporation. Муллис продолжит выигрывать Нобелевская премия по химии в 1993 году в результате воздействия, которое ПЦР имел во многих областях, таких как Клонирование ДНК, Секвенирование ДНК, и генный анализ.[22]
Методы биомолекулярной инженерии, используемые в ПЦР
Ряд стратегий биомолекулярной инженерии сыграли очень важную роль в развитии и практике ПЦР. Например, решающим шагом в обеспечении точной репликации желаемого фрагмента ДНК является создание правильного Праймер ДНК. Наиболее распространенный метод синтеза праймеров - это фосфорамидит метод. Этот метод включает биомолекулярную инженерию ряда молекул для достижения желаемой последовательности праймера. Самый известный метод биомолекулярной инженерии, представленный в этом грунтовка Метод конструирования - первоначальная биоиммобилизация нуклеотида на твердой основе. Этот этап обычно выполняется путем образования ковалентной связи между 3’-гидроксильной группой первого нуклеотида праймера и твердым материалом носителя.[23]
Кроме того, как Праймер ДНК создаются определенные функциональные группы нуклеотидов для добавления к растущим грунтовка требуется блокировка для предотвращения нежелательных побочных реакций. Это блокирование функциональных групп, а также последующее деблокирование групп, связывание последующих нуклеотидов и возможное отщепление от твердой подложки[23] - это все методы манипулирования биомолекулами, которые можно отнести к биомолекулярной инженерии. Повышение уровня интерлейкина прямо пропорционально увеличению смертности больных раком груди. ПЦР в сочетании с вестерн-блоттингом и ELISA помогает определить взаимосвязь между раковыми клетками и IL-6.[24]
Иммуноферментный анализ (ELISA)
Иммуноферментный анализ это анализ, в котором используется принцип антитело -антиген распознавание для проверки наличия определенных веществ. Три основных типа ELISA косвенные тесты ELISA, бутерброд ELISA, и конкурентоспособные ELISA все полагаются на то, что антитела иметь сходство только с одним конкретным антиген. Кроме того, эти антигены или же антитела может быть прикреплен к ферменты который может реагировать на создание колориметрического результата, указывающего на присутствие антитело или же антиген представляет интерес.[25] Иммуноферментные анализы чаще всего используются в качестве диагностических тестов для обнаружения антител к ВИЧ в образцах крови для тестирования на ВИЧ, хорионический гонадотропин человека молекулы в моче, указывающие на беременность, и Микобактерии туберкулеза антитела в крови для тестирования пациентов на туберкулез. Более того, ELISA также широко используется в качестве токсикологического скрининга для проверки сыворотки людей на наличие запрещенных наркотиков.
Методы ИФА
Хотя есть три разных типа твердотельных иммуноферментные анализы, все три типа начинаются с биоиммобилизации либо антитело или же антиген на поверхность. Эта биоиммобилизация - первый пример биомолекулярной инженерии, который можно увидеть в ELISA выполнение. Этот этап может быть выполнен несколькими способами, включая ковалентную связь с поверхностью, которая может быть покрыта белком или другим веществом. Биоиммобилизацию также можно проводить через гидрофобные взаимодействия между молекулой и поверхностью. Потому что есть много разных типов ELISA используется для многих различных целей, биомолекулярная инженерия, которая требуется на этом этапе, зависит от конкретной цели ELISA.
Другой метод биомолекулярной инженерии, который используется в ELISA развитие - это биоконъюгация фермента к антитело или же антиген в зависимости от типа ELISA. В этом есть что учесть фермент биоконъюгация например, избегая вмешательства в активный сайт из фермент так же хорошо как антитело сайт связывания в случае, если антитело сопряжен с фермент. Этот биоконъюгация обычно осуществляется путем создания поперечных связей между двумя представляющими интерес молекулами и может потребовать большого количества различных реагентов в зависимости от природы конкретных молекул.[26]
Интерлейкин (IL-6) - это сигнальный белок, который, как известно, присутствует во время иммунного ответа. Использование бутербродного типа ELISA количественно определяет наличие этого цитокина в спинномозговой жидкости или образцах костного мозга.[27]
Приложения и поля
В промышленности
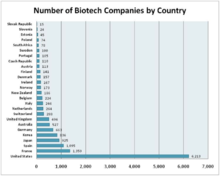

Биомолекулярная инженерия - обширная дисциплина, находящая применение во многих различных отраслях и областях. Таким образом, трудно определить общий взгляд на профессию биомолекулярной инженерии. Тем не менее, биотехнологическая промышленность дает адекватное представление. Индустрия биотехнологий или биотехнологическая промышленность охватывает все фирмы, которые используют биотехнологию для производства товаров или услуг или для выполнения биотехнологических исследований и разработок.[28] Таким образом, он охватывает многие из промышленных приложений дисциплины биомолекулярной инженерии. Изучив отрасль биотехнологий, можно сделать вывод, что основным лидером отрасли являются США, за которыми следуют Франция и Испания.[28] Верно также и то, что сфера биотехнологической промышленности и применения биомолекулярной инженерии в первую очередь клиническая и медицинская. Люди готовы платить за хорошее здоровье, поэтому большая часть денег, направляемых в биотехнологическую промышленность, остается в предприятиях, связанных со здоровьем.[нужна цитата ]
Увеличить масштаб
Масштабирование процесса включает использование данных экспериментальной операции (модель или пилотная установка) для проектирования большой (увеличенной в масштабе) установки коммерческого размера. Расширение масштабов - важная часть коммерциализации процесса. Например, инсулин произведены генетически модифицированными кишечная палочка бактерии были инициированы в лабораторных условиях, но для того, чтобы они стали коммерчески жизнеспособными, их необходимо было довести до промышленного уровня. Чтобы добиться такого масштабирования, необходимо было использовать множество лабораторных данных для проектирования устройств коммерческого размера. Например, один из этапов производства инсулина включает кристаллизацию инсулина гларгин высокой чистоты.[30] Чтобы осуществить этот процесс в крупном масштабе, мы хотим, чтобы соотношение мощность / объем как в лабораторных, так и в крупномасштабных кристаллизаторах было одинаковым, чтобы добиться гомогенного перемешивания.[31] Мы также предполагаем, что лабораторный кристаллизатор имеет геометрическое сходство с крупномасштабным кристаллизатором. Следовательно,
P / V α Nя3dя3
где Dя= диаметр крыльчатки кристаллизатора
Nя= скорость вращения рабочего колеса
Связанные отрасли
Биоинженерия
Широкий термин, охватывающий все инженерное дело, применяемое к наукам о жизни. В этой области исследования используются принципы биология наряду с инженерными принципами для создания рыночных продуктов. Немного биоинженерия приложения включают:
- Биомиметики - Изучение и разработка синтетических систем, имитирующих форму и функции природных веществ и процессов, полученных биологическим путем.
- Биопроцессная инженерия - Изучение и разработка технологического оборудования и оптимизации, которое помогает в производстве многих продуктов, таких как продукты питания и фармацевтические препараты.
- Промышленная микробиология - Реализация микроорганизмы в производстве промышленных товаров, таких как продукты питания и антибиотики. Еще одно распространенное применение промышленная микробиология это очистка сточных вод на химических предприятиях с использованием определенных микроорганизмы.
Биохимия
Биохимия - это изучение химических процессов в живых организмах, включая, помимо прочего, живую материю. Биохимические процессы управляют всеми живыми организмами и жизненными процессами, а область биохимии стремится понять эти процессы и управлять ими.
Биохимическая инженерия
- Биокатализ - Химические превращения с использованием ферменты.
- Биосепарации - Разделение биологически активных молекул.
- Термодинамика и Кинетика (химия) - Анализ реакций, связанных с ростом клеток и биохимическими веществами.
- Биореактор проектирование и анализ - Проектирование реакторов для проведения биохимических превращений.
Биотехнологии
- Биоматериалы - Разработка, синтез и производство новых материалов для поддержки клеток и тканей.
- Генная инженерия - Целенаправленное манипулирование геномами организмов для получения новых фенотипических признаков.
- Биоэлектроника, Биосенсор и Биочип - Разработанные устройства и системы для измерения, мониторинга и контроля биологических процессов.
- Биопроцессная инженерия - Разработка и обслуживание клеточных и ферментных процессов для производства тонкой химии и фармацевтических препаратов.
Биоэлектрическая инженерия
Биоэлектрическая инженерия включает электрические поля, создаваемые живыми клетками или организмами. Примеры включают электрический потенциал развивается между мышцами или нервами тела. Эта дисциплина требует знаний в области электричество и биология понять и использовать эти концепции для улучшения или улучшения существующих биопроцессов или технологий.
- Биоэлектрохимия - Химия, связанная с транспортом электронов / протонов по клетке
- Биоэлектроника - Область исследований сопряжения биологии и электроники
Биомедицинская инженерия
Биомедицинская инженерия - это подкатегория биоинженерия в котором используются многие из тех же принципов, но больше внимания уделяется медицинскому применению различных инженерных разработок. Некоторые приложения биомедицинская инженерия включают:
- Биоматериалы - Разработка новых материалов для имплантации в организм человека и анализ их воздействия на организм.
- Сотовая инженерия - Дизайн новых ячеек с использованием рекомбинантная ДНК и разработка процедур, позволяющих нормальным клеткам прилипать к искусственным имплантированным биоматериалы
- Тканевая инженерия - Дизайн новой ткани из основных биологических строительных блоков, чтобы сформировать новые ткани
- Искусственные органы - Применение тканевой инженерии ко всем органам
- Медицинская визуализация - Визуализация ткани с помощью Томография, МРТ, УЗИ, рентгеновский снимок или другие технологии
- Медицинская оптика и лазеры - применение лазеров для медицинской диагностики и лечения
- Реабилитационная техника - Дизайн устройств и систем, используемых для помощи инвалидам
- Человеко-машинный интерфейс - управление хирургическими роботами и дистанционными диагностическими и терапевтическими системами с использованием отслеживания взгляда, распознавания голоса и управления мышцами и мозгом.
- Человеческий фактор и эргономика - Разработка систем для повышения производительности человека в широком спектре приложений
Химическая инженерия
Химическая инженерия - это переработка сырья в химические продукты. Он включает в себя подготовку сырья для производства реагентов, химическую реакцию этих реагентов в контролируемых условиях, разделение продуктов, переработку побочных продуктов и удаление отходов. Каждый шаг включает в себя определенные базовые строительные блоки, называемые «единичные операции», такие как экстракция, фильтрация и дистилляция.[32] Эти единичные операции присутствуют во всех химических процессах. Биомолекулярная инженерия - это часть химической инженерии, которая применяет те же принципы к обработке химических веществ, производимых живыми организмами.
Образование и программы
Недавно разработанные и предлагаемые программы бакалавриата в Соединенных Штатах, часто в сочетании с программой химического машиностроения, позволяют студентам достичь Б.С. степень. В соответствии с ABET (Совет по аккредитации в области инженерии и технологий), учебные программы по биомолекулярной инженерии "должны обеспечивать тщательное обучение фундаментальным наукам, включая химию, физику и биологию, с некоторым содержанием на продвинутом уровне… [и] инженерное применение этих фундаментальных наук для проектирования, анализа и контроль химических, физических и / или биологических процессов ".[33] Общие учебные программы состоят из основных инженерных курсов, включая транспорт, термодинамику, разделение и кинетику, с добавлением Науки о жизни курсы, в том числе биология и биохимия, а также специализированные биомолекулярные курсы, посвященные клеточной биологии, нано- и биотехнологии, биополимерам и т. д.[34]
Смотрите также
- Биомиметики
- Биофармацевтические препараты
- Биопроцессная инженерия
- Список биомолекул
- Молекулярная инженерия
Рекомендации
- ^ Стейнерт, Дэвид (2000) История медицины Второй мировой войны: «Архивная копия». Архивировано из оригинал на 2010-04-13. Получено 2012-04-12.CS1 maint: заархивированная копия как заголовок (связь)
- ^ Ryu, D. D. Y .; Нам, Д.-Х. (2000). «Последние достижения в биомолекулярной инженерии». Biotechnol. Прог. 16 (1): 2–16. Дои:10.1021 / bp088059d. PMID 10662483.
- ^ Слабо, Майкл Р. и Сигер, Спенсер Л. (2007). Органическая и биохимия сегодня (6-е изд.). Пасифик Гроув: Брукс Коул. ISBN 978-0-495-11280-8.
- ^ Редди, О. (2000). Технология рекомбинантной ДНК: лабораторное руководство. Нью-Дели: Allied Publishers. С. 65–80.
- ^ Даценко, К.А.; Ваннер, Б. (6 июня 2000 г.). «Одноступенчатая инактивация хромосомных генов в Escherichia coli K-12 с использованием продуктов ПЦР». PNAS. 97 (12): 6640–6645. Bibcode:2000PNAS ... 97.6640D. Дои:10.1073 / pnas.120163297. ЧВК 18686. PMID 10829079.
- ^ Шаран, К.; Томасон, Л.; Кузнецов, С.; Суд, Д.Л. (29 января 2009 г.). «Рекомбинирование: метод генной инженерии, основанный на гомологичной рекомбинации». Протоколы природы. 4 (2): 206–223. Дои:10.1038 / nprot.2008.227. ЧВК 2790811. PMID 19180090.
- ^ Gualandi-Signorini, A .; Георгий, Г. (2001). «Препараты инсулина - обзор». Европейский обзор медицинских и фармакологических наук. 5 (3): 73–83. PMID 12004916.
- ^ «Инсулин человеческий».
- ^ Von Fange, T .; McDiarmid, T .; MacKler, L .; Золотор, А. (2008). «Клинические исследования: Может ли рекомбинантный гормон роста эффективно лечить идиопатический низкий рост?». Журнал семейной практики. 57 (9): 611–612. PMID 18786336.
- ^ Е., X.; Аль-Бабили, С.; Клоти, А.; Чжан, Дж.; Лукка, П.; Бейер, П. (2000). «Разработка пути биосинтеза провитамина А (бета-каротин) в (не содержащий каротиноидов) эндосперм риса». Наука. 287 (5451): 303–305. Bibcode:2000Sci ... 287..303Y. Дои:10.1126 / science.287.5451.303. PMID 10634784.
- ^ Funke, T .; Han, H .; Healy-Fried, M .; Фишер, М .; Шенбрунн, Э. (2006). «Молекулярная основа устойчивости к гербицидам культур Roundup Ready». Труды Национальной академии наук. 103 (35): 13010–13015. Bibcode:2006PNAS..10313010F. Дои:10.1073 / pnas.0603638103. ЧВК 1559744. PMID 16916934.
- ^ Пейн, Дж.; Шиптон, К.А.; Чаггер, С.; Хауэллс, Р.; Кеннеди, М.Дж.; Вернон, Г.; Райт, С.Ю.; Хинчлифф, Э. (2005). «Повышение питательной ценности золотого риса за счет увеличения содержания провитамина А». Природа Биотехнологии. 23 (4): 482–487. Дои:10.1038 / nbt1082. PMID 15793573.
- ^ Хатчисон Калифорния, 3-й; Филлипс, S; Edgell, M. H .; Гиллам, S; Jahnke, P; Смит, М. (сентябрь 1978 г.). «Мутагенез в определенной позиции в последовательности ДНК» (PDF). J. Biol. Chem. 253 (18): 6551–60. PMID 681366.
- ^ Пэн Вуа, Венцин Шуйя, Брайан Л. Карлсона, Нэнси Хуа, Дэвид Рабукаа, Джулия Лиа и Кэролайн Р. Бертоцци (2008). «Сайт-специфическая химическая модификация рекомбинантных белков, продуцируемых в клетках млекопитающих с использованием генетически кодируемой альдегидной метки». PNAS.
- ^ Braconi, C .; Huang, N .; Патель, Т. (2010). «MicroRNA-зависимая регуляция ДНК-метилтрансферазы-1 в злокачественных холангиоцитах человека. Гепатология». Гепатология. ppg 881-890.
- ^ Youngman, PJ; Perkins, JB; Лосик, Р. (1983). «Генетическая транспозиция и инсерционный мутагенез в Bacillus subtilis с транспозоном Streptococcus faecalis Tn917». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 80 (8): 2305–9. Bibcode:1983PNAS ... 80.2305Y. Дои:10.1073 / pnas.80.8.2305. ЧВК 393808. PMID 6300908.
- ^ Накао, Кацуми; Кифнер, Андреас; Фурумото, Кейджи; Харада, Цуёси (1997). «Производство глюконовой кислоты с иммобилизованной глюкозооксидазой в эрлифтных реакторах». Химическая инженерия. 52 (21–22): 4127–4133. Дои:10.1016 / с0009-2509 (97) 88932-4.
- ^ Хинберг; Капулас, А .; Корус, Р .; О'Дрисколл, К. (1974). «Гель-захват ферментов: кинетические исследования иммобилизованной глюкозооксидазы». Биотехнологии и биоинженерия. 16 (2): 159–168. Дои:10.1002 / бит. 260160202. PMID 4817138.
- ^ Чжан Я-Тао, Чжи, Тянь-Тянь, Чжан, Линь, Хуан, Хэ, Чен, Хуан-Линь. (2009). «Иммобилизация карбоангидразы путем встраивания и ковалентного связывания в нанокомпозитный гидрогель, содержащий гидротальцит». Полимер Том 50, выпуск 24; стр. 5693-5700.
- ^ Чжоу, Куинн З. К.; Чен, Сяо Донг (2001). «Влияние температуры и pH на каталитическую активность иммобилизованной β-галактозидазы из Kluyveromyces lactis». Журнал биохимической инженерии. 9 (1): 33–40. Дои:10.1016 / s1369-703x (01) 00118-8.
- ^ Чао; Чаунг; Ву (2010). «Количественное определение интерлейкина-6 в среде для культивирования клеток с использованием биосенсоров поверхностного плазмонного резонанса». Цитокин. 51 (1): 107–111. Дои:10.1016 / j.cyto.2010.04.004. PMID 20430640.
- ^ Бартлетт, Джон М.С., изд. (2003). Протоколы ПЦР (2-е изд.). Тотова, Нью-Джерси: Humana Press. С. 3–6. ISBN 978-0896036277.
- ^ а б Окор, Марси Осгуд, Карен (2008). Абсолютное и полное руководство по Принципам биохимии Ленингера: учебное пособие и руководство по решениям (5-е изд.). Нью-Йорк: W.H. Фримен. ISBN 978-1429212410.
- ^ Sullivan, N .; Sasser, A .; Axel, A .; Vesuna, F .; Raman, V .; Ramirez, N .; Оберышин, Т .; Холл, Б. (2009). «Интерлейкин-6 индуцирует фенотип эпителиально-мезенхимального перехода в клетках рака молочной железы человека». Онкоген. 28 (33): 2940–2947. Дои:10.1038 / onc.2009.180. ЧВК 5576031. PMID 19581928.
- ^ Lequin, RM (декабрь 2005 г.). «Иммуноферментный анализ (EIA) / иммуноферментный анализ (ELISA)». Клиническая химия. 51 (12): 2415–8. Дои:10.1373 / Clinchem.2005.051532. PMID 16179424.
- ^ Хермансон, Грег Т. (1995). Методы биоконъюгирования ([2. Доктор]. Ред.). Сан-Диего: академический. ISBN 978-0123423368.
- ^ Китантани, К.; Шелдон, К.; Анелли, В.; Дженкинс, Р.; Вс, Ю.; Грабовский, Г.; Обейд, Л.; Ханнун, Ю. (2009). «Кислая β-глюкозидаза 1 противодействует p38δ-зависимой индукции интерлейкина-6». Журнал биологической химии. 284 (19): 12979–12988. Дои:10.1074 / jbc.m809500200. ЧВК 2676030. PMID 19279008.
- ^ а б c Организация Экономического Сотрудничества и Развития. Ключевые показатели биотехнологии: биотехнологические фирмы. http://www.oecd.org/document/30/0,3746,en_2649_34451_40146462_1_1_1_1,00.html (по состоянию на 10 апреля 2012 г.).
- ^ Организация Экономического Сотрудничества и Развития. Ключевые показатели биотехнологии: приложения биотехнологии. http://www.oecd.org/document/30/0,3746,en_2649_34451_40146462_1_1_1_1,00.html (по состоянию на 10 апреля 2012 г.).
- ^ Мендельсон, Йенс-Петер. «Биотехнологический завод по производству инсулина» (PDF). Архивировано из оригинал (PDF) 12 июня 2013 г.. Получено 12 апреля, 2012.
- ^ Харрисон, Роджер Г. (2003). Наука и техника биоразделений. Тодд, Пол, Радж, Скотт Р., Петридес, Деметри, П. Нью-Йорк, Нью-Йорк: Издательство Оксфордского университета. С. 284–285. ISBN 978-0-19-512340-1.
- ^ Ауян, Санни, Ю. «Почему химическое машиностроение возникло в Америке, а не в Германии». Eidgenossische Technische Hochschule. Получено 11 апреля, 2012.
- ^ «Критерии аккредитации инженерных программ». ABET. Архивировано из оригинал на 2012-04-18. Получено 2012-04-11.
- ^ «Бакалавр биомолекулярной инженерии». Инженерная школа Милуоки. Архивировано из оригинал на 2012-04-20. Получено 2012-04-11.
дальнейшее чтение
- Биомолекулярная инженерия на интерфейсах (статья)
- Последние достижения в биомолекулярной инженерии
- Биомолекулярные сенсоры ISBN 074840791X (алк. бумага)

