Тетрафторид циркония - Zirconium tetrafluoride
 | |
| Имена | |
|---|---|
| Имена ИЮПАК Фторид циркония (IV) Тетрафторид циркония | |
| Идентификаторы | |
| |
3D модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.029.107 |
| Номер ЕС |
|
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| ZrF4 | |
| Молярная масса | 167,21 г / моль |
| Внешность | белый кристаллический порошок |
| Плотность | 4,43 г / см3 (20 ° С) |
| Температура плавления | 910 ° С (1670 ° F, 1180 К) |
| 1,32 г / 100 мл (20 ° С) 1,388 г / 100 мл (25 ° C) | |
| Структура | |
| Моноклиника, мс60 | |
| C12 / c1, № 15 | |
| Опасности | |
| точка возгорания | Негорючий |
| Смертельная доза или концентрация (LD, LC): | |
LD50 (средняя доза ) | 98 мг / кг (перорально, мышь) 98 мг / кг (перорально, крыса)[1] |
| Родственные соединения | |
Другой анионы | Хлорид циркония (IV) Бромид циркония (IV) Иодид циркония (IV) |
Другой катионы | Фторид титана (IV) Фторид гафния (IV) |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Фторид циркония (IV) (ZrF4 ) является неорганический химическое соединение. Это компонент ZBLAN фтористое стекло. Не растворяется в воде. Это главный компонент фторцирконатные стекла.
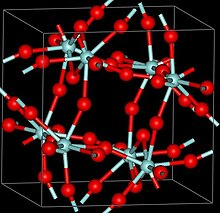
Три кристаллические фазы ZrF4 сообщалось, α (моноклинический ), β (четырехугольный, Символ Пирсона tP40, космическая группа P42 / m, № 84) и γ (структура неизвестна). β- и γ-фазы нестабильны и необратимо переходят в α-фазу при 400 ° C.[2]
Фторид циркония используется в качестве источника циркония в приложениях, чувствительных к кислороду, например производство металла.[3] Фторид циркония можно очистить дистилляция или же сублимация.[4]
Условия / вещества, которых следует избегать: влага, активные металлы, кислоты и окислители.
Фторид циркония в смеси с другими фториды это охлаждающая жидкость за реакторы на расплаве солей. В смеси с фторид натрия это кандидат охлаждающей жидкости для Усовершенствованный высокотемпературный реактор.
Вместе с урановой солью фторид циркония может быть компонентом теплоносителя топлива в расплавленных солевых реакторах. Смесь фторида натрия, фторида циркония и тетрафторид урана (53-41-6 мол.%) Использовалась в качестве теплоносителя в Эксперимент с реактором на самолете. Смесь фторид лития, фторид бериллия, фторид циркония и тетрафторид урана-233 использовался в Эксперимент в реакторе с расплавленной солью. (Уран-233 используется в ториевый топливный цикл реакторы.)
Рекомендации
- ^ «Соединения циркония (как Zr)». Немедленно опасные для жизни и здоровья концентрации (IDLH). Национальный институт охраны труда и здоровья (NIOSH).
- ^ Пол Л. Браун; Федерико Дж. Момпин; Джейн Перроне; Мириам Иллемассен (2005). Химическая термодинамика циркония. Gulf Professional Publishing. п. 144. ISBN 0-444-51803-7.
- ^ «Фторид циркония». Американские элементы. Получено 2009-07-07.
- ^ «Способ получения сверхчистых тетрафторидов циркония и гафния. Патент США 4578252». Получено 2009-07-07.
- ORNL / TM-2006/12 Оценка потенциальных жидких солевых хладагентов для Усовершенствованный высокотемпературный реактор (AHTR), март 2006 г. (по состоянию на 2008/9/18)
| Этот неорганический сложный –Связанная статья является заглушка. Вы можете помочь Википедии расширяя это. |
