Побочная реакция на препарат - Adverse drug reaction
| Побочная реакция на препарат | |
|---|---|
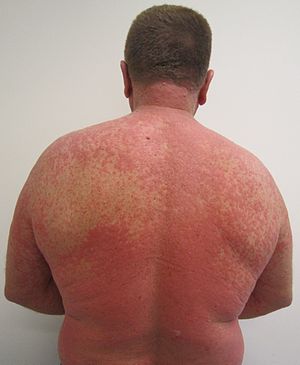 | |
| Сыпь из-за реакции на лекарство |
An побочная реакция на лекарство (ADR) - травма, вызванная медикамент.[1] Нежелательные реакции могут возникать после однократного приема или длительного приема препарат, средство, медикамент или результат комбинации двух или более лекарств. Значение этого термина отличается от термина "побочный эффект «потому что побочные эффекты могут быть как полезными, так и вредными.[2] Изучение ADR - это проблема области, известной как фармаконадзор. An побочное действие препарата (ADE) относится к любой травме, произошедшей во время употребления наркотика, независимо от того, определена ли она как причина травмы.[1] ADR - это особый тип ADE, в котором может быть показана причинная связь. Нежелательные реакции - это только один из видов вреда, связанного с лекарствами, так как вред также может быть вызван отказом от приема указанных лекарств.[3]
Классификация
ADR можно классифицировать, например, по причина и серьезность.
Причина
- Тип A: усиленные фармакологические эффекты - дозозависимые и предсказуемые
- Реакции типа А, составляющие примерно 80% побочных реакций на лекарства, обычно являются следствием первичного фармакологического эффекта лекарства (например, кровотечение при применении антикоагулянта. варфарин ) или низкий терапевтический индекс препарата (например, тошнота от дигоксин ), и поэтому они предсказуемы. Они зависят от дозы и обычно легкие, хотя могут быть серьезными или даже смертельными (например, внутричерепное кровотечение от варфарина). Такие реакции обычно возникают из-за неправильной дозировки, особенно при нарушении выведения препарата. Термин «побочные эффекты» часто применяется к незначительным реакциям типа А.[4]
- Тип B: Идиосинкразия
Типы A и B были предложены в 1970-х годах,[5] а другие типы были предложены впоследствии, когда первых двух оказалось недостаточно для классификации ADR.[6]
Серьезность
Соединенные штаты Управление по контролю за продуктами и лекарствами определяет серьезное нежелательное явление как одно, когда исход для пациента является одним из следующих:[7]
- Смерть
- Опасный для жизни
- Госпитализация (первоначальная или длительная)
- Инвалидность - значительное, стойкое или постоянное изменение, нарушение, повреждение или нарушение функции / структуры тела пациента, физической активности или качества жизни.
- Врожденная аномалия
- Требуется вмешательство для предотвращения необратимого ухудшения или повреждения
Серьезность - это балл по произвольной шкале интенсивности рассматриваемого нежелательного явления. Термины «тяжелый» и «серьезный» применительно к нежелательным явлениям технически сильно различаются. Их легко спутать, но их нельзя использовать взаимозаменяемо, что требует осторожности при использовании.
Головная боль является сильной, если вызывает сильную боль. Существуют шкалы вроде «визуальной аналоговой шкалы», которые помогают клиницистам оценить степень тяжести. С другой стороны, головная боль обычно не является серьезной (но может быть в случае субарахноидального кровотечения, субдурального кровотечения, даже мигрень может временно соответствовать критериям), если она также не удовлетворяет критериям серьезности, перечисленным выше.
Расположение
Побочные эффекты может быть локальным, то есть ограниченным определенным местом, или системным, когда лекарство вызывало побочные эффекты на протяжении всего Систематическая циркуляция.
Например, некоторые глазные гипотензивные средства вызывают системные эффекты,[8] хотя они управляются на местном уровне как слезы, так как фракция уходит в системный кровоток.
Механизмы
Поскольку исследования лучше объясняют биохимию употребления наркотиков, меньше нежелательных реакций относятся к типу B и больше - к типу A. Общие механизмы:
- Аномальная фармакокинетика из-за
- генетический факторы
- сопутствующий болезненные состояния
- Синергетический эффекты между
- лекарство и болезнь
- два препарата
- Антагонизм эффекты между
- лекарство и болезнь
- два препарата
Аномальная фармакокинетика
Коморбидные болезненные состояния
Различные заболевания, особенно те, которые вызывают почечный или печеночный недостаточность, может изменить метаболизм лекарств. Доступны ресурсы, в которых сообщается об изменениях в метаболизме лекарства из-за болезненных состояний.[9]
Инструмент подбора лекарств для лечения коморбидных состояний при деменции[10] (МАТЧ-D ) предупреждает, что люди с деменцией с большей вероятностью испытают побочные эффекты и с меньшей вероятностью смогут достоверно сообщить о симптомах.[11]
Генетические факторы
Аномальный метаболизм лекарств может быть вызван унаследованными факторами окисления фазы I или конъюгации фазы II.[12][13] Фармакогеномика это исследование наследственной основы патологических реакций на лекарства.
Реакции фазы I
Наследование ненормального аллели из цитохром P450 может изменить метаболизм лекарств. Доступны таблицы для проверки лекарственных взаимодействий из-за взаимодействий P450.[14][15]
Наследование ненормального бутирилхолинэстераза (псевдохолинэстераза ) может повлиять на метаболизм таких препаратов, как сукцинилхолин[16]
Фаза II реакции
Наследование ненормального N-ацетилтрансфераза которые конъюгировали некоторые препараты для облегчения выведения, могут влиять на метаболизм таких препаратов, как изониазид, гидралазин, и прокаинамид.[15][16]
Наследование ненормального тиопурин S-метилтрансфераза может повлиять на метаболизм тиопурин наркотики меркаптопурин и азатиоприн.[15]
Взаимодействие с другими лекарствами
Риск лекарственные взаимодействия увеличивается с полипрагмазия.
Связывание с белками
Эти взаимодействия обычно временные и незначительные, пока не будет достигнуто новое устойчивое состояние.[17][18] В основном они предназначены для лекарств без значительного метаболизма в печени. Основными белками плазмы для связывания лекарств являются:[19]
- альбумин
- α1-кислотный гликопротеин
- липопротеины
Некоторые лекарственные взаимодействия с варфарин связаны с изменениями связывания с белками.[19]
Цитохром P450
У пациентов наблюдается нарушение метаболизма цитохром P450 из-за наследственности ненормального аллели или из-за лекарственного взаимодействия. Доступны таблицы для проверки лекарственных взаимодействий из-за взаимодействий P450.[14]
Синергетические эффекты
Примером синергизма являются два препарата, которые продлевают QT интервал.
Оценка причинно-следственной связи
Оценка причинно-следственной связи используется для определения вероятности того, что лекарство вызвало подозрение на нежелательную реакцию. Существует ряд различных методов, используемых для оценки причинно-следственной связи, в том числе Алгоритм Наранхо, алгоритм Венулет и критерии оценки причинно-следственной связи ВОЗ. У каждого из них есть свои плюсы и минусы, и большинство из них требует определенного уровня экспертной оценки.[20]ADR не следует маркировать как «определенный», если только ADR не отменяется вызов-отказ-повторный вызов протокол (остановка и запуск рассматриваемого агента). Важна хронология начала подозреваемого НР, поскольку в качестве причины может быть задействовано другое вещество или фактор; сопутствующие лекарственные препараты и основные психические расстройства могут быть факторами в ADR.[2]
Присвоение причинно-следственной связи конкретному агенту часто оказывается трудным, если только событие не обнаружено во время клинического исследования или не используются большие базы данных. Оба метода имеют трудности и могут быть чреваты ошибкой. Даже в клинических исследованиях некоторые нежелательные реакции могут быть пропущены, поскольку требуется большое количество испытуемых, чтобы обнаружить эту побочную реакцию на лекарство. Психиатрические побочные эффекты часто упускаются из виду, поскольку они группируются в анкетах, используемых для оценки населения.[21][22]
Органы контроля
Во многих странах есть официальные органы, которые контролируют безопасность лекарств и реакции. На международном уровне КТО управляет Центр мониторинга Упсалы, а Европейский Союз управляет Европейское агентство по лекарствам (EMEA). в Соединенные Штаты, то Управление по контролю за продуктами и лекарствами (FDA) отвечает за мониторинг постмаркетинговых исследований. В Канаде Управление по продвижению товаров для здоровья Министерства здравоохранения Канады отвечает за надзор за продаваемыми товарами для здоровья. В Австралия, то Управление терапевтических товаров (TGA) проводит постмаркетинговый мониторинг терапевтических продуктов. В Великобритании Схема желтой карточки была основана в 1963 году.
Эпидемиология
Исследование Агентство медицинских исследований и качества (AHRQ) обнаружил, что в 2011 году седативные и снотворные средства были основным источником побочных эффектов, наблюдаемых в больницах. Примерно 2,8% всех нежелательных явлений, присутствующих при поступлении, и 4,4% нежелательных явлений, возникших во время пребывания в больнице, были вызваны седативным или снотворным препаратом.[23] Второе исследование, проведенное AHRQ, показало, что в 2011 году наиболее частыми конкретно выявленными причинами побочных эффектов лекарственных препаратов, которые возникли во время пребывания в больнице в США, были стероиды, антибиотики, опиаты / наркотики и антикоагулянты. Пациенты, проходившие лечение в городских клинических больницах, имели более высокий уровень НЯ, связанных с антибиотиками и опиатами / наркотиками, по сравнению с пациентами, лечившимися в городских больницах без обучения. Те, кто лечился в частных некоммерческих больницах, имели более высокие показатели большинства причин ADE по сравнению с пациентами, лечившимися в государственных или частных коммерческих больницах.[24]
В США в 2011 году у женщин была более высокая частота НЯ, связанных с опиатами и наркотиками, чем у мужчин, тогда как у пациентов мужского пола была более высокая частота НЯ с антикоагулянтами. Почти 8 из 1000 взрослых в возрасте 65 лет и старше испытали одно из четырех наиболее распространенных побочных эффектов (стероиды, антибиотики, опиаты / наркотики и антикоагулянты) во время госпитализации.[24] Исследование показало, что у 48% пациентов наблюдалась нежелательная лекарственная реакция хотя бы на одно лекарство, и участие фармацевта помогает выявить нежелательные лекарственные реакции.[25]
В 2012 году McKinsey & Co. пришли к выводу, что стоимость 35 миллионов предотвратимых побочных эффектов лекарственных препаратов составит 115 миллиардов долларов США.[26]
Смотрите также
- Предполагаемые проблемы в процессе одобрения лекарств
- Классификация фармако-терапевтических направлений
- Проблемы медикаментозной терапии
- EudraVigilance (Европейский Союз )
- История аптеки
- Ятрогенез
- Смертельная доза
- Список изъятых препаратов
- Парадоксальная реакция
- Полипрагмазия
- Токсичность
- Токсикология
- Медицинское письмо о лекарствах и терапевтических средствах
- Схема желтой карточки (ВЕЛИКОБРИТАНИЯ)
использованная литература
- ^ а б «Руководство по надлежащей клинической практике» (PDF). Международная конференция по гармонизации технических требований к регистрации лекарственных средств для человека. 10 июня 1996 г. с. 2. Получено 12 июля 2014.[постоянная мертвая ссылка ]
- ^ а б Небекер Дж. Р., Барач П., Самор М. Х. (май 2004 г.). «Разъяснение побочных эффектов лекарств: руководство для клинициста по терминологии, документации и отчетности». Анналы внутренней медицины. 140 (10): 795–801. Дои:10.7326/0003-4819-140-10-200405180-00017. PMID 15148066. S2CID 32296353.
- ^ Бозе К.С., Сарма Р.Х. (октябрь 1975 г.). «Определение интимных деталей конформации остова пиридиннуклеотидных коферментов в водном растворе». Сообщения о биохимических и биофизических исследованиях. 66 (4): 1173–9. Дои:10.1016 / 0006-291X (75) 90482-9. PMID 2.
- ^ Риттер, Дж. М. (2008). Учебник клинической фармакологии и терапии. Великобритания. п. 62. ISBN 978-0-340-90046-8.
- ^ Роулинз, доктор медицины, Томпсон Дж. У. Патогенез побочных реакций на лекарства. В: Дэвис Д.М., изд. Учебник нежелательных лекарственных реакций. Оксфорд: Издательство Оксфордского университета, 1977: 10.
- ^ Аронсон Дж. Медикаментозная терапия. В: Haslett C, Chilvers ER, Boon NA, Colledge NR, Hunter JAA, ред. Принципы и практика медицины Дэвидсона 19-е изд. Эдинбург: Elsevier Science, 2002: 147-
- ^ «MedWatch - что такое серьезное нежелательное явление?». В архиве из оригинала 29 сентября 2007 г.. Получено 18 сентября 2007.
- ^ Ранг, Х. П. (2003). Фармакология. Эдинбург: Черчилль Ливингстон. ISBN 978-0-443-07145-4. Стр. Решебника 146
- ^ «Клиническое употребление лекарств». Архивировано из оригинал 1 ноября 2007 г.. Получено 18 сентября 2007.
- ^ «Инструмент соответствия лекарств MATCH-D при коморбидных состояниях здоровья при деменции». www.match-d.com.au. Получено 1 июня 2019.
- ^ Пейдж А.Т., Поттер К., Клиффорд Р., Маклахлан А.Дж., Этертон-Бир С. (октябрь 2016 г.). «Инструмент адекватности лекарств для сопутствующих заболеваний при деменции: согласованные рекомендации многопрофильной группы экспертов». Журнал внутренней медицины. 46 (10): 1189–1197. Дои:10.1111 / imj.13215. ЧВК 5129475. PMID 27527376.
- ^ Филлипс К.А., Винстра Д.Л., Орен Э., Ли Дж.К., Сади В. (ноябрь 2001 г.). «Потенциальная роль фармакогеномики в уменьшении побочных реакций на лекарства: систематический обзор». JAMA. 286 (18): 2270–9. Дои:10.1001 / jama.286.18.2270. PMID 11710893.
- ^ Goldstein DB (февраль 2003 г.). «Фармакогенетика в лаборатории и клинике». Медицинский журнал Новой Англии. 348 (6): 553–6. Дои:10.1056 / NEJMe020173. PMID 12571264.
- ^ а б "Drug-Interactions.com". В архиве с оригинала от 30 августа 2007 г.. Получено 18 сентября 2007.
- ^ а б c Weinshilboum R (февраль 2003 г.). «Наследование и лекарственная реакция». Медицинский журнал Новой Англии. 348 (6): 529–37. Дои:10.1056 / NEJMra020021. PMID 12571261.
- ^ а б Evans WE, McLeod HL (февраль 2003 г.). «Фармакогеномика - расположение лекарств, мишени и побочные эффекты». Медицинский журнал Новой Англии. 348 (6): 538–49. Дои:10.1056 / NEJMra020526. PMID 12571262.
- ^ ДеВейн CL (2002). «Клиническое значение связывания лекарств, связывания белков и взаимодействий смещения связывания с лекарствами». Вестник психофармакологии. 36 (3): 5–21. PMID 12473961.
- ^ Бенет Л.З., Хенер Б.А. (март 2002 г.). «Изменения связывания с белками плазмы не имеют большого клинического значения». Клиническая фармакология и терапия. 71 (3): 115–21. Дои:10.1067 / mcp.2002.121829. PMID 11907485.OVID полный текст сводная таблица на OVID
- ^ а б CD Sands, Chan ES, Welty TE (октябрь 2002 г.). «Возвращаясь к значению взаимодействий смещения связывания варфарина с белками». Летопись фармакотерапии. 36 (10): 1642–4. Дои:10.1345 / aph.1A208. PMID 12369572. S2CID 20855578. Архивировано из оригинал 7 сентября 2008 г.. Получено 18 сентября 2007.
- ^ Дэвис EC, Роу PH, Джеймс С. и др. (2011). «Исследование разногласий в оценке причинно-следственной связи побочных реакций на лекарства». Фарм Мед. 25 (1): 17–24. Дои:10.1007 / bf03256843. S2CID 37301370. Архивировано из оригинал 1 июля 2012 г.. Получено 2 июн 2011.
- ^ Холви С., Коннолли А., Тейлор Д. (август 2010 г.). «Психиатрические побочные эффекты непсихиатрических препаратов». Британский журнал госпитальной медицины. 71 (8): 432–6. Дои:10.12968 / hmed.2010.71.8.77664. PMID 20852483.
- ^ Оцубо Т. (2003). «[Психиатрические осложнения лекарств]». Рёикибецу Шокогун Ширизу (40): 369–73. PMID 14626141.
- ^ Вайс А.Дж., Эликсхаузер А. (июль 2013 г.). «Происхождение побочных эффектов лекарственных препаратов в больницах США, 2011 г.» (Статистический отчет HCUP № 158). Роквилл, Мэриленд: Агентство медицинских исследований и качества.
- ^ а б Weiss A.J .; Эликсхаузер А. (октябрь 2013 г.). «Характеристики побочных эффектов лекарственных препаратов, возникших во время пребывания в больнице, 2011 г.» (Статистический отчет HCUP № 164). Роквилл, Мэриленд: Агентство медицинских исследований и качества.
- ^ Yeung EY (октябрь 2015 г.). «Побочные реакции на лекарства: потенциальная роль для фармацевтов». Британский журнал общей практики. 65 (639): 511.1–511. Дои:10.3399 / bjgp15X686821. ЧВК 4582849. PMID 26412813.
- ^ http://www.gs1.org/docs/healthcare/McKinsey_Healthcare_Report_Strength_in_Unity.pdf
дальнейшее чтение
- Частота нежелательных лекарственных реакций у пациентов с вирусом иммунодефицита человека, получающих высокоактивную антиретровирусную терапию ЧВК 3312730
внешние ссылки
| Классификация |
|---|