Clostridioides difficile инфекция - Clostridioides difficile infection
| Clostridioides difficile инфекционное заболевание | |
|---|---|
| Другие имена | C. difficile ассоциированная диарея (CDAD), Clostridium difficile инфекционное заболевание, C. difficile колит |
 | |
| Патологический образец, показывающий псевдомембранозный колит | |
| Специальность | Инфекционное заболевание |
| Симптомы | Диарея, лихорадка, тошнота, боль в животе[1] |
| Осложнения | Псевдомембранозный колит, токсичный мегаколон, перфорация толстой кишки, сепсис[1] |
| Причины | Clostridioides difficile распространение фекально-оральный путь[2] |
| Факторы риска | Антибиотики, ингибиторы протонной помпы, госпитализация, другие проблемы со здоровьем, пожилой возраст[1] |
| Диагностический метод | Культура стула, тестирование на бактерии ДНК или же токсины[1] |
| Профилактика | Мытье рук, уборка терминала в больнице[2] |
| Уход | Метронидазол, ванкомицин, фидаксомицин, трансплантация фекальной микробиоты[1][3] |
| Частота | 453 000 (США, 2011 г.)[2][4] |
| Летальные исходы | 29,000 (США)[2][4] |
Clostridioides difficile инфекционное заболевание (CDI или же C-diff), также известный как Clostridium difficile инфекционное заболевание, является симптоматическим инфекционное заболевание из-за спора -образующая бактерия Clostridioides difficile.[2][5] Симптомы включают водянистый понос, лихорадка, тошнота и боль в животе.[1] Это около 20% случаев диарея, связанная с антибиотиками.[1] Осложнения могут включать: псевдомембранозный колит, токсичный мегаколон, перфорация толстой кишки, и сепсис.[1]
Clostridioides difficile инфекция распространяется бактериальными спорами, обнаруженными в кал.[1] Поверхности могут быть заражены спорами с дальнейшим распространением через руки медицинских работников.[1] Факторы риска заражения включают: антибиотик или же ингибитор протонной помпы употребление, госпитализация, другие проблемы со здоровьем и пожилой возраст.[1] Диагноз ставится посев стула или тестирование на бактерии ДНК или же токсины.[1] Если у человека положительный результат теста, но нет никаких симптомов, это состояние известно как C. difficile колонизация а не инфекция.[1]
Меры профилактики включают: уборка терминала в больницах, ограничение использования антибиотиков, и мытье рук походы в больницы.[2] Санитайзер для рук на основе спирта не кажется эффективным.[2] Прекращение приема антибиотиков может привести к исчезновению симптомов в течение трех дней примерно у 20% инфицированных.[1] Антибиотики метронидазол, ванкомицин или же фидаксомицин, вылечит инфекцию.[1][3] Повторное тестирование после лечения, пока симптомы не исчезнут, не рекомендуется, так как человек может часто оставаться колонизированным.[1] О рецидивах сообщалось до 25% людей.[6] Некоторые предварительные доказательства указывают на трансплантация фекальной микробиоты и пробиотики может снизить риск рецидива.[2]
C. difficile инфекции встречаются во всех регионах мира.[7] В 2011 году в США было зарегистрировано 453 000 случаев заболевания, в результате которых погибло 29 000 человек.[2][4] В период с 2001 по 2016 год глобальные показатели заболеваемости увеличились.[2][7] C. difficile инфекции чаще возникают у женщин, чем у мужчин.[2] Бактерия была открыта в 1935 году и признана вызывающей болезнь в 1978 году.[7] В Соединенных Штатах, инфекции, связанные со здоровьем увеличивать стоимость лечения на 1,5 миллиарда долларов США каждый год.[8] Несмотря на то что C. difficile является распространенной инфекцией, связанной со здоровьем, не более 30% инфекций передаются в больницах.[9] Большинство инфекций передается за пределами больниц, где есть лекарства и недавние диарейные заболевания (например, злоупотребление слабительным или пищевое отравление из-за Сальмонеллез ), как полагают, создают риск колонизации.[10]
Признаки и симптомы
Признаки и симптомы ИКД варьируются от легкой диареи до тяжелой, угрожающей жизни. воспаление толстой кишки.[11]
У взрослых правило клинического прогноза нашел лучшее приметы быть значительной диареей («новое начало более трех частично сформированных или водянистых стула за 24-часовой период»), недавнее воздействие антибиотиков, боль в животе, лихорадка (до 40,5 ° C или 105 ° F) и характерный неприятный запах до табурета, напоминающего конский навоз.[12] В больнице предыдущее лечение антибиотиками плюс диарея или боль в животе имели чувствительность 86% и специфичность 45%.[13] В этом исследовании с преобладанием положительных тестов на цитотоксин 14%, положительная прогностическая ценность было 18%, а отрицательная прогностическая ценность было 94%.
У детей наиболее распространенным симптомом ИКД является водянистая диарея с как минимум тремя испражнениями в день в течение двух или более дней, которые могут сопровождаться лихорадкой, потерей аппетита, тошнотой и / или болью в животе.[14] У людей с тяжелой инфекцией также может развиться серьезное воспаление толстой кишки, и диарея будет незначительной или совсем не будет.
Причина

Заражение C. difficile бактерии Ответственный за C. difficile понос.
C. difficile

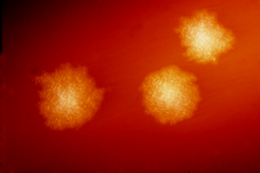
Клостридии анаэробный подвижный бактерии, повсеместно распространены в природе и особенно распространены в почве. Под микроскопом они выглядят как длинные клетки неправильной формы (часто в форме голени или веретена) с выпуклостью на концах. Под Окрашивание по Граму, C. difficile клетки Грамположительный и показать оптимальный рост на кровяной агар при температурах человеческого тела при отсутствии кислород. При стрессе бактерии производят споры которые способны переносить экстремальные условия, которые не переносятся активными бактериями.[15]
C. difficile может колонизировать человека двоеточие без симптомов; примерно 2–5% взрослого населения являются носителями, хотя в зависимости от демография.[15] Риск колонизации был связан с историей несвязанных диарейных заболеваний (например, злоупотребление слабительными и пищевое отравление из-за сальмонеллеза или Холерный вибрион инфекционное заболевание).[10]
Патогенный C. difficile штаммы производят несколько токсины.[16] Наиболее хорошо охарактеризованы энтеротоксин (Clostridium difficile токсин А ) и цитотоксин (Clostridium difficile токсин B ), оба из которых могут производить понос и воспаление у инфицированных людей, хотя их относительный вклад обсуждался.[15] Токсины A и B представляют собой глюкозилтрансферазы, которые нацелены и инактивируют Семейство Rho GTPases. Токсин B (цитотоксин) вызывает актин деполимеризация по механизму, коррелирующему с уменьшением АДФ-рибозилирование низкомолекулярных GTP-связывающих белков Rho.[17] Другой токсин, бинарный токсин, также был описан, но его роль в заболевании до конца не изучена.[18]
Лечение ИКД антибиотиками может быть затруднено как из-за: устойчивость к антибиотикам и физиологические факторы бактерий (образование спор, защитные эффекты псевдомембраны).[15] Появление нового высокотоксичного штамма C. difficile что устойчиво к фторхинолон антибиотики, такие как ципрофлоксацин и левофлоксацин, который, как утверждается, вызывает географически рассредоточенные вспышки в Северной Америке, было сообщено в 2005 году.[19] Соединенные штаты. Центры по контролю и профилактике заболеваний в Атланте предупредили о появлении эпидемического штамма с повышенной вирулентностью, устойчивостью к антибиотикам или и тем, и другим.[20]
C. difficile передается от человека к человеку фекально-оральный путь. Организм образует термостойкие споры, которые не уничтожаются средствами для мытья рук на спиртовой основе или обычной очисткой поверхностей. Таким образом, эти споры выживают в клинических условиях в течение длительного времени. Благодаря этому бактерии можно выращивать практически с любой поверхности. Когда споры попадают в организм, их кислотостойкость позволяет им проходить через желудок невредимыми. При воздействии желчные кислоты они прорастают и размножаются в вегетативные клетки толстой кишки. Люди, у которых в анамнезе не было желудочно-кишечных расстройств из-за использования антибиотиков или диарейных заболеваний, с меньшей вероятностью подверглись колонизации C. difficile.[10]
В 2005 году молекулярный анализ привел к идентификации C. difficile тип штамма, характеризуемый как группа BI эндонуклеаза рестрикции анализ, как североамериканский импульс-поле типа NAP1 по гель-электрофорез в импульсном поле и, как риботип 027; различная терминология отражает преобладающие методы, используемые для эпидемиологического типирования. Этот штамм упоминается как C. difficile BI / NAP1 / 027.[21]
Факторы риска
Антибиотики
C. difficile колит наиболее сильно связан с применением этих антибиотиков: фторхинолоны, цефалоспорины, и клиндамицин.[22]
Некоторые исследования предлагают распорядок дня использование антибиотиков в животноводстве способствует вспышкам бактериальных инфекций, таких как C. difficile.[23]
Среда здравоохранения
Люди чаще всего заражаются больницы, дома престарелых,[24] или другие медицинские учреждения, хотя инфекция за пределами медицинских учреждений растет. У человека может развиться инфекция, если он коснется предметов или поверхностей, загрязненных фекалиями, а затем коснется рта или слизистых оболочек. Медицинские работники могут распространять бактерии или загрязнять поверхности через контакт с руками.[25] Скорость C. difficile По оценкам, приобретение составляет 13% среди тех, кто находится в больнице до двух недель, и 50% при пребывании в больнице более четырех недель.[26]
Длительная госпитализация или проживание в доме престарелых в течение предыдущего года являются независимыми факторами риска повышенного колонизация.[27]
Лекарства, подавляющие кислотность
Увеличение частоты внебольничной ИКД связано с использованием лекарств для подавления Желудочный сок производство: Антагонисты Н2-рецепторов увеличили риск в 1,5 раза, а ингибиторы протонной помпы на 1,7 при использовании один раз в день и на 2,4 при использовании более одного раза в день.[28][29]
Диарейные заболевания
Люди, недавно перенесшие диарейные заболевания, подвергаются повышенному риску колонизации C. difficile при контакте со спорами, в том числе при злоупотреблении слабительными и патогенами желудочно-кишечного тракта.[10] Считается, что нарушения, которые увеличивают перистальтику кишечника, временно повышают концентрацию доступных пищевых сахаров, что позволяет C. difficile чтобы размножаться и закрепиться в кишечнике.[30] Хотя не все события колонизации приводят к заболеванию, бессимптомные носители остаются колонизированными в течение многих лет.[10] За это время обилие C. difficile значительно меняется изо дня в день, вызывая периоды повышенного выделения, что может существенно способствовать распространению внебольничных инфекций.[10]
Другой
В результате подавления здоровых бактерий из-за потери источника бактериальной пищи длительное использование элементарная диета увеличивает риск развития C. difficile инфекционное заболевание.[31] Низкий уровень сывороточного альбумина является фактором риска развития C. difficile инфекции и при заражении при тяжелом течении болезни.[32][33] Защитные эффекты сывороточного альбумина могут быть связаны со способностью этого белка связывать C. difficile токсин A и токсин B, что затрудняет проникновение в энтероциты.[33]
Патофизиология
Использование системных антибиотиков, включая пенициллины / цефалоспорины широкого спектра действия, фторхинолоны и клиндамицин, вызывает изменение нормальной микробиоты кишечника. В частности, когда антибиотик убивает другие конкурирующие бактерии в кишечнике, у оставшихся бактерий будет меньше конкуренции за пространство и питательные вещества. В конечном итоге, некоторые бактерии могут расти быстрее обычного. C. difficile один из таких видов бактерий. Помимо размножения в кишечнике, C. difficile также производит токсины. Без токсина A или токсина B, C. difficile может колонизировать кишечник, но вряд ли вызовет псевдомембранозный колит.[34] Колит, связанный с тяжелой инфекцией, является частью воспалительной реакции, когда «псевдомембрана» образована вязким скоплением воспалительных клеток, фибрин, и некротические клетки.[15]
Диагностика
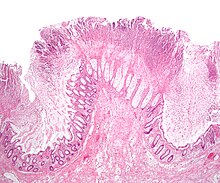


До появления тестов на обнаружение C. difficile токсинов, диагноз чаще всего ставили колоноскопия или же ректороманоскопия. Появление «псевдомембран» на слизистой оболочке двоеточие или же прямая кишка наводит на размышления, но не является диагностическим признаком заболевания.[35] Псевдомембраны состоят из экссудата из воспалительного мусора, белые кровяные клетки. Хотя колоноскопия и ректороманоскопия все еще используются, в настоящее время анализ стула на наличие C. difficile токсины часто являются диагностическим методом первой линии. Обычно проверяются только два токсина - токсин A и токсин B - но организм производит несколько других. Этот тест не является точным на 100%, со значительным количеством ложноотрицательных результатов даже при повторном тестировании.
Анализ цитотоксичности
C. difficile токсины имеют цитопатический эффект в культуре клеток, и нейтрализация любого эффекта, наблюдаемого с помощью специфических антисывороток, является практическим Золотой стандарт для исследований, изучающих новые диагностические методы ИКД.[15] Токсигенная культура, в которой организмы культивируются на селективных средах и тестируются на выработку токсинов, остается золотым стандартом и является наиболее чувствительным и специфическим тестом, хотя он медленный и трудоемкий.[36]
Токсин ELISA
Оценка токсинов A и B с помощью иммуноферментного анализа (ELISA ) для токсина A или B (или обоих) имеет чувствительность 63–99% и специфичность 93–100%.
Ранее эксперты рекомендовали отправить до трех образцов стула, чтобы исключить заболевание, если первоначальные тесты были отрицательными, но данные свидетельствуют о том, что повторное тестирование во время одного и того же эпизода диареи имеет ограниченную ценность и не поощряется.[37] C. difficile токсин должен выводиться из стула ранее инфицированного человека, если лечение эффективно. Многие больницы проверяют только распространенный токсин А. Штаммы, которые экспрессируют только токсин В, в настоящее время присутствуют во многих больницах, поэтому необходимо проводить тестирование на оба токсина.[38][39] Отсутствие тестирования на оба эти фактора может привести к задержке в получении лабораторных результатов, что часто является причиной длительного заболевания и плохих результатов.
Другие анализы стула
Табурет лейкоциты измерения и стул лактоферрин уровни также были предложены в качестве диагностических тестов, но могут иметь ограниченную диагностическую точность.[40]
ПЦР
Анализ образцов стула полимеразная цепная реакция в реальном времени способен обнаруживать C. difficile примерно в 93% случаев, а когда положительный результат является неверно положительным, примерно в 3% случаев.[41] Это более точно, чем анализ цитотоксигенной культуры или клеточной цитотоксичности.[41] Еще одно преимущество - результат достигается в течение трех часов.[41] К недостаткам можно отнести более высокую стоимость и тот факт, что тест ищет только ген токсина, а не сам токсин.[41] Последнее означает, что при использовании теста без подтверждения может возникнуть гипердиагностика.[41] Повторное тестирование может ввести в заблуждение, а тестирование образцов чаще одного раза в семь дней у людей без новых симптомов вряд ли даст полезную информацию.[42]
Профилактика
Самостоятельное размещение людей в частных комнатах важно для предотвращения распространения C. difficile.[43] Меры предосторожности при контакте - важная часть предотвращения распространения C. difficile. C. difficile не часто встречается у людей, которые не принимают антибиотики, поэтому ограничение использования антибиотиков снижает риск.[44]
Антибиотики
Самый эффективный метод предотвращения CDI - правильный антибиотик прописывание. В условиях больницы, где ИКД является наиболее распространенным явлением, большинство людей, у которых развивается ИКД, подвергаются воздействию антибиотиков. Хотя правильное назначение антибиотиков настоятельно рекомендуется, около 50% считаются нецелесообразными. Это одинаково, будь то в больнице, клинике, сообществе или академической среде. Было продемонстрировано, что снижение ИКД за счет ограничения приема антибиотиков или ограничения ненужных рецептов в целом, как во время вспышки, так и в условиях отсутствия вспышки, наиболее тесно связано со снижением ИКД. Кроме того, реакции на лекарства могут быть серьезными: инфекции ИКД были наиболее частой причиной побочных эффектов, наблюдаемых в больницах США в 2011 году.[45] В некоторых регионах Великобритании снижено использование фторхинолон антибиотики, по-видимому, снижают частоту ИКД.[46]
Пробиотики
Некоторые свидетельства указывают пробиотики может быть полезно для предотвращения инфекции и рецидива.[47][48] Лечение с Saccharomyces boulardii у тех, кто не ослаблен иммунитетом с C. difficile также может быть полезно.[49][50] Первоначально в 2010 г. Общество инфекционных болезней Америки не рекомендуется их использование из-за риска осложнений.[47][49] Однако в последующих обзорах не было обнаружено увеличения побочных эффектов при лечении.[48] и в целом лечение кажется безопасным и умеренно эффективным для предотвращения диареи, связанной с Clostridium difficile.[51]
Инфекционный контроль
Чтобы минимизировать риск передачи, необходимы строгие протоколы заражения.[52] Меры инфекционного контроля, такие как ношение перчаток и некритических медицинских устройств, используемых для одного человека с ИКД, эффективны для профилактики.[53] Это работает, ограничивая распространение C. difficile в условиях больницы. Кроме того, мытье с мылом и водой удалит споры с загрязненных рук, но протирка рук на спиртовой основе неэффективна.[54] Эти меры предосторожности должны оставаться в силе среди пациентов, находящихся в больнице, по крайней мере, в течение 2 дней после прекращения диареи.[55]
Отбеливающие салфетки, содержащие 0,55% гипохлорит натрия было показано, что убивают споры и предотвращают передачу.[56] Установка туалетов с крышкой и закрытие крышки перед смывом также снижает риск загрязнения.[57]
Те, у кого есть ИКД, должны находиться в палатах с другими людьми с ИКД или в одиночестве в больнице.[53]
Общая больница дезинфицирующие средства неэффективны против C. difficile споры и могут способствовать образованию спор, но дезинфицирующие средства, содержащие воду в соотношении 10: 1 отбеливать эффективно убивает споры.[58] Пары перекиси водорода (ВПЧ) системы, используемые для стерилизации комнаты после завершения лечения, показали, что они снижают уровень инфицирования и риск заражения других. Заболеваемость ИКД снизилась на 53%.[59] или 42%[60] через использование ВПЧ. Устройства для ультрафиолетовой очистки и обслуживающий персонал, специально предназначенный для дезинфекции комнат людей с C. difficile после выписки может оказаться эффективным.[61]
Уход
Проведение C. difficile без симптомов встречается часто. Лечение бессимптомных пациентов противоречиво. Как правило, легкие случаи не требуют специального лечения.[3][15] Пероральная регидратационная терапия полезен при лечении обезвоживания, связанного с диареей.
Лекарства
Несколько разных антибиотиков используются для C. difficile, причем доступные агенты более или менее эффективны.[62]
Ванкомицин или же фидаксомицин перорально обычно рекомендуются при легких, умеренных и тяжелых инфекциях.[63] Они также являются препаратами первой линии для беременных, особенно потому, что метронидазол может вызывать врожденные дефекты.[64] Типичный ванкомицин принимают внутрь четыре раза в день в течение 10 дней.[64] Его также можно вводить ректально, если у человека развивается кишечная непроходимость.[63]
Фидаксомицин переносится так же, как ванкомицин,[65] и может иметь более низкий риск рецидива.[62] Было обнаружено, что фидаксомицин так же эффективен, как ванкомицин, у пациентов с легким или умеренным заболеванием, и может быть лучше, чем ванкомицин, у пациентов с тяжелым заболеванием.[3][66] Фидаксомицин можно использовать у пациентов с рецидивирующими инфекциями, которые не реагируют на другие антибиотики.[66] Метронидазол внутрь рекомендуется в качестве альтернативного лечения только для C. difficile инфекции, когда пострадавший аллергический к лечению первой линии, не может их переносить или испытывает финансовые трудности, не позволяющие получить к ним доступ.[63][67] При молниеносной болезни ванкомицин внутрь и метронидазол внутривенно обычно используются вместе.[63]
Лекарства, используемые для замедления или остановки понос, Такие как лоперамид, считалось, что они могут ухудшить C. difficile болезнь, и они обычно не рекомендуются.[68] Однако свидетельств в пользу худших результатов при использовании недостаточно.[69] Холестирамин, ионообменная смола, эффективно связывает токсин А и В, замедляет перистальтику кишечника и помогает предотвратить обезвоживание.[70] Холестирамин рекомендуется с ванкомицином. Последним средством лечения людей с ослабленным иммунитетом является внутривенный иммуноглобулин.[70] Моноклональные антитела против C. difficile токсин А и C. difficile токсин B одобрены для предотвращения повторения C. difficile инфекция в том числе безлотоксумаб.[71]
Пробиотики
Доказательств в пользу использования пробиотиков для лечения активного заболевания недостаточно.[49][72][73][74]
Пересадка стула
Пересадка фекальной микробиоты, также известный как пересадка стула, эффективен примерно на 85–90% у тех, у кого антибиотики не помогли.[75][76] Он включает в себя инфузию микробиоты, полученной из фекалий здорового донора, чтобы обратить вспять бактериальный дисбаланс, ответственный за рецидивирующий характер инфекции.[77] Процедура восстанавливает нормальную микробиоту толстой кишки, уничтоженную антибиотиками, и восстанавливает устойчивость к колонизации путем Clostridioides difficile.[78] Побочных эффектов, по крайней мере на начальном этапе, немного.[76]
Некоторые свидетельства обнадеживают, что трансплантация фекалий может быть доставлена в виде таблеток.[79] Они доступны в США, но не одобрены FDA по состоянию на 2015 год.[80]
Хирургия
У тех, у кого тяжелая C. difficile колит, колэктомия может улучшить результаты.[81] Для определения того, кому операция принесет наибольшую пользу, могут использоваться конкретные критерии.[82]
Рецидивирующая инфекция
Рецидив ИКД встречается у 20–30% пациентов, частота рецидивов увеличивается с каждым последующим эпизодом.[83] В клинических условиях практически невозможно отличить рецидив, развивающийся как рецидив ИКД с тем же штаммом C. difficile по сравнению с повторным заражением, которое является результатом нового штамма.
Существует несколько вариантов лечения рецидивирующего Cdifficile инфекционное заболевание. Для первого эпизода повторяющегося Cdifficile В соответствии с рекомендациями IDSA от 2017 г. ванкомицин перорально принимается в дозе 125 мг четыре раза в день в течение 10 дней, если метронидазол использовался в начальном эпизоде. Если пероральный ванкомицин применялся для начального эпизода, то длительная пульсовая доза перорального ванкомицина 125 мг четыре раза в день в течение 10-14 дней с последующим снижением дозы (два раза в день в течение одной недели, затем каждые два-три дня в течение 2-8 недель. ) или фидаксомицин 200 мг два раза в день в течение 10 дней. Для второго рецидивирующего эпизода IDSA рекомендует варианты, включая вышеупомянутую пульсовую дозу перорального ванкомицина с последующим продолжительным снижением дозы; пероральный ванкомицин 125 мг четыре раза в день в течение 10 дней с последующим рифаксимин 400 мг 3 раза в сутки в течение 20 дней; фидаксомицин 200 мг два раза в день в течение 10 дней или трансплантация фекальной микробиоты.[67]
Для пациентов с инфекциями C. diff, которые не удается вылечить с помощью традиционных схем лечения антибиотиками, трансплантаты фекального микробиома могут похвастаться средним показателем излечения> 90%.[84] В обзоре 317 пациентов было показано, что это приводит к разрешению в 92% случаев стойких и рецидивирующих заболеваний.[85] Понятно, что восстановление кишечной флоры имеет первостепенное значение в борьбе с рецидивирующей ИКД. С помощью эффективной антибактериальной терапии можно уменьшить количество C. difficile, и со временем может развиться естественная резистентность к колонизации по мере восстановления естественного микробного сообщества. До завершения этого процесса может произойти повторное заражение или рецидив. Пересадка фекальной микробиоты может ускорить это выздоровление, напрямую заменяя отсутствующих членов микробного сообщества.[86] Однако фекалии человеческого происхождения трудно стандартизировать, и они связаны с множеством потенциальных рисков, включая передачу инфекционного материала и долгосрочные последствия инокуляции кишечника чужеродным фекальным материалом. В результате необходимы дальнейшие исследования для изучения долгосрочных эффективных результатов FMT.
Прогноз
После первого лечения метронидазолом или ванкомицином C. difficile рецидивирует примерно у 20% людей. Это увеличивается до 40% и 60% с последующими рецидивами.[87]
Эпидемиология
C. difficile диарея, по оценкам, случается у восьми из 100 000 человек ежегодно.[88] Среди тех, кто попадает в больницу, она встречается от четырех до восьми человек на 1000.[88] В 2011 году это привело к примерно полумиллиону инфекций и 29 000 смертей в США.[4]
Отчасти из-за появления фторхинолон -устойчивый штамм, C. difficileсмертность, связанная с этим заболеванием, увеличилась на 400% с 2000 по 2007 год в США.[89] Согласно CDC, "C. difficile стала наиболее распространенной микробной причиной инфекций, связанных с оказанием медицинской помощи, в больницах США и обходится до 4,8 млрд долларов в год в виде дополнительных затрат на здравоохранение только для учреждений неотложной помощи ".[90]
История
Иван Холл и Элизабет О'Тул первыми назвали бактерию Bacillus difficilis в 1935 году, выбрав свой специфический эпитет, потому что он был устойчив к первым попыткам изоляции и очень медленно рос в культуре.[87][91] Андре Ромен Прево впоследствии передал его в род Clostridium, что сделало его биномен Clostridium difficile.[92][93] Позднее его комбинация была изменена на Clostridiodes difficile после перехода в новый род Clostridioides.[94]
Псевдомембранозный колит впервые был описан как осложнение C. difficile инфекция 1978 г.,[95] когда токсин был изолирован от людей, страдающих псевдомембранозным колитом и Постулаты Коха были встречены.
Заметные вспышки
- 4 июня 2003 г. были зарегистрированы две вспышки высоковирулентного штамма этой бактерии в г. Монреаль, Квебек, и Калгари, Альберта. Источники сообщают, что число смертей составляет от 36 до 89, при этом в 2003 г. и в первые несколько месяцев 2004 г. было зарегистрировано около 1400 случаев. В конце 2004 г. ИКД продолжали оставаться проблемой в системе здравоохранения Квебека. По состоянию на март 2005 г. , он распространился на Торонто области, госпитализировано 10 человек. Один умер, а остальные выписывались.
- Аналогичная вспышка произошла в г. Больница Сток-Мандевиль в объединенное Королевство с 2003 по 2005 год. эпидемиология из C. difficile может помочь понять, как его распространение может быть связано со временем, которое пациент проводит в больнице и / или реабилитационном центре.Он также проверяет способность учреждений выявлять повышенные показатели и их способность реагировать более агрессивными кампаниями по мытью рук, карантинными методами и доступностью йогурта, содержащего живые культуры, для пациентов с риском заражения.
- Как канадские, так и английские вспышки, возможно, были связаны с более вирулентным штаммом бактерии NAP1 / 027. Известный как штамм Квебека, он был замешан в эпидемии в двух голландских больницах (Harderwijk и Амерсфорт, оба 2005 г.). Теория, объясняющая повышенную вирулентность 027, заключается в том, что он является гиперпродуцентом как токсинов A, так и B, и что определенные антибиотики могут стимулировать гиперпродукцию бактерий.
- 1 октября 2006 г. C. difficile как сообщается, убил по меньшей мере 49 человек в больницах Лестер, Англия, более восьми месяцев, согласно Национальный центр здоровья изучение. Еще 29 подобных дел расследовали коронеры.[96] Вскоре после этого просочилась служебная записка Министерства здравоохранения Великобритании, которая выявила серьезную обеспокоенность правительства по поводу бактерии, которая описывается как «эндемичная для всей системы здравоохранения».[97]
- 27 октября 2006 года в Квебеке от этой бактерии было приписано девять смертей.[98]
- 18 ноября 2006 года сообщалось, что эта бактерия стала причиной 12 смертей в Квебеке. Эта 12-я зарегистрированная смерть произошла всего через два дня после того, как в отеле Saint Hyacinthe's Honoré Mercier объявили, что вспышка находится под контролем. У 31 человека был диагностирован ИКД. Бригады по уборке приняли меры, чтобы устранить очаг.[99]
- C. difficile упоминался в 6 480 свидетельствах о смерти в 2006 году в Великобритании.[100]
- 27 февраля 2007 г. новая вспышка была выявлена в г. Центр здоровья Триллиум в Миссиссога, Онтарио, где 14 человек были диагностированы ИКД. Бактерии были того же штамма, что и в Квебеке. Официальные лица не смогли определить, C. difficile был ответственен за смерть четырех человек за предыдущие два месяца.[101]
- В период с февраля по июнь 2007 г. трое пациентов в больнице Лафлинстаун в Дублине, Ирландия, были обнаружены коронером как умершие в результате C. difficile инфекционное заболевание. В ходе расследования коронерский суд установил, что в больнице не было назначенной группы инфекционного контроля или консультанта-микробиолога в штате.[102]
- В период с июня 2007 г. по август 2008 г. объектом расследования был Северный фонд здравоохранения и социального обеспечения Северной Ирландии, район Антрим, долина Брейд, больницы Мид Ольстера. В ходе расследования рецензенты пришли к выводу, что C. difficile был причастен к 31 из этих смертей, как основная причина в 15 и как сопутствующая причина в 16. За это время обзор также выявил 375 случаев ИКД у тех, кто лечился в больнице.[103]
- В октябре 2007 г. Мейдстон и Танбридж Уэллс NHS Trust подвергся резкой критике со стороны Комиссия по здравоохранению относительно его обработки крупной вспышки C. difficile в своих больницах в Кент с апреля 2004 г. по сентябрь 2006 г. В своем отчете Комиссия оценила приблизительно 90 человек, «определенно или вероятно» умерших в результате инфекции.[104][105]
- В ноябре 2007 года штамм 027 распространился по нескольким больницам на юге Финляндии, при этом 10 смертей из 115 инфицированных были зарегистрированы 14 декабря 2007 года.[106]
- В ноябре 2009 года четыре смерти в больнице Богоматери Лурдес в Ирландии, возможно, связаны с CDI. Еще 12 человек дали положительный результат на инфекцию, и еще у 20 были обнаружены признаки инфекции.[107]
- С февраля 2009 года по февраль 2010 года 199 человек в больнице Херлев в Дании подозревались в заражении штаммом 027. В первой половине 2009 года 29 умерли в больницах Копенгагена после заражения этой бактерией.[108]
- В мае 2010 года 138 человек в четырех разных больницах Дании были инфицированы штаммом 027. [109] плюс были отдельные случаи в других больницах.[110]
- В мае 2010 года в австралийском штате Виктория от бактерии погибло 14 человек. Два года спустя такой же штамм бактерии был обнаружен в Новой Зеландии.[111]
- 28 мая 2011 года было сообщено о вспышке болезни в Онтарио, в результате чего по состоянию на 24 июля 2011 года погибло 26 человек.[112]
- В 2012/2013 гг. В одной больнице на юге Швеции (Истад) в общей сложности 27 человек были инфицированы и умерли 10 человек. Пятеро умерли от штамма 017.[113]
Этимология и произношение
Название рода от Греческий Klōstēr (κλωστήρ), "шпиндель",[114] и конкретное имя от латинский difficile, средний род единственного числа difficilis "трудный, упорный",[115] выбранный в отношении разборчивость при культивировании.
Что касается произношения текущего и прежнего родового присвоения, Clostridioides является /kлɒˌsтрɪdяˈɔɪdяs/ и Clostridium является /kлɒˈsтрɪdяəm/. Оба рода до сих пор имеют приписанные к ним виды, но теперь этот вид классифицируется как первый. По нормам биноминальная номенклатура, предполагается, что прежнее биномиальное название этого вида теперь является псевдонимом.
Что касается конкретного имени, /dɪˈжɪsɪля/[116] является традиционной нормой, отражающей то, как в медицинском английском обычно произносятся натурализованные новые латинские слова (что, в свою очередь, в значительной степени отражает традиционное английское произношение латыни ), хотя восстановленное произношение /dɪˈжɪkɪлeɪ/ также иногда используется ( классическая латынь произношение реконструируется как [kloːsˈtrɪdɪ.ũː dɪfˈfɪkɪlɛ]). Специфическое имя также часто произносится /ˌdяжяˈsял/, как если бы это был французский, который из предписывающий точка зрения - это "неправильное произношение"[116] но из лингвистически описательный точку зрения нельзя назвать ошибочной, потому что она так широко используется профессионалами здравоохранения; его можно охарактеризовать как «нежелательный вариант» с точки зрения наиболее регулярного использования Новой латыни в биноминальная номенклатура, что также является допустимой точкой зрения, хотя новые латинские специфические имена содержат такой широкий спектр внелатинских корней (включая фамилии и шутливые отсылки), что в любом случае задействовано внелатинское произношение (как видно, например, с Ба Хумбуги, Spongiforma squarepantsii, и сотни других).
Исследование
- По состоянию на 2019 год вакцины-кандидаты, обеспечивающие иммунитет против C. difficile токсин А и C. difficile токсин B наиболее продвинулись в клинических исследованиях, но не предотвращают бактериальную колонизацию.[117] Кандидат на вакцину от Pfizer находится в фазе 3 клинических испытаний, которые, как ожидается, будут завершены в сентябре 2020 г., кандидат вакцины - к GlaxoSmithKline находится в фазе 1 клинического исследования, которое, как ожидается, будет завершено в июне 2021 года.[118][119]
- CDA-1 и CDB-1 (также известные как MDX-066 / MDX-1388 и MBL-CDA1 / MBL-CDB1) - это экспериментальная комбинация моноклональных антител, совместно разработанная Медарекс и Массачусетские биологические лаборатории (MBL) для нацеливания и нейтрализации C. difficile токсины A и B для лечения ИКД. Merck & Co., Inc. получил всемирные права на разработку и коммерциализацию CDA-1 и CDB-1 по эксклюзивному лицензионному соглашению, подписанному в апреле 2009 года. Он предназначен в качестве дополнительной терапии к одному из существующих антибиотиков для лечения ИКД.[120][121][122]
- Нитазоксанид синтетическое производное нитротиазолилсалициламида, указанное в качестве противопротозойного средства (одобрено FDA для лечения инфекционной диареи, вызванной Криптоспоридиум парвум и Лямблии лямблии ), а также в настоящее время изучается в C. difficile инфекции против ванкомицина.[123]
- Рифаксимин,[123] представляет собой полусинтетический несистемный антибиотик на основе рифамицина для лечения ИКД клинической стадии. Он одобрен FDA для лечения инфекционной диареи и разрабатывается Salix Pharmaceuticals.
- Другие препараты для лечения ИКД находятся в стадии разработки и включают: рифалазил,[123] тигециклин,[123] рамопланин,[123] ридинилазол и SQ641.[124]
- Исследования изучали, насколько приложение имеет какое-либо значение, C. difficile. Считается, что аппендикс содержит хорошую кишечную флору. В исследовании, проведенном в 2011 году, было показано, что когда C. difficile Бактерии были введены в кишечник, в аппендиксе были клетки, которые усиливали реакцию организма на антитела. В В-клетки аппендикса мигрируют, созревают и увеличивают производство токсина А, специфичного IgA и IgG антитела, что приводит к повышению вероятности выживания хорошей кишечной флоры против C. difficile бактерии.[125]
- Принимая нетоксичные виды C. difficile после того, как инфекция дает многообещающие результаты в отношении предотвращения будущих инфекций.[126]
- Лечение бактериофагами направлено против специфических токсин-продуцирующих штаммов Cdifficile также проходят испытания.[67]
- Исследование, проведенное в 2017 году, связывало тяжелое заболевание с трегалоза в диете.[127]
Другие животные
- Колит-Х (в лошадях)
Рекомендации
- ^ а б c d е ж грамм час я j k л м п о п «Часто задаваемые вопросы о Clostridium difficile для медицинских работников». CDC. 6 марта 2012 г. В архиве из оригинала 2 сентября 2016 г.. Получено 5 сентября 2016.
- ^ а б c d е ж грамм час я j k Батлер М., Олсон А., Дреконья Д., Шаукат А., Швер Н., Шиппи Н., Уилт Т. Дж. (Март 2016 г.). «Ранняя диагностика, профилактика и лечение Clostridium difficile: обновление». Сравнительные обзоры эффективности AHRQ.: vi, 1. PMID 27148613.
- ^ а б c d Нельсон Р.Л., Суда К.Дж., Эванс СТ (март 2017 г.). «Лечение антибиотиками диареи, связанной с Clostridium difficile, у взрослых». Кокрановская база данных систематических обзоров. 3: CD004610. Дои:10.1002 / 14651858.CD004610.pub5. ЧВК 6464548. PMID 28257555.
- ^ а б c d Lessa FC, Mu Y, Bamberg WM, Beldavs ZG, Dumyati GK, Dunn JR и др. (Февраль 2015 г.). «Бремя инфекции Clostridium difficile в Соединенных Штатах». Медицинский журнал Новой Англии. 372 (9): 825–34. Дои:10.1056 / NEJMoa1408913. PMID 25714160.
- ^ Гух А.Ю., Кутти П.К. (октябрь 2018 г.). «Инфекция Clostridioides difficile». Анналы внутренней медицины. 169 (7): ITC49 – ITC64. Дои:10.7326 / AITC201810020. ЧВК 6524133. PMID 30285209.
- ^ Лонг СС, Пикеринг Л.К., Пробер К.Г. (2012). Принципы и практика детских инфекционных болезней (4-е изд.). Elsevier Health Sciences. п. 979. ISBN 978-1455739851. В архиве из оригинала 14 сентября 2016 г.
- ^ а б c Lessa FC, Gould CV, McDonald LC (август 2012 г.). «Текущее состояние эпидемиологии инфекции Clostridium difficile». Клинические инфекционные болезни. 55 Приложение 2: S65-70. Дои:10.1093 / cid / cis319. ЧВК 3388017. PMID 22752867.
- ^ Леффлер Д.А., Ламонт Дж. Т. (апрель 2015 г.). «Инфекция Clostridium difficile». Медицинский журнал Новой Англии. 372 (16): 1539–48. Дои:10.1056 / NEJMra1403772. PMID 25875259. S2CID 2536693.
- ^ Эйр Д. В., Кул М. Л., Уилсон Д. Д., Гриффитс Д., Воан А., О'Коннор Л. и др. (Сентябрь 2013). «Различные источники инфекции C. difficile идентифицированы при секвенировании всего генома». Медицинский журнал Новой Англии. 369 (13): 1195–205. Дои:10.1056 / NEJMoa1216064. ЧВК 3868928. PMID 24066741.
- ^ а б c d е ж VanInsberghe D, Elsherbini JA, Varian B, Poutahidis T, Erdman S, Polz MF (апрель 2020 г.). «Диарейные явления могут вызвать длительную колонизацию Clostridium difficile с периодическим цветением». Природная микробиология. 5 (4): 642–650. Дои:10.1038 / s41564-020-0668-2. PMID 32042128. S2CID 211074075.
- ^ Джоши Н.М., Маккен Л., Рэмптон Д.С. (декабрь 2012 г.). «Стационарная диарея и инфекция Clostridium difficile». Клиническая медицина. 12 (6): 583–8. Дои:10.7861 / Clinmedicine.12-6-583. ЧВК 5922602. PMID 23342416.
- ^ Bomers MK, Menke FP, Savage RS, Vandenbroucke-Grauls CM, van Agtmael MA, Covington JA, Smulders YM (апрель 2015 г.). «Быстрое, точное и обнаружение на месте C. difficile в образцах стула». Американский журнал гастроэнтерологии. 110 (4): 588–94. Дои:10.1038 / ajg.2015.90. PMID 25823766. S2CID 3051623.
- ^ Кац Д.А., Линч М.Э., Литтенберг Б. (май 1996 г.). «Правила клинического прогнозирования для оптимизации тестирования цитотоксинов на Clostridium difficile у госпитализированных пациентов с диареей». Американский журнал медицины. 100 (5): 487–95. Дои:10.1016 / S0002-9343 (95) 00016-X. PMID 8644759.
- ^ Морено М.А., Фуртнер Ф., Ривара Ф.П. (июнь 2013 г.). «Clostridium difficile: причина диареи у детей». JAMA Педиатрия. 167 (6): 592. Дои:10.1001 / jamapediatrics.2013.2551. PMID 23733223.
- ^ а б c d е ж грамм Райан К.Дж., Рэй К.Г., ред. (2004). Шеррис Медицинская микробиология (4-е изд.). Макгроу Хилл. С. 322–4. ISBN 978-0-8385-8529-0.
- ^ Ди Белла С., Асчензи П., Сиаракас С., Петросилло Н., ди Маси А. (май 2016 г.). «Токсины A и B Clostridium difficile: понимание патогенных свойств и внекишечных эффектов». Токсины. 8 (5): 134. Дои:10.3390 / токсины8050134. ЧВК 4885049. PMID 27153087.
- ^ Just I, Selzer J, von Eichel-Streiber C, Aktories K (март 1995). «На низкомолекулярный GTP-связывающий белок Rho влияет токсин А из Clostridium difficile». Журнал клинических исследований. 95 (3): 1026–31. Дои:10.1172 / JCI117747. ЧВК 441436. PMID 7883950.
- ^ Барт Х., Акторис К., Попофф М.Р., Стайлз Б.Г. (сентябрь 2004 г.). «Бинарные бактериальные токсины: биохимия, биология и применение общих белков Clostridium и Bacillus». Обзоры микробиологии и молекулярной биологии. 68 (3): 373–402, содержание. Дои:10.1128 / MMBR.68.3.373-402.2004. ЧВК 515256. PMID 15353562.
- ^ Лу В.Г., Пуарье Л., Миллер М.А., Огтон М., Либман М.Д., Мишо С. и др. (Декабрь 2005 г.). «Преимущественно клональная мультиинституциональная вспышка диареи, связанной с Clostridium difficile, с высокой заболеваемостью и смертностью». Медицинский журнал Новой Англии. 353 (23): 2442–9. Дои:10.1056 / NEJMoa051639. PMID 16322602. S2CID 14818750.
- ^ McDonald LC (август 2005 г.). «Clostridium difficile: ответ на новую угрозу со стороны старого врага» (PDF). Инфекционный контроль и больничная эпидемиология. 26 (8): 672–5. Дои:10.1086/502600. PMID 16156321. В архиве (PDF) из оригинала от 4 июня 2011 г.
- ^ Рупник М., Уилкокс М.Х., Гердинг Д.Н. (июль 2009 г.). «Инфекция Clostridium difficile: новые разработки в эпидемиологии и патогенезе». Обзоры природы. Микробиология. 7 (7): 526–36. Дои:10.1038 / nrmicro2164. PMID 19528959. S2CID 23376891.
- ^ Лучано Дж. А., Цукербраун Б. С. (декабрь 2014 г.). «Инфекция Clostridium difficile: профилактика, лечение и хирургическое лечение». Хирургические клиники Северной Америки. 94 (6): 1335–49. Дои:10.1016 / j.suc.2014.08.006. PMID 25440127.
- ^ "Ученые исследуют, C. difficile связано с употреблением мяса ". CBC News. 4 октября 2006 г. Архивировано с оригинал 24 октября 2006 г.
- ^ Думяти Г., Стоун Н.Д., Нейс Д.А., Црних С.Дж., Джамп Р.Л. (апрель 2017 г.). «Проблемы и стратегии профилактики передачи микроорганизмов с множественной лекарственной устойчивостью в домах престарелых». Текущие отчеты об инфекционных заболеваниях. 19 (4): 18. Дои:10.1007 / s11908-017-0576-7. ЧВК 5382184. PMID 28382547.
- ^ «Информация об инфекции Clostridium difficile для пациентов | HAI | CDC». www.cdc.gov. В архиве с оригинала 30 марта 2017 г.. Получено 19 апреля 2017.
- ^ Clabots CR, Johnson S, Olson MM, Peterson LR, Gerding DN (сентябрь 1992 г.). «Приобретение Clostridium difficile госпитализированными пациентами: доказательства колонизированных новых поступлений в качестве источника инфекции». Журнал инфекционных болезней. 166 (3): 561–7. Дои:10.1093 / infdis / 166.3.561. PMID 1323621.
- ^ Хэлси Дж. (Апрель 2008 г.). «Текущие и будущие методы лечения заболеваний, связанных с Clostridium difficile». Американский журнал фармации системы здравоохранения. 65 (8): 705–15. Дои:10.2146 / ajhp070077. PMID 18387898.
- ^ Howell MD, Novack V, Grgurich P, Soulliard D, Novack L, Pencina M, Talmor D (май 2010 г.). «Ятрогенное подавление кислоты в желудке и риск внутрибольничной инфекции Clostridium difficile». Архивы внутренней медицины. 170 (9): 784–90. Дои:10.1001 / archinternmed.2010.89. PMID 20458086.
- ^ Deshpande A, Pant C, Pasupuleti V, Rolston DD, Jain A, Deshpande N, et al. (Март 2012 г.). «Связь между терапией ингибиторами протонной помпы и инфекцией Clostridium difficile в метаанализе». Клиническая гастроэнтерология и гепатология. 10 (3): 225–33. Дои:10.1016 / j.cgh.2011.09.030. PMID 22019794.
- ^ Феррейра Дж. А., Ву К. Дж., Грицковиан А. Дж., Були Д. М., Веймер Британская Колумбия, Зонненбург Дж. Л. (декабрь 2014 г.). «Сукцинат, продуцируемый кишечной микробиотой, способствует развитию инфекции C. difficile после лечения антибиотиками или нарушения моторики». Клеточный хозяин и микроб. 16 (6): 770–7. Дои:10.1016 / j.chom.2014.11.003. ЧВК 4859344. PMID 25498344.
- ^ О'Киф SJ (январь 2010 г.). «Питание через зонд, микробиота и инфекция Clostridium difficile». Всемирный журнал гастроэнтерологии. 16 (2): 139–42. Дои:10.3748 / wjg.v16.i2.139. ЧВК 2806551. PMID 20066732.
- ^ Crook DW, Walker AS, Kean Y, Weiss K, Cornely OA, Miller MA и др. (Август 2012 г.). «Фидаксомицин против ванкомицина при инфекции Clostridium difficile: метаанализ основных рандомизированных контролируемых исследований». Клинические инфекционные болезни. 55 Приложение 2: S93-103. Дои:10.1093 / cid / cis499. ЧВК 3388031. PMID 22752871.
- ^ а б Сартелли М., Ди Белла С., МакФарланд Л. В., Кханна С., Фуруя-Канамори Л., Абузейд Н. и др. (2019). "difficile-инфекция у хирургических пациентов". Всемирный журнал неотложной хирургии. 14: 8. Дои:10.1186 / s13017-019-0228-3. ЧВК 6394026. PMID 30858872.
- ^ Кюне С.А., Картман С.Т., Хип Дж.Т., Келли М.Л., Кокейн А., Минтон Н.П. (октябрь 2010 г.). «Роль токсина А и токсина В в инфекции Clostridium difficile» (PDF). Природа. 467 (7316): 711–3. Bibcode:2010Натура.467..711K. Дои:10.1038 / природа09397. HDL:10044/1/15560. PMID 20844489. S2CID 4417414.
- ^ «Критерии хирургической патологии: псевдомембранозный колит». Стэнфордская школа медицины. В архиве из оригинала от 3 сентября 2014 г.
- ^ Мюррей PR, Барон EJ, Pfaller EA, Tenover F, Yolken RH, ред. (2003). Руководство по клинической микробиологии (8-е изд.). Вашингтон, округ Колумбия: ASM Press. ISBN 978-1-55581-255-3.[страница нужна ]
- ^ Дешпанде А., Пасупулети В., Патель П., Аджани Г., Холл Г., Ху Б. и др. (Август 2011 г.). «Повторный анализ стула для диагностики инфекции Clostridium difficile с использованием иммуноферментного анализа не увеличивает диагностический результат». Клиническая гастроэнтерология и гепатология. 9 (8): 665–669.e1. Дои:10.1016 / j.cgh.2011.04.030. PMID 21635969.
- ^ Салле А (2 марта 2009 г.). «Исследователи опровергают мифы о гастробуках». ABC Science Online. В архиве из оригинала 3 марта 2009 г.. Получено 2 марта 2009.
- ^ Лирас Д., О'Коннор-младший, Ховарт П.М., Самбол С.П., Картер Г.П., Фумунна Т. и др. (Апрель 2009 г.). «Токсин B необходим для вирулентности Clostridium difficile». Природа. 458 (7242): 1176–9. Bibcode:2009 Натур.458.1176L. Дои:10.1038 / природа07822. ЧВК 2679968. PMID 19252482.
- ^ а б c d е Chen S, Gu H, Sun C, Wang H, Wang J (июнь 2017 г.). «Быстрое обнаружение токсинов Clostridium difficile и лабораторная диагностика инфекций Clostridium difficile». Инфекционное заболевание. 45 (3): 255–262. Дои:10.1007 / s15010-016-0940-9. PMID 27601055. S2CID 30286964.
- ^ ЖУРНАЛ КЛИНИЧЕСКОЙ МИКРОБИОЛОГИИ, октябрь 2010 г., с. 3738–3741
- ^ «FAQ (часто задаваемые вопросы)» Clostridium Difficile"" (PDF). В архиве (PDF) из оригинала 7 декабря 2016 г.
- ^ «Информация об инфекции Clostridium difficile для пациентов | HAI | CDC». www.cdc.gov. В архиве из оригинала 16 декабря 2016 г.. Получено 18 декабря 2016.
- ^ Вайс А.Дж., Эликсхаузер А. Происхождение побочных эффектов лекарственных препаратов в больницах США, 2011 г. Статистический отчет HCUP № 158. Агентство медицинских исследований и качества, Роквилл, Мэриленд. Июль 2013. «Происхождение побочных эффектов лекарственных препаратов в больницах США, 2011 г. - статистический отчет № 158». В архиве из оригинала 7 апреля 2016 г.. Получено 9 февраля 2016.
- ^ Сдерживание антибиотиков, связанных с падением в Великобритании C. diff. Янв 2017 В архиве 6 февраля 2017 в Wayback Machine
- ^ а б Хайнеман Дж., Бубеник С., Макклейв С., Мартиндейл Р. (август 2012 г.). «Тушение пожара с помощью огня: не пора ли использовать пробиотики для борьбы с патогенными бактериальными заболеваниями?». Текущие отчеты гастроэнтерологии. 14 (4): 343–8. Дои:10.1007 / s11894-012-0274-4. PMID 22763792. S2CID 22813174.
- ^ а б Джонстон BC, Ma SS, Голденберг JZ, Thorlund K, Vandvik PO, Loeb M, Guyatt GH (декабрь 2012 г.). «Пробиотики для профилактики диареи, связанной с Clostridium difficile: систематический обзор и метаанализ». Анналы внутренней медицины. 157 (12): 878–88. Дои:10.7326/0003-4819-157-12-201212180-00563. PMID 23362517. S2CID 72364505.
- ^ а б c Na X, Келли C (ноябрь 2011 г.). «Пробиотики при инфекции Clostridium difficile». Журнал клинической гастроэнтерологии. 45 Дополнение (Suppl): S154-8. Дои:10.1097 / MCG.0b013e31822ec787. ЧВК 5322762. PMID 21992956.
- ^ McFarland LV (апрель 2006 г.). «Мета-анализ пробиотиков для профилактики диареи, связанной с антибиотиками, и лечения болезни Clostridium difficile». Американский журнал гастроэнтерологии (Представлена рукопись). 101 (4): 812–22. PMID 16635227.
- ^ Гольденберг Дж. З., Яп С., Литвин Л., Ло К. К., Бердсли Дж., Мертц Д., Джонстон BC (декабрь 2017 г.). «Пробиотики для профилактики диареи, связанной с Clostridium difficile, у взрослых и детей». Кокрановская база данных систематических обзоров. 12: CD006095. Дои:10.1002 / 14651858.CD006095.pub4. ЧВК 6486212. PMID 29257353.
- ^ Клиника Майо C. diff профилактика В архиве 8 октября 2013 г. Wayback Machine
- ^ а б Dubberke ER, Carling P, Carrico R, Donskey CJ, Loo VG, McDonald LC и др. (Июнь 2014 г.). «Стратегии профилактики инфекций Clostridium difficile в больницах неотложной помощи: обновление 2014 г.». Инфекционный контроль и больничная эпидемиология (Представлена рукопись). 35 (6): 628–45. Дои:10.1086/676023. PMID 24799639.
- ^ Рор Б. (21 сентября 2007 г.). «Спиртовая втирка, антисептические салфетки, непригодные для удаления. Clostridium difficile". Medscape. В архиве из оригинала 30 октября 2013 г.
- ^ Банах Д. Б., Бирман Г., Барнден М., Ханрахан Дж. А., Лика С., Морган Д. Д. и др. (Февраль 2018). «Срок действия контактных мер предосторожности при оказании неотложной помощи». Инфекционный контроль и больничная эпидемиология. 39 (2): 127–144. Дои:10.1017 / ice.2017.245. PMID 29321078.
- ^ Сэвидж Т.С., Урвил П., Озгуен Н., Али К., Чоудхури А., Ачарья В. и др. (Август 2011 г.). «S-нитрозилирование хозяина ингибирует гликозилирующие токсины, активируемые клостридиальными низкими молекулами». Природа Медицина. 17 (9): 1136–41. Дои:10,1038 / нм.2405. ЧВК 3277400. PMID 21857653. Сложить резюме – ScienceDaily (21 августа 2011 г.).
- ^ Лайдман Дж. (29 декабря 2011 г.). "Промывка микробов: распространение туалетов без крышки" C. difficile". Medscape. В архиве из оригинала от 20 апреля 2016 г.
- ^ «Чистящие средства делают насекомых сильными»'". BBC News Online. 3 апреля 2006 г. В архиве из оригинала 8 ноября 2006 г.. Получено 17 ноября 2008.
- ^ Бойс и другие. 2008
- ^ Manian и другие. 2010
- ^ «Эффективная обратная связь, устройство для ультрафиолетовой очистки и специальная бригада по уборке помещений значительно улучшают уборку помещений, снижают вероятность распространения обычных опасных инфекций». Агентство медицинских исследований и качества. 15 января 2014 г.. Получено 20 января 2014.
- ^ а б Дреконья Д.М., Батлер М., Макдональд Р., Блисс Д., Филис Г.А., Ректор Т.С., Уилт Т.Дж. (декабрь 2011 г.). «Сравнительная эффективность лечения Clostridium difficile: систематический обзор». Анналы внутренней медицины. 155 (12): 839–47. Дои:10.7326/0003-4819-155-12-201112200-00007. PMID 22184691.
- ^ а б c d McDonald LC, Gerding DN, Johnson S, Bakken JS, Carroll KC, Coffin SE и др. (Март 2018 г.). «Рекомендации по клинической практике для лечения инфекции Clostridium difficile у взрослых и детей: обновление 2017 года Американского общества инфекционных болезней (IDSA) и Общества эпидемиологии здравоохранения Америки (SHEA)». Клинические инфекционные болезни. 66 (7): 987–994. Дои:10.1093 / cid / ciy149. PMID 29562266.
- ^ а б Суравич С.М., Брандт Л.Дж., Бинион Д.Г., Анантакришнан А.Н., Карри С.Р., Гиллиган П.Х. и др. (Апрель 2013). «Рекомендации по диагностике, лечению и профилактике инфекций Clostridium difficile». Американский журнал гастроэнтерологии. 108 (4): 478–98, викторина 499. Дои:10.1038 / ajg.2013.4. PMID 23439232. S2CID 54629762.
- ^ Корнели О.А. (декабрь 2012 г.). «Текущие и новые варианты лечения инфекции Clostridium difficile: какова роль фидаксомицина?». Клиническая микробиология и инфекции. 18 Дополнение 6: 28–35. Дои:10.1111/1469-0691.12012. PMID 23121552.
- ^ а б Кроуфорд Т., Хьюсген Э, Данцигер Л. (июнь 2012 г.). «Фидаксомицин: новый макроциклический антибиотик для лечения инфекции Clostridium difficile». Американский журнал фармации системы здравоохранения. 69 (11): 933–43. Дои:10.2146 / ajhp110371. PMID 22610025.
- ^ а б c Рао К., Малани П.Н. (март 2020 г.). «Диагностика и лечение инфекции Clostridioides (Clostridium) difficile у взрослых в 2020 году». JAMA. 323 (14): 1403. Дои:10.1001 / jama.2019.3849. PMID 32150234.
- ^ Cunha BA (2013). Основные антибиотики 2013 (12-е изд.). п. 133. ISBN 978-1-284-03678-7. В архиве из оригинала от 8 сентября 2017 г.
- ^ Ку HL, Ку, округ Колумбия, Musher DM, DuPont HL (март 2009 г.). «Средства против моторики для лечения диареи и колита, вызванных Clostridium difficile». Клинические инфекционные болезни. 48 (5): 598–605. Дои:10.1086/596711. PMID 19191646.
- ^ а б Stroehlein JR (июнь 2004 г.). «Лечение инфекции Clostridium difficile». Современные варианты лечения в гастроэнтерологии. 7 (3): 235–239. Дои:10.1007 / s11938-004-0044-у. PMID 15149585. S2CID 25356792.
- ^ "Merck Newsroom Home". В архиве из оригинала 3 ноября 2016 г.. Получено 1 ноября 2016., FDA одобряет препарат ZINPLAVA ™ (безлотоксумаб) компании Merck для снижения частоты рецидивов инфекции Clostridium difficile (CDI) у взрослых пациентов, получающих антибактериальную медикаментозную терапию для лечения CDI, которые подвержены высокому риску рецидива CDI
- ^ Член парламента Бауэр, ван Диссель Дж. Т., Куйпер Э. Дж. (Декабрь 2009 г.). «Clostridium difficile: противоречия и подходы к лечению». Современное мнение об инфекционных заболеваниях. 22 (6): 517–24. Дои:10.1097 / QCO.0b013e32833229ce. PMID 19738464. S2CID 24040330.
- ^ Пиллаи А., Нельсон Р. (январь 2008 г.). Пиллай А (ред.). «Пробиотики для лечения колита, связанного с Clostridium difficile, у взрослых». Кокрановская база данных систематических обзоров (1): CD004611. Дои:10.1002 / 14651858.CD004611.pub2. PMID 18254055.
- ^ Уилкинс Т., Секвойя Дж. (Август 2017 г.). «Пробиотики для желудочно-кишечных состояний: краткое изложение доказательств». Американский семейный врач. 96 (3): 170–178. PMID 28762696.
тем не менее, существуют противоречивые результаты для инфекции C. difficile.
- ^ Берк К.Э., Ламонт Дж. Т. (август 2013 г.). «Фекальная трансплантация при рецидивирующей инфекции Clostridium difficile у пожилых людей: обзор». Журнал Американского гериатрического общества. 61 (8): 1394–8. Дои:10.1111 / jgs.12378. PMID 23869970.
- ^ а б Drekonja D, Reich J, Gezahegn S, Greer N, Shaukat A, MacDonald R и др. (Май 2015 г.). «Трансплантация фекальной микробиоты при инфекции Clostridium difficile: систематический обзор». Анналы внутренней медицины. 162 (9): 630–8. Дои:10,7326 / м 14-2693. PMID 25938992. S2CID 1307726.
- ^ ван Нуд Е., Вризе А., Ньивдорп М., Фуэнтес С., Зоетендал Е. Г., де Вос В. М. и др. (Январь 2013). «Дуоденальное вливание донорских фекалий при рецидивирующем Clostridium difficile». Медицинский журнал Новой Англии. 368 (5): 407–15. Дои:10.1056 / NEJMoa1205037. PMID 23323867. S2CID 25879411.
- ^ де Вриз J (август 2013 г.). «Медицинские исследования. Обещание кормы». Наука. 341 (6149): 954–7. Дои:10.1126 / science.341.6149.954. PMID 23990540.
- ^ Келлер JJ, Kuijper EJ (2015). «Лечение рецидивирующей и тяжелой инфекции Clostridium difficile». Ежегодный обзор медицины. 66: 373–86. Дои:10.1146 / annurev-med-070813-114317. PMID 25587656.
- ^ Смит PA (10 ноября 2015 г.). «Фекальные трансплантаты стали (в некоторой степени) более вкусными». Нью-Йорк Таймс. стр. D5. В архиве из оригинала 13 ноября 2015 г.. Получено 13 ноября 2015.
- ^ Бхангу А., Непогодиев Д., Гупта А., Торранс А., Сингх П. (ноябрь 2012 г.). «Систематический обзор и метаанализ результатов неотложной операции по поводу колита Clostridium difficile». Британский журнал хирургии. 99 (11): 1501–13. Дои:10.1002 / bjs.8868. PMID 22972525.
- ^ Осман К.А., Ахмед М.Х., Хамад М.А., Матур Д. (октябрь 2011 г.). «Экстренная колэктомия при фульминантном колите Clostridium difficile: достижение правильного баланса». Скандинавский журнал гастроэнтерологии. 46 (10): 1222–7. Дои:10.3109/00365521.2011.605469. PMID 21843039. S2CID 27187695.
- ^ Келли С. П., Ламонт Дж. Т. Clostridium difficile - сложнее, чем когда-либо. N Engl J Med. 2008. 359 (18): 1932–1940.
- ^ Ролке Ф. и Столлман Н. (2012). Трансплантация фекальной микробиоты при рецидиве инфекции Clostridium difficile. Терапевтические достижения в гастроэнтерологии, 5 (6), 403–420. https://doi.org/10.1177/1756283X12453637
- ^ Коул, С. А., и Шталь, Т. Дж. (2015). Стойкий и рецидивирующий колит, вызванный Clostridium difficile.Клиники хирургии толстой и прямой кишки, 28 (2), 65–69. https://doi.org/10.1055/s-0035-1547333
- ^ Дитерле, М. Г., Рао, К., и Янг, В. Б. (2019). Новые методы лечения и профилактические стратегии для первичных и рецидивирующих инфекций Clostridium difficile. Анналы Нью-Йоркской академии наук, 1435 (1), 110–138. https://doi.org/10.1111/nyas.13958
- ^ а б Kelly CP, LaMont JT (октябрь 2008 г.). «Clostridium difficile - сложнее, чем когда-либо». Медицинский журнал Новой Англии. 359 (18): 1932–40. Дои:10.1056 / NEJMra0707500. PMID 18971494.
- ^ а б Domino FJ, Baldor RA, ред. (2014). 5-минутная клиническая консультация 2014 г. (22-е изд.). Филадельфия: Wolters Kluwer Health / Lippincott Williams & Wilkins. п. 258. ISBN 978-1-4511-8850-9. В архиве из оригинала от 8 сентября 2017 г.
- ^ «Угрозы устойчивости к антибиотикам в США, 2013 г.» (PDF). Центры США по контролю и профилактике заболеваний. 2013. В архиве (PDF) из оригинала 17 ноября 2014 г.. Получено 3 ноября 2014.
- ^ «Инфекции, приобретенные в больницах, представляют серьезный риск - сообщения потребителей». www.consumerreports.org. В архиве с оригинала 10 декабря 2016 г.. Получено 18 декабря 2016.
- ^ Холл IC, О'Тул Э (1935). «Флора кишечника новорожденных с описанием нового патогенного анаэроба», Bacillus difficilis". Американский журнал болезней детей. 49 (2): 390–402. Дои:10.1001 / архпеди.1935.01970020105010.
- ^ Прево А.Р. (1938). "Études de systématique bactérienne. IV. Critique de la concept actuelle du genre Clostridium". Annales de l'Institut Pasteur. 61 (1): 84.
- ^ Де Вос П., Гаррити ГМ, Джонс Д., Криг Н.Р., Людвиг В., Рейни Ф.А., Шлейфер К., Уитман В.Б., ред. (2009). «Семья I. Clostridiaceae". В Фирмикуты. Руководство Берджи по систематической бактериологии. 3 (2-е изд.). Дордрехт: Спрингер. п. 771. ISBN 978-0-387-68489-5.
- ^ Лоусон PA, Citron DM, Tyrrell KL, Finegold SM (август 2016 г.). «Реклассификация Clostridium difficile как Clostridioides difficile (Холл и О'Тул, 1935 г.), Прево, 1938 г.». Анаэроб. 40: 95–9. Дои:10.1016 / j.anaerobe.2016.06.008. PMID 27370902.
- ^ Ларсон Х.Э., Прайс А.Б., Хонор П., Борриелло С.П. (май 1978 г.). «Clostridium difficile и этиология псевдомембранозного колита». Ланцет. 1 (8073): 1063–6. Дои:10.1016 / S0140-6736 (78) 90912-1. PMID 77366. S2CID 2502330.
- ^ «Доверие подтверждает 49 смертей супербактерий». BBC News Online. 1 октября 2006 г. В архиве из оригинала от 22 марта 2007 г.
- ^ Хоукс Н. (11 января 2007 г.). «Просочившаяся служебная записка показывает, что цели по борьбе с MRSA не будут достигнуты» (фрагмент). Времена. Лондон. Получено 11 января 2007.(требуется подписка)
- ^ "C. difficile обвиняется в 9 смертях в больнице недалеко от Монреаля ». Canoe.ca. 27 октября 2006 г. В архиве из оригинала 8 июля 2012 г.. Получено 11 января 2007.
- ^ "12 человек умер от C. difficile в больнице Квебека ". CBC Новости. 18 ноября 2006 г. Архивировано с оригинал 21 октября 2007 г.
- ^ Больницы поражены новой смертельной ошибкой В архиве 20 мая 2008 г. Wayback Machine Статья манчестерской бесплатной газеты «Метро», 7 мая 2008 г.
- ^ "C. difficile вспышка связана со смертельным исходом " В архиве 3 марта 2007 г. Wayback Machine. Новости CTV. 28 февраля 2007 г.
- ^ «Супербактерий в больницах стал причиной четырех смертей». Irish Independent. 10 октября 2007 г.
- ^ "Добро пожаловать на общественное расследование вспышки Clostridium difficile в больницах Northern Trust » В архиве 4 марта 2016 г. Wayback Machine
- ^ Наблюдательный орган за здравоохранением обнаружил серьезные недостатки в контроле за инфекциями в Мейдстоне и Танбридж-Уэллс NHS Trust (пресс-релиз), Великобритания: Комиссия по здравоохранению, 11 октября 2007 г., архивировано из оригинал 21 декабря 2007 г.
- ^ Смит Р., Рейнер Г., Адамс С. (11 октября 2007 г.). «Министр здравоохранения вмешивается в ссору с супербактериями». Daily Telegraph. Лондон. В архиве с оригинала от 20 апреля 2008 г.
- ^ Ärhäkkä suolistobakteeri on tappanut jo kymmenen potilasta - HS.fi - Kotimaa В архиве 15 декабря 2007 г. Wayback Machine
- ^ "Возможная связь C Diff со смертью Дроэды". Новости RTÉ. 10 ноября 2009 г. В архиве из оригинала от 23 октября 2012 г.
- ^ 199 человек пострадал от смертельной диареи в больнице Херлев В архиве 6 января 2016 г. Wayback Machine, BT 3 марта 2010 г.
- ^ (Херлев, Амагер, Гентофте и Видовре)
- ^ Четыре больницы поражены опасной бактерией В архиве 5 июля 2013 г. Wayback Machine, Новости ТВ2 7 мая 2010 г.
- ^ «Смертельный супербактерий достигает Новой Зеландии». 3 Новости NZ. 30 октября 2012 г. Архивировано с оригинал 15 апреля 2014 г.. Получено 29 октября 2012.
- ^ «C. difficile связана с 26-й смертью в Онтарио». CBC News. 25 июля 2011 г. В архиве из оригинала 24 июля 2011 г.. Получено 24 июля 2011.
- ^ "10 punkter for att förhindra smittspridning i Region Skåne" [10 баллов по предотвращению распространения инфекции в регионе Сконе] (на шведском языке). Архивировано из оригинал 5 марта 2015 г.
- ^ Лидделл-Скотт. «κλωστήρ». Греко-английский лексикон{{противоречивые цитаты}}
- ^ Коули К. "Difficilis". Латинский словарь и грамматика. Получено 16 марта 2013{{противоречивые цитаты}}
- ^ а б Медицинский словарь Стедмана, Вольтерс-Клувер, получено 11 апреля 2019.
- ^ Broecker F, Wegner E, Seco BM, Kaplonek P, Bräutigam M, Ensser A, et al. (Декабрь 2019 г.). «Инфекции, вызванные Clostridioides difficile». ACS Химическая биология. 14 (12): 2720–2728. Дои:10.1021 / acschembio.9b00642. ЧВК 6929054. PMID 31692324.
- ^ «Испытание эффективности вакцины против Clostridium Difficile (Clover)». Clinicaltrials.gov. 21 февраля 2020 г.. Получено 28 апреля 2020.
- ^ «Исследование вакцины против Clostridium Difficile от GlaxoSmithKline (GSK) для изучения безопасности и способности вызывать иммунный ответ в организме при введении здоровым взрослым в возрасте 18-45 лет и 50-70 лет». Clinicaltrials.gov. 13 апреля 2020 г.. Получено 28 апреля 2020.
- ^ «Оперативные данные рандомизированного, двойного слепого, плацебо-контролируемого клинического исследования фазы 2 указывают на статистически значимое снижение частоты рецидивов CDAD». Кампус Массачусетского университета в Вустере. Архивировано из оригинал 27 декабря 2010 г.. Получено 16 августа 2011.
- ^ CenterWatch. "Clostridium Difficile-Связанная диарея ». Архивировано из оригинал 29 сентября 2011 г.. Получено 16 августа 2011.
- ^ Бизнес, дальний свет. «MDX 066, MDX 1388 Medarex, Медицинская школа Массачусетского университета, клинические данные (фаза II) (диарея)». Архивировано из оригинал 14 октября 2012 г.. Получено 16 августа 2011.
- ^ а б c d е Шах Д., Данг, доктор медицины, Хасбун Р., Ку HL, Цзян З.Д., DuPont HL, Гарей К.В. (май 2010 г.). «Инфекция Clostridium difficile: обновленная информация о новых вариантах лечения антибиотиками и устойчивости к антибиотикам». Экспертная оценка противоинфекционной терапии. 8 (5): 555–64. Дои:10.1586 / eri.10.28. ЧВК 3138198. PMID 20455684.
- ^ Мур Дж. Х., ван Опсталь Е., Коллинг Г. Л., Шин Дж. Х., Богачева Е., Никоненко Б. и др. (Май 2016). «Лечение инфекции Clostridium difficile с использованием SQ641, аналога капурамицина, увеличивает выживаемость после лечения и улучшает клинические показатели заболевания на мышиной модели». Журнал антимикробной химиотерапии. 71 (5): 1300–6. Дои:10.1093 / jac / dkv479. ЧВК 4830414. PMID 26832756.
- ^ Барлоу А., Мухлеман М., Гелеки Дж., Матуш П., Таббс Р.С., Лукас М. (октябрь 2013 г.). «Червеобразный отросток: обзор». Клиническая анатомия. 26 (7): 833–42. Дои:10.1002 / ок. 22269. PMID 23716128.
- ^ Гердинг Д.Н., Мейер Т., Ли С., Коэн С.Х., Мурти, Великобритания, Пуарье А. и др. (Май 2015 г.). «Введение спор нетоксигенного штамма M3 Clostridium difficile для предотвращения рецидива инфекции C. difficile: рандомизированное клиническое испытание». JAMA. 313 (17): 1719–27. Дои:10.1001 / jama.2015.3725. PMID 25942722.
- ^ Коллинз Дж., Робинсон К., Данхоф Х., Кнетч К.В., ван Лиувен Х.С., Лоули Т.Д. и др. (Январь 2018). «Диетическая трегалоза увеличивает вирулентность эпидемии Clostridium difficile». Природа. 553 (7688): 291–294. Bibcode:2018Натура.553..291C. Дои:10.1038 / природа25178. ЧВК 5984069. PMID 29310122.
внешняя ссылка
- Псевдомембранозный колит в Керли
- Обновленное руководство по ведению и лечению Clostridium difficile инфекционное заболевание
| Классификация | |
|---|---|
| Внешние ресурсы |
