EF-Tu - Википедия - EF-Tu
| Фактор удлинения Термонестабильный | |||||||||
|---|---|---|---|---|---|---|---|---|---|
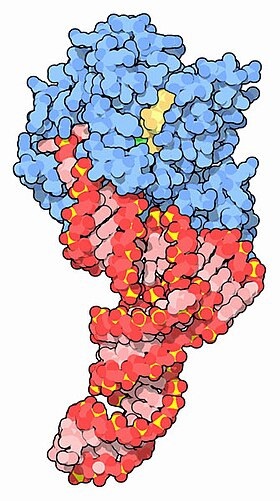 EF-Tu (синий) в комплексе с тРНК (красный) и GTP (желтый) [1] | |||||||||
| Идентификаторы | |||||||||
| Символ | EF-Tu | ||||||||
| Pfam | GTP_EFTU | ||||||||
| Pfam клан | CL0023 | ||||||||
| ИнтерПро | IPR004541 | ||||||||
| PROSITE | PDOC00273 | ||||||||
| CATH | 1ETU | ||||||||
| SCOP2 | 1ETU / Объем / СУПФАМ | ||||||||
| CDD | cd00881 | ||||||||
| |||||||||
| EF-Tu | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| Символ | GTP_EFTU_D2 | ||||||||
| Pfam | PF03144 | ||||||||
| ИнтерПро | IPR004161 | ||||||||
| CDD | cd01342 | ||||||||
| |||||||||
| Фактор удлинения Tu домен 3 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| Символ | GTP_EFTU_D3 | ||||||||
| Pfam | PF03143 | ||||||||
| ИнтерПро | IPR004160 | ||||||||
| CDD | cd01513 | ||||||||
| |||||||||
EF-Tu (коэффициент удлинения термо нестабильный) это фактор удлинения прокариот отвечает за катализирование связывания аминоацил-тРНК (аа-тРНК) к рибосома. Это G-белок и облегчает отбор и связывание аа-тРНК с А-сайтом рибосомы. Как отражение его решающей роли в перевод, EF-Tu - один из наиболее распространенных и высококонсервативных белков у прокариот.[2][3][4] Он обнаружен в митохрондриях эукариот как TUFM.[5]
Как семейство факторов элонгации, EF-Tu также включает его эукариотический и архейный гомолог, альфа-субъединицу eEF-1 (EF-1A).
Фон
Факторы удлинения являются частью механизма, который синтезирует новые белки через перевод в рибосоме. Трансферные РНК (тРНК) несут индивидуальную аминокислоты которые интегрируются в последовательность белка и имеют антикодон для конкретной аминокислоты, которой они заряжены. Посланник РНК (мРНК) несет генетическую информацию, которая кодирует первичная структура белка и содержит кодоны этот код для каждой аминокислоты. Рибосома создает белковую цепь, следуя коду мРНК и интегрируя аминокислоту аминоацил-тРНК (также известную как заряженная тРНК) в растущие клетки. полипептид цепь.[6][7]
На рибосоме есть три сайта для связывания тРНК. Это аминоацильный / акцепторный сайт (сокращенно A), пептидильный сайт (сокращенно P) и сайт выхода (сокращенно E). P-сайт содержит тРНК, связанную с синтезируемой полипептидной цепью, а A-сайт является сайтом связывания заряженной тРНК с антикодоном, комплементарным кодону мРНК, ассоциированному с этим сайтом. После связывания заряженной тРНК с A-сайтом a пептидная связь образуется между растущей полипептидной цепью на тРНК P-сайта и аминокислотой тРНК A-сайта, и весь полипептид переносится с тРНК P-сайта на тРНК A-сайта. Затем, в процессе, катализируемом фактором удлинения прокариот EF-G (исторически известная как транслоказа) происходит скоординированная транслокация тРНК и мРНК, когда тРНК P-сайта перемещается в E-сайт, где она отделяется от рибосомы, а тРНК A-сайта перемещается, чтобы занять свое место в П-сайт.[6][7]
Биологические функции
Синтез белка
EF-Tu участвует в процессе удлинения полипептидов при синтезе белка. У прокариот основной функцией EF-Tu является транспортировка правильной аа-тРНК к А-сайту рибосомы. В качестве G-протеина он использует GTP чтобы облегчить его функцию. Вне рибосомы EF-Tu образует комплекс с комплексами GTP (EF-Tu • GTP) с aa-тРНК с образованием стабильного EF-Tu • GTP • aa-тРНК тройной комплекс.[8] EF-Tu • GTP связывает все правильно заряженные аа-тРНК примерно с одинаковым сродством, за исключением тех, которые заряжены инициирующие остатки и селеноцистеин.[9][10] Это может быть достигнуто, потому что, хотя разные аминокислотные остатки имеют разные боковая цепь Свойства, тРНК, связанные с этими остатками, имеют различные структуры, чтобы компенсировать различия в аффинности связывания боковых цепей.[11][12]
Связывание aa-тРНК с EF-Tu • GTP позволяет тройному комплексу перемещаться в A-сайт активной рибосомы, в котором антикодон тРНК связывается с кодоном мРНК. Если правильный антикодон связывается с кодоном мРНК, рибосома изменяет конфигурацию и изменяет геометрию GTPase домен EF-Tu, в результате чего гидролиз GTP, связанного с EF-Tu, до ВВП и число Пи. Таким образом, рибосома функционирует как Белок, активирующий ГТФазу (GAP) для EF-Tu. При гидролизе GTP конформация EF-Tu резко изменяется и диссоциирует от аа-тРНК и комплекса рибосом.[4][13] Затем aa-тРНК полностью входит в A-сайт, где ее аминокислота приближается к P-сайту. полипептид и рибосома катализирует ковалентный перенос полипептида на аминокислоту.[10]
В цитоплазме на деактивированный EF-Tu • GDP действует фактор удлинения прокариот. ЭФ-Ц, что заставляет EF-Tu освободить связанный ВВП. После диссоциации EF-Ts, EF-Tu способен образовывать комплекс с GTP из-за того, что концентрация GTP в 5–10 раз выше, чем GDP. цитоплазма, что приводит к реактивированию EF-Tu • GTP, который затем может связываться с другой aa-тРНК.[8][13]
Сохранение точности перевода
EF-Tu способствует точности перевода тремя способами. При трансляции фундаментальная проблема заключается в том, что близкие к родственным антикодоны обладают сходной аффинностью связывания с кодоном, как родственные антикодоны, так что связывания антикодон-кодон в одной рибосоме недостаточно для поддержания высокой точности трансляции. Это решается рибосомой, не активирующей ГТФазную активность EF-Tu, если тРНК в A-сайте рибосомы не соответствует кодону мРНК, что предпочтительно увеличивает вероятность того, что неправильная тРНК покинет рибосому.[14] Кроме того, независимо от соответствия тРНК, EF-Tu также вызывает задержку после освобождения от аа-тРНК, прежде чем аа-тРНК полностью войдет в А-сайт (процесс, называемый аккомодацией). Этот период задержки является второй возможностью для неправильно заряженных аа-тРНК выйти из A-сайта до того, как неправильная аминокислота будет необратимо добавлена к полипептидной цепи.[15][16] Третий механизм - это менее изученная функция EF-Tu по грубой проверке ассоциаций аа-тРНК и отклонению комплексов, в которых аминокислота не связана с правильной тРНК, кодирующей ее.[11]
Прочие функции
ЭФ-Ту в большом количестве обнаружен в цитоскелеты бактерий, локализующихся под клеточная мембрана с MreB, цитоскелетный элемент, поддерживающий форму клетки.[17][18] Было показано, что дефекты в EF-Tu приводят к дефектам бактериальной морфологии.[19] Кроме того, EF-Tu показал некоторые сопровождающий -подобные характеристики, с некоторыми экспериментальными данными, предполагающими, что он способствует рефолдинг ряда денатурированный белки in vitro.[20][21]
Структура
EF-Tu - это мономерный белок с молекулярный вес около 43 кДа в кишечная палочка.[22][23][24] Белок состоит из трех структурных домены: GTP-связывающий домен и два олигонуклеотид -связывающие домены, часто называемые доменом 2 и доменом 3. N-концевой домен I EF-Tu представляет собой GTP-связывающий домен. Он состоит из шести бета-нить ядро в окружении шести альфа-спирали.[8] Домены II и III EF-Tu, олигонуклеотид-связывающие домены, оба принимают бета-баррель конструкции.[25][26]
GTP-связывающий домен I претерпевает драматические конформационные изменения при гидролизе GTP до GDP, позволяя EF-Tu диссоциировать от аа-тРНК и покидать рибосому.[27] Реактивация EF-Tu достигается за счет связывания GTP в цитоплазме, что приводит к значительным конформационным изменениям, которые реактивируют сайт связывания тРНК EF-Tu. В частности, связывание GTP с EF-Tu приводит к повороту домена I на ~ 90 ° относительно доменов II и III, обнажая остатки активного сайта связывания тРНК.[28]
Домен 2 принимает бета-баррель структура и участвует в связывании с заряженной тРНК.[29] Этот домен структурно относящиеся к C-концевому домену EF2, которому он показывает слабое сходство последовательностей. Этот домен также встречается в других белки например, фактор инициации перевода IF-2 и тетрациклин -резистентные белки. Домен 3 представляет C-терминал домен, который принимает бета-баррель структура, и участвует в связывании как с заряженной тРНК, так и с EF1B (или EF-Ts).[30]
Эволюция
GTP-связывающий домен консервированный как в EF-1alpha / EF-Tu, так и в EF-2 /EF-G и, таким образом, кажется типичным для GTP-зависимых белков, которые связывают неинициатор тРНК к рибосома. GTP-связывание синтез белка семейство факторов также включает эукариотический пептид фактор высвобождения цепи GTP-связывание подразделения[31] и прокариотический фактор высвобождения пептидной цепи 3 (RF-3);[32] то прокариотический ГТФ-связывающий белок lepA и его гомолог в дрожжах (GUF1) и Caenorhabditis elegans (ZK1236.1); дрожжи HBS1;[33] крыса статины S1;[34] и прокариотический селеноцистеин -специфический коэффициент удлинения selB.[35]
Актуальность болезни
Наряду с рибосомой EF-Tu является одной из важнейших мишеней для антибиотик -опосредованное торможение перевода.[8] Антибиотики, нацеленные на EF-Tu, можно разделить на одну из двух групп, в зависимости от механизма действия, и на одно из четырех структурных семейств. В первую группу входят антибиотики пульвомицин и GE2270A, ингибирующие образование тройного комплекса.[36] Вторая группа включает антибиотики кирромицин и энацилоксин и предотвращает высвобождение EF-Tu из рибосомы после гидролиза GTP.[37][38][39]
Смотрите также
- Факторы удлинения прокариот
- ЭФ-Ц (коэффициент удлинения термостабильный)
- EF-G (коэффициент удлинения G)
- EF-P (коэффициент удлинения P)
- eEF-1
- EFR (рецептор EF-Tu)
Рекомендации
- ^ PDB Молекула месяца EF-Tu
- ^ Weijland A, Harmark K, Cool RH, Anborgh PH, Parmeggiani A (март 1992 г.). «Фактор удлинения Tu: молекулярный переключатель в биосинтезе белка». Молекулярная микробиология. 6 (6): 683–8. Дои:10.1111 / j.1365-2958.1992.tb01516.x. PMID 1573997.
- ^ "TIGR00485: EF-Tu". Национальный центр биотехнологической информации. 3 марта 2017 г.
- ^ а б Ямамото Х., Цинь Й., Ахенбах Дж., Ли С., Киджек Дж., Спан С.М., Нирхаус К.Х. (февраль 2014 г.). «EF-G и EF4: транслокация и обратная транслокация на бактериальной рибосоме». Обзоры природы. Микробиология. 12 (2): 89–100. Дои:10.1038 / nrmicro3176. PMID 24362468. S2CID 27196901.
- ^ Линг М., Меранте Ф., Чен Х.С., Дафф С., Дункан А.М., Робинсон Б.Х. (ноябрь 1997 г.). «Ген фактора удлинения митохондрий человека tu (EF-Tu): последовательность кДНК, геномная локализация, геномная структура и идентификация псевдогена». Ген. 197 (1–2): 325–36. Дои:10.1016 / S0378-1119 (97) 00279-5. PMID 9332382.
- ^ а б Лаурсен Б.С., Соренсен Х.П., Мортенсен К.К., Сперлинг-Петерсен Х.У. (март 2005 г.). «Инициирование синтеза белка у бактерий». Обзоры микробиологии и молекулярной биологии. 69 (1): 101–23. Дои:10.1128 / MMBR.69.1.101-123.2005. ЧВК 1082788. PMID 15755955.
- ^ а б Рамакришнан V (февраль 2002 г.). «Структура рибосом и механизм трансляции». Клетка. 108 (4): 557–72. Дои:10.1016 / s0092-8674 (02) 00619-0. PMID 11909526. S2CID 2078757.
- ^ а б c d Краб И.М., Пармеджиани А (01.01.2002). Механизмы EF-Tu, пионера ГТФазы. Прогресс в исследованиях нуклеиновых кислот и молекулярной биологии. 71. С. 513–51. Дои:10.1016 / S0079-6603 (02) 71050-7. ISBN 9780125400718. PMID 12102560.
- ^ «Фактор удлинения трансляции EFTu / EF1A, бактериальный / органелла (IPR004541)». ИнтерПро.
- ^ а б Диван, Джойс (2008). «Перевод: синтез белка». Политехнический институт Ренсселера.
- ^ а б ЛаРивьер Ф.Дж., Вольфсон А.Д., Уленбек О.К. (октябрь 2001 г.). «Равномерное связывание аминоацил-тРНК с фактором элонгации Tu путем термодинамической компенсации». Наука. 294 (5540): 165–8. Дои:10.1126 / science.1064242. PMID 11588263. S2CID 26192336.
- ^ Луи А., Рибейро Н.С., Рид Б.Р., Джурнак Ф. (апрель 1984 г.). «Относительное сродство всех аминоацил-тРНК Escherichia coli к фактору элонгации Tu-GTP». Журнал биологической химии. 259 (8): 5010–6. PMID 6370998.
- ^ а б Кларк Б.Ф., Нюборг Дж. (Февраль 1997 г.). «Тройной комплекс EF-Tu и его роль в биосинтезе белка». Текущее мнение в структурной биологии. 7 (1): 110–6. Дои:10.1016 / s0959-440x (97) 80014-0. PMID 9032056.
- ^ Нильссон Дж., Ниссен П. (июнь 2005 г.). «Факторы удлинения рибосомы». Текущее мнение в структурной биологии. 15 (3): 349–54. Дои:10.1016 / j.sbi.2005.05.004. PMID 15922593.
- ^ Whitford PC, Geggier P, Altman RB, Blanchard SC, Onuchic JN, Санбонмацу, Кентукки (Июнь 2010 г.). «Размещение аминоацил-тРНК в рибосоме включает обратимые экскурсии по множеству путей». РНК. 16 (6): 1196–204. Дои:10.1261 / rna.2035410. ЧВК 2874171. PMID 20427512.
- ^ Ноэль Дж. К., Whitford PC (октябрь 2016 г.). «Как EF-Tu может способствовать эффективному считыванию аа-тРНК рибосомой». Nature Communications. 7: 13314. Дои:10.1038 / ncomms13314. ЧВК 5095583. PMID 27796304.
- ^ Дефеу Суфо Х.Дж., Реймольд С., Линне У., Кнуст Т., Гешер Дж., Грауманн П.Л. (февраль 2010 г.). «Бактериальный фактор элонгации трансляции EF-Tu взаимодействует и колокализуется с актин-подобным белком MreB». Труды Национальной академии наук Соединенных Штатов Америки. 107 (7): 3163–8. Дои:10.1073 / pnas.0911979107. ЧВК 2840354. PMID 20133608.
- ^ Майер Ф (01.01.2003). «Цитоскелеты прокариот». Cell Biology International. 27 (5): 429–38. Дои:10.1016 / с1065-6995 (03) 00035-0. PMID 12758091. S2CID 40897586.
- ^ Майер Ф (1 января 2006 г.). «Элементы цитоскелета у бактерий Mycoplasma pneumoniae, Thermoanaerobacterium sp. И Escherichia coli, выявленные с помощью электронной микроскопии». Журнал молекулярной микробиологии и биотехнологии. 11 (3–5): 228–43. Дои:10.1159/000094057. PMID 16983198. S2CID 23701662.
- ^ Ричарм Дж. (Ноябрь 1998 г.). «Протеин-дисульфидизомеразная активность фактора элонгации EF-Tu». Сообщения о биохимических и биофизических исследованиях. 252 (1): 156–61. Дои:10.1006 / bbrc.1998.9591. PMID 9813162.
- ^ Кудлики В., Коффман А., Крамер Г., Хардести Б. (декабрь 1997 г.). «Ренатурация роданезы с помощью фактора удлинения трансляции (EF) Tu. Рефолдинг белка с помощью флексии EF-Tu». Журнал биологической химии. 272 (51): 32206–10. Дои:10.1074 / jbc.272.51.32206. PMID 9405422.
- ^ Caldas TD, El Yaagoubi A, Kohiyama M, Richarme G (октябрь 1998 г.). «Очистка факторов элонгации EF-Tu и EF-G из Escherichia coli ковалентной хроматографией на тиол-сефарозе». Экспрессия и очистка белков. 14 (1): 65–70. Дои:10.1006 / преп.1998.0922. PMID 9758752.
- ^ Wiborg O, Andersen C, Knudsen CR, Clark BF, Nyborg J (август 1996). «Картирование остатков Tu фактора элонгации Escherichia coli, участвующих в связывании аминоацил-тРНК». Журнал биологической химии. 271 (34): 20406–11. Дои:10.1074 / jbc.271.34.20406. PMID 8702777.
- ^ Вурмбах П., Нирхаус К. Х. (1 января 1979 г.). Выделение факторов элонгации синтеза белка EF-Tu, EF-Ts и EF-G из Escherichia coli. Методы в энзимологии. 60. стр.593–606. Дои:10.1016 / с0076-6879 (79) 60056-3. ISBN 9780121819606. PMID 379535.
- ^ Ван И, Цзян И, Мейеринг-Фосс М., Спринзл М., Сиглер ПБ (август 1997 г.). «Кристаллическая структура комплекса ЭФ-Ту.ЭФ-Ц из Thermus thermophilus». Структурная биология природы. 4 (8): 650–6. Дои:10.1038 / nsb0897-650. PMID 9253415. S2CID 10644042.
- ^ Ниссен П., Кьельдгаард М., Тируп С., Полехина Г., Решетникова Л., Кларк Б.Ф., Нюборг Дж. (Декабрь 1995 г.). «Кристаллическая структура тройного комплекса Phe-tRNAPhe, EF-Tu и аналога GTP». Наука. 270 (5241): 1464–72. Дои:10.1126 / science.270.5241.1464. PMID 7491491. S2CID 24817616.
- ^ Мёллер В., Шиппер А., Амонс Р. (сентябрь 1987 г.). «Консервативная аминокислотная последовательность вокруг Arg-68 фактора элонгации 1 альфа артемии участвует в связывании нуклеотидов гуанина и РНК переноса аминоацила». Биохимия. 69 (9): 983–9. Дои:10.1016 / 0300-9084 (87) 90232-х. PMID 3126836.
- ^ Кьельдгаард М., Ниссен П., Тируп С., Нюборг Дж. (Сентябрь 1993 г.). «Кристаллическая структура фактора удлинения EF-Tu из Thermus aquaticus в конформации GTP». Структура. 1 (1): 35–50. Дои:10.1016/0969-2126(93)90007-4. PMID 8069622.
- ^ Ниссен П., Кьельдгаард М., Тируп С., Полехина Г., Решетникова Л., Кларк Б.Ф., Нюборг Дж. (Декабрь 1995 г.). «Кристаллическая структура тройного комплекса Phe-tRNAPhe, EF-Tu и аналога GTP». Наука. 270 (5241): 1464–72. Дои:10.1126 / science.270.5241.1464. PMID 7491491. S2CID 24817616.
- ^ Ван И, Цзян И, Мейеринг-Фосс М., Спринзл М., Сиглер ПБ (август 1997 г.). «Кристаллическая структура комплекса ЭФ-Ту.ЭФ-Ц из Thermus thermophilus». Nat. Struct. Биол. 4 (8): 650–6. Дои:10.1038 / nsb0897-650. PMID 9253415. S2CID 10644042.
- ^ Стэнсфилд И., Джонс К.М., Кушниров В.В., Дагкесаманская А.Р., Позняковский А.И., Паушкин С.В., Ниеррас Ч.Р., Кокс Б.С., Тер-Аванесян М.Д., Туите М.Ф. (сентябрь 1995 г.). «Продукты генов SUP45 (eRF1) и SUP35 взаимодействуют, опосредуя терминацию трансляции в Saccharomyces cerevisiae». EMBO J. 14 (17): 4365–73. Дои:10.1002 / j.1460-2075.1995.tb00111.x. ЧВК 394521. PMID 7556078.
- ^ Grentzmann G, Brechemier-Baey D, Heurgué-Hamard V, Buckingham RH (май 1995 г.). «Функция фактора высвобождения полипептидной цепи RF-3 в Escherichia coli. Действие RF-3 при терминации преимущественно проявляется при стоп-сигналах, содержащих UGA». J. Biol. Chem. 270 (18): 10595–600. Дои:10.1074 / jbc.270.18.10595. PMID 7737996.
- ^ Нельсон Р.Дж., Зигельхоффер Т., Николет С., Вернер-Вашберн М., Крейг Е.А. (октябрь 1992 г.). «Машины трансляции и белок теплового шока 70 кДа взаимодействуют в синтезе белка». Клетка. 71 (1): 97–105. Дои:10.1016 / 0092-8674 (92) 90269-И. PMID 1394434. S2CID 7417370.
- ^ Энн Д.К., Муцацос И.К., Накамура Т., Линь Х.Х., Мао П.Л., Ли М.Дж., Чин С., Лием Р.К., Ван Э. (июнь 1991 г.). «Выделение и характеристика хромосомного гена крысы для полипептида (pS1), антигенно связанного со статином». J. Biol. Chem. 266 (16): 10429–37. PMID 1709933.
- ^ Форчхаммер К., Лейнфельдер В., Бок А. (ноябрь 1989 г.). «Идентификация нового фактора трансляции, необходимого для включения селеноцистеина в белок». Природа. 342 (6248): 453–6. Дои:10.1038 / 342453a0. PMID 2531290. S2CID 4251625.
- ^ Сельва Е., Беретта Дж., Монтанини Н., Сэддлер Г. С., Гастальдо Л., Феррари П., Лоренцетти Р., Ландини П., Рипамонти Ф., Голдштейн Б. П. (июль 1991 г.). «Антибиотик GE2270 a: новый ингибитор синтеза бактериального белка. I. Выделение и характеристика». Журнал антибиотиков. 44 (7): 693–701. Дои:10.7164 / антибиотики.44.693. PMID 1908853.
- ^ Хогг Т., Местерс-младший, Хильгенфельд Р. (февраль 2002 г.). «Механизмы ингибирования антибиотиков, нацеленных на фактор удлинения Tu». Современная наука о белках и пептидах. 3 (1): 121–31. Дои:10.2174/1389203023380855. PMID 12370016.
- ^ Андерсен Г.Р., Ниссен П., Нюборг Дж. (Август 2003 г.). «Факторы удлинения в биосинтезе белков». Тенденции в биохимических науках. 28 (8): 434–41. Дои:10.1016 / S0968-0004 (03) 00162-2. PMID 12932732.
- ^ Пармеджиани А., Ниссен П. (август 2006 г.). «Антибиотики, нацеленные на фактор элонгации Tu: четыре разные структуры, два механизма действия». Письма FEBS. 580 (19): 4576–81. Дои:10.1016 / j.febslet.2006.07.039. PMID 16876786. S2CID 20811259.
внешняя ссылка
- Пептид + удлинение + фактор + Tu в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Обзор всей структурной информации, доступной в PDB за UniProt: P49410 (Фактор элонгации Tu, митохондриальный) на PDBe-KB.


