Волосатоклеточный лейкоз - Hairy cell leukemia
| Волосатоклеточный лейкоз | |
|---|---|
 | |
| Специальность | Гематология и онкология |
Волосатоклеточный лейкоз это редкость гематологическая злокачественная опухоль характеризуется накоплением аномальных В-лимфоциты.[1] Обычно его относят к подтипу хронический лимфолейкоз (CLL). Волосатоклеточный лейкоз составляет примерно 2% всех лейкемии, при этом в Северной Америке и Западной Европе, вместе взятых, ежегодно диагностируется менее 2000 новых случаев.
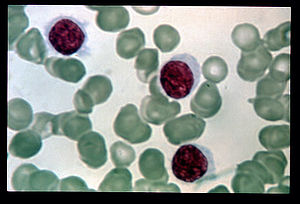
Волосатоклеточный лейкоз был первоначально описан как гистиоцитарный лейкоз, злокачественный ретикулез или лимфоидный миелофиброз в публикациях, датированных 1920-ми годами. Заболевание было официально названо лейкемическим ретикулоэндотелиозом, и его характеристика значительно улучшилась. Берта Буронкле и коллеги в Медицинский колледж Университета штата Огайо в 1958 году. Его общее название, которое было придумано в 1966 году,[2] происходит из-за «волосатости» злокачественных В-клеток под микроскопом.[3]
Признаки и симптомы
При лейкемии волосатых клеток "волосатые клетки" (злокачественные В-лимфоциты) накапливаются в костном мозге, препятствуя выработке нормальных белые кровяные клетки, красные кровяные тельца, и тромбоциты. Следовательно, у пациентов могут развиться инфекции, связанные с низкое количество лейкоцитов, анемия и усталость из-за недостатка эритроцитов или легкое кровотечение из-за низкое количество тромбоцитов.[4] Лейкозные клетки могут собираться в селезенка и вызвать его набухание; это может иметь побочный эффект, заставляя человека чувствовать себя сытым, даже если он или она мало ел.
Волосатоклеточный лейкоз обычно диагностируется после того, как обычный анализ крови показывает неожиданно низкое количество одного или нескольких видов нормальных клеток крови, или после необъяснимых синяков или рецидивирующих инфекций у внешне здорового пациента.
У пациентов с HCL функция тромбоцитов может быть несколько нарушена, хотя это не оказывает значительного практического эффекта.[5] Это может привести к несколько более легкому синяку, чем можно было бы ожидать при данном количестве тромбоцитов, или к умеренному увеличению времени кровотечения при небольшом порезе. Вероятно, это результат производства слегка ненормальных тромбоцитов в чрезмерно напряженной ткани костного мозга.
У пациентов с высокой опухолевой нагрузкой также может быть несколько сниженный уровень холестерина,[6] особенно у пациентов с увеличенной селезенкой.[7] Уровень холестерина возвращается к более нормальным значениям при успешном лечении HCL.
Причина
Как и в случае многих других видов рака, причина лейкемии волосатых клеток неизвестна. Воздействие табачного дыма, ионизирующего излучения, или промышленные химикаты (за возможным исключением дизель ) не увеличивает риск развития HCL.[8] В некоторых исследованиях земледелие и садоводство коррелируют с повышенным риском развития HCL, что не обязательно подразумевает причинно-следственную связь.[9]
В исследовании 2011 года были выявлены соматические мутации BRAF V600E у всех 47 изученных пациентов с волосатоклеточным лейкозом (HCL), и не было таких мутаций в 193 периферических B-клеточных лимфомах / лейкозах, кроме HCL.[10]
Соединенные штаты. Институт медицины (IOM) видит корреляцию, которая допускает связь между воздействием гербицидов и более поздним развитием хронических В-клеточных лейкозов и лимфом в целом. В отчете IOM подчеркивается, что ни исследования на животных, ни на людях не указывают на конкретную связь гербицидов с HCL. Тем не менее, МОМ экстраполировала данные хронического лимфолейкоза и неходжкинская лимфома сделать вывод, что HCL и другие редкие B-клеточные новообразования могут разделять этот фактор риска.[11] В результате отчета МОМ США Управление по делам ветеранов считает HCL заболеванием, предположительно связанным с инвалидностью (см. Агент апельсин ).
Т-лимфотропный вирус человека 2 (HTLV-2) был изолирован у небольшого числа пациентов с вариантной формой HCL.[12] В 1980-х годах HTLV-2 был идентифицирован у пациента с Т-клеточным лимфопролиферативным заболеванием; у этого пациента позже развился лейкоз волосатых клеток (В-клеточная болезнь), но HTLV-2 не был обнаружен в клонах волосатых клеток.[13] Нет никаких доказательств того, что HTLV-II вызывает какие-либо гематологические злокачественные новообразования, включая HCL.[14]
Патофизиология
Панцитопения в HCL вызвано в первую очередь недостаточностью костного мозга и спленомегалия. Недостаточность костного мозга вызвана накоплением волосяных клеток и ретикулина. фиброз в костном мозге, а также из-за пагубного воздействия дисрегуляции выработки цитокинов.[15] Спленомегалия снижает показатели крови за счет секвестрации, маргинализации и разрушения здоровых клеток крови внутри селезенки.[15]
Волосатые клетки почти созрели В-клетки, которые представляют собой активированные клональные клетки с признаками дифференцировки гена VH.[16] Они могут быть связаны с пре-плазмой. краевая зона В-клетки[15] или же ячейки памяти.
Цитокин нарушена продукция в HCL. Волосатые клетки производят и развивают TNF-альфа.[15] Этот цитокин также подавляет нормальное производство здоровых клеток крови в костном мозге.[15]
В отличие от здоровых В-клеток, волосатые клетки экспрессируют и секретируют белок иммунной системы, называемый Рецептор интерлейкина-2 (ИЛ-2Р).[15] В HCL-V экспрессируется только часть этого рецептора.[15] В результате статус заболевания можно отслеживать, измеряя изменения количества IL-2R в сыворотке крови.[15] Уровень увеличивается по мере размножения волосистых клеток и уменьшается, когда они погибают. Хотя этот тест редко используется в Северной Америке и Северной Европе, этот тест лучше коррелирует со статусом болезни и предсказывает рецидив более точно, чем любой другой тест.
Волосатые клетки реагируют на нормальную продукцию некоторых цитокинов путем Т-клетки с повышенным ростом. Лечение интерфероном-альфа подавляет выработку этого цитокина, способствующего росту, Т-клетками.[15] Низкий уровень Т-клеток, который обычно наблюдается после лечения кладрибин или же пентостатин, и последующее снижение этих цитокинов также связано со снижением уровня волосатых клеток.
В июне 2011 года Э. Тиаччи и другие[17][18] обнаружил, что 100% проанализированных образцов волосатоклеточного лейкоза имели онкогенные BRAF мутации V600E, и предположил, что это мутация драйвера заболевания. До этого момента только несколько геномный дисбаланс был обнаружен в волосатых клетках, таких как трисомия 5 были найдены.[15] В экспрессия генов также дисрегулируется по сложной и специфической схеме. Клетки недоэкспрессируют 3p24, 3p21, 3q13.3-q22, 4p16, 11q23, 14q22-q24, 15q21-q22, 15q24-q25 и 17q22-q24 и сверхэкспрессируют 13q31 и Xq13.3-q21.[19] Еще не было продемонстрировано, что какие-либо из этих изменений имеют какое-либо практическое значение для пациента.
Диагностика
Диагноз HCL может быть предложен по аномальным результатам на полный анализ крови (CBC), но для подтверждения диагноза необходимо дополнительное тестирование. Общий анализ крови обычно показывает низкие уровни лейкоцитов, эритроцитов и тромбоцитов у пациентов с HCL. Однако, если в кровотоке присутствует большое количество волосатых клеток, то нормальный или даже высокое количество лимфоцитов можно найти.
При физикальном осмотре 80–90% пациентов имеют увеличенная селезенка, который может быть огромным.[15] Это менее вероятно среди пациентов, которым поставлен диагноз на ранней стадии. Периферийный лимфаденопатия (увеличенные лимфатические узлы) нечасто (менее 5% пациентов), но брюшная лимфаденопатия - относительно частая находка на компьютерная томография (КТ) сканирование.[15]
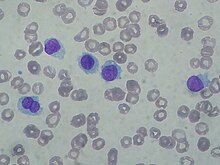
Самый важный лабораторный результат - наличие волосатых клеток в кровотоке.[15] Волосатые клетки ненормальны белые кровяные клетки с волосковыми выступами цитоплазма; их можно увидеть, изучив мазок крови или же биопсия костного мозга образец. Исследование мазка крови проводится окрашивание клетки крови с Пятно Райта и глядя на них под микроскоп. Волосатые клетки видны в этом тесте примерно в 85% случаев.[15]
Большинству пациентов для окончательного диагноза требуется биопсия костного мозга. Биопсия костного мозга используется как для подтверждения наличия HCL, так и для отсутствия каких-либо дополнительных заболеваний, таких как Лимфома маргинальной зоны селезенки или же В-клеточный пролимфоцитарный лейкоз. Диагноз можно подтвердить, просмотрев клетки специальным красителем, известным как TRAP (тартрат-устойчивая кислая фосфатаза ). Совсем недавно тестирование DB44 обеспечивает более точные результаты.
Также возможно окончательно диагностировать лейкоз волосатых клеток с помощью проточной цитометрии на кровь или костный мозг. Волосатые клетки больше обычного и положительны для CD19, CD20, CD22, CD11c, CD25, CD103, и FMC7.[20] (CD103, CD22, и CD11c сильно выражены.)[21]
Вариант волосатоклеточного лейкоза (HCL-V), который имеет некоторые общие характеристики с пролимфоцитарным лейкозом B-клеток (B-PLL), не обнаруживает CD25 (также называемый рецептором интерлейкина-2, альфа). Поскольку это относительно новая и дорогая технология, ее применяют врачи неодинаково, несмотря на преимущества комфорта, простоты и безопасности для пациента по сравнению с биопсией костного мозга. Наличие дополнительных лимфопролиферативные заболевания легко проверяется во время теста проточной цитометрии, где они обычно показывают разные результаты.[16]
Дифференциальный диагноз включает: несколько видов анемия, включая миелофтиз и апластическая анемия,[22] и большинство видов новообразований крови, в том числе гипопластические миелодиспластический синдром, атипичный хронический лимфолейкоз, В-клеточный пролимфоцитарный лейкоз, или идиопатический миелофиброз.[16]
Классификация
Если не указано иное, часто подразумевается «классическая» форма. Однако описаны два варианта: Вариант волосатоклеточного лейкоза.[23] и японский вариант. Неяпонский вариант лечить труднее, чем «классический» HCL или японский вариант HCL.
Волосатоклеточный вариант лейкемии
Вариант волосатоклеточного лейкоза, или HCL-V, обычно описывается как пролимфоцитарный вариант волосистого клеточного лейкоза.[24] Впервые он был официально описан в 1980 году в статье из лаборатории Хейхо Кембриджского университета.[25] Около 10% людей с HCL имеют эту вариантную форму заболевания, что составляет около 60-75 новых случаев HCL-V каждый год в США. В то время как классический HCL в основном поражает мужчин, HCL-V более равномерно распределяется между мужчинами и женщинами.[26] Хотя заболевание может появиться в любом возрасте, средний возраст постановки диагноза составляет более 70 лет.[27]
Похожий на В-клеточный пролимфоцитарный лейкоз ("B-PLL") в Хронический лимфолейкоз, HCL-V - более агрессивное заболевание. Исторически считалось, что его лечение будет менее успешным, чем классическая HCL, а ремиссии, как правило, были короче.
Однако введение комбинированной терапии с одновременной терапией ритуксимабом и кладрибином показало отличные результаты в раннем периоде наблюдения.[28] По состоянию на 2016 год эта терапия считается лечением первой линии выбора для многих людей с HCL-V.[29]
Многие старые подходы к лечению, такие как Интерферон -альфа, режим комбинированной химиотерапии "CHOP" и обычные алкилирующие агенты, такие как циклофосфамид показал очень небольшую пользу.[26] Пентостатин и кладрибин, назначаемые в виде монотерапии (без одновременного применения ритуксимаба), приносят определенную пользу многим людям с HCL-V, но обычно вызывают более короткие периоды ремиссии и меньшую частоту ответа, чем при их использовании в классической HCL. Более половины людей частично отвечают на спленэктомию.[26]
Что касается развития B-клеток, пролимфоциты менее развиты, чем лимфоциты или же плазматические клетки, но все же более зрелые, чем их лимфобластный прекурсоры.
HCL-V принципиально отличается от классического HCL в следующих отношениях:
- Выше лейкоцит подсчитывает, иногда превышая 100 000 клеток на микролитр;
- Более агрессивное течение болезни, требующее более частого лечения;
- Волосатые клетки с необычно большим ядрышко за их размер;
- Производство небольшого избытка фибронектин производится классическими волосатыми клетками;[30] препятствовать биопсии костного мозга; и
- Низкая или отсутствующая экспрессия на клеточной поверхности CD25 (также называемый рецептором интерлейкина-2 [IL-2] альфа цепь, или p55).[31]
Низкий уровень CD25, части рецептора ключевого иммунорегулирующего гормона, может объяснить, почему случаи HCL-V обычно гораздо более устойчивы к лечению гормонами иммунной системы.[24]
HCL-V, который обычно содержит большое количество волосистых клеток без функциональных p53 ген-супрессор опухоли, с большей вероятностью трансформируется в злокачественное новообразование более высокой степени. Типичная скорость трансформации 5-6% постулируется в Великобритании, как и Преобразование Рихтера ставка для SLVL и CLL.[26][32] Среди пациентов с HCL-V в наиболее агрессивных случаях обычно наблюдается наименьшая активность гена p53.[33] Волосатые клетки без гена p53 имеют тенденцию со временем вытеснять менее агрессивные волосатые клетки p53 (+).
Есть некоторые свидетельства того, что перестройка гена иммуноглобулина VH4-34, которая обнаруживается примерно у 40% пациентов с HCL-V и 10% пациентов с классической HCL, может быть более важным плохим прогностическим фактором, чем вариантный статус с HCL. Пациенты -V без перегруппировки VH4-34 реагируют примерно так же, как пациенты с классической HCL.[34]
Волосатоклеточный лейкоз - японский вариант
Существует вариант, называемый японским вариантом волосатоклеточного лейкоза или HCL-J, который легче поддается лечению.
Лечение с кладрибин было сообщено.[35]
Профилактика
Поскольку причина неизвестна, никакие эффективные профилактические меры не могут быть приняты.
Поскольку заболевание встречается редко, рутинный скрининг не является рентабельным.
Уход
Доступно несколько методов лечения, и успешный контроль над болезнью является обычным явлением.
Не всем нужно лечение немедленно. Лечение обычно назначается, когда симптомы заболевания мешают повседневной жизни пациента или когда количество лейкоцитов или тромбоцитов снижается до опасно низкого уровня, например абсолютное количество нейтрофилов менее тысячи клеток на микролитр (1,0 К / мкл). Не всем пациентам требуется лечение сразу после постановки диагноза.
Отсрочка лечения менее важна, чем при солидных опухолях. В отличие от большинства видов рака, успех лечения не зависит от лечения болезни на ранней стадии. Поскольку задержки не влияют на успех лечения, не существует стандартов того, как быстро пациент должен получить лечение. Однако слишком долгое ожидание может вызвать собственные проблемы, такие как инфекция, которой можно было бы избежать с помощью надлежащего лечения для восстановления функции иммунной системы. Кроме того, наличие большего количества волосатых клеток во время лечения может несколько усугубить определенные побочные эффекты, поскольку некоторые побочные эффекты в основном вызваны естественной реакцией организма на умирающие волосатые клетки. Это может привести к госпитализации пациента, лечение которого в противном случае проводилось бы полностью в кабинете гематолога.
Типично лечение одним лекарством. В отличие от большинства видов рака, пациенту обычно дают только одно лекарство. В то время как монотерапия является нормальным явлением, комбинированная терапия - обычно с использованием одной терапии первой линии и одной терапии второй линии - изучается в текущих клинических испытаниях и чаще используется в рефрактерных случаях. Комбинирование ритуксимаба с кладрибином или пентостатином может принести или не принести какую-либо практическую пользу пациенту.[36] Комбинированная терапия почти никогда не применяется с новым пациентом. Поскольку показатели успеха монотерапии аналогами пурина уже настолько высоки, дополнительная польза от немедленного лечения вторым препаратом для пациента, ранее не получавшего лечения, считается очень низкой. Например, один курс кладрибина или пентостатина дает среднему пациенту, впервые обращающемуся за лечением, десятилетнюю ремиссию; Добавление ритуксимаба, которое дает среднему пациенту только три или четыре года, может не дать дополнительной ценности для этого легко лечимого пациента. Однако в более сложном случае польза от первого лекарства может быть существенно снижена, и поэтому комбинация может дать некоторую пользу.
Первая линия терапии
Кладрибин (2CDA) и пентостатин (DCF) - два наиболее распространенных метода лечения первой линии. Оба они принадлежат к классу лекарств, называемых аналоги пурина, которые имеют легкие побочные эффекты по сравнению с традиционными химиотерапия режимы.
Кладрибин можно вводить путем инъекции под кожу, путем инфузии в вену в течение нескольких часов или с помощью насоса, который носит пациент, который обеспечивает медленное капание в вену, 24 часа в сутки в течение 7 дней. Большинство пациентов получают кладрибин путем внутривенной инфузии один раз в день в течение пяти-семи дней, но большему количеству пациентов предоставляется возможность принимать этот препарат один раз в неделю в течение шести недель. Различные схемы дозирования кладрибина примерно одинаково эффективны и одинаково безопасны.[37]Относительно немногие пациенты имеют серьезные побочные эффекты, кроме усталости и высокой температуры, вызванные отмиранием раковых клеток, хотя наблюдались такие осложнения, как инфекция и острая почечная недостаточность.
Пентостатин химически подобен кладрибину и имеет аналогичный показатель эффективности и профиль побочных эффектов, но его всегда вводят в течение гораздо более длительного периода времени, обычно одна доза путем внутривенной инфузии каждые две недели в течение трех-шести месяцев.
В течение нескольких недель после лечения у пациента иммунная система сильно ослаблен, но их Костный мозг снова начнет производить нормальные клетки крови. Лечение часто приводит к длительной ремиссии. Около 85% пациентов достигают полного ответа от лечения кладрибином или пентостатином, а еще 10% получают некоторую пользу от этих препаратов, хотя постоянного лечения от этого заболевания не существует. Если раковые клетки возвращаются, лечение можно повторить и снова должно привести к ремиссии, хотя шансы на успех снижаются при повторном лечении.[38] Продолжительность ремиссии значительно различается - от одного года до более двадцати лет. Средний пациент может ожидать перерыв в лечении около десяти лет.
Кажется, не имеет значения, какое лекарство получает пациент. Пациент, который не получил успешного лечения одним из этих двух препаратов, имеет меньшие шансы на успешное лечение другим. Однако есть и другие варианты.
Вторая линия терапии
Если пациент устойчив к кладрибину или пентостатину, назначают терапию второй линии.
Моноклональные антитела Наиболее распространенное лечение резистентного к кладрибину заболевания - введение моноклональных антител, разрушающих раковые В-клетки. Ритуксимаб является наиболее часто используемым. Большинство пациентов получают одну внутривенную инфузию в течение нескольких часов каждую неделю в течение четырех-восьми недель. В публикации 2003 г. было обнаружено два частичных и десять полных ответов из 15 пациентов с рецидивом болезни, что в общей сложности дало 80% ответов.[39] Средний пациент (включая не ответивших на лечение) не нуждался в дальнейшем лечении более трех лет. Это исследование с восемью дозами имело более высокую частоту ответа, чем исследование с четырьмя дозами в Скриппсе, которое показало только 25% ответов.[40] Ритуксимаб успешно вызвал полный ответ в варианте с волосатыми клетками.[41]
Основным побочным эффектом ритуксимаба является сывороточная болезнь, обычно описываемая как «аллергическая реакция», которая может быть тяжелой, особенно при первой инфузии. Сывороточная болезнь в первую очередь вызвана скоплением антител во время инфузии и запуском дополнять каскад. Хотя большинство пациентов считают, что побочные эффекты адекватно контролируются противоаллергическими препаратами, все же имели место серьезные и даже фатальные реакции. Следовательно, первая доза всегда вводится в условиях стационара, хотя последующие инфузии могут быть сделаны в кабинете врача. Ремиссия обычно короче, чем при применении предпочтительных препаратов первого ряда, но гематологические ремиссии продолжительностью несколько лет не редкость.
Другие моноклональные антитела, разрушающие В-клетки, такие как Алемтузумаб, Ибритумомаб тиуксетан и I-131 Тозитумомаб может быть рассмотрен для невосприимчивых случаев.
Интерферон-альфа Интерферон-альфа это гормон иммунной системы, который очень полезен для относительно небольшого числа пациентов и в некоторой степени полезен для большинства пациентов. Примерно у 65% пациентов[42] препарат помогает стабилизировать заболевание или вызвать медленное, незначительное улучшение с частичным ответом.[43]
Типичный график дозирования вводит не менее 3 миллионов единиц интерферона-альфа (не пегилированных версий) три раза в неделю, хотя первоначальный протокол начинался с шести месяцев ежедневных инъекций.
Некоторые пациенты очень хорошо переносят IFN-альфа после первых двух недель, в то время как другие считают, что его характерные особенности симптомы гриппа сопротивляться. Около 10% пациентов развивают уровень депрессия. Возможно, что, поддерживая более стабильный уровень гормона в организме, ежедневные инъекции могут вызвать меньше побочных эффектов у отдельных пациентов. Ежедневное употребление не менее двух литров воды, избегая при этом кофеина и алкоголя, может уменьшить многие побочные эффекты.
Падение показателей крови обычно наблюдается в течение первых одного-двух месяцев лечения. Большинство пациентов обнаруживают, что их показатели крови ухудшаются в течение нескольких недель сразу после начала лечения, хотя некоторые пациенты обнаруживают, что их показатели крови начинают улучшаться уже через две недели.[44]
Обычно требуется шесть месяцев, чтобы выяснить, полезно ли это лечение. Общие критерии успеха лечения включают:
- нормализация уровня гемоглобина (выше 12,0 г / дл),
- нормальное или несколько низкое количество тромбоцитов (выше 100 К / мкл), и
- нормальное или несколько низкое абсолютное количество нейтрофилов (выше 1,5 К / мкл).[44]
Если он хорошо переносится, пациенты обычно принимают гормон от 12 до 18 месяцев. Затем может быть предпринята попытка прекратить лечение, но большинство пациентов обнаруживают, что им нужно продолжать прием препарата, чтобы оно было успешным. Эти пациенты часто продолжают принимать этот препарат в течение неопределенного времени, пока либо болезнь не станет устойчивой к этому гормону, либо организм не вызовет реакцию иммунной системы, которая ограничит способность препарата действовать. Некоторые пациенты могут достичь стойкой клинической ремиссии после приема этого препарата от шести месяцев до одного года. Это может быть более вероятно, если IFN-альфа был начат вскоре после другой терапии. Интерферон-альфа считается препаратом выбора для беременных с активным HCL, хотя он несет в себе некоторые риски, такие как возможность снижения притока крови к плаценте.
Интерферон-альфа работает, повышая чувствительность волосатых клеток к убивающему эффекту гормона иммунной системы TNF-альфа, выработке которого он способствует.[45] IFN-альфа лучше всего работает с классическими волосатыми клетками, которые не имеют защитного сцепления с витронектином или фибронектином, что позволяет предположить, что пациенты, у которых в биоптатах костного мозга обнаруживается меньше фиброзной ткани, могут с большей вероятностью ответить на терапию интерфероном-альфа. Это также объясняет, почему неприлипшие волосатые клетки, такие как клетки в кровотоке, исчезают во время лечения IFN-альфа задолго до того, как наблюдается уменьшение в прикрепленных волосатых клетках, таких как клетки костного мозга и селезенки.[45]
Другие методы лечения
Спленэктомия может привести к длительной ремиссии у пациентов, чья селезенка сильно поражена, но его эффективность заметно ниже, чем у кладрибина или пентостатина. Спленэктомия также выполняется пациентам, у которых постоянно увеличенные селезенки вызывают значительный дискомфорт, или пациентам, у которых постоянно низкий уровень тромбоцитов предполагает идиопатическая тромбоцитопеническая пурпура.
Пересадка костного мозга обычно избегают при этом заболевании, которое поддается лечению, из-за присущих процедуре рисков. Их можно рассматривать при рефрактерных случаях у более молодых, в остальном здоровых людей. Возможны «мини-трансплантаты».
Люди с низкое количество красных кровяных телец или же тромбоциты также может получать эритроциты и тромбоциты через переливание крови. При переливании крови всегда проводится облучение, чтобы удалить лейкоциты и тем самым снизить риск болезнь трансплантат против хозяина. Больные также могут получать гормон, стимулирующий выработку эритроцитов. Эти методы лечения могут быть с медицинской точки зрения, но не убивают волосатые клетки.
Люди с низким нейтрофил счет может быть дан филграстим или аналогичный гормон для стимуляции производства лейкоцитов. Однако исследование 1999 года показывает, что рутинное введение этого дорогостоящего инъекционного препарата не имеет практической ценности для пациентов с HCL после введения кладрибина.[46] В этом исследовании пациенты, получавшие филграстим, с такой же вероятностью испытывали высокую температуру и были госпитализированы, как и те, кто этого не делал, даже несмотря на то, что препарат искусственно завышал их количество лейкоцитов. Это исследование оставляет открытой возможность того, что филграстим по-прежнему может быть подходящим для пациентов с симптомами инфекции или в другое время, чем вскоре после лечения кладрибином.
Хотя волосатые клетки технически долговечны, вместо быстрого деления некоторых пациентов на поздних стадиях лечат химиотерапевтическими агентами широкого спектра действия, такими как метотрексат которые эффективны при уничтожении быстро делящихся клеток. Обычно это не предпринимается, если не исчерпаны все другие варианты, и обычно это не удается.
Прогноз
Успех лечения
Более 95% новых пациентов получают хорошее или, по крайней мере, адекватное лечение кладрибином или пентостатином.[47] Большинство новых пациентов могут ожидать ремиссии без признаков заболевания около десяти лет, а иногда и намного дольше после однократного приема одного из этих препаратов. Если в будущем потребуется повторное лечение, препараты обычно снова становятся эффективными, хотя средняя продолжительность ремиссии несколько короче при последующих курсах лечения.
Как и в случае B-клеточного хронического лимфоцитарного лейкоза, мутации в IGHV на волосистых клетках связаны с лучшими ответами на начальное лечение и с более длительным выживанием.[48]
Как скоро после лечения пациент снова почувствует себя «нормальным», зависит от нескольких факторов, в том числе:
- насколько прогрессировала болезнь на момент лечения;
- основное состояние здоровья пациента;
- был ли у пациента «полный ответ» или только частичный ответ на лечение;
- испытывал ли пациент какие-либо из редких, но серьезных побочных эффектов, таких как почечная недостаточность;
- насколько агрессивно заболевание человека;
- переживает ли пациент необычную психологическую травму из-за диагноза «рак»; и
- как пациент воспринимал свой уровень энергии до лечения и повседневное функционирование.
Срок жизни
При соответствующем лечении общая прогнозируемая продолжительность жизни пациентов нормальная или почти нормальная. У всех пациентов первые два года после постановки диагноза имеют самый высокий риск летального исхода; как правило, выживание в течение пяти лет означает хороший контроль над болезнью. После пятилетней клинической ремиссии пациенты в Соединенных Штатах с нормальными показателями крови часто могут иметь право на частное страхование жизни в некоторых американских компаниях.[49]
Точное измерение выживаемости пациентов с вариантной формой заболевания (HCL-V) затруднено из-за относительно высокого среднего возраста (70 лет) на момент постановки диагноза. Однако пациенты с HCL-V обычно выживают более 10 лет, а более молодые пациенты, вероятно, могут рассчитывать на долгую жизнь.
Ожидается, что во всем мире ежегодно умирает около 300 пациентов с HCL.[50] Некоторым из этих пациентов был поставлен диагноз HCL из-за серьезного заболевания, которое помешало им вовремя получить начальное лечение; многие другие умерли, прожив нормальную жизнь и испытав годы хорошего контроля над болезнью. Возможно, до пяти из шести пациентов с HCL умирают по какой-то другой причине.[оригинальное исследование? ]
Последующий уход
Несмотря на десятилетние ремиссии и годы нормальной жизни после лечения, волосатоклеточный лейкоз официально считается неизлечимым заболеванием. В то время как люди, пережившие солидные опухоли, обычно объявляются навсегда излеченными через два, три или пять лет, люди с волосатоклеточным лейкозом никогда не считаются «излеченными». Рецидивы HCL случаются даже после более чем двадцати лет непрерывной ремиссии. Пациентам потребуется пожизненное наблюдение, и они должны знать, что болезнь может повториться даже после десятилетий хорошего здоровья.
Хотя большинство онкологов считает волосатоклеточный лейкоз неизлечимым, есть некоторые свидетельства того, что некоторые пациенты действительно излечиваются после лечения. Из исходной группы из 358 пациентов, получавших кладрибин в клинике Скриппса, 9 из 19 пациентов с непрерывной полной ремиссией в течение в среднем 16 лет не имели MRD HCL по данным проточной цитометрии и IHC. Это говорит о том, что болезнь хотя бы некоторых пациентов может быть излечена.[51]
Люди в стадии ремиссии нуждаются в регулярных контрольных обследованиях после окончания лечения. Большинство врачей настаивают на том, чтобы посещать пациентов не реже одного раза в год на протяжении всей оставшейся жизни пациента и делать анализы крови примерно два раза в год. Регулярное последующее наблюдение обеспечивает тщательное наблюдение за пациентами, обсуждение любых изменений в состоянии здоровья, а также возможность выявления и лечения нового или рецидивирующего рака в кратчайшие сроки. Между регулярными назначенными приемами люди с волосатоклеточным лейкозом должны сообщать о любых проблемах со здоровьем, особенно вирусных или бактериальных инфекциях, как только они появляются.
Пациенты с HCL также имеют несколько более высокий, чем средний риск, риск развития второго типа рака, такого как рак толстой кишки или рак легких, в какой-то момент в течение своей жизни (в том числе до постановки диагноза HCL). Это, по-видимому, лучше всего связано с количеством волосяных клеток, а не с различными формами лечения.[52] В среднем пациенты могли бы разумно ожидать, что риск развития другого рака увеличится вдвое, с пиком примерно через два года после постановки диагноза HCL и стабильным падением после этого, если предположить, что HCL было успешно вылечено. Как правило, необходимы агрессивные меры по надзору и профилактике, хотя шансы развития второго рака в течение жизни после постановки диагноза HCL по-прежнему составляют менее 50%.
Также существует более высокий риск развития аутоиммунное заболевание.[15] Узелковый полиартериит в некоторых случаях был связан с лежащим в основе волосатоклеточным лейкозом. Аутоиммунные заболевания также могут перейти в ремиссию после лечения HCL.[15]
Эпидемиология
Это заболевание встречается редко, менее чем у 1 из 10000 человек в течение жизни диагностировали HCL. У мужчин в четыре-пять раз больше шансов заболеть волосатоклеточным лейкозом, чем у женщин.[53] В США ежегодный заболеваемость составляет примерно 3 случая на 1 000 000 мужчин в год и 0,6 случая на 1 000 000 женщин в год.[15]
Большинство пациентов - белые мужчины старше 50 лет.[15] хотя он был диагностирован как минимум у одного подростка.[54] Это реже встречается у людей африканского и азиатского происхождения по сравнению с людьми европейского происхождения.
По всей видимости, это не наследственное заболевание, хотя сообщалось о единичных семейных случаях, предполагающих предрасположенность,[55] обычно показывает общий Человеческий лейкоцитарный антиген (HLA) типа.[15]
Направления исследований
Консорциум волосатой клеточной лейкемии был основан в 2008 году с целью развеять опасения исследователей в отношении долгосрочного будущего исследований этого заболевания.[56] Отчасти потому, что существующие методы лечения настолько успешны, эта область привлекла очень мало новых исследователей.
В 2013 г. Фонд волосатоклеточного лейкоза была создана, когда Консорциум волосатых клеток лейкемии и Фонд исследования волосатых клеток лейкемии объединились. HCLF направлен на улучшение результатов для пациентов, продвигая исследования причин и лечения волосатоклеточного лейкоза, а также предоставляя образовательные ресурсы и комфорт всем, кто страдает от волосистоклеточного лейкоза.[57]
Три препарата иммунотоксина были изучены у пациентов в Национальные институты здравоохранения США Национальный институт рака в США.: BL22,[58] HA22[59] и ЛКМ-2.[60] Все эти препараты на основе белка объединяют часть антитела против В-клеток с бактериальным токсином, чтобы убивать клетки при интернализации. BL22 и HA22 атакуют общий белок CD22, который присутствует на волосатых клетках и здоровых В-клетках. LMB-2 атакует белок CD25, которого нет в варианте HCL, поэтому LMB-2 полезен только для пациентов с классическим HCL или японским вариантом. HA-22, теперь переименованный в моксетумомаб пасудотокс, изучается на пациентах с рецидивом волосатоклеточного лейкоза в Национальном институте рака в Бетесде, штат Мэриленд, в онкологическом центре доктора медицины Андерсона в Хьюстоне, штат Техас, и в Государственном университете Огайо в Колумбусе, штат Огайо. Ожидается, что в конце 2014 года начнут принимать пациентов и другие центры исследования, в том числе Королевская больница Марсдена в Лондоне, Англия.[61]
Другие клинические испытания[62] изучают эффективность кладрибина и ритуксимаба в устранении остаточные волосатые клетки которые остаются после лечения кладрибином или пентостатином. В настоящее время неизвестно, приведет ли устранение таких остаточных клеток к более длительным ремиссиям.
Мутация BRAF часто выявлялась в HCL (Tiacci et al. NEJM 2011), и некоторые пациенты могут реагировать на вемурафениб.
Основные оставшиеся вопросы исследования - это определение причины HCL и определение того, что мешает нормальному созреванию волосяных клеток.[63]
Смотрите также
Рекомендации
- ^ «Волосатоклеточный лейкоз: Медицинская энциклопедия MedlinePlus». medlineplus.gov. Получено 2018-04-17.
- ^ Шрек Р., Доннелли В. Дж. (Февраль 1966 г.). ""Волосатые «клетки крови при лимфоретикулярной неопластической болезни и« жгутиковые »клетки нормальных лимфатических узлов». Кровь. 27 (2): 199–211. Дои:10.1182 / blood.V27.2.199.199. PMID 5322749. Архивировано из оригинал на 2007-09-29. Получено 2007-04-20.
- ^ «Волосатоклеточный лейкоз | Информационный центр по генетическим и редким заболеваниям (GARD) - программа NCATS». rarediseases.info.nih.gov. Получено 2018-04-17.
- ^ «Лечение волосатоклеточного лейкоза». Национальный институт рака. Архивировано из оригинал на 2008-05-14. Получено 2007-09-07.
- ^ Зузель М., Коули Дж. К., Патон Р. К., Бернс Г. Ф., Макникол Г. П. (1979). «Функция тромбоцитов при волосисто-клеточном лейкозе». J. Clin. Патол. 32 (8): 814–21. Дои:10.1136 / jcp.32.8.814. ЧВК 1145815. PMID 512041.
- ^ Пандольфино Дж., Хакимиан Д., Радемейкер А.В., Таллман М.С. (июль 1997 г.). «Гипохолестеринемия при лейкемии волосатых клеток: маркер пролиферативной активности». Являюсь. J. Hematol. 55 (3): 129–33. Дои:10.1002 / (SICI) 1096-8652 (199707) 55: 3 <129 :: AID-AJH2> 3.0.CO; 2-U. PMID 9256291.
- ^ Джулиуссон Дж., Витолс С., Лилиемарк Дж. (Июль 1995 г.). «Механизмы гипохолестеринемии при волосатоклеточном лейкозе». BMJ. 311 (6996): 27. Дои:10.1136 / bmj.311.6996.27. ЧВК 2550084. PMID 7613319.
- ^ Клавель Дж., Мандеро Л., Кордье С., Ле Гоастер С., Хемон Д., Консо Ф, Фландрин Дж. (1995). «Волосатоклеточный лейкоз, род занятий и курение». Br. J. Haematol. 91 (1): 154–61. Дои:10.1111 / j.1365-2141.1995.tb05261.x. PMID 7577624.
- ^ Орланди Дж., Фануччи С., Страта Дж., Паталео Л., Ландуччи Пеллегрини Л., Пронтера С., Мартини А., Мурри Л. (2000). «Преходящая дисфункция вегетативной нервной системы при остром инсульте». Acta Neurol. Сканд. 102 (5): 317–21. Дои:10.1034 / j.1600-0404.2000.102005317.x. PMID 11083509.
- ^ Тиаччи Э., Трифонов В., Скьявони Дж., Холмс А., Керн В., Мартелли М. П., Пуччарини А., Бигерна Б., Пачини Р., Уэллс В. А., Спортолетти П., Петтиросси В., Маннуччи Р., Эллиотт О, Лизо А., Амброзетти А., Пульсони А. , Forconi F, Trentin L, Semenzato G, Inghirami G, Capponi M, Di Raimondo F, Patti C, Arcaini L, Musto P, Pileri S, Haferlach C, Schnittger S, Pizzolo G, Foà R, Farinelli L, Haferlach T, Паскуалуччи Л., Рабадан Р., Фалини Б. (2011). «Мутации BRAF при волосисто-клеточном лейкозе». N Engl J Med. 364 (24): 2305–2315. Дои:10.1056 / NEJMoa1014209. ЧВК 3689585. PMID 21663470.
- ^ Комитет по рассмотрению воздействия гербицидов на здоровье ветеранов Вьетнама (седьмое обновление за два года) (2009 г.). Ветераны и агент Orange: обновление 2008 г.. Институт медицины. С. 349–350. Дои:10.17226/12662. ISBN 978-0-309-13884-0. PMID 25032343.
- ^ Feuer G, Green PL (сентябрь 2005 г.). «Сравнительная биология Т-клеточного лимфотропного вируса типа 1 (HTLV-1) и HTLV-2». Онкоген. 24 (39): 5996–6004. Дои:10.1038 / sj.onc.1208971. ЧВК 2659530. PMID 16155606.
- ^ Розенблатт Дж. Д., Джорджи Дж. В., Голд Д. В., Эзра Дж. Б., Ву А., Винберг С. Д., Гласпи Дж., Ваксман В., Чен И. С. (февраль 1988 г.). «Интегрированный геном вируса Т-клеточного лейкоза II человека в CD8 + Т-клетках от пациента с« атипичным »волосатоклеточным лейкозом: доказательства различных лимфопролиферативных расстройств Т- и В-клеток». Кровь. 71 (2): 363–9. Дои:10.1182 / blood.V71.2.363.363. PMID 2827811.
- ^ Руку Д.Ф., Мерфи Е.Л. (2004). «Эпидемиология и исходы заболевания человеческим Т-лимфотропным вирусом II типа». СПИД Rev. 6 (3): 144–54. PMID 15595431.
- ^ а б c d е ж грамм час я j k л м п о п q р s Винтроб, Максвелл Майер (2004). Клиническая гематология Винтроба. Джон Г. Грир; Джон Ферстер, Джон Н. Люкенс, Джордж М. Роджерс, Фриксос Параскевас (11-е изд.). Хагерстаун, Мэриленд: Липпинкотт Уильямс и Уилкинс. С. 2465–2466. ISBN 978-0-7817-3650-3.
- ^ а б c Ванко С.О., де Кастро К. (2006). «Волосатоклеточный лейкоз: неуловимое, но излечимое заболевание». Онколог. 11 (7): 780–9. Дои:10.1634 / теонколог. 11-7-780. PMID 16880237.
Таблица 4. Фенотипическая дифференциальная диагностика волосатоклеточного лейкоза. - ^ Тиаччи Э., Трифонов В., Скьявони Дж., Холмс А., Керн В., Мартелли М. П., Пуччарини А., Бигерна Б., Пачини Р., Уэллс В. А., Спортолетти П., Петтиросси В., Маннуччи Р., Эллиотт О, Лизо А., Амброзетти А., Пульсони А. , Forconi F, Trentin L, Semenzato G, Inghirami G, Capponi M, Di Raimondo F, Patti C, Arcaini L, Musto P, Pileri S, Haferlach C, Schnittger S, Pizzolo G, Foà R, Farinelli L, Haferlach T, Паскуалуччи Л., Рабадан Р., Фалини Б. (июнь 2011 г.). «Мутации BRAF при волосисто-клеточном лейкозе». N. Engl. J. Med. 364 (24): 2305–15. Дои:10.1056 / NEJMoa1014209. ЧВК 3689585. PMID 21663470.
- ^ Исследования волосатоклеточного лейкоза показывают перспективность новых технологий сканирования ДНК - Британский научный блог "Исследования рака"
- ^ Ванхентенрейк В., Де Вольф-Петерс С., Влодарска I (2004). «Сравнительные исследования гибридизации экспрессированной последовательности волосатоклеточного лейкоза показывают однородный профиль экспрессии и отпечаток сигнатуры селезенки». Кровь. 104 (1): 250–5. Дои:10.1182 / кровь-2004-01-0181. PMID 15016649.
- ^ «Клинический случай проточной цитометрии №54». Архивировано из оригинал на 2007-10-09. Получено 2007-09-07.
- ^ Кэннон Т., Мобарек Д., Вегге Дж., Таббара И.А. (октябрь 2008 г.). «Волосатоклеточный лейкоз: современные концепции». Рак Инвест. 26 (8): 860–5. Дои:10.1080/07357900801965034. PMID 18798068. S2CID 6196898.
- ^ Волосатоклеточный лейкоз ~ Дифференциалы в eMedicine
- ^ "Американский журнал клинической патологии". Получено 2009-01-31. Цитировать журнал требует
| журнал =(помощь)[постоянная мертвая ссылка ] - ^ а б Сайнати Л., Матутес Е., Маллиган С., де Оливейра М.П., Рани С., Ламперт И.А., Катовски Д. (июль 1990 г.). "Вариант формы волосатоклеточного лейкоза, устойчивый к альфа-интерферон: клинико-фенотипическая характеристика 17 пациентов ». Кровь. 76 (1): 157–62. Дои:10.1182 / blood.V76.1.157.157. PMID 2364167.
- ^ Коули Дж. К., Бернс Г. Ф., Хейхо Ф. Г. (1980). «Хроническое лимфопролиферативное заболевание с отличительными особенностями: особый вариант волосисто-клеточного лейкоза». Лейк. Res. 4 (6): 547–59. Дои:10.1016/0145-2126(80)90066-1. PMID 7206776.
- ^ а б c d Матутес Э., Уотерспун А, Брито-Бабапулле В, Катовски Д. (2001). «Естественное течение и клинико-патологические особенности вариантной формы волосатоклеточного лейкоза». Лейкемия. 15 (1): 184–6. Дои:10.1038 / sj.leu.2401999. PMID 11243388. S2CID 6609635.
- ^ Я-Ин С, Брандвейн Дж, Панталони Д., Чанг Х (2005). «Вариант волосатоклеточного лейкоза с особенностями интрасинусоидального поражения костного мозга». Arch. Патол. Лаборатория. Med. 129 (3): 395–8. Дои:10.1043 / 1543-2165 (2005) 129 <395: HCLVWF> 2.0.CO; 2 (неактивно 01.09.2020). PMID 15737038.CS1 maint: DOI неактивен по состоянию на сентябрь 2020 г. (связь)
- ^ Крейтман, Роберт Дж .; Уилсон, Виндхэм; Calvo, Katherine R .; Аронс, Евгений; Рот, Лаура; Сапольски, Джеффри; Чжоу, Хун; Раффельд, Марк; Стетлер-Стивенсон, Марьялис (2013-12-15). «Кладрибин с ритуксимабом немедленного действия для лечения пациентов с вариантным волосатоклеточным лейкозом». Клинические исследования рака. 19 (24): 6873–6881. Дои:10.1158 / 1078-0432.CCR-13-1752. ISSN 1078-0432. ЧВК 3867590. PMID 24277451.
- ^ "HCL-V | Фонд волосатоклеточного лейкоза". www.hairycellleukemia.org. Получено 2016-05-31.
- ^ Бертхем Дж., Коули Дж. С. (январь 1994 г.). «Фиброз костного мозга при волосисто-клеточном лейкозе вызывается синтезом и сборкой фибронектинового матрикса волосатыми клетками». Кровь. 83 (2): 497–504. Дои:10.1182 / blood.V83.2.497.497. PMID 8286747.
- ^ de Totero D, Tazzari PL, Lauria F, Raspadori D, di Celle PF, Carbone A, Gobbi M, Foa R (июль 1993 г.). «Фенотипический анализ волосатоклеточного лейкоза:« вариантные »случаи экспрессии рецептора интерлейкина-2 бета цепочка, но не альфа цепь (CD25) ". Кровь. 82 (2): 528–35. Дои:10.1182 / blood.V82.2.528.528. PMID 8329708.
- ^ Матутес Э, Уотерспун А, Катовски Д. (2003). «Вариантная форма волосисто-клеточного лейкоза». Лучшая практика Res Clin Haematol. 16 (1): 41–56. Дои:10.1016 / S1521-6926 (02) 00086-5. PMID 12670464.
- ^ Валлианату К., Брито-Бабапулле В., Матутес Е., Аткинсон С., Катовски Д. (1999). «Делеция гена p53 и трисомия 12 при лейкемии волосатых клеток и ее вариант». Лейк. Res. 23 (11): 1041–5. Дои:10.1016 / S0145-2126 (99) 00127-7. PMID 10576509.
- ^ Аронс, Евгений; Сунтум, Тара; Стетлер-Стивенсон, Мариалис; Крейтман, Роберт Дж. (19 ноября 2009 г.). «VH4-34 + волосатоклеточный лейкоз, новый вариант с плохим прогнозом, несмотря на стандартную терапию». Кровь. 114 (21): 4687–4695. Дои:10.1182 / кровь-2009-01-201731. ISSN 0006-4971. ЧВК 2780305. PMID 19745070.
- ^ Миядзаки М., Тагучи А., Сакураги С., Митани Н., Мацуда К., Шинохара К. (май 2004 г.). «[Волосатоклеточный лейкоз, японский вариант, успешно вылеченный кладрибином]». Риншо Кецуэки (на японском языке). 45 (5): 405–7. PMID 15199752.
- ^ Раванди Ф., Йоргенсен Дж. Л., О'Брайен С. М., Верстовсек С., Коллер К. А., Фадерл С., Джайлс Ф. Дж., Ферраджоли А., Виерда В. Г., Одинга С., Хуанг Х, Томас Д. А., Фрейрих Э. Дж., Джонс Д., Китинг М. Дж., Кантарджиан Х. М. ( Июнь 2006 г.). «Искоренение минимальной остаточной болезни при волосатоклеточном лейкозе». Кровь. 107 (12): 4658–62. Дои:10.1182 / кровь-2005-11-4590. PMID 16497968.
- ^ Робак Т., Ямрозяк К., Гора-Тайбор Дж., Блонски Дж. З., Кашницки М., Двилевич-Троячек Дж., Виатер Е., Здунчик А., Дибович Дж., Дмошинска А., Войташко М., Здзярска Б, Кальбекра Аевицка, М, Костярска К., Стелла-Холовецка Б., Сулек К., Гавронски К., Скотницки А.Б., Новак В., Завильска К., Молендович-Портала Л., Клоцко Ю., Соколовски Дж., Варзоча К., Сеферинска И., Цегларек Б., Конопка Л. (2007). «Кладрибин в еженедельном и ежедневном графике лечения нелеченой активной волосисто-клеточной лейкемии: окончательный отчет Польской группы по лейкемии взрослых (PALG) о проспективном рандомизированном многоцентровом исследовании». Кровь. 109 (9): 3672–5. Дои:10.1182 / кровь-2006-08-042929. PMID 17209059. Архивировано из оригинал на 2007-09-29. Получено 2007-07-04.
- ^ Эльза М., Рухлемер Р., Осуджи Н., Дель Джудис И., Матутес Е., Вудман А., Уотерспун А., Суансбери Дж., Дирден С., Катовски Д. (2005). «Длительные ремиссии волосатоклеточного лейкоза с пуриновыми аналогами: отчет о 219 пациентах со средним периодом наблюдения 12,5 лет». Рак. 104 (11): 2442–8. Дои:10.1002 / cncr.21447. PMID 16245328.
- ^ Томас Д.А., О'Брайен С., Буэсо-Рамос С., Фадерл С., Китинг М.Дж., Джайлс Ф.Дж., Кортес Дж., Кантарджан Х.М. (2003). «Ритуксимаб при рецидивирующем или рефрактерном волосатоклеточном лейкозе». Кровь. 102 (12): 3906–11. Дои:10.1182 / кровь-2003-02-0630. PMID 12816862. Архивировано из оригинал на 2007-09-09. Получено 2007-07-04.
- ^ Ниева Дж., Бетел К., Савен А. (2003). «Фаза 2 исследования ритуксимаба в лечении пациентов с волосатоклеточным лейкозом, не получавших кладрибина». Кровь. 102 (3): 810–3. Дои:10.1182 / кровь-2003-01-0014. PMID 12663446. Архивировано из оригинал на 2007-09-29. Получено 2007-07-04.
- ^ Нарат С., Гандла Дж., Доган А., Мехта А. (август 2005 г.). «Успешное лечение варианта волосатоклеточного лейкоза ритуксимабом». Лейк. Лимфома. 46 (8): 1229–32. Дои:10.1080/10428190500083433. PMID 16085567. S2CID 20116705.
- ^ Волосатоклеточный лейкоз ~ лекарства в eMedicine
- ^ Кесада Дж. Р., Рубен Дж., Мэннинг Дж. Т., Херш Е. М., Гаттерман Дж. Ю (январь 1984 г.). «Альфа-интерферон для индукции ремиссии волосисто-клеточного лейкоза». N. Engl. J. Med. 310 (1): 15–8. Дои:10.1056 / NEJM198401053100104. PMID 6689734.
- ^ а б Ратейн MJ, Голомб HM, Вардиман JW, Вокс EE, Джейкобс RH, Дейли К. (1985). «Лечение волосатоклеточного лейкоза рекомбинантным альфа-2 интерфероном». Кровь. 65 (3): 644–8. Дои:10.1182 / кровь.V65.3.644.644. PMID 3971043.
- ^ а б Бейкер П.К., Петтитт А.Р., Слупски Дж. Р., Чен Х. Дж., Гленн М. А., Зузель М., Коули Дж. К. (2002). «Ответ волосатых клеток на IFN-альфа включает индукцию апоптоза через аутокринный TNF-альфа и защиту за счет адгезии». Кровь. 100 (2): 647–53. Дои:10.1182 / blood.V100.2.647. PMID 12091360. S2CID 6712599.
- ^ Савен А., Буриан С., Адусумалли Дж., Козиол Дж. А. (1999). «Филграстим от кладрибин-индуцированной нейтропенической лихорадки у пациентов с волосатоклеточной лейкемией». Кровь. 93 (8): 2471–7. Дои:10.1182 / кровь.V93.8.2471. PMID 10194424. Архивировано из оригинал 21.09.2007. Получено 2007-07-16.
- ^ Else M, Ruchlemer R, Osuji N, Del Giudice I, Matutes E, Woodman A, Wotherspoon A, Swansbury J, Dearden C, Catovsky D (декабрь 2005 г.). «Длительные ремиссии волосатоклеточного лейкоза с пуриновыми аналогами: отчет о 219 пациентах со средним периодом наблюдения 12,5 лет». Рак. 104 (11): 2442–8. Дои:10.1002 / cncr.21447. PMID 16245328.
- ^ Forconi F, Sozzi E, Cencini E, Zaja F, Intermesoli T, Stelitano C, Rigacci L, Gherlinzoni F, Cantaffa R, Baraldi A, Gallamini A, Zaccaria A, Pulsoni A, Gobbi M, Tassi M, Raspadori D, Leoncini L , Ринальди А., Сабаттини Э, Бертони Ф., Пилери С.А., Лаурия Ф. (ноябрь 2009 г.). «Волосатоклеточные лейкозы с немутантными генами IGHV определяют второстепенную подгруппу, невосприимчивую к кладрибину одного агента и с более агрессивным поведением». Кровь. 114 (21): 4696–4702. Дои:10.1182 / кровь-2009-03-212449. PMID 19667403.
- ^ «Архивная копия» (PDF). Архивировано из оригинал (PDF) на 2012-02-24. Получено 2018-11-29.CS1 maint: заархивированная копия как заголовок (связь)
- ^ «Архивная копия». Архивировано из оригинал на 2007-08-13. Получено 2007-07-30.CS1 maint: заархивированная копия как заголовок (связь)
- ^ «Последняя информация о волосатоклеточном лейкозе - гематология и онкология».
- ^ Au WY, Klasa RJ, Gallagher R, Le N, Gascoyne RD, Connors JM (август 1998 г.). «Вторые злокачественные новообразования у пациентов с волосатоклеточной лейкемией в Британской Колумбии: 20-летний опыт». Кровь. 92 (4): 1160–4. Дои:10.1182 / кровь.V92.4.1160. PMID 9694703.
- ^ «Волосатоклеточный лейкоз». Получено 2007-09-07.
- ^ Йетгин С., Олчай Л., Еникесу И., Онер А.Ф., Каглар М. (сентябрь 2001 г.). «Рецидив лейкемии волосатых клеток из-за изолированной узловатой инфильтрации кожи». Педиатр Гематол Онкол. 18 (6): 415–7. Дои:10.1080/088800101316922047. PMID 11554237. S2CID 793191.
- ^ Граматович М., Беннетт Дж. М., Хискок Дж. Г., Гревал К.С. (апрель 1993 г.). «Три случая семейного волосатоклеточного лейкоза». Являюсь. J. Hematol. 42 (4): 337–9. Дои:10.1002 / ajh.2830420402. PMID 8493982.
- ^ Хольцман Д. (март 2009 г.). «Помешал ли успех исследованиям волосатоклеточного лейкоза? Ключевые вопросы остаются без ответа, несмотря на большие успехи». J. Natl. Институт рака. 101 (6): 370–3. Дои:10.1093 / jnci / djp051. PMID 19276454.
- ^ "| Фонд волосатоклеточной лейкемии". Hairycellleukemia.org. 2014-06-20. Получено 2015-12-24.
- ^ Номер клинического исследования NCT00074048 для "Иммунотоксина BL22 в лечении пациентов, ранее получавших кладрибин от волосатоклеточного лейкоза" на ClinicalTrials.gov
- ^ Номер клинического исследования NCT00462189 за "Исследование безопасности иммунооксина CAT-8015 у пациентов с HCL с прогрессирующим заболеванием" в ClinicalTrials.gov
- ^ Номер клинического исследования NCT00337311 на "LMB-2 для лечения волосатоклеточного лейкоза" на ClinicalTrials.gov
- ^ "Моксетумомаб Пасудотокс для лечения продвинутого волосатоклеточного лейкоза - Просмотр полного текста". ClinicalTrials.gov. Получено 2015-12-24.
- ^ Например, испытание NCT00412594 и NCT00923013
- ^ Коули, Джон. "Биология болезни, включая вопросы без ответов | HairyCell.org". Архивировано из оригинал на 2011-07-26. Получено 2010-06-23.
внешняя ссылка
| Классификация | |
|---|---|
| Внешние ресурсы |
