Мышечная дистрофия - Muscular dystrophy
| Мышечная дистрофия | |
|---|---|
 | |
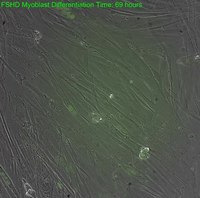
| В пораженной мышце (справа) ткань дезорганизована, и концентрация дистрофин (зеленый) значительно сокращен по сравнению с нормальной мышцей (слева). | |
| Специальность | Педиатрия, медицинская генетика |
| Симптомы | Нарастающее ослабление, распад скелетные мышцы, проблемы с ходьбой[1][2] |
| Продолжительность | Долгосрочный[1] |
| Типы | > 30 в том числе Мышечная дистрофия Дюшенна, Мышечная дистрофия Беккера, фасциально-лопаточно-плечевая мышечная дистрофия, конечностно-поясная мышечная дистрофия, миотоническая дистрофия[1][2] |
| Причины | Генетический (Х-сцепленный рецессивный, аутосомно-рецессивный, или же аутосомно-доминантный )[2] |
| Диагностический метод | Анализы крови, генетическое тестирование[2] |
| Уход | Физиотерапия, подтяжки, корректирующий хирургия, вспомогательная вентиляция легких[1][2] |
| Прогноз | Зависит от типа[1] |
Мышечная дистрофия (MD) - это группа мышечные заболевания что приводит к усилению ослабления и разрушения скелетные мышцы через некоторое время.[1] Заболевания различаются по тому, какие мышцы поражаются в первую очередь, по степени слабости, по скорости их обострения и по времени появления симптомов.[1] Многие люди со временем перестают ходить.[2] Некоторые типы также связаны с проблемами в других органы.[2]
Группа мышечной дистрофии включает тридцать различных генетических заболеваний, которые обычно подразделяются на девять основных категорий или типов.[1][2] Самый распространенный тип - Мышечная дистрофия Дюшенна (DMD), который обычно поражает мужчин, начиная с четырехлетнего возраста.[1] Другие типы включают Мышечная дистрофия Беккера, фасциально-лопаточно-плечевая мышечная дистрофия, конечностно-поясная мышечная дистрофия, и миотоническая дистрофия.[1] Они связаны с мутациями в гены которые участвуют в производстве мышечных белков.[2] Это может произойти из-за наследование дефекта от родителей или мутации, происходящей во время ранняя разработка.[2] Расстройства могут быть Х-сцепленный рецессивный, аутосомно-рецессивный, или же аутосомно-доминантный.[2] Диагноз часто включает анализы крови и генетическое тестирование.[2]
Лекарства от мышечной дистрофии нет.[1] Физиотерапия, подтяжки, и корректирующие хирургия может помочь с некоторыми симптомами.[1] Вспомогательная вентиляция легких может потребоваться тем, у кого слабость дыхательные мышцы.[2] Используемые лекарства включают: стероиды для замедления дегенерации мышц, противосудорожные препараты контролировать припадки и некоторая мышечная активность, и иммунодепрессанты отложить повреждение до смерти мышечные клетки.[1] Результаты зависят от конкретного типа расстройства.[1]
Мышечная дистрофия Дюшенна, составляющая примерно половину всех случаев мышечной дистрофии, поражает примерно одного из 5000 мужчин при рождении.[2] Мышечная дистрофия была впервые описана в 1830-х гг. Чарльз Белл.[2] Слово «дистрофия» происходит от греческого умирает, что означает "трудный" и трофей что означает «питать».[2] Генная терапия, как лечение, находится на ранних стадиях изучения на людях.[2]
Признаки и симптомы
Признаки и симптомы мышечной дистрофии:[3]
- Прогрессирующее мышечное истощение
- Плохой баланс
- Сколиоз (искривление позвоночника и спины)
- Прогрессирующая неспособность ходить
- Вразвалочку походка
- Деформация теленка
- Ограниченный диапазон движения
- Респираторный трудность
- Кардиомиопатия
- Мышечные спазмы
- Знак Гауэрса
Причина

Эти условия обычно унаследованный, и различные мышечные дистрофии следуют разным образцам наследования. Мышечная дистрофия может передаваться по наследству как Х-связанный беспорядок рецессивный или же доминирующий беспорядок. Кроме того, это может быть спонтанная мутация что означает ошибки в воспроизведении ДНК и спонтанные поражения. Спонтанные поражения возникают в результате естественного повреждения ДНК, наиболее распространенными из которых являются депуринизация и дезаминирование.[4][5]
Дистрофин белок содержится в мембране мышечных волокон; его спиральная природа позволяет ему действовать как пружина или амортизатор. Дистрофин ссылки актин в цитоскелет и дистрогликаны плазматической мембраны мышечной клетки, известной как сарколемма (внеклеточная). Помимо механической стабилизации, дистрофин также регулирует уровень кальция.[6][7]Ген дистрофина расположен на Х-хромосоме. У мужчин одиночная Х-хромосома имеет только один ген дистрофина. Если в этом гене есть мутация, мышцы мужчины будут испытывать недостаток в дистрофине и будут медленно дегенерировать; Мутации в гене дистрофина были идентифицированы как причина МДД исследователями MDA в 1986 году. У женщины почти всегда есть два гена дистрофина, по одному на каждой Х-хромосоме, и даже если один из них не работает, другого гена достаточно. чтобы поддерживать уровень дистрофина на достаточно высоком уровне, чтобы сохранить мышечную функцию как сердца, так и скелетных мышц. Тем не менее, исследования показали, что у небольшого количества женщин, имеющих как рабочий, так и неработающий ген дистрофина, могут проявляться симптомы МДД.[нужна цитата ]Недавние исследования взаимодействия белков с миссенс-мутации и его соседи показали высокую степень жесткости, связанную с центральными белками-концентраторами, участвующими в связывании белков, и гибкими подсетями, имеющими молекулярные функции, связанные с кальцием.[8]
Диагностика
Диагноз мышечной дистрофии ставится по результатам: биопсия мышц, повысился креатинфосфокиназа (CpK3), электромиография, и генетическое тестирование. Медицинский осмотр и история болезни пациента помогут врачу определить тип мышечной дистрофии. Определенные группы мышц подвержены различным типам мышечной дистрофии.[9]
Другие тесты, которые можно сделать, - это грудь рентгеновский снимок, эхокардиограмма, компьютерная томография и сканирование магнитно-резонансного изображения, которое с помощью магнитного поля может создавать изображения, детали которых помогают диагностировать мышечную дистрофию.[10] Качество жизни можно измерить с помощью специальных анкет.[11]
Классификация
| Название расстройства | OMIM | Ген | Описание |
|---|---|---|---|
| Мышечная дистрофия Беккера | 300376 | DMD | Мышечная дистрофия Беккера (МПК) - менее тяжелый вариант Мышечная дистрофия Дюшенна и вызывается выработкой урезанной, но частично функциональной формы дистрофина.[12] Выживание обычно длится до старости и затрагивает только мальчиков (за очень редкими исключениями).[13] |
| Врожденная мышечная дистрофия | Несколько | Несколько |  Гидроцефалия Возраст начала - это рождение, симптомы включают общую мышечную слабость и возможные деформации суставов, болезнь прогрессирует медленно, а продолжительность жизни укорачивается. Врожденная мышечная дистрофия включает несколько расстройств с рядом симптомов. Дегенерация мышц может быть легкой или тяжелой. Проблемы могут быть ограничены скелетные мышцы, или дегенерация мышц может сочетаться с воздействием на мозг и другие системы органов.[14] Некоторые формы врожденных мышечных дистрофий вызываются дефектами белков, которые, как считается, имеют некоторое отношение к комплексу дистрофин-гликопротеин и к связям между мышечными клетками и окружающей их клеточной структурой. Некоторые формы врожденной мышечной дистрофии проявляются серьезными пороками развития головного мозга, такими как лиссэнцефалия и гидроцефалия.[12] |
| Мышечная дистрофия Дюшенна | 310200 | DMD | Мышечная дистрофия Дюшенна (МДД) является наиболее распространенной формой мышечной дистрофии у детей; обычно он поражает только мальчиков (за очень редкими исключениями) и становится клинически очевидным, когда ребенок начинает ходить. К 10 годам ребенку могут потребоваться подтяжки для ходьбы, а к 12 годам большинство пациентов не могут ходить.[15] Продолжительность жизни колеблется от 15 до 45, хотя бывает и несколько исключений.[15] Исследователи определили ген белка дистрофина, который в отсутствие которого вызывает МДД.[16] Поскольку ген находится на Х-хромосоме, это заболевание поражает в первую очередь мужчин, а у женщин-носителей симптомы более легкие. Спорадические мутации в этом гене происходят часто.[17] Дистрофин является частью сложной структуры, включающей несколько других белковых компонентов. «Дистрофин-гликопротеиновый комплекс» помогает закрепить структурный скелет (цитоскелет) внутри мышечных клеток через внешнюю мембрану (сарколемму) каждой клетки на тканевом каркасе (внеклеточном матриксе), который окружает каждую клетку. Из-за дефектов в этой сборке сокращение мышцы приводит к разрушению внешней мембраны мышечных клеток и, в конечном итоге, к ослаблению и истощению мышцы.[12] |
| Дистальная мышечная дистрофия | 254130 | DYSF | Возраст начала дистальных мышечных дистрофий составляет от 20 до 60 лет; симптомы включают слабость и истощение мышц рук, предплечий и голеней; прогресс медленный и не опасный для жизни.[18] Миопатия Миёси, одна из дистальных мышечных дистрофий, вызывает первоначальную слабость в икроножных мышцах и вызывается дефектами того же гена, ответственного за одну форму мышечная дистрофия конечностей.[12] |
| Мышечная дистрофия Эмери – Дрейфуса | 310300, 181350 | EMD, LMNA | Пациенты с мышечной дистрофией Эмери – Дрейфуса обычно в детстве и раннем подростковом возрасте имеют контрактуры. Клинические признаки включают мышечную слабость и истощение, начинающееся с дистальных мышц конечностей и прогрессирующее с вовлечением мышц пояснично-конечностей. Большинство пациентов также страдают нарушениями сердечной проводимости и аритмиями.[19][20] Три подтипа Emery – Dreifuss MD различаются по типу наследования: Х-сцепленный, аутосомно-доминантный и аутосомно-рецессивный. Х-связанная форма является наиболее распространенной. Каждый тип различается по распространенности и симптомам. Болезнь вызывается мутациями в LMNA ген, или чаще EMD ген. Оба гена кодируют белковые компоненты ядерной оболочки. Однако не совсем понятно, как эти мутации вызывают патогенез.[21] |
| Лице-лопаточно-плечевая мышечная дистрофия | 158900 | DUX4 | Интервальная экспрессия белка DUX4 в клетках FSHD Фациоскапуло-плечевая мышечная дистрофия (ЛЛД) вызывает прогрессирующую слабость, первоначально в мышцах лица, плеч и предплечий. Часто поражаются дополнительные мышцы.[22] Симптомы обычно проявляются в подростковом возрасте.[12] Пострадавшие люди могут стать инвалидами, при этом 20% нуждаются в инвалидной коляске к 50 годам.[23] Тип наследования аутосомно-доминантный для наиболее распространенного подтипа (FSHD1); 30% случаев связаны со спонтанными мутациями.[23] Проникновение и степень тяжести у женщин ниже, чем у мужчин.[23][24] Причина - дерепрессия DUX4, что требует двух мутаций: одна мутация вызывает деметилирование из DUX4 регион, позволяющий DUX4 транскрипция, и еще одна мутация, образующая последовательность полиаденилирования ниже по течению DUX4, обеспечивая стабильность DUX4 информационная РНК и повышенная вероятность перевод.[23][25] |
| Мышечная дистрофия конечностей | Несколько | Несколько | Мышечная дистрофия конечностей и поясов (LGMD) поражает как мальчиков, так и девочек.[26] Все LGMD демонстрируют одинаковое распределение мышечной слабости, поражающей как верхнюю часть рук, так и ноги. Были идентифицированы многие формы LGMD, демонстрирующие различные модели наследования (аутосомно-рецессивный против аутосомно-доминантного). При аутосомно-рецессивном типе наследования человек получает две копии дефектного гена, по одной от каждого родителя. Рецессивные LGMD встречаются чаще, чем доминантные формы, и обычно начинаются в детстве или подростковом возрасте. Доминирующие LGMD обычно проявляются во взрослом возрасте. Некоторые из рецессивных форм были связаны с дефектами белков, которые составляют комплекс дистрофин-гликопротеин.[12] Хотя человек обычно ведет нормальный образ жизни с некоторой помощью, в некоторых крайних случаях смерть от LGMD наступает из-за сердечно-легочных осложнений.[27] |
| Миотоническая мышечная дистрофия | 160900, 602668 | ДМПК, ZNF9 | Миотоническая мышечная дистрофия - это аутосомно-доминантное заболевание, которое проявляется миотония (замедленное расслабление мышц), а также мышечное истощение и слабость.[28] Миотонический MD различается по степени тяжести и проявлениям и влияет на многие системы организма, помимо скелетных мышц, включая сердце, эндокринные органы и глаза.[29] Миотонический MD типа 1 (DM1) - наиболее распространенная форма мышечной дистрофии у взрослых. Это происходит в результате расширения короткого (CTG) повтора в последовательности ДНК гена протеинкиназы миотонической дистрофии. Миотоническая мышечная дистрофия 2 типа (СД2) встречается реже и является результатом экспансии повтора CCTG в гене белка 9 цинкового пальца.[12] |
| Окулофарингеальная мышечная дистрофия | 164300 | PABPN1 | Окулофарингеальный возраст MD в начале заболевания составляет от 40 до 70 лет; симптомы поражают мышцы век, лица и горла, за которыми следует слабость мышц таза и плеч; это приписывают экспансии коротких повторов в геноме, которые регулируют трансляцию некоторых генов в функциональные белки.[12] |
Управление
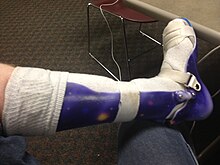
В настоящее время не существует лекарства от мышечной дистрофии. Что касается менеджмента, физиотерапия, трудотерапия ортопедическое вмешательство (например, ортез на голеностопный сустав ),[30][31] логопед и респираторная терапия могут быть полезны.[30] Кортикостероиды низкой интенсивности, такие как преднизон, и дефлазакорт может помочь поддерживать мышечный тонус.[32] Ортезы (ортопедические приспособления, используемые для поддержки) и корректирующие ортопедическая хирургия в некоторых случаях может потребоваться для улучшения качества жизни.[2] Сердечные проблемы, возникающие при EDMD и миотонической мышечной дистрофии, могут потребовать кардиостимулятор.[33] В миотония (отсроченное расслабление мышцы после сильного сокращения), возникающее при миотонической мышечной дистрофии, можно лечить такими лекарствами, как хинин.[34]
Трудотерапия помогает пациенту с MD участвовать в повседневной деятельности (например, самостоятельное питание и уход за собой) и в досуге на максимально независимом уровне. Это может быть достигнуто с использованием адаптивного оборудования или использования методов энергосбережения. Трудотерапия может вносить изменения в среду обитания человека, как дома, так и на работе, для улучшения функций и доступности человека; кроме того, он направлен на психосоциальные изменения и снижение когнитивных способностей, которые могут сопровождать MD, и обеспечивает поддержку и просвещение о болезни для семьи и отдельного человека.[35]
Прогноз
Прогноз зависит от индивидуальной формы МД. В некоторых случаях человек с мышечным заболеванием будет становиться все слабее до такой степени, что сокращается продолжительность жизни из-за сердечных и дыхательных осложнений. Однако некоторые мышечные заболевания вообще не влияют на продолжительность жизни, и продолжающиеся исследования пытаются найти лекарства и методы лечения, чтобы замедлить мышечную слабость.[2]
История
В 1860-х годах описания мальчиков, которые становились все слабее, утратили способность ходить и умерли в раннем возрасте, стали более заметными в медицинских журналах. В следующее десятилетие[36] Французский невролог Гийом Дюшенн дал исчерпывающий отчет о наиболее распространенной и тяжелой форме болезни, которая теперь носит его имя - Дюшенн MD.[37]
Исследование
Всемирная организация здравоохранения провела испытания оптимальной схемы приема стероидов для лечения MD в Великобритании в 2012 году.[38] Что касается исследований в Соединенных Штатах, то основные финансируемые из федерального бюджета организации, которые занимаются исследованиями мышечной дистрофии, включая генную терапию и регенеративная медицина, являются Национальный институт неврологических расстройств и инсульта, Национальный институт артрита, скелетно-мышечных и кожных заболеваний, и Национальный институт детского здоровья и развития человека.[12]
В 1966 г. Ассоциация мышечной дистрофии начал свой ежегодный Джерри Льюис MDA Telethon, который, вероятно, сделал больше для повышения осведомленности о мышечной дистрофии, чем любое другое мероприятие или инициатива. Однако защитники прав инвалидов критиковали телемарафон за изображение жертв болезни как заслуживающих скорее жалости, чем уважения.[39]
18 декабря 2001 г. Закон о MD CARE был подписан закон в США; это исправляет Закон об общественном здравоохранении провести исследования различных мышечных дистрофий. Этот закон также установил Координационный комитет по мышечной дистрофии чтобы помочь сосредоточить исследовательские усилия с помощью последовательной исследовательской стратегии.[40][41]
Смотрите также
Рекомендации
- ^ а б c d е ж грамм час я j k л м п "Информационная страница NINDS о мышечной дистрофии". NINDS. 4 марта 2016 г. Архивировано с оригинал 30 июля 2016 г.. Получено 12 сентября 2016.
- ^ а б c d е ж грамм час я j k л м п о п q р s «Мышечная дистрофия: надежда благодаря исследованиям». NINDS. 4 марта 2016 г. Архивировано с оригинал 30 сентября 2016 г.. Получено 12 сентября 2016.
- ^ Клиническая картина мышечной дистрофии в eMedicine
- ^ Выбор, NHS. «Мышечная дистрофия - Причины - Выбор NHS». www.nhs.uk. В архиве из оригинала от 02.04.2016. Получено 2016-04-10.
- ^ Гриффитс, Энтони Дж. Ф.; Миллер, Джеффри Х .; Судзуки, Дэвид Т .; Левонтин, Ричард С .; Гелбарт, Уильям М. (2000). Спонтанные мутации.[страница нужна ]
- ^ «Ген DMD». Домашний справочник по генетике. 2016-03-28. В архиве из оригинала от 16.04.2016. Получено 2016-04-10.
- ^ Лапидос, Карен А .; Каккар, Рахул; МакНелли, Элизабет М. (30 апреля 2004 г.). «Дистрофин-гликопротеиновый комплекс». Циркуляционные исследования. 94 (8): 1023–1031. Дои:10.1161 / 01.RES.0000126574.61061.25. PMID 15117830.
- ^ Шарма, Анкуш (2014). «Публикация: Жесткость и гибкость сетей белок-белкового взаимодействия: тематическое исследование нервно-мышечных расстройств». www.openaire.eu. В архиве из оригинала 22 апреля 2016 г.. Получено 10 апреля 2016.
- ^ "NIH / Как диагностируется мышечная дистрофия?". NIH.gov. НАЦИОНАЛЬНЫЕ ИНСТИТУТЫ ЗДРАВООХРАНЕНИЯ США. 2015 г. В архиве из оригинала 7 апреля 2016 г.. Получено 10 апреля 2016.
- ^ «Диагностика мышечной дистрофии». NHS Choices. NHS.uk. 2015 г. В архиве из оригинала 19 апреля 2016 г.. Получено 10 апреля 2016.
- ^ Дэни, Антуан; Барб, Корали; Рапин, Амандин; Ревейер, Кристиан; Хардуэн, Жан-Бенуа; Морроне, Изабелла; Волак-Тьерри, Аврора; Драме, Мустафа; Кальмус, Арно; Саккони, Сабрина; Бассез, Гийом; Тиффро, Винсент; Ричард, Изабель; Галле, Бенджамин; Приджент, Элен; Тайар, Редха; Веселый, Дэмиен; Новелла, Жан-Люк; Бойер, Франсуа Констан (4 июля 2015 г.). «Составление опросника качества жизни для медленно прогрессирующих нервно-мышечных заболеваний». Исследование качества жизни. 24 (11): 2615–2623. Дои:10.1007 / s11136-015-1013-8. PMID 26141500. S2CID 25834947.
- ^ а б c d е ж грамм час я Отчет Конгрессу за май 2006 г. В архиве 2014-04-05 в Wayback Machine по реализации Закон о MD CARE, как представлено Министерством здравоохранения и социальных служб Национальные институты здоровья
- ^ «Мышечная дистрофия Беккера: Медицинская энциклопедия MedlinePlus». medlineplus.gov. В архиве из оригинала 15 марта 2017 г.. Получено 14 марта 2017.
- ^ Врожденная мышечная дистрофия ~ клинические в eMedicine
- ^ а б «Мышечная дистрофия Дюшенна: Медицинская энциклопедия MedlinePlus». medlineplus.gov. В архиве из оригинала на 2017-04-05. Получено 2017-03-14.
- ^ «Мышечная дистрофия Дюшенна и Беккера - Домашний справочник по генетике». Ghr.nlm.nih.gov. 2017-03-07. В архиве из оригинала от 24.03.2017. Получено 2017-03-14.
- ^ «Мышечная дистрофия Дюшенна. Что такое мышечная дистрофия? | Пациент». Patient.info. 2016-04-15. В архиве из оригинала от 02.12.2016. Получено 2017-03-14.
- ^ Удд, Бьярне (2011). «Дистальные мышечные дистрофии». Справочник по клинической неврологии. 101. С. 239–62. Дои:10.1016 / B978-0-08-045031-5.00016-5. ISBN 978-0-08-045031-5. PMID 21496636.
- ^ "OMIM Entry - # 310300 - МЫШЕЧНАЯ ДИСТРОФИЯ EMERYDREIFUSS 1, X-LINKED; EDMD1". Omim.org. Архивировано из оригинал на 2017-03-10. Получено 2017-03-14.
- ^ «Мышечная дистрофия Эмери-Дрейфуса - Домашний справочник по генетике». Ghr.nlm.nih.gov. 2017-03-07. В архиве из оригинала на 2017-03-12. Получено 2017-03-14.
- ^ Мышечная дистрофия Эмери – Дрейфуса в eMedicine
- ^ "Facioscapulohumeral мышечная дистрофия - Genetics Home Reference". Ghr.nlm.nih.gov. В архиве из оригинала от 24.03.2017. Получено 2017-03-14.
- ^ а б c d Statland, JM; Тавил, Р. (декабрь 2016 г.). «Фациоскапуло-плечевая мышечная дистрофия». Continuum (Миннеаполис, Миннесота). 22 (6, Заболевания мышц и нервно-мышечного соединения): 1916–1931. Дои:10.1212 / CON.0000000000000399. ЧВК 5898965. PMID 27922500.
- ^ «Фациоскапуло-плечевая мышечная дистрофия: Медицинская энциклопедия MedlinePlus». Nlm.nih.gov. 2017-03-09. В архиве из оригинала на 2016-07-04. Получено 2017-03-14.
- ^ Розенберг, Роджер Н .; Паскуаль, Хуан М. (28 октября 2014 г.). Молекулярно-генетические основы неврологических и психических заболеваний Розенберга. п. 1174. ISBN 978-0124105492. В архиве из оригинала от 15.03.2017. Получено 2017-03-14.
- ^ Pegoraro, E; Хоффман, EP; Адам, депутат; Ardinger, HH; Пагон, РА; Уоллес, ЮВ; Бин, LJH; Стивенс, К; Амемия, А (2012). «Обзор мышечной дистрофии конечностей и пояса». PMID 20301582. Цитировать журнал требует
| журнал =(помощь) - ^ Дженкинс, Саймон П.Р. (2005). Справочник по спортивной науке: I - Z. Брентвуд, Эссекс: Multi-Science Publ. Co. p. 121. ISBN 978-0906522-37-0.
- ^ Тернер, С .; Хилтон-Джонс, Д. (2010). «Миотонические дистрофии: диагностика и лечение» (PDF). Журнал неврологии, нейрохирургии и психиатрии. 81 (4): 358–67. Дои:10.1136 / jnnp.2008.158261. PMID 20176601. S2CID 2453622.
- ^ «Миотоническая дистрофия 1 типа». Миотоническая дистрофия 1 типа - GeneReviews® - Книжная полка NCBI. Ncbi.nlm.nih.gov. Вашингтонский университет, Сиэтл. 1993 г. В архиве из оригинала от 18.01.2017. Получено 2017-03-14.
- ^ а б «Какие методы лечения мышечной дистрофии?». NIH.gov. НАЦИОНАЛЬНЫЕ ИНСТИТУТЫ ЗДРАВООХРАНЕНИЯ США. 2015 г. В архиве из оригинала 7 апреля 2016 г.. Получено 10 апреля 2016.
- ^ «Мышечная дистрофия-ОртоИнфо - AAOS». orthoinfo.aaos.org. В архиве из оригинала на 2016-04-12. Получено 2016-04-10.
- ^ McAdam, Laura C .; Мэйо, Аманда Л .; Алман, Бенджамин А .; Биггар, У. Дуглас (2012). «Канадский опыт длительного лечения дефлазакортом при мышечной дистрофии Дюшенна». Acta Myologica. 31 (1): 16–20. ЧВК 3440807. PMID 22655512.
- ^ Верхаерт, Дэвид; Ричардс, Кэтрин; Рафаэль-Фортни, Джилл А .; Раман, Субха В. (январь 2011 г.). «Поражение сердца у пациентов с мышечными дистрофиями». Циркуляция: сердечно-сосудистая визуализация. 4 (1): 67–76. Дои:10.1161 / CIRCIMAGING.110.960740. ЧВК 3057042. PMID 21245364.
- ^ Эдди, Линда Л. (2013). Забота о детях с особыми потребностями в медицинской помощи и их семьях: справочник для медицинских работников. Джон Вили и сыновья. ISBN 978-1-118-51797-0.[страница нужна ]
- ^ Lehman, R.M .; Маккормак, Г. Л. (2001). «Нейрогенная и миопатическая дисфункция». В Педретти - Лоррейн Уильямс; Рано, Мэри Бет (ред.). Трудотерапия: практические навыки при физической дисфункции (5-е изд.). Мосби. С. 802–3. ISBN 978-0-323-00765-8.
- ^ Лэйнг, Найджел Джи; Дэвис, Марк Р; Бейли, Клер; Флетчер, Сью; Уилтон, Стив Д. (2011). «Молекулярная диагностика мышечной дистрофии Дюшенна: прошлое, настоящее и будущее в отношении применения методов лечения». Обзоры клинических биохимиков. 32 (3): 129–134. ЧВК 3157948. PMID 21912442.
- ^ «Мышечная дистрофия: надежда благодаря исследованиям». Национальный институт неврологических расстройств и инсульта. 23 марта 2020 г.. Получено 7 апреля 2020.
- ^ Выбор, Н. Х. С. (2011-11-09). «Мышечная дистрофия - Детали клинических испытаний - Выбор NHS». В архиве из оригинала от 21.04.2016. Получено 2016-04-10.
- ^ Берман, Ари (2011-09-02). «Конец телемарафона Джерри Льюиса - самое время». Нация. Получено 2017-03-14.
- ^ HR 717--107-й Конгресс (2001) В архиве 2012-02-19 в Wayback Machine: MD-CARE Act, GovTrack.us (база данных федерального законодательства), (по состоянию на 29 июля 2007 г.)
- ^ Публичное право 107-84 В архиве 2012-11-07 в Wayback Machine, PDF, полученный из Национальные институты здравоохранения США интернет сайт
дальнейшее чтение
- Де Лос-Анджелес Бейтия, Мария; Врай, Джулия; Киршнер, Янбернд (2012). «Медикаментозное лечение мышечной дистрофии Дюшенна: имеющиеся данные и перспективы». Acta Myologica. 31 (1): 4–8. ЧВК 3440798. PMID 22655510.
- Бертини, Энрико; Д'Амико, Адель; Гуаланди, Франческа; Петрини, Стефания (декабрь 2011 г.). «Врожденные мышечные дистрофии: краткий обзор». Семинары по детской неврологии. 18 (4): 277–288. Дои:10.1016 / j.spen.2011.10.010. ЧВК 3332154. PMID 22172424.
внешняя ссылка
| Классификация | |
|---|---|
| Внешние ресурсы |
| Scholia имеет тема профиль для Мышечная дистрофия. |