Атрофический гастрит - Atrophic gastritis
| Атрофический гастрит | |
|---|---|
| Другие имена | Гастрит типа А или типа В[1] |
 | |
| Атрофический гастрит | |
| Специальность | Гастроэнтерология |
Атрофический гастрит это процесс хронического воспаление из слизистая желудка из желудок, что приводит к потере железистые клетки желудка и их возможное замещение кишечными и фиброзными тканями. В результате секреция желудком необходимых веществ, таких как соляная кислота, пепсин, и внутренний фактор нарушен, что приводит к пищеварительный проблемы. Наиболее распространены витамин B12 недостаток что приводит к мегалобластная анемия и нарушение всасывания железа, что приводит к железодефицитная анемия.[2] Это может быть вызвано стойким заражением Helicobacter pylori, или может быть аутоиммунный по происхождению. Те, у кого аутоиммунная версия атрофического гастрита, статистически более склонны к развитию. рак желудка, Тиреоидит Хашимото, и ахлоргидрия.
Гастрит типа А в первую очередь поражает тело / дно желудка и чаще встречается при злокачественной анемии.[1]Гастрит типа B в первую очередь поражает антрум, и чаще встречается с Хеликобактер пилори инфекция.[1]
Признаки и симптомы
У некоторых людей атрофический гастрит может протекать бессимптомно. При этом пациенты с симптомами - в основном женщины, а признаки атрофического гастрита связаны с дефицитом железа: усталость, синдром беспокойных ног, ломкость ногтей, выпадение волос, нарушение иммунной функции и нарушение заживления ран.[3] А другие симптомы, такие как задержка опорожнения желудка (80%), симптомы рефлюкса (25%), периферическая невропатия (25% случаев), вегетативные аномалии и потеря памяти, встречаются реже и встречаются в 1–2% случаев. Сообщается также о других психических расстройствах, таких как мания, депрессия, обсессивно-компульсивное расстройство, психоз и когнитивные нарушения. [4]
Сопутствующие условия
Люди с атрофическим гастритом также подвержены повышенному риску развития аденокарциномы желудка.[5]
Причины
Недавние исследования показали, что аутоиммунный метапластический атрофический гастрит (AMAG) является результатом атаки иммунной системы на париетальные клетки.[6]
Экологический метапластический атрофический гастрит (EMAG) возникает из-за факторов окружающей среды, таких как диета и Хеликобактер пилори инфекция. EMAG обычно ограничивается телом желудка. Пациенты с ЭМАГ также подвержены повышенному риску рака желудка.[нужна цитата ]
Патофизиология
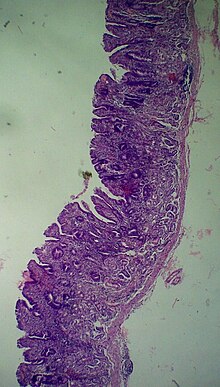
Аутоиммунный метапластический атрофический гастрит (AMAG) - это наследственная форма атрофического гастрита, характеризующаяся иммунным ответом, направленным на париетальные клетки и внутренний фактор.[6] Характерным признаком является наличие сывороточных антител к париетальным клеткам и внутреннему фактору. Аутоиммунный ответ впоследствии приводит к разрушению париетальных клеток, что приводит к глубокому Ахлоргидрия (и повышенный гастрин уровней). Недостаточное производство внутреннего фактора также приводит к выработке витамина B12 мальабсорбция и злокачественная анемия. AMAG обычно ограничивается телом желудка и дном.[нужна цитата ]
Ахлоргидрия вызывает G клетка (продуцирующая гастрин) гиперплазия, которая приводит к гипергастринемии. Гастрин оказывает трофический эффект на энтерохромаффиноподобные клетки (клетки ECL отвечают за гистамин секреция) и предполагается, что это один из механизмов, объясняющих злокачественную трансформацию клеток ECL в карциноид опухоли в AMAG.[нужна цитата ]
Диагностика
Обнаружение APCA, антитело против внутреннего фактора (AIFA) и Helicobacter pylori (HP) антитела в сочетании с сывороточный гастрин эффективны в диагностических целях.[7]
Классификация
Представление о том, что атрофический гастрит можно классифицировать в зависимости от уровня развития как «закрытый тип» или «открытый тип», было предложено в ранних исследованиях.[8] но по состоянию на 2017 год общепринятой классификации не существует.[7]
лечение
Добавление фолиевой кислоты пациентам с дефицитом может улучшить гистопатологические данные хронического атрофического гастрита и снизить частоту рака желудка.[9]
Смотрите также
использованная литература
- ^ а б c Блазер MJ (май 1988 г.). «Гастрит типа B, старение и Campylobacter pylori». Arch. Междунар. Med. 148 (5): 1021–2. Дои:10.1001 / archinte.1988.00380050027005. ISSN 0003-9926. PMID 3365072.
- ^ Аннибале Б., Капурсо Г., Ланер Е., Пасси С., Риччи Р., Маджио Ф, Делле Фаве Г. (апрель 2003 г.). «Сопутствующие изменения внутрижелудочного рН и концентрации аскорбиновой кислоты у пациентов с гастритом Helicobacter pylori и связанной с ним железодефицитной анемией». Кишечник. 52 (4): 496–501. Дои:10.1136 / гут.52.4.496. ISSN 0017-5749. ЧВК 1773597. PMID 12631657.
- ^ Стефани Кульнигг-Дабш (2016). «Аутоиммунный гастрит». Wien Med Wochenschr. 166 (13–14): 424–430. Дои:10.1007 / s10354-016-0515-5. ЧВК 5065578. PMID 27671008.CS1 maint: использует параметр авторов (ссылка на сайт)
- ^ Сара Массирони, Алессандра Зилли, Алессандра Эльвеви, Пьетро Инверницци (2019). «Меняющееся лицо хронического аутоиммунного атрофического гастрита: обновленная всеобъемлющая перспектива». Аутоиммунный. Rev. 18 (3): 215–222. Дои:10.1016 / j.autrev.2018.08.011. PMID 30639639.CS1 maint: использует параметр авторов (ссылка на сайт)
- ^ Гианнакис М., Чен С.Л., Карам С.М., Энгстранд Л., Гордон Дж. И. (март 2008 г.). «Эволюция Helicobacter pylori при прогрессировании от хронического атрофического гастрита до рака желудка и ее влияние на стволовые клетки желудка». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 105 (11): 4358–63. Bibcode:2008PNAS..105.4358G. Дои:10.1073 / pnas.0800668105. ЧВК 2393758. PMID 18332421.
- ^ а б Нимиш Вакил, доктор медицинских наук, адъюнкт-профессор кафедры медицины и общественного здравоохранения Университета Мэдисона. "Аутоиммунный метапластический атрофический гастрит: гастрит и пептическая язва: руководство Merck Professional". Профессиональная версия руководства MSD. Merck & Co.
- ^ а б Миналян А., Бенхамму Дж. Н., Арташесян А., Льюис М. С., Писенья Дж. Р. (2017). «Аутоиммунный атрофический гастрит: современные перспективы». Клин Эксп Гастроэнтерол. 10: 19–27. Дои:10.2147 / CEG.S109123. ЧВК 5304992. PMID 28223833.
- ^ Kimura, K .; Такемото, Т. (2008). «Эндоскопическое распознавание атрофической границы и ее значение при хроническом гастрите». Эндоскопия. 1 (3): 87–97. Дои:10.1055 / с-0028-1098086. ISSN 0013-726X.
- ^ Fang JY, Du YQ, Liu WZ, Ren JL, Li YQ, Chen XY, Lv NH, Chen YX, Lv B; Китайское общество гастроэнтерологов, Китайская медицинская ассоциация (2018). «Китайский консенсус по хроническому гастриту (2017, Шанхай)». J Dig Dis. 19 (4): 182–203. Дои:10.1111/1751-2980.12593. PMID 29573173.CS1 maint: использует параметр авторов (ссылка на сайт)
внешние ссылки
| Классификация | |
|---|---|
| Внешние ресурсы |
