Т-клетка - T cell
| Т-лимфоцитячейка | |
|---|---|
 Сканирующая электронная микрофотография Т-клетки человека | |
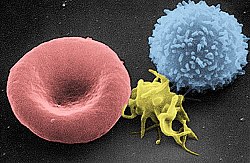 Сканирующая электронная микрофотография Красная кровяная клетка (слева), а тромбоцит (в центре) и Т-лимфоцит (справа) | |
| подробности | |
| Система | Иммунная система |
| Идентификаторы | |
| латинский | лимфоцит Т |
| MeSH | D013601 |
| TH | H2.00.04.1.02007 |
| FMA | 62870 |
| Анатомические термины микроанатомии | |

А Т-клетка это тип лимфоцит. Т-клетка происходит от гемопоэтические стволовые клетки,[1] которые находятся в костном мозге; однако Т-лимфоциты созревают в вилочковая железа железа (отсюда и название) и играет центральную роль в иммунная реакция. Т-клетки можно отличить от других лимфоцитов по наличию Рецептор Т-клеток на поверхность клетки. Эти иммунные клетки возникают как клетки-предшественники, полученный из Костный мозг,[2] и после миграции в вилочковую железу развиваются в несколько различных типов Т-клеток. Дифференцировка Т-клеток продолжается даже после того, как они покинули вилочковую железу.
Группы специфических дифференцированных Т-клеток играют важную роль в контроле и формировании иммунного ответа, обеспечивая множество функций, связанных с иммунитетом. Одна из этих функций - иммуноопосредованная гибель клеток, и она осуществляется Т-клетками несколькими способами: CD8 + Т-клетки, также известные как «клетки-киллеры», цитотоксический - это означает, что они могут напрямую убивать инфицированные вирусом клетки, а также раковые клетки. CD8 + Т-клетки также способны использовать небольшие сигнальные белки, известные как цитокины, чтобы привлечь другие клетки при создании иммунного ответа. Другая популяция Т-клеток, CD4 + Т-клетки, функционируют как «клетки-помощники». В отличие от Т-киллеров CD8 +, эти Т-хелперы CD4 + функционируют, косвенно убивая клетки, идентифицированные как чужеродные: они определяют, реагируют ли и как другие части иммунной системы на конкретную предполагаемую угрозу. Хелперные Т-клетки также используют передачу сигналов цитокинов, чтобы влиять на регуляторные В-клетки прямо, а другие клеточные популяции косвенно. Регуляторные Т-клетки являются еще одной особой популяцией этих клеток, которые обеспечивают критический механизм толерантность, посредством чего иммунные клетки способны отличать вторгшиеся клетки от «себя», тем самым предотвращая ненадлежащую выработку иммунными клетками ответа против самого себя (что по определению будет «аутоиммунный По этой причине эти регуляторные Т-клетки также называют «супрессорными» Т-клетками. Эти же самотолерантные клетки кооптируются раковыми клетками, чтобы предотвратить распознавание и иммунный ответ против опухолевых клеток.
Разработка
Происхождение, раннее развитие и миграция в тимус
Все Т-клетки происходят из c-kit+Sca1+ гемопоэтические стволовые клетки (HSC), которые находятся в костном мозге. В некоторых случаях причиной может быть печень плода во время эмбрионального развития. Затем HSC дифференцируются в мультипотентные предшественники (MPP), которые сохраняют потенциал превращаться как в миелоидные, так и лимфоидные клетки. Затем процесс дифференцировки переходит к общему лимфоидному предшественнику (CLP), который может дифференцироваться только в T, B или NK-клетки.[3] Эти клетки CLP затем мигрируют через кровь в тимус, где они приживаются. Самые ранние клетки, попавшие в вилочковую железу, называются дважды отрицательными, поскольку они не экспрессируют ни CD4 ни CD8 ко-рецептор. Новоприбывшие клетки CLP - это CD4.−CD8−CD44+CD25−ckit+ клетки и называются ранними клетками-предшественниками тимуса (ETP).[4] Эти клетки затем подвергаются циклу деления и подавляют c-kit и называются клетками DN1.
Выбор TCR-Beta
На этапе DN2 (CD44+CD25+), клетки активируют гены рекомбинации RAG1 и RAG2 и перестраивают локус TCRβ, объединяя V-D-J и гены константной области в попытке создать функциональную цепь TCRβ. По мере того, как развивающийся тимоцит достигает стадии DN3 (CD44−CD25+), Т-клетка вместе с геном TCRβ экспрессирует инвариантную α-цепь, называемую pre-Tα. Если перестроенная β-цепь успешно соединяется с инвариантной α-цепью, возникают сигналы, которые прекращают перестройку β-цепи (и заглушают альтернативный аллель).[5] Хотя эти сигналы требуют наличия этого пре-TCR на поверхности клетки, они не зависят от связывания лиганда с пре-TCR. Если формируется пре-TCR, то эта клетка подавляет CD25 и называется клеткой DN4 (CD25−CD44−). Затем эти клетки подвергаются раунду пролиферации и начинают перестраивать локус TCRα.
Положительный выбор
Двойной положительный тимоциты (CD4+/ CD8+) мигрируют глубоко в тимус кора, где они представленыантигены. Эти аутоантигены экспрессируются эпителиальными клетками коры тимуса на MHC молекулы на поверхности корковых эпителиальных клеток. Только те тимоциты, которые взаимодействуют с MHC-I или MHC-II, получат жизненно важный «сигнал выживания». Все, что не может (если они не взаимодействуют достаточно сильно), умрет «смертью из-за пренебрежения» (без сигнала выживания). Этот процесс гарантирует, что выбранные Т-клетки будут обладать аффинностью MHC, которая может выполнять полезные функции в организме (т.е. клетки должны иметь возможность взаимодействовать с MHC и пептидными комплексами, чтобы вызывать иммунные ответы). Подавляющее большинство развивающихся тимоцитов погибнет во время этого процесса. Процесс положительного отбора занимает несколько дней.[6]
Судьба тимоцита определяется во время положительного отбора. Двойные положительные клетки (CD4+/ CD8+), которые хорошо взаимодействуют с молекулами MHC класса II, в конечном итоге станут CD4+ клетки, тогда как тимоциты, которые хорошо взаимодействуют с молекулами MHC класса I, созревают в CD8+ клетки. Т-клетка становится CD4+ клетка путем подавления экспрессии ее рецепторов на поверхности клетки CD8. Если клетка не потеряет свой сигнал, она продолжит подавлять CD8 и станет CD4.+, одиночная положительная ячейка.[7]
Этот процесс не удаляет тимоциты, которые могут вызвать аутоиммунитет. Потенциально аутоиммунные клетки удаляются в процессе отрицательного отбора, который происходит в мозговом веществе тимуса (обсуждается ниже).
Отрицательный выбор
Отрицательный отбор удаляет тимоциты, которые способны прочно связываться с «собственными» пептидами MHC. Тимоциты, пережившие положительный отбор, мигрируют к границе коры и мозгового вещества в тимусе. Находясь в мозговом веществе, они снова представлены аутоантигеном, представленным на комплексе МНС медуллярных эпителиальных клеток тимуса (mTECs).[8] mTEC должны быть AIRE+ для правильной экспрессии аутоантигенов из всех тканей тела на своих пептидах MHC класса I. Некоторые mTEC фагоцитируются дендритными клетками тимуса; это позволяет представлять аутоантигены на молекулах MHC класса II (положительно выбранные CD4+ клетки должны взаимодействовать с молекулами MHC класса II, таким образом, APC, которые обладают MHC класса II, должны присутствовать для CD4+ Отрицательный отбор Т-клеток). Тимоциты, которые слишком сильно взаимодействуют с аутоантигеном, получают апоптотический сигнал, который приводит к гибели клеток. Однако некоторые из этих ячеек выбраны, чтобы стать Трег клетки. Оставшиеся клетки выходят из вилочковой железы в зрелом состоянии. наивные Т-клетки (также известные как недавние эмигранты из тимуса[9]). Этот процесс является важной составляющей центральная терпимость и служит для предотвращения образования самореактивных Т-клеток, которые способны вызывать аутоиммунные заболевания у хозяина.
β-отбор - это первая контрольная точка, где Т-клетки, которые способны формировать функциональный пре-TCR с инвариантной альфа-цепью и функциональной бета-цепью, получают возможность продолжать развитие в тимусе. Затем положительный отбор проверяет, успешно ли Т-клетки перестроили свой локус TCRα и способны распознавать комплексы пептид-MHC с соответствующей аффинностью. Отрицательный отбор в мозговом веществе затем уничтожает Т-клетки, которые слишком сильно связываются с аутоантигенами, экспрессируемыми на молекулах MHC. Эти процессы отбора позволяют иммунной системе проявлять терпимость к себе. Типичные Т-клетки, которые покидают вилочковую железу (через кортикомедуллярное соединение), являются саморегулирующимися, самотолерантными и однократно положительными.
Тимический вывод
Около 98% тимоцитов умирают во время процессов развития в тимусе из-за неудач либо положительного, либо отрицательного отбора, тогда как другие 2% выживают и покидают тимус, чтобы стать зрелыми иммунокомпетентными Т-клетками. С возрастом тимус вносит меньше клеток. Поскольку вилочковая железа сокращается примерно на 3%[10] в год в среднем возрасте, соответствующее снижение производства тимуса наивные Т-клетки происходит, в результате чего расширение и регенерация периферических Т-клеток играет большую роль в защите пожилых людей.
Типы Т-лимфоцитов
Т-клетки сгруппированы в серию подмножеств в зависимости от их функции. CD4 и CD8 Т-клетки отбираются в тимусе, но подвергаются дальнейшей дифференцировке на периферии в специализированные клетки, выполняющие разные функции. Подмножества Т-клеток изначально определялись функцией, но также имели связанные паттерны экспрессии генов или белков.
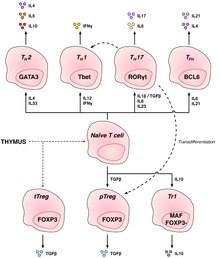
Обычные адаптивные Т-клетки
Хелперные CD4 + Т-клетки
Т-хелперные клетки (ТЧАС клетки) помогают другим лимфоцитам, включая созревание В-клетки в плазматические клетки и В-клетки памяти, и активация цитотоксические Т-клетки и макрофаги. Эти клетки также известны как CD4+ Т-клетки как они выражают CD4 на их поверхности. Т-хелперные клетки активируются, когда им предъявляют пептид антигены от MHC класс II молекулы, которые выражаются на поверхности антигенпрезентирующие клетки (БТР). После активации они быстро делятся и выделяют цитокины которые регулируют или помогают иммунному ответу. Эти клетки могут дифференцироваться в один из нескольких подтипов, которые выполняют разные роли. Цитокины направляют Т-клетки на определенные подтипы.[11]
| Тип ячейки | Цитокины производятся | Ключевой фактор транскрипции | Роль в иммунной защите | Сопутствующие заболевания |
|---|---|---|---|---|
| Чт1 | IFNγ | Tbet | Вызывают воспалительную реакцию, ключевую для защиты от внутриклеточных бактерий, вирусов и рака. | РС, диабет 1 типа |
| Чт2 | Ил-4 | ГАТА-3 | Содействовать дифференцировке и выработке антител В-клетками | Астма и другие аллергические заболевания |
| Чт17 | Ил-17 | RORγt | Защита от кишечных патогенов и слизистых оболочек | РС, ревматоидный артрит, псориаз |
| Чт9 | Ил-9 | ИРФ4, ПУ.1 | Защита от гельминтов (паразитарных червей) | Рассеянный склероз |
| Tfh | Ил-21, Ил-4 | Bcl-6 | Помогите В-клеткам вырабатывать антитела | Астма и другие аллергические заболевания |
Цитотоксические CD8 + Т-клетки
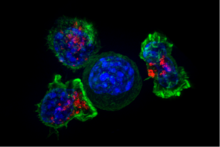
Цитотоксические Т-клетки (ТC клетки, CTL, Т-киллерные клетки, киллерные Т-клетки) разрушают инфицированные вирусом клетки и опухолевые клетки, а также участвуют в пересадить отказ. Эти клетки определяются экспрессией CD8.+ на поверхности клетки. Эти клетки распознают свои мишени путем связывания с короткими пептидами (8-11AA), связанными с MHC класс I молекулы, присутствующие на поверхности всех ядерных клеток. CD8 + Т-клетки также продуцируют ключевые цитокины IL-2 и IFNγ, которые влияют на эффекторные функции других клеток, в частности макрофагов и NK-клеток.
Т-клетки памяти
Наивные Т-клетки расширяются и дифференцируются в память и эффекторные Т-клетки после того, как они сталкиваются со своим родственным антигеном в контексте молекулы MHC на поверхности профессиональной антигенпрезентирующей клетки (например, дендритной клетки). Чтобы этот процесс происходил, во время встречи с антигеном должна присутствовать соответствующая костимуляция. Исторически считалось, что Т-клетки памяти принадлежат либо к эффекторному, либо к подтипу центральной памяти, каждый со своим собственным отличительным набором маркеров клеточной поверхности (см. Ниже).[12] Впоследствии были обнаружены многочисленные новые популяции Т-клеток памяти, включая резидентные в тканях Т-клетки памяти (Trm), стволовые клетки памяти TSCM и Т-клетки виртуальной памяти. Единая объединяющая тема для всех Т-клетка памяти подтипов заключается в том, что они являются долгоживущими и могут быстро увеличиваться до большого количества эффекторных Т-клеток при повторном воздействии на их родственный антиген. Посредством этого механизма они обеспечивают иммунную систему «памятью» против ранее встреченных патогенов. Т-клетки памяти могут быть CD4+ или CD8+ и обычно выражают CD45RO.[13]
Подтипы Т-клеток памяти:
- Т-клетки центральной памяти (ТСМ клетки) экспрессируют CD45RO, C-C хемокиновый рецептор типа 7 (CCR7) и L-селектин (CD62L). Т-клетки центральной памяти также имеют среднюю или высокую экспрессию CD44. Эта подгруппа памяти обычно встречается в лимфатический узел и в периферическом кровообращении. (Примечание. Экспрессия CD44 обычно используется для отличия наивных мышей от Т-клеток памяти).
- Эффекторные Т-клетки памяти (ТЭМ клетки и ТEMRA клетки) экспрессируют CD45RO, но не экспрессируют CCR7 и L-селектин. Они также имеют среднюю и высокую степень выраженности CD44. Эти Т-клетки памяти лишены рецепторов, возвращающих к лимфатическим узлам, и поэтому находятся в периферическом кровообращении и тканях.[14] ТEMRA означает терминально дифференцированные эффекторные клетки памяти, повторно экспрессирующие CD45RA, который является маркером, обычно обнаруживаемым на наивных Т-клетках.[15]
- Резидентные Т-клетки памяти в тканях (TRM) занимают ткани (кожу, легкие и т. д.) без рециркуляции. Один маркер клеточной поверхности, связанный с TRM внутренний αeβ7, также известный как CD103.[16]
- Т-клетки виртуальной памяти отличаются от других подмножеств памяти тем, что они не возникают после сильного события клональной экспансии. Таким образом, хотя эта популяция в целом многочисленна в периферическом кровообращении, отдельные клоны Т-клеток виртуальной памяти располагаются на относительно низких частотах. Одна из теорий состоит в том, что гомеостатическая пролиферация дает начало этой популяции Т-клеток. Хотя Т-клетки виртуальной памяти CD8 были описаны первыми,[17] теперь известно, что клетки виртуальной памяти CD4 также существуют.[18]
Регуляторные CD4 + Т-клетки
Регуляторные Т-клетки имеют решающее значение для поддержания иммунологическая толерантность. Их основная роль состоит в том, чтобы отключать опосредованный Т-клетками иммунитет к концу иммунной реакции и подавлять аутореактивные Т-клетки которые избежали процесса отрицательного отбора в тимусе.
Два основных класса CD4+ Трег описаны клетки - FOXP3+ Трег клетки и FOXP3− Трег клетки.
Регуляторные Т-клетки могут развиваться либо во время нормального развития в тимусе, и тогда они известны как Treg-клетки тимуса, либо могут индуцироваться периферически и называются Treg-клетками периферического происхождения. Эти два подмножества ранее назывались «естественным» и «адаптивным» или «индуцированным» соответственно.[19] Оба подмножества требуют выражения фактор транскрипции FOXP3 который можно использовать для идентификации ячеек. Мутации FOXP3 ген может предотвратить развитие регуляторных Т-лимфоцитов, вызывая фатальный аутоиммунное заболевание IPEX.
Некоторые другие типы Т-клеток обладают подавляющей активностью, но не экспрессируют FOXP3. К ним относятся клетки Tr1 и клетки Th3, которые, как полагают, возникают во время иммунного ответа и действуют, производя супрессивные молекулы. Клетки Tr1 связаны с IL-10, а клетки Th3 связаны с TGF-бета. Недавно, Клетки Treg17 были добавлены в этот список.[20]
Врожденные Т-клетки
Природные Т-клетки-киллеры
Природные Т-клетки-киллеры (Клетки NKT - не путать с естественные клетки-киллеры врожденной иммунной системы) адаптивная иммунная система с врожденная иммунная система. В отличие от обычных Т-клеток, которые распознают пептидные антигены, представленные главный комплекс гистосовместимости (MHC), NKT-клетки распознают гликолипидный антиген, представленный CD1d. После активации эти клетки могут выполнять функции, приписываемые как Tчас и тc клетки (то есть производство цитокинов и высвобождение цитолитических / убивающих клетки молекул). Они также способны распознавать и устранять некоторые опухолевые клетки и клетки, инфицированные вирусами герпеса.[21]
Инвариант, связанный со слизистой
Связанные со слизистой оболочкой инвариантные Т-клетки (MAIT) отображают врожденный, эффекторные качества.[22][23] У человека клетки MAIT обнаруживаются в крови, печени, легких и слизистая оболочка, защищая от микробной активности и инфекции.[22] В MHC класс I -подобный белок, MR1, отвечает за представление производимых бактериями витамин B метаболиты в клетки MAIT.[24][25][26] После презентации чужеродного антигена MR1 клетки MAIT секретируют провоспалительный цитокины и способны лизать бактериально инфицированные клетки.[22][26] Клетки MAIT также могут быть активированы посредством MR1-независимой передачи сигналов.[26] Помимо функций, подобных врожденным, это подмножество Т-клеток поддерживает адаптивный иммунный ответ и имеет фенотип, напоминающий память.[22] Кроме того, считается, что клетки MAIT играют роль в аутоиммунные заболевания, такие как рассеянный склероз, артрит и воспалительное заболевание кишечника,[27][28] хотя окончательные доказательства еще не опубликованы.[29][30][31][32]
Гамма-дельта Т-клетки
Гамма-дельта Т-клетки (γδ T-клетки) представляют собой небольшое подмножество T-клеток, которые обладают γδ TCR, а не αβ TCR на поверхности клетки. Большинство Т-клеток экспрессируют цепи αβ TCR. Эта группа Т-клеток гораздо реже встречается у людей и мышей (около 2% от общего количества Т-клеток) и обнаруживается в основном в кишечнике. слизистая оболочка, среди населения интраэпителиальные лимфоциты. У кроликов, овец и кур количество γδ Т-клеток может достигать 60% от общего количества Т-клеток. Антигенные молекулы, активирующие γδ Т-клетки, по большей части неизвестны. Однако γδ Т-клетки не ограничиваются MHC и, по-видимому, способны распознавать целые белки, а не требовать, чтобы пептиды представлялись молекулами MHC на БТР. Немного мышиный γδ Т-клетки распознают молекулы MHC класса IB. Человеческие γδ Т-клетки, которые используют фрагменты генов Vγ9 и Vδ2, составляют основную популяцию γδ Т-клеток в периферической крови и уникальны тем, что они специфично и быстро реагируют на набор непептидных фосфорилированных изопреноид предшественники, вместе названные фосфоантигены, которые производятся практически всеми живыми клетками. Наиболее распространенными фосфоантигенами из клеток животных и человека (включая раковые клетки) являются: изопентенилпирофосфат (IPP) и его изомер диметилаллил пирофосфат (ДМПП). Многие микробы производят высокоактивное соединение гидрокси-DMAPP (HMB-PP ) и соответствующие мононуклеотидные конъюгаты в дополнение к IPP и DMAPP. Клетки растений продуцируют оба типа фосфоантигенов. Лекарства, активирующие человеческие Т-клетки Vγ9 / Vδ2, включают синтетические фосфоантигены и аминобисфосфонаты, которые активируют эндогенный IPP / DMAPP.
Активация
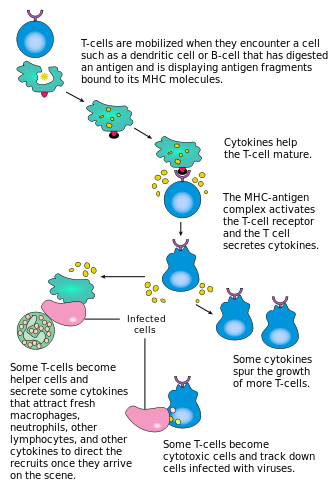
Активация CD4+ Т-клетки возникают при одновременном задействовании Рецептор Т-клеток и костимулирующая молекула (например, CD28, или ICOS ) на Т-клетку главным комплексом гистосовместимости (MHCII) пептид и костимулирующие молекулы на APC. Оба необходимы для выработки эффективного иммунного ответа; в отсутствие совместная стимуляция, Одна только передача сигналов Т-клеточного рецептора приводит к анергия. Сигнальные пути, расположенные ниже костимулирующих молекул, обычно включают PI3K путь создания PIP3 на плазматической мембране и рекрутинг Домен PH содержащие сигнальные молекулы, такие как PDK1 которые необходимы для активации PKC-θ, и в конечном итоге Ил-2 производство. Оптимальный CD8+ Ответ Т-клеток зависит от CD4+ сигнализация.[34] CD4+ клетки полезны для начальной антигенной активации наивных CD8 Т-клеток и поддержания памяти CD8+ Т-клетки после острой инфекции. Следовательно, активация CD4+ Т-клетки могут быть полезны для действия CD8+ Т-клетки.[35][36][37]
Первый сигнал обеспечивается связыванием рецептора Т-клетки с его родственным пептидом, представленным на MHCII на APC. MHCII ограничен так называемыми профессиональными антигенпрезентирующие клетки, таких как дендритные клетки, В-клетки и макрофаги, и это лишь некоторые из них. Пептиды, представленные CD8+ Т-клетки молекулами MHC класса I состоят из 8–13 аминокислот в длину; пептиды, представленные CD4+ клетки молекулами MHC класса II длиннее, обычно 12-25 аминокислот в длину,[38] поскольку концы связывающей щели молекулы MHC класса II открыты.
Второй сигнал исходит от костимуляции, при которой поверхностные рецепторы на APC индуцируются относительно небольшим количеством стимулов, обычно продуктов патогенов, но иногда продуктов распада клеток, таких как некротический -тела или белки теплового шока. Единственным костимулирующим рецептором, конститутивно экспрессируемым наивными Т-клетками, является CD28, поэтому костимуляция этих клеток происходит от CD80 и CD86 белки, которые вместе составляют B7 белок (B7.1 и B7.2 соответственно) на APC. Другие рецепторы экспрессируются при активации Т-лимфоцитов, такие как OX40 и ICOS, но их экспрессия во многом зависит от CD28. Второй сигнал позволяет Т-клетке реагировать на антиген. Без него Т-клетка становится анергический, и его активация в будущем станет труднее. Этот механизм предотвращает неадекватные реакции на себя, так как самопептиды обычно не проявляются при подходящей костимуляции. После того, как Т-клетка была соответствующим образом активирована (т.е. получила сигнал один и сигнал два), она изменяет экспрессию различных белков на своей клеточной поверхности. Маркеры активации Т-клеток включают CD69, CD71 и CD25 (также маркер для Treg-клеток) и HLA-DR (маркер активации Т-клеток человека). Экспрессия CTLA-4 также повышается на активированных Т-клетках, которые, в свою очередь, опережают CD28 за связывание с белками B7. Это механизм контрольной точки для предотвращения чрезмерной активации Т-лимфоцитов. Активированные Т-клетки также изменяют профиль гликозилирования клеточной поверхности.[39]
В Рецептор Т-клеток существует как комплекс нескольких белков. Фактический рецептор Т-клеток состоит из двух отдельных пептидных цепей, которые продуцируются независимыми рецепторами Т-клеток альфа и бета (TCRα и TCRβ) гены. Другие белки в комплексе - это CD3 белки: гетеродимеры CD3εγ и CD3εδ и, что наиболее важно, гомодимер CD3ζ, который имеет в общей сложности шесть ITAM мотивы. Мотивы ITAM на CD3ζ могут фосфорилироваться Lck и в свою очередь набирать ЗАП-70. Lck и / или ZAP-70 также могут фосфорилировать тирозины на многие другие молекулы, не в последнюю очередь на CD28, LAT и SLP-76, что позволяет агрегировать сигнальные комплексы вокруг этих белков.
Фосфорилированный LAT набирает SLP-76 на мембрану, откуда он затем может доставить PLC-γ, VAV1, Itk и потенциально PI3K. PLC-γ расщепляет PI (4,5) P2 на внутренней створке мембраны с образованием активных посредников диацилглицерин (DAG ), инозитол-1,4,5-трифосфат (IP3 ); PI3K также действует на PIP2, фосфорилируя его с образованием фосфатидлинозитол-3,4,5-трифосфата (PIP3). DAG связывает и активирует некоторые PKC. Наиболее важным в Т-клетках является PKC-θ, критически важный для активации факторов транскрипции. NF-κB и АП-1. IP3 высвобождается из мембраны PLC-γ и быстро диффундирует для активации рецепторов кальциевых каналов на ER, что вызывает высвобождение кальций в цитозоль. Низкий уровень кальция в эндоплазматическом ретикулуме вызывает кластеризацию STIM1 на мембране ER и приводит к активации каналов CRAC клеточной мембраны, что позволяет дополнительному кальцию поступать в цитозоль из внеклеточного пространства. Этот агрегированный цитозольный кальций связывает кальмодулин, который затем может активировать кальциневрин. Кальциневрин, в свою очередь, активирует NFAT, который затем перемещается в ядро. NFAT - это фактор транскрипции который активирует транскрипцию плейотропного набора генов, в первую очередь IL-2, цитокина, который способствует длительной пролиферации активированных Т-клеток.
PLC-γ также может инициировать Путь NF-κB. DAG активирует PKC-θ, который затем фосфорилирует CARMA1, заставляя его разворачиваться и функционировать как каркас. Цитозольные домены связывают адаптер BCL10 через КАРТА (Домены активации и рекрутирования каспаз) домены; это затем связывает TRAF6, который убиквитинируется по K63.:513–523[40] Эта форма убиквитинирования не приводит к деградации целевых белков. Скорее, он служит для набора NEMO, IKKα и -β и TAB1-2 / TAK1.[41] TAK 1 фосфорилирует IKK-β, который затем фосфорилирует IκB, обеспечивая убиквитинирование K48: приводит к протеасомной деградации. Rel A и p50 могут затем проникать в ядро и связывать ответный элемент NF-κB. Это в сочетании с передачей сигналов NFAT позволяет полностью активировать ген IL-2.[40]
Хотя в большинстве случаев активация зависит от распознавания антигена TCR, описаны альтернативные пути активации. Например, было показано, что цитотоксические Т-клетки активируются под действием других Т-лимфоцитов CD8, что приводит к толеризации последних.[42]
Весной 2014 г. Активация Т-клеток в космосе (TCAS) был запущен эксперимент Международная космическая станция на SpaceX CRS-3 Миссия по изучению того, как «на недостатки иммунной системы человека влияет микрогравитация».[43]
Активация Т-клеток модулируется активные формы кислорода.[44]
Дискриминация антигена
Уникальной особенностью Т-клеток является их способность различать здоровые и аномальные (например, инфицированные или раковые) клетки в организме.[45] Здоровые клетки обычно экспрессируют большое количество собственных pMHC на своей клеточной поверхности, и хотя рецептор Т-клеточного антигена может взаимодействовать по крайней мере с подмножеством этих собственных pMHC, Т-клетка обычно игнорирует эти здоровые клетки. Однако, когда эти же самые клетки содержат даже незначительные количества pMHC, происходящего от патогена, Т-клетки могут активироваться и инициировать иммунные ответы. Способность Т-клеток игнорировать здоровые клетки, но реагировать, когда эти же клетки содержат pMHC, полученную от патогена (или рака), известна как дискриминация антигена. Молекулярные механизмы, лежащие в основе этого процесса, противоречивы.[45][46]
Клиническое значение
Дефицит
Причины Дефицит Т-клеток включают лимфоцитопения Т-клеток и / или дефекты функции отдельных Т-клеток. Полная недостаточность функции Т-лимфоцитов может быть результатом: наследственные условия такие как тяжелый комбинированный иммунодефицит (SCID), Синдром Оменна, и гипоплазия волос и хрящей.[47] Причины частичной недостаточности функции Т-лимфоцитов включают: синдром приобретенного иммунодефицита (СПИД) и наследственные заболевания, такие как Синдром ДиДжорджи (DGS), синдромы хромосомного разрыва (CBS) и комбинированные нарушения В-клеток и Т-клеток, такие как атаксия-телеангиэктазия (AT) и Синдром Вискотта – Олдрича (БЫЛ).[47]
Основными патогенами, вызывающими дефицит Т-клеток, являются: внутриклеточные патогены, в том числе Вирус простого герпеса, Микобактерии и Листерия.[48] Также, грибковая инфекция также более распространены и тяжелы при дефиците Т-клеток.[48]
Рак
Рак Т-лимфоцитов называется Т-клеточная лимфома, и составляет примерно один из десяти случаев неходжкинская лимфома.[49] Основными формами Т-клеточной лимфомы являются:
- Экстранодальная Т-клеточная лимфома
- Кожные Т-клеточные лимфомы: Синдром Сезари и Грибовидный микоз
- Анапластическая крупноклеточная лимфома
- Ангиоиммунобластная Т-клеточная лимфома
Истощение
Истощение Т-клеток - это состояние дисфункциональных Т-клеток. Он характеризуется прогрессирующей потерей функции, изменениями транскрипционных профилей и устойчивой экспрессией ингибирующих рецепторов. Сначала клетки теряют способность производить Ил-2 и TNFα с последующей потерей высокой пролиферативной способности и цитотоксического потенциала, что в конечном итоге приводит к их делеции. Истощенные Т-клетки обычно указывают на более высокий уровень CD43, CD69 и ингибирующие рецепторы в сочетании с более низкой экспрессией CD62L и CD127. Истощение может развиться при хронических инфекциях, сепсисе и раке.[50] Истощенные Т-клетки сохраняют свое функциональное истощение даже после многократного воздействия антигена.[51]
При хронической инфекции и сепсисе
Истощение Т-лимфоцитов может быть вызвано несколькими факторами, такими как постоянное воздействие антигена и отсутствие помощи Т-лимфоцитов CD4.[52] Воздействие антигена также влияет на течение истощения, поскольку более длительное время воздействия и более высокая вирусная нагрузка увеличивают серьезность истощения Т-клеток. Для установления истощения необходимо воздействие как минимум 2–4 недели.[53] Еще одним фактором, способным вызвать истощение, являются тормозные рецепторы, включая белок запрограммированной гибели клеток 1 (PD1), CTLA-4, Белок-3 Т-клеточной мембраны (TIM3) и белок гена активации лимфоцитов 3 (LAG3).[54][55] Растворимые молекулы, такие как цитокины Ил-10 или TGF-β также могут вызвать истощение.[56][57] Последними известными факторами, которые могут играть роль в истощении Т-клеток, являются регуляторные клетки. Трег клетки могут быть источником IL-10 и TGF-β, и поэтому они могут играть роль в истощении Т-клеток.[58] Более того, истощение Т-лимфоцитов восстанавливается после истощения Т-рег-клеток и блокады PD1.[59] Истощение Т-лимфоцитов также может произойти при сепсисе в результате цитокинового шторма. Позже, после первоначального заражения, противовоспалительные цитокины и проапоптотические белки вступают во владение, чтобы защитить организм от повреждений. Сепсис также несет в себе высокую антигенную нагрузку и воспаление. На этой стадии сепсиса истощение Т-лимфоцитов увеличивается.[60][61] В настоящее время проводятся исследования, направленные на использование блокад ингибиторных рецепторов при лечении сепсиса.[62][63][64]
Во время трансплантации
В то время как во время инфекции истощение Т-клеток может развиваться после стойкого воздействия антигена после трансплантации трансплантата, аналогичная ситуация возникает с присутствием аллоантигена.[65] Было показано, что ответ Т-клеток снижается со временем после трансплантации почки.[66] Эти данные предполагают, что истощение Т-клеток играет важную роль в толерантности трансплантата, главным образом за счет истощения аллореактивных Т-лимфоцитов CD8.[61][67] Несколько исследований показали положительное влияние хронической инфекции на прием трансплантата и его долгосрочное выживание, частично опосредованное истощением Т-клеток.[68][69][70] Также было показано, что истощение Т-клеток реципиента обеспечивает достаточные условия для NK клетка перевод.[71] Хотя есть данные, показывающие, что индукция истощения Т-клеток может быть полезной для трансплантации, она также имеет недостатки, среди которых можно отметить повышенное количество инфекций и риск развития опухоли.[72]
Во время рака
Во время рака истощение Т-клеток играет роль в защите опухоли. Согласно исследованиям, некоторые связанные с раком клетки, а также сами опухолевые клетки могут активно вызывать истощение Т-клеток в месте опухоли.[73][74][75] Истощение Т-клеток также может играть роль в рецидивах рака, как было показано на лейкемии.[76] Некоторые исследования даже предположили, что можно предсказать рецидив лейкемии на основе экспрессии Т-клетками ингибирующих рецепторов PD-1 и TIM-3.[77] В последние годы было проведено множество экспериментов и клинических испытаний блокаторов иммунных контрольных точек в терапии рака. Некоторые из них были одобрены как действующие методы лечения и теперь используются в клиниках.[78] Тормозящие рецепторы, на которые нацелены эти медицинские процедуры, жизненно важны для истощения Т-клеток, и их блокирование может обратить эти изменения вспять.[79]
Смотрите также
- Химерные антигенные рецепторы Т-клетки
- Специфическое для кишечника самонаведение
- Иммунобласт
- Иммунное старение
использованная литература
- ^ "5. Гематопоэтические стволовые клетки | stemcells.nih.gov". stemcells.nih.gov. Получено 2020-11-21.
- ^ Альбертс Б., Джонсон А., Льюис Дж., Рафф М., Робертс К., Уолтер П. (2002) Молекулярная биология клетки. Garland Science: New York, NY pg 1367. «Т-клетки и В-клетки получили свои названия от органов, в которых они развиваются. Т-клетки развиваются [созревают] в тимусе, а В-клетки у млекопитающих развиваются [созревают] в тимусе. костный мозг у взрослых или печень у плода ».
- ^ Кондо, Мотонари (декабрь 2016 г.). «Единая ниша для управления как поддержанием, так и потерей ствола в HSC». Иммунитет. 45 (6): 1177–1179. Дои:10.1016 / j.immuni.2016.12.003. PMID 28002722.
- ^ Осборн, Лиза С .; Дханджи, Салим; Сноу, Джонатан В .; Приатель, Джон Дж .; Ma, Melissa C .; Горняки, М. Джилл; Тех, Хунг-Сиа; Goldsmith, Mark A .; Авраам, Нинан (19 марта 2007 г.). «Нарушение памяти Т-лимфоцитов CD8 и первичные ответы Т-лимфоцитов CD4 у мышей с мутантным IL-7Rα». Журнал экспериментальной медицины. 204 (3): 619–631. Дои:10.1084 / jem.20061871. ЧВК 2137912. PMID 17325202.
- ^ Джейнвей, Чарльз (2012). Иммунобиология. Наука о гирляндах. С. 301–305. ISBN 9780815342434.
- ^ Старр Т.К., Джеймсон СК, Хогквист К.А. (01.01.2003). «Положительный и отрицательный отбор Т-клеток». Ежегодный обзор иммунологии. 21 (1): 139–176. Дои:10.1146 / annurev.immunol.21.120601.141107. PMID 12414722.
- ^ Zerrahn J, Held W., Raulet DH (март 1997 г.). «Реактивность MHC репертуара Т-клеток до положительного и отрицательного отбора». Ячейка. 88 (5): 627–636. Дои:10.1016 / S0092-8674 (00) 81905-4. PMID 9054502.
- ^ Hinterberger M, Aichinger M, Prazeres da Costa O, Voehringer D, Hoffmann R, Klein L (июнь 2010 г.). «Автономная роль мозговых эпителиальных клеток тимуса в толерантности центральных CD4 (+) Т-клеток» (PDF). Иммунология природы. 11 (6): 512–519. Дои:10.1038 / ni.1874. PMID 20431619.
- ^ Пекальски М.Л., Гарсия А.Р., Феррейра Р.С., Радуга ДБ, Смит Диджей, Машар М., Брэди Дж., Савиных Н., Допико XC, Махмуд С., Дули С., Стивенс Х.Э., Уокер Н. Шеннон-Лоу С., Коулз А.Дж., Джонс Дж. Л., Уоллес С., Тодд Дж. А., Уикер Л.С. (август 2017 г.). «Новорожденные и взрослые недавние эмигранты из тимуса продуцируют IL-8 и экспрессируют рецепторы комплемента CR1 и CR2». JCI Insight. 2 (16). Дои:10.1172 / jci.insight.93739. ЧВК 5621870. PMID 28814669.
- ^ Хейнс Б.Ф., Маркерт М.Л., Семповски Г.Д., Патель Д.Д., Хейл Л.П. (2000). «Роль тимуса в восстановлении иммунитета при старении, трансплантации костного мозга и ВИЧ-1 инфекции». Анну. Rev. Immunol. 18: 529–560. Дои:10.1146 / annurev.immunol.18.1.529. PMID 10837068.
- ^ Гатчер I, Бехер Б (2007). «Цитокины, производные APC, и поляризация Т-клеток при аутоиммунном воспалении». J. Clin. Вкладывать деньги. 117 (5): 1119–27. Дои:10.1172 / JCI31720. ЧВК 1857272. PMID 17476341.
- ^ Саллусто Ф, Лениг Д., Фёрстер Р., Липп М., Ланзавеккья А. (1999). «Два подмножества Т-лимфоцитов памяти с различными потенциалами самонаведения и эффекторными функциями». Природа. 401 (6754): 708–712. Bibcode:1999Натура.401..708С. Дои:10.1038/44385. PMID 10537110.
- ^ Акбар А.Н., Терри Л., Тиммс А., Беверли П.К., Джаносси Дж. (Апрель 1988 г.). «Потеря CD45R и повышение реактивности UCHL1 - это особенность примированных Т-клеток». J. Immunol. 140 (7): 2171–8. PMID 2965180.
- ^ Виллинджер Т., Фриман Т., Хасегава Х, МакМайкл А.Дж., Каллан М.Ф. (2005). «Молекулярные сигнатуры отличают центральную память человека от субнаборов Т-лимфоцитов CD8 эффекторной памяти» (PDF). Журнал иммунологии. 175 (9): 5895–903. Дои:10.4049 / jimmunol.175.9.5895. PMID 16237082.
- ^ Кох С., Ларби А., Дерхованесян Е., Озчелик Д., Наумова Е., Павелец Г. (2008). «Многопараметрический проточный цитометрический анализ субпопуляций CD4 и CD8 Т-клеток у молодых и пожилых людей». Иммунитет и старение. 5 (6): 6. Дои:10.1186/1742-4933-5-6. ЧВК 2515281. PMID 18657274.
- ^ Шин Х., Ивасаки А. (сентябрь 2013 г.). «Резидентные Т-клетки памяти». Иммунологические обзоры. 255 (1): 165–81. Дои:10.1111 / imr.12087. ЧВК 3748618. PMID 23947354.
- ^ Ли Ю.Дж., Джеймсон СК, Хогквист К.А. (2011). «Альтернативная память в линии CD8 Т-клеток». Тенденции в иммунологии. 32 (2): 50–56. Дои:10.1016 / j.it.2010.12.004. ЧВК 3039080. PMID 21288770.
- ^ Марусина А.И., Оно Ю., Мерлеев А.А., Шимода М., Огава Х., Ван Э.А., Кондо К., Олни Л., Люксарди Дж., Миямура Ю., Йилма Т.Д., Виллалобос И.Б., Бергстром Дж. В., Кроненберг Д. Г., Сулика А. М., Адамопулос И. Э., Маверакис Э (2017). «Виртуальная память CD4 +: Т-клетки, не обладающие антигеном, находятся в наивных, регуляторных и Т-клеточных компартментах памяти с одинаковой частотой, что влияет на аутоиммунитет». Журнал аутоиммунитета. 77: 76–88. Дои:10.1016 / j.jaut.2016.11.001. ЧВК 6066671. PMID 27894837.
- ^ Аббас А.К., Бенойст С., Блюстоун Дж. А., Кэмпбелл Д. Д., Гош С., Хори С., Цзян С., Кучро В. К., Матис Д., Ронкароло М. Г., Руденски А., Сакагути С., Шевач Е. М., Вигнали Д. А., Циглер С.Ф. (2013). «Регуляторные Т-клетки: рекомендации по упрощению номенклатуры». Nat. Иммунол. 14 (4): 307–8. Дои:10.1038 / ni.2554. PMID 23507634.
- ^ Сингх Б., Шварц Дж. А., Сандрок С., Беллемор С. М., Никоопур Е. (2013). «Модуляция аутоиммунных заболеваний с помощью продуцирующих интерлейкин (IL) -17 регуляторных Т-хелперных (Th17) клеток». Indian J. Med. Res. 138 (5): 591–4. ЧВК 3928692. PMID 24434314.
- ^ Маллевей Т., Фонтейн Дж., Брей Л., Пэджет С., Кастро-Келлер А., Вендевиль С., Капрон М., Лейте-де-Мораес М., Троттейн Ф., Фавью С. (май 2007 г.). «Инвариантные и неинвариантные естественные Т-клетки-киллеры выполняют противоположные регуляторные функции в отношении иммунного ответа во время шистосомоза у мышей». Инфекция и иммунитет. 75 (5): 2171–80. Дои:10.1128 / IAI.01178-06. ЧВК 1865739. PMID 17353286.
- ^ а б c d Напье Р.Дж., Адамс Э.Дж., Gold MC, Левинсон Д.М. (06.07.2015). «Роль инвариантных Т-клеток, ассоциированных со слизистой оболочкой, в противомикробном иммунитете». Границы иммунологии. 6: 344. Дои:10.3389 / fimmu.2015.00344. ЧВК 4492155. PMID 26217338.
- ^ Gold MC, Lewinsohn DM (август 2011 г.). «Инвариантные Т-клетки, ассоциированные со слизистой и иммунный ответ на инфекцию». Микробы и инфекции. 13 (8–9): 742–8. Дои:10.1016 / j.micinf.2011.03.007. ЧВК 3130845. PMID 21458588.
- ^ Экл С.Б., Корбетт А.Дж., Келлер А.Н., Чен З., Годфри Д.И., Лю Л., Мак Дж.Й., Фэрли Д.П., Россджон Дж., Маккласки Дж. (Декабрь 2015 г.). "Распознавание предшественников и побочных продуктов витамина B инвариантными Т-клетками, ассоциированными со слизистой". Журнал биологической химии. 290 (51): 30204–11. Дои:10.1074 / jbc.R115.685990. ЧВК 4683245. PMID 26468291.
- ^ Ушер Дж. Э., Кленерман П., Уиллберг CB (2014-10-08). «Ассоциированные со слизистой оболочкой инвариантные Т-клетки: новые игроки в антибактериальном иммунитете». Границы иммунологии. 5: 450. Дои:10.3389 / fimmu.2014.00450. ЧВК 4189401. PMID 25339949.
- ^ а б c Хаусон Л.Дж., Салио М, Церундоло V (16.06.2015). "MR1-ограниченные инвариантные Т-клетки слизистой оболочки и их активация при инфекционных заболеваниях". Границы иммунологии. 6: 303. Дои:10.3389 / fimmu.2015.00303. ЧВК 4468870. PMID 26136743.
- ^ Hinks TS (май 2016 г.). «Связанные со слизистой оболочкой инвариантные Т-клетки при аутоиммунитетах, иммуноопосредованных заболеваниях и заболеваниях дыхательных путей». Иммунология. 148 (1): 1–12. Дои:10.1111 / imm.12582. ЧВК 4819138. PMID 26778581.
- ^ Bianchini E, De Biasi S, Simone AM, Ferraro D, Sola P, Cossarizza A, Pinti M (март 2017 г.). «Инвариантные естественные Т-клетки-киллеры и инвариантные Т-клетки, связанные со слизистой оболочкой при рассеянном склерозе». Письма иммунологии. 183: 1–7. Дои:10.1016 / j.imlet.2017.01.009. PMID 28119072.
- ^ Серриари NE, Eoche M, Lamotte L, Lion J, Fumery M, Marcelo P, Chatelain D, Barre A, Nguyen-Khac E, Lantz O, Dupas JL, Treiner E (май 2014 г.). «Врожденные инвариантные Т-клетки, ассоциированные со слизистой оболочкой (MAIT), активируются при воспалительных заболеваниях кишечника». Клиническая и экспериментальная иммунология. 176 (2): 266–74. Дои:10.1111 / cei.12277. ЧВК 3992039. PMID 24450998.
- ^ Хуанг С., Мартин Э., Ким С., Ю Л., Судейс К., Фремонт Д.Х., Ланц О., Хансен Т.Х. (май 2009 г.). «Презентация антигена MR1 ассоциированным со слизистой оболочкой инвариантным Т-клеткам была высококонсервативной в процессе эволюции». Труды Национальной академии наук Соединенных Штатов Америки. 106 (20): 8290–5. Bibcode:2009PNAS..106.8290H. Дои:10.1073 / pnas.0903196106. ЧВК 2688861. PMID 19416870.
- ^ Чуа В.Дж., Хансен Т.Х. (ноябрь 2010 г.). «Бактерии, инвариантные Т-клетки, ассоциированные со слизистой оболочкой, и MR1». Иммунология и клеточная биология. 88 (8): 767–9. Дои:10.1038 / icb.2010.104. PMID 20733595.
- ^ Кьер-Нильсен Л., Патель О., Корбетт А. Дж., Ле Нур Дж., Михан Б., Лю Л., Бхати М., Чен З., Костенко Л., Реантрагун Р., Уильямсон Н. А., Перселл А. В., Дудек Н. Л., МакКонвилл М. Дж., О'Хэр Р. А., Хайралла Г. Н., Годфри Д. И., Фэрли Д. П., Россджон Дж., Маккласки Дж. (Ноябрь 2012 г.). «MR1 представляет метаболиты микробного витамина B для клеток MAIT» (PDF). Природа. 491 (7426): 717–23. Bibcode:2012Натура.491..717K. Дои:10.1038 / природа11605. PMID 23051753.
- ^ В НИАИД буклет ресурсов «Понимание иммунной системы (pdf)».
- ^ Уильямс М.А., Беван М.Дж. (01.01.2007). «Эффекторная дифференциация ЦТЛ памяти». Ежегодный обзор иммунологии. 25 (1): 171–92. Дои:10.1146 / annurev.immunol.25.022106.141548. PMID 17129182.
- ^ Янссен Э.М., Лемменс Э.Е., Вулф Т., Кристен У., фон Херрат М.Г., Шенбергер С.П. (февраль 2003 г.). «CD4 + Т-клетки необходимы для вторичного размножения и памяти в CD8 + Т-лимфоцитах». Природа. 421 (6925): 852–6. Bibcode:2003Натура.421..852J. Дои:10.1038 / природа01441. PMID 12594515.
- ^ Shedlock DJ, Шен Х (апрель 2003 г.). «Потребность в помощи Т-лимфоцитов CD4 в создании функциональной памяти Т-лимфоцитов CD8». Наука. 300 (5617): 337–9. Bibcode:2003Sci ... 300..337S. Дои:10.1126 / science.1082305. PMID 12690201.
- ^ Сан Дж. К., Уильямс М. А., Беван М. Дж. (Сентябрь 2004 г.). «CD4 + Т-клетки необходимы для поддержания, а не программирования, CD8 + Т-клеток памяти после острой инфекции». Иммунология природы. 5 (9): 927–33. Дои:10.1038 / ni1105. ЧВК 2776074. PMID 15300249.
- ^ Дженнифер Ролланд и Робин О'Хехир, «Отключение Т-клеток: пептиды для лечения аллергических заболеваний», Today's Life Science Publishing, 1999, стр. 32
- ^ Маверакис Э., Ким К., Шимода М., Гершвин М., Патель Ф, Уилкен Р., Райчаудхури С., Рухак Л. Р., Лебрилла CB (2015). "Гликаны в иммунной системе и измененная теория аутоиммунитета гликанов". J Аутоиммунный. 57 (6): 1–13. Дои:10.1016 / j.jaut.2014.12.002. ЧВК 4340844. PMID 25578468.
- ^ а б Татам П., Гомпертс Б.Д., Крамер И.М. (2003). Передача сигнала. Амстердам: Elsevier Academic Press. ISBN 978-0-12-289632-3.
- ^ Ву Х., Аррон-младший (ноябрь 2003 г.). «TRAF6, молекулярный мост, соединяющий адаптивный иммунитет, врожденный иммунитет и остеоиммунологию». BioEssays. 25 (11): 1096–105. Дои:10.1002 / bies.10352. PMID 14579250.
- ^ Milstein O, Hagin D, Lask A, Reich-Zeliger S, Shezen E, Ophir E, Eidelstein Y, Afik R, Antebi YE, Dustin ML, Reisner Y (январь 2011 г.). «CTL реагируют активацией и секрецией гранул, когда служат мишенями для распознавания Т-клеток». Кровь. 117 (3): 1042–52. Дои:10.1182 / кровь-2010-05-283770. ЧВК 3035066. PMID 21045195.
- ^ Грэм, Уильям (2014-04-14). «SpaceX готова к запуску CRS-3 Dragon и новым этапам». NASAspaceflight.com. Получено 2014-04-14.
- ^ Беликов А.В., Шравен Б., Симеони Л. (октябрь 2015 г.). «Т-клетки и активные формы кислорода». Журнал биомедицинских наук. 22: 85. Дои:10.1186 / s12929-015-0194-3. ЧВК 4608155. PMID 26471060.
- ^ а б Файнерман О., Жермен Р. Н., Альтан-Бонне Г. (2008). «Количественные проблемы в понимании дискриминации лиганда Т-лимфоцитами». Мол. Иммунол. 45 (3): 619–31. Дои:10.1016 / j.molimm.2007.03.028. ЧВК 2131735. PMID 17825415.
- ^ Душек О., Ван дер Мерве ПА (2014). «Модель индуцированного повторного связывания дискриминации антигена». Тенденции Иммунол. 35 (4): 153–8. Дои:10.1016 / j.it.2014.02.002. ЧВК 3989030. PMID 24636916.
- ^ а б Medscape> Т-клеточные заболевания. Автор: Роберт А. Шварц, доктор медицины, магистр здравоохранения; Главный редактор: Харуми Джионучи, доктор медицины. Обновлено: 16 мая 2011 г.
- ^ а б Джонс Дж., Баннистер Б.А., Гиллеспи С.Х., ред. (2006). Инфекция: микробиология и лечение. Вили-Блэквелл. п. 435. ISBN 978-1-4051-2665-6.
- ^ «Лимфомы» (PDF). Общество лейкемии и лимфомы. Май 2006. с. 2. Получено 2008-04-07.
- ^ Yi JS, Cox MA, Zajac AJ (апрель 2010 г.). «Истощение Т-лимфоцитов: характеристики, причины и преобразование». Иммунология. 129 (4): 474–81. Дои:10.1111 / j.1365-2567.2010.03255.x. ЧВК 2842494. PMID 20201977.
- ^ Ван Цюй, Пан В, Лю И, Ло Дж, Чжу Д., Лу И, Фэн Х, Ян Х, Диттмер У, Лу М, Ян Д., Лю Дж (2018). «Специфические CD8 + Т-клетки вируса гепатита В сохраняют функциональное истощение после повторного воздействия антигена в иммунной среде с острой активацией». Фронт Иммунол. 9: 219. Дои:10.3389 / fimmu.2018.00219. ЧВК 5816053. PMID 29483916.
- ^ Матлоубиан М., Консепсьон Р. Дж., Ахмед Р. (декабрь 1994 г.). «CD4 + Т-клетки необходимы для поддержания CD8 + цитотоксических Т-клеточных ответов во время хронической вирусной инфекции». Журнал вирусологии. 68 (12): 8056–63. Дои:10.1128 / JVI.68.12.8056-8063.1994. ЧВК 237269. PMID 7966595.
- ^ Ангелосанто Дж. М., Блэкберн С. Д., Кроуфорд А., Уэрри Э. Дж. (Август 2012 г.). «Прогрессирующая потеря потенциала Т-клеток памяти и стремление к истощению во время хронической вирусной инфекции». Журнал вирусологии. 86 (15): 8161–70. Дои:10.1128 / JVI.00889-12. ЧВК 3421680. PMID 22623779.
- ^ Wherry EJ (июнь 2011 г.). «Истощение Т-лимфоцитов». Иммунология природы. 12 (6): 492–9. Дои:10.1038 / ni.2035. PMID 21739672.
- ^ Окагава Т., Коннаи С., Нисимори А., Маэкава Н., Гото С., Икебути Р., Кохара Дж., Судзуки Ю., Ямада С., Като Ю., Мурата С., Охаши К. (июнь 2018 г.). «+ Т-клетки при инфицировании вирусом лейкемии крупного рогатого скота». Ветеринарные исследования. 49 (1): 50. Дои:10.1186 / s13567-018-0543-9. ЧВК 6006750. PMID 29914540.
- ^ Brooks DG, Trifilo MJ, Edelmann KH, Teyton L, McGavern DB, Oldstone MB (ноябрь 2006 г.). «Интерлейкин-10 определяет вирусный клиренс или персистентность in vivo». Природа Медицина. 12 (11): 1301–9. Дои:10,1038 / нм 1492. ЧВК 2535582. PMID 17041596.
- ^ Тиноко Р., Алькальд В., Ян Й., Зауэр К., Зунига Е. И. (июль 2009 г.). «Внутренняя передача сигналов трансформирующего фактора роста-бета опосредует вирус-специфическую делецию Т-лимфоцитов CD8 + и вирусную персистенцию in vivo». Иммунитет. 31 (1): 145–57. Дои:10.1016 / j.immuni.2009.06.015. ЧВК 3039716. PMID 19604493.
- ^ Вейга-Парга Т., Сехрават С., Роуз Б.Т. (сентябрь 2013 г.). «Роль регуляторных Т-клеток при вирусной инфекции». Иммунологические обзоры. 255 (1): 182–96. Дои:10.1111 / imr.12085. ЧВК 3748387. PMID 23947355.
- ^ Penaloza-MacMaster P, Kamphorst AO, Wieland A, Araki K, Iyer SS, West EE, O'Mara L, Yang S, Konieczny BT, Sharpe AH, Freeman GJ, Rudensky AY, Ahmed R (август 2014 г.). «Взаимодействие между регуляторными Т-клетками и PD-1 в модулировании истощения Т-клеток и вирусном контроле во время хронической инфекции LCMV». Журнал экспериментальной медицины. 211 (9): 1905–18. Дои:10.1084 / jem.20132577. ЧВК 4144726. PMID 25113973.
- ^ Отто Г.П., Соссдорф М., Клаус Р.А., Рёдел Дж., Менге К., Рейнхарт К., Бауэр М., Ридеманн Н.К. (июль 2011 г.). «Поздняя фаза сепсиса характеризуется повышенным микробиологическим бременем и смертностью». Критический уход. 15 (4): R183. Дои:10.1186 / cc10332. ЧВК 3387626. PMID 21798063.
- ^ а б Boomer JS, To K, Chang KC, Takasu O, Osborne DF, Walton AH, Bricker TL, Jarman SD, Kreisel D, Krupnick AS, Srivastava A, Swanson PE, Green JM, Hotchkiss RS (декабрь 2011 г.). «Иммуносупрессия у пациентов, умирающих от сепсиса и полиорганной недостаточности». JAMA. 306 (23): 2594–605. Дои:10.1001 / jama.2011.1829. ЧВК 3361243. PMID 22187279.
- ^ Шиндо Ю., Макдоно Дж. С., Чанг К. К., Рамачандра М., Сасикумар П. Г., Хотчкисс Р. С. (февраль 2017 г.). «Пептид Anti-PD-L1 улучшает выживаемость при сепсисе». Журнал хирургических исследований. 208: 33–39. Дои:10.1016 / j.jss.2016.08.099. ЧВК 5535083. PMID 27993215.
- ^ Patera AC, Drewry AM, Chang K, Beiter ER, Osborne D, Hotchkiss RS (декабрь 2016 г.). «Передовая наука: дефекты иммунной функции у пациентов с сепсисом связаны с экспрессией PD-1 или PD-L1 и могут быть восстановлены антителами, нацеленными на PD-1 или PD-L1». Журнал биологии лейкоцитов. 100 (6): 1239–1254. Дои:10.1189 / jlb.4hi0616-255r. ЧВК 5110001. PMID 27671246.
- ^ Вэй З, Ли П, Яо И, Дэн Х, Йи С, Чжан Ч, Ву Х, Се Х, Ся М, Хэ Р, Ян XP, Тан Чж (июль 2018). «Альфа-лактоза устраняет повреждение печени посредством блокады Тим-3-опосредованного апоптоза CD8 при сепсисе». Клиническая иммунология. 192: 78–84. Дои:10.1016 / j.clim.2018.04.010. PMID 29689313.
- ^ Wells AD, Li XC, Strom TB, Турка, Лос-Анджелес (май 2001 г.). «Роль делеции периферических Т-клеток в толерантности к трансплантации». Философские труды Лондонского королевского общества. Серия B, Биологические науки. 356 (1409): 617–23. Дои:10.1098 / rstb.2001.0845. ЧВК 1088449. PMID 11375065.
- ^ Халлоран П.Ф., Чанг Дж., Фамульски К., Идальго Л.Г., Салазар И.Д., Мерино Лопес М., Матас А., Пиктон М., де Фрейтас Д., Бромберг Дж., Серон Д., Селларес Дж., Эйнеке Дж., Рив Дж. (Июль 2015 г.). «Исчезновение опосредованного Т-клетками отторжения, несмотря на продолжающееся опосредованное антителами отторжение у пациентов с поздней трансплантацией почки». Журнал Американского общества нефрологов. 26 (7): 1711–20. Дои:10.1681 / ASN.2014060588. ЧВК 4483591. PMID 25377077.
- ^ Стегер У., Денеке С., Савицки Б., Карим М., Джонс Н.Д., Вуд К.Дж. (май 2008 г.). «Исчерпывающая дифференцировка аллореактивных CD8 + Т-клеток: критически важна для определения принятия или отторжения трансплантата» (PDF). Трансплантация. 85 (9): 1339–47. Дои:10.1097 / TP.0b013e31816dd64a. PMID 18475193.
- ^ de Mare-Bredemeijer EL, Shi XL, Mancham S, van Gent R, van der Heide-Mulder M, de Boer R, Heemskerk MH, de Jonge J, van der Laan LJ, Metselaar HJ, Kwekkeboom J (август 2015 г.). «Вызванная цитомегаловирусом экспрессия CD244 после трансплантации печени связана с гипореактивностью CD8 + Т-клеток к аллоантигену». Журнал иммунологии. 195 (4): 1838–48. Дои:10.4049 / jimmunol.1500440. PMID 26170387.
- ^ Гасса А., Цзян Ф., Калкаван Х., Духан В., Хонке Н., Шаабани Н., Фридрих С. К., Дольф С., Уолерс Т., Криббен А., Хардт С., Ланг ПА, Витцке О., Ланг К. С. (2016). «IL-10 вызывает истощение Т-клеток во время трансплантации зараженных вирусом сердец». Клеточная физиология и биохимия. 38 (3): 1171–81. Дои:10.1159/000443067. PMID 26963287.
- ^ Ши XL, де Маре-Бредемейер Э.Л., Тапирдамаз Ö, Хансен Б.Э., ван Гент Р., ван Кампенхаут М.Дж., Манчам С., Литдженс Н.Х., Бетджес М.Г., ван дер Эйк А.А., Ся К. HJ, Kwekkeboom J (сентябрь 2015 г.). «Первичная инфекция ЦМВ связана с гипореактивностью донорских Т-лимфоцитов и меньшим количеством поздних острых отторжений после трансплантации печени». Американский журнал трансплантологии. 15 (9): 2431–42. Дои:10.1111 / ajt.13288. PMID 25943855.
- ^ Williams RL, Cooley S, Bachanova V, Blazar BR, Weisdorf DJ, Miller JS, Verneris MR (март 2018 г.). «Истощение реципиентных Т-клеток и успешный перенос гаплоидентичных естественных киллерных клеток». Биология трансплантации крови и костного мозга. 24 (3): 618–622. Дои:10.1016 / j.bbmt.2017.11.022. ЧВК 5826878. PMID 29197679.
- ^ Woo SR, Turnis ME, Goldberg MV, Bankoti J, Selby M, Nirschl CJ, Bettini ML, Gravano DM, Vogel P, Liu CL, Tangsombatvisit S, Grosso JF, Netto G, Smeltzer MP, Chaux A, Utz PJ, Workman CJ , Пардолл Д.М., Корман А.Дж., Дрейк К.Г., Виньяли Д.А. (февраль 2012 г.). «Иммунные ингибирующие молекулы LAG-3 и PD-1 синергетически регулируют функцию Т-клеток, способствуя ускользанию от опухолевого иммунитета». Исследования рака. 72 (4): 917–27. Дои:10.1158 / 0008-5472.CAN-11-1620. ЧВК 3288154. PMID 22186141.
- ^ Zelle-Rieser C, Thangavadivel S, Biedermann R, Brunner A, Stoitzner P, Willenbacher E, Greil R, Jöhrer K (ноябрь 2016 г.). «Т-клетки при множественной миеломе демонстрируют признаки истощения и старения в месте опухоли». Журнал гематологии и онкологии. 9 (1): 116. Дои:10.1186 / s13045-016-0345-3. ЧВК 5093947. PMID 27809856.
- ^ Лакинс М.А., Горани Э., Мунир Х., Мартинс С.П., Шилдс Д.Д. (март 2018 г.). «+ Т-клетки для защиты опухолевых клеток». Nature Communications. 9 (1): 948. Дои:10.1038 / s41467-018-03347-0. ЧВК 5838096. PMID 29507342.
- ^ Конфорти, Лаура (2012-02-10). «Сеть ионных каналов в Т-лимфоцитах, мишень для иммунотерапии». Клиническая иммунология. 142 (2): 105–106. Дои:10.1016 / j.clim.2011.11.009. PMID 22189042.
- ^ Лю Л., Чанг ИДж, Сюй Л.П., Чжан XH, Ван И, Лю К.Й., Хуанг XJ (май 2018 г.). «Истощение Т-клеток, характеризующееся нарушением цитотоксической активности класса I и II по МНС, ассоциируется с острым рецидивом В-лимфобластного лейкоза после аллогенной трансплантации гемопоэтических стволовых клеток». Клиническая иммунология. 190: 32–40. Дои:10.1016 / j.clim.2018.02.009. PMID 29477343.
- ^ Kong Y, Zhang J, Claxton DF, Ehmann WC, Rybka WB, Zhu L, Zeng H, Schell TD, Zheng H (июль 2015 г.). «PD-1 (hi) TIM-3 (+) T-клетки связываются с и предсказывают рецидив лейкемии у пациентов с AML после трансплантации аллогенных стволовых клеток». Журнал рака крови. 5 (7): e330. Дои:10.1038 / bcj.2015.58. ЧВК 4526784. PMID 26230954.
- ^ «Утвержденные FDA США ингибиторы иммунных контрольных точек и иммунотерапия». Агентство медицинских писателей |香港 醫學 作家 | MediPR | MediPaper Гонконг. 2018-08-21. Получено 2018-09-22.
- ^ Бхадра Р., Джигли Дж. П., Вайс Л. М., Хан И. А. (май 2011 г.). «Контроль реактивации токсоплазмы путем восстановления дисфункционального ответа CD8 + Т-клеток посредством блокады PD-1-PDL-1». Труды Национальной академии наук Соединенных Штатов Америки. 108 (22): 9196–201. Дои:10.1073 / pnas.1015298108. ЧВК 3107287. PMID 21576466.
внешняя ссылка
- Иммунобиология, 5-е издание
- Иммунная система в Национальном институте аллергии и инфекционных болезней
- Группа Т-клеток - Кардиффский университет
