IgA нефропатия - IgA nephropathy
| Болезнь Бергера (IgA-нефропатия) | |
|---|---|
| Другие имена | IgA нефрит |
 | |
| Иммуноглобулин А димер | |
| Специальность | Нефрология Ревматология Онкология |
IgA нефропатия (IgAN), также известный как Болезнь Бергера (/бɛərˈʒeɪ/) (и варианты), или синфарингитный гломерулонефрит, это заболевание почек (или нефропатия) и иммунная система; в частности, это форма гломерулонефрит или воспаление из клубочки из почка. Агрессивная болезнь Бергера (более редкая форма болезни) может поражать другие основные органы, такие как печень, кожа и сердце.
IgA-нефропатия - самый распространенный гломерулонефрит во всем мире; тем не менее, агрессивная болезнь Бергера находится на NORD список редких заболеваний.[1] Первичная IgA-нефропатия характеризуется отложением IgA антитело в клубочках. Есть и другие заболевания, связанные с отложениями IgA в клубочках, наиболее частым из которых является: IgA васкулит (ранее известный как Генох – пурпура Шенлейна [HSP]), который многие считают системной формой IgA-нефропатии.[2] IgA-васкулит имеет характерную пурпурный кожная сыпь, артрит, и боль в животе, и чаще возникает у молодых людей (16–35 лет). HSP ассоциируется с более благоприятным прогнозом, чем IgA-нефропатия. При неагрессивной IgA-нефропатии обычно в 25–30% случаев в течение 20 лет наблюдается медленное прогрессирование хронической почечной недостаточности.
Признаки и симптомы
Классическое проявление неагрессивной формы (в 40–50% случаев) - эпизодическое. гематурия, который обычно начинается в течение дня или двух неспецифических Инфекция верхних дыхательных путей (следовательно синфарингитный), в отличие от постстрептококковый гломерулонефрит, что происходит через некоторое время (недели) после первоначального заражения. Как при агрессивной, так и при неагрессивной болезни Бергера боль в пояснице также может произойти. Однако макрогематурия может исчезнуть через несколько дней. микроскопическая гематурия сохраняется, однако при агрессивной болезни Бергера макрогематурия чаще сохраняется, чем при микроскопической гематурии. Почечная функция обычно остается нормальной при неагрессивной болезни Бергера, хотя редко. острая почечная недостаточность может произойти (см. ниже). Это представление чаще встречается у молодых людей.
Ниже приводится основной список симптомов, взятых в основном из клиники Мэйо;
- Сильная боль в боку / животе
- Высокое кровяное давление
- Гематурия (макроскопическая, явная, микроскопическая)
- Ослабленная иммунная система
- Отеки кистей и стоп
- Моча коло- или чайного цвета
Меньшая часть (20–30%), обычно пожилое население, имеет микроскопическую гематурию и протеинурия (менее 2 грамм / сутки). Эти пациенты могут протекать бессимптомно и обнаруживаться только на основании анализа мочи. Следовательно, заболевание чаще диагностируется в ситуациях, когда обследование мочи является обязательным (например, школьники в Япония ).
Очень редко (по 5%) анамнез:
- Нефротический синдром (3–3,5 грамма потери белка с мочой, что связано с худшим прогнозом)
- Острая почечная недостаточность (либо как осложнение явной гематурии, когда она обычно излечивается, либо из-за быстро прогрессирующий гломерулонефрит что часто приводит к хроническая почечная недостаточность )
- Хроническая почечная недостаточность (без предыдущих симптомов, присутствует анемия, гипертония и другие симптомы почечной недостаточности у людей, у которых, вероятно, была длительная необнаруженная микроскопическая гематурия и / или протеинурия)
С агрессивной IgA нефропатией (болезнью Бергера) связаны различные системные заболевания, такие как отказ печени, рак, глютеновая болезнь, системная красная волчанка, ревматоидный артрит, сердечная недостаточность, реактивный артрит, анкилозирующий спондилоартрит и ВИЧ. Диагностика болезни Бергера и поиск любого связанного с ней заболевания иногда выявляют такое основное серьезное системное заболевание. Иногда появляются одновременные симптомы Генох – пурпура Шенлейна; подробнее об ассоциации см. ниже. Некоторые аллели HLA, наряду с фенотипами комплемента, считаются генетическими факторами. Неагрессивная болезнь Бергера также может быть связана с любым из перечисленных выше системных заболеваний, однако это бывает редко.
Морфология
Гистологически IgA-нефропатия может показывать мезангиальное расширение и очаговое и сегментарное воспаление. Также может присутствовать диффузная мезангиальная пролиферация или серповидный гломерулонефрит. Иммунофлуоресценция показывает мезангиальное отложение IgA, часто с C3 и пропердин и меньшее количество других иммуноглобулинов (IgG или же IgM ). Ранние компоненты классический путь комплемента (C1q или же C4 ) обычно не видны. Электронная микроскопия подтверждает электронно-плотные отложения в мезангиуме, которые могут распространяться на субэндотелиальную область прилегающих стенок капилляров в небольшом подмножестве случаев, обычно с очаговой пролиферацией.
Патофизиология
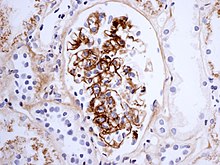
Болезнь получила свое название от отложений иммуноглобулин А (IgA) в виде гранул в мезангиуме (по иммунофлуоресценция ), область почечной клубочки. Мезангий при световой микроскопии может быть гиперклеточным и показывать повышенное отложение внеклеточный матрикс белки. Что касается почечного проявления Генох – пурпура Шенлейна было обнаружено, что, хотя он имеет тот же гистологический спектр, что и нефропатия IgA, наблюдалась большая частота тяжелых поражений, таких как гломерулярный некроз и серповидные образования. Соответственно, нефрит HSP имеет более высокую частоту окрашивания клубочков на фибрин по сравнению с IgAN, но с аналогичным профилем иммунофлуоресценции.[3]
Нет четкого известного объяснения накопления IgA. Экзогенный антигены IgA в почках не обнаружены, но возможно, что этот антиген был выведен до того, как болезнь проявит себя. Также было высказано предположение, что сам IgA может быть антигеном.
Недавно выдвинутая теория фокусируется на аномалиях молекулы IgA1. IgA1 - это один из двух подклассов иммуноглобулинов (другой - IgD), который О-гликозилированный по ряду серин и треонин остатки в специальном пролин -богатая навеска. Аберрантное гликозилирование IgA, по-видимому, приводит к полимеризация молекул IgA в тканях, особенно в мезангиуме клубочков.[4] Утверждается, что аналогичный механизм лежит в основе Генох – пурпура Шенлейна, а васкулит это в основном поражает детей и может иметь поражение почек, почти неотличимое от IgA-нефрита. Однако исследования на людях показали, что дегалактозилирование IgA1 происходит у пациентов с нефропатией IgA в ответ только на воздействие антигена кишечника (не системное), и происходит у здоровых людей в меньшей степени.[5] Это убедительно свидетельствует о том, что дегалактозилирование IgA1 является результатом основного явления (ненормальная обработка антигена слизистой оболочки), а не основной причиной нефропатии IgA. Имеющиеся данные свидетельствуют о том, что для образования комплексов иммуноглобулинов и их накопления в клубочках необходимы как о-гликаны с дефицитом галактозы в шарнирной области IgA1, так и синтез и связывание антител против IgA1.[6]
Исходя из того факта, что IgAN может рецидивировать после трансплантации почки, можно предположить, что заболевание вызвано проблемой в иммунная система а не сама почка. Примечательно, что IgA1, который накапливается в почках, по-видимому, происходит не из лимфоидной ткани, связанной со слизистой оболочкой (MALT), которая является очагом большинства инфекций верхних дыхательных путей, а из Костный мозг. Это тоже указывает на иммунную патологию, а не на прямое вмешательство внешних агентов.
Естественная история
Поскольку IgA-нефропатия обычно проявляется бессимптомно из-за отклонений от нормы на анализ мочи, существует значительная возможность вариации в любой изучаемой популяции в зависимости от скрининг политика. Аналогичным образом, местная политика в отношении почки биопсия берет на себя решающую роль; если это политика - просто наблюдать за пациентами с изолированными кровавая моча, группа с в целом благоприятным прогноз будут исключены. Если, напротив, у всех таких пациентов проводится биопсия, то группа с изолированными микроскопическая гематурия и изолированный мезангиальный IgA будет включен и «улучшит» прогноз для этой конкретной серии.
Тем не менее, IgA-нефропатия, которая изначально считалась доброкачественным заболеванием, не является доброкачественным заболеванием, особенно если у пациента имеется агрессивная форма. Хотя в большинстве сообщений болезнь Бергера описывается как медленная эволюция в сторону заживления или повреждения почек, иногда наблюдается более агрессивное течение, связанное с обширными серповидными лучами и проявляющееся как острая почечная недостаточность. В общем, вступление в хроническая почечная недостаточность протекает медленно по сравнению с большинством других гломерулонефритов - происходит в течение 30 лет и более (в отличие от 5-15 лет для других гломерулонефритов), однако при агрессивной болезни Бергера временной масштаб находится в пределах 5-10 лет и часто раньше . Это может отражать ранее поставленный диагноз из-за явной гематурии.
Полный ремиссия агрессивной болезни Бергера, редко встречается у взрослых. Однако примерно в 5% случаев вероятность ремиссии при неагрессивной болезни Бергера выше (по оценкам, это составляет около 7,4% случаев). Вероятность рецидива высока, особенно при агрессивной болезни Бергера. Однако, учитывая развитие этого заболевания, более долгосрочный (10–20 лет) исход для таких пациентов еще не установлен.
В целом, текущая 10-летняя выживаемость при агрессивной болезни Бергера составляет 25% и 73% при неагрессивной болезни Бергера.
Диагностика
Для взрослого пациента с изолированным гематурия, тесты, такие как УЗИ почки и цистоскопия обычно делаются в первую очередь, чтобы точно определить источник кровотечение. Эти тесты исключили бы камни в почках и Рак мочевого пузыря, два других общих урологический причины гематурии. У детей и молодых людей история болезни и связь с респираторной инфекцией могут вызвать подозрение на IgA-нефропатию. Почка биопсия необходимо для подтверждения диагноза. Образец биопсии показывает разрастание мезангиум, с отложениями IgA на иммунофлуоресценция и электронная микроскопия. Однако пациенты с изолированными микроскопическая гематурия (т.е. без сопутствующей протеинурии и с нормальным функция почек ) обычно не биопсии, так как это связано с отличным прогноз. А анализ мочи покажет красные кровяные тельца, обычно в виде эритроцитов мочевые цилиндры. Протеинурия, обычно менее 2 граммов в день, также может присутствовать. Другой почечный причины изолированной гематурии включают: болезнь тонкой базальной мембраны и Синдром Альпорта, последний наследственное заболевание связана с нарушение слуха и проблемы с глазами.
Другой анализы крови сделано, чтобы помочь в диагностике, включает CRP или же СОЭ, дополнять уровни АНА, и LDH. Белковый электрофорез и иммуноглобулин уровни IgA могут быть повышены у 50% всех пациентов.
Уход
Идеальное лечение IgAN должно удалить IgA из клубочков и предотвратить дальнейшее отложение IgA. Эта цель все еще остается отдаленной перспективой. Есть несколько дополнительных предостережений, которые необходимо учитывать при лечении IgA-нефропатии. IgA-нефропатия имеет очень вариабельное течение, от доброкачественной рецидивирующей гематурия до быстрого продвижения к хроническая почечная недостаточность и отказ других основных органов. Следовательно, решение о том, каких пациентов лечить, должно основываться на прогностических факторах и риске прогрессирования. Кроме того, IgA-нефропатия рецидивирует у трансплантаты несмотря на использование циклоспорин, азатиоприн или же микофенолят мофетил, циклофосфамид, Изотретиноин и стероиды у этих пациентов. Сохраняются неопределенности из-за ограниченного числа пациентов, включенных в немногочисленные контролируемые рандомизированные исследования, проведенные на сегодняшний день. Эти исследования практически не дают статистически значимых доказательств гетерогенности пациентов с IgA-нефропатией, разнообразия протоколов исследуемого лечения и продолжительности наблюдения.
В случаях, когда тонзиллит является провоцирующим фактором эпизодической гематурии, a тонзиллэктомия было заявлено, что снижает частоту этих эпизодов. Однако это не снижает частоту прогрессирования почечная недостаточность.[7] Диетический глютен ограничение, используемое для уменьшения слизистой оболочки антиген вызов, также не было показано, чтобы сохранить функция почек. Фенитоин также был опробован без всякой пользы.[8]
Подгруппа пациентов с IgA-нефропатией, у которых болезнь минимальных изменений на свете микроскопия и клинически нефротический синдром, покажите изысканный ответ на стероиды, ведя себя более или менее как болезнь минимальных изменений. Для других пациентов доказательства применения стероидов неубедительны. Доказано, что короткие курсы стероидов в высоких дозах не приносят пользы. Однако у пациентов с агрессивной болезнью Бергера 6-месячный курс стероидов в дополнение к другим лекарствам может уменьшить протеинурию и сохранить функцию почек.[9] В исследовании использовались данные наблюдения за пациентами в течение 10 лет, и оно показало пользу стероидной терапии; в группе стероидов была более низкая вероятность достижения терминальной стадии почечной недостаточности (функция почек настолько плохая, что требовался диализ). Важно отметить, что ингибиторы ангиотензинпревращающего фермента использовались в обеих группах одинаково.
Циклофосфамид (торгуется как эндоксан & цитоксан ) и Изотретиноин обычно использовались, часто с антитромбоцитарный /антикоагулянты Однако у пациентов с агрессивной болезнью Бергера профиль побочных эффектов этих препаратов, включая долгосрочный риск злокачественная опухоль и бесплодие, сделали их неблагоприятным выбором для молодых людей. Однако одно недавнее исследование, проведенное среди тщательно отобранной популяции пациентов с высоким риском СКФ, показали, что сочетание стероидов и циклофосфамид в течение первых 3 месяцев с последующим азатиоприн в течение минимум 2 лет привело к значительному сохранению функции почек.[10] Другие агенты, такие как микофенолят мофетил, циклоспорин и мизорибин также были опробованы с разными результатами.
Исследование, проведенное в Mayo Clinic, показало, что длительное лечение омега-3 жирные кислоты приводит к небольшому снижению прогрессирования до почечная недостаточность, однако без уменьшения протеинурия в подгруппе пациентов с высоким риском ухудшения функция почек.[11] Однако эти результаты не были воспроизведены другими исследовательскими группами и в двух последующих метаанализах.[12][13] Однако терапия рыбьим жиром не имеет недостатков иммуносупрессивная терапия. Кроме того, помимо неприятного вкуса и дискомфорта в животе, его употреблять относительно безопасно.
События, которые имеют тенденцию к прогрессирующей почечной недостаточности, не являются уникальными для IgA-нефропатии, и неспецифические меры по их снижению были бы одинаково полезны. К ним относятся диета с низким содержанием белка и оптимальный контроль артериальное давление. Выбор антигипертензивный агент открыт до тех пор, пока артериальное давление поддерживается на желаемом уровне. Тем не мение, Ингибиторы ангиотензинпревращающего фермента и Антагонисты рецепторов ангиотензина II пользуются популярностью из-за их антипротеинурического эффекта.
Прогноз
Мужской пол, протеинурия (особенно> 2 г / день), гипертония, курение, гиперлипидемия, пожилой возраст, семейные заболевания и повышенные креатинин концентрации являются маркерами неблагоприятного исхода. откровенный гематурия показал противоречивые результаты с большинством исследований, показывающих лучший прогноз, возможно, связанный с ранней диагностикой, за исключением одной группы, которая сообщила о более плохом прогнозе. Протеинурия и гипертония являются наиболее сильными прогностическими факторами в этой группе.[14]
Есть некоторые другие особенности почек биопсия такие как интерстициальные рубцы, которые связаны с плохим прогнозом. Ген АПФ полиморфизм недавно было показано, что он влияет на DD генотип чаще ассоциируется с прогрессированием почечная недостаточность.
Эпидемиология
Мужчины поражаются в три раза чаще, чем женщины. Также существуют заметные географические различия в распространенности IgA-нефропатии во всем мире. Это наиболее распространенное гломерулярное заболевание в Дальний Восток и Юго-Восточная Азия, что составляет почти половину всех пациентов с гломерулярной патологией.[нужна цитата ] Однако на его долю приходится только около 25% доли среди европейцев и около 10% среди североамериканцев, причем афроамериканцы имеют очень низкий уровень распространенности - около 2%.[нужна цитата ] Смешивающим фактором в этом анализе является существующая политика скрининг и использование почек биопсия как инструмент расследования. Школьники в Япония проходить рутину анализ мочи (как и новобранцы в Сингапур ), и при любых подозрительных отклонениях проводится биопсия почки, что может частично объяснить наблюдаемое высокое заболеваемость IgA-нефропатии в этих странах.
Генетика
Несмотря на то, что были описаны различные ассоциации, на сегодняшний день не выявлено последовательной закономерности, указывающей на один чувствительный ген. Описанные ассоциации включают ассоциации с нулевым аллелем C4, аллелями фактора B Bf, антигенами MHC и изотипами IgA. ТУЗ ген полиморфизм (Аллель D) связан с прогрессированием почечной недостаточности, так же как и его связь с другими причинами хроническая почечная недостаточность. Однако более 90% случаев нефропатии IgA носят спорадический характер, и несколько крупных родословных описаны из Кентукки и Италия (Онлайн-менделевское наследование в человеке (OMIM): 161950 ).
История

Уильям Хеберден, старший впервые описал болезнь в 1801 году у 5-летнего ребенка с болями в животе, гематурия, гематохезия, и пурпура ног.[15] В 1837 г. Иоганн Лукас Шенлайн описал синдром пурпуры, связанный с болью в суставах и выделениями из мочевого пузыря у детей. Эдуард Генрих Генох, студент Schönlein, еще больше связал боль в животе и поражение почек с синдромом.
В 1968 году Жан Бергер (1930–2011), французский новатор. нефролог, соавтором, электронным микроскопистом Николь Хинглэйс, была первой, кто описал отложение IgA в этой форме гломерулонефрит поэтому ее иногда называют болезнью Бергера.[16]
Рекомендации
- ^ Д'Амико, G (1987). «Самый распространенный гломерулонефрит в мире: нефропатия IgA». Q J Med. 64 (245): 709–27. PMID 3329736.
- ^ C, Дэвин Дж. (2001). «В чем разница между IgA-нефропатией и пурпурным нефритом Геноха-Шенлейна?». Kidney International. 59 (3): 823–34. Дои:10.1046 / j.1523-1755.2001.059003823.x. PMID 11231337.
- ^ Магистрони, Риккардо (2015). «Новые разработки в генетике, патогенезе и терапии IgA-нефропатии». Kidney International. 88 (5): 974–89. Дои:10.1038 / ки.2015.252. ЧВК 4653078. PMID 26376134.
- ^ Маверакис Э., Ким К., Шимода М., Гершвин М., Патель Ф., Уилкен Р., Райчаудхури С., Рухак Л. Р., Лебрилла CB (2015). "Гликаны в иммунной системе и измененная теория аутоиммунитета гликанов". J Аутоиммунный. 57 (6): 1–13. Дои:10.1016 / j.jaut.2014.12.002. ЧВК 4340844. PMID 25578468.
- ^ Смит А.С., Молинье К., Фихалли Дж., Барратт Дж. (2006). «О-гликозилирование сывороточных антител IgA1 против слизистых и системных антигенов при нефропатии IgA». J Am Soc Nephrol. 17 (12): 3520–28. Дои:10.1681 / ASN.2006060658. PMID 17093066.
- ^ Судзуки, Хитоши; Кирилюк, Кшиштоф; Новак, Ян; Молдовяну, Зина; Герр, Эндрю; Ренфроу, Мэтью; Вятт, Роберт; Сколари, Франческо; Местецкий, Иржи; Гарави, Али; Джулиан, Брюс (1 октября 2011 г.). «Патофизиология IgA нефропатии». Журнал Американского общества нефрологов. 22 (10): 1795–1803. Дои:10.1681 / ASN.2011050464. ЧВК 3892742. PMID 21949093.
- ^ Се И, Чен Икс, Ниши С., Нарита И., Геджё Ф (2004). «Связь между миндалинами и нефропатией IgA, а также показания к тонзиллэктомии». Почка Int. 65 (4): 1135–44. Дои:10.1111 / j.1523-1755.2004.00486.x. PMID 15086452.
- ^ Кларксон А.Р., Сеймур А.Э., Вудрофф А.Дж., Маккензи П.Е., Чан Ю.Л., Вуттон А.М. (1980). «Контролируемое испытание терапии фенитоином при IgA-нефропатии». Clin. Нефрол. 13 (5): 215–18. PMID 6994960.
- ^ Кобаяши Ю., Хики Ю., Кокубо Т., Хории А., Татено С. (1996). «Стероидная терапия на ранней стадии прогрессирующей IgA нефропатии. Последующее 10-летнее исследование». Нефрон. 72 (2): 237–42. Дои:10.1159/000188848. PMID 8684533.
- ^ Балларди Ф.В., Робертс И.С. (2002). «Контролируемое проспективное исследование преднизолона и цитотоксических средств при прогрессирующей IgA-нефропатии». Варенье. Soc. Нефрол. 13 (1): 142–48. PMID 11752031.
- ^ Донадио СП, Бергстраль Э.Дж., Оффорд К.П., Спенсер, округ Колумбия, Холли К.Э. (1994). «Контролируемое испытание рыбьего жира при нефропатии IgA. Совместная группа Mayo Nephrology». N. Engl. J. Med. 331 (18): 1194–99. Дои:10.1056 / NEJM199411033311804. PMID 7935657.
- ^ Стрипполи Г.Ф., Манно С., Шена Ф.П. (2003). «Основанный на фактах» обзор терапевтических возможностей IgA-нефропатии: оценка и критика ». Являюсь. J. Kidney Dis. 41 (6): 1129–39. Дои:10.1016 / S0272-6386 (03) 00344-5. PMID 12776264.
- ^ Диллон Дж. Дж. (1997). «Терапия рыбьим жиром при IgA-нефропатии: эффективность и вариабельность между исследованиями». Варенье. Soc. Нефрол. 8 (11): 1739–44. PMID 9355077.
- ^ Bartosik LP, Lajoie G, Sugar L, Cattran DC (2001). «Прогнозирование прогрессирования IgA-нефропатии». Являюсь. J. Kidney Dis. 38 (4): 728–35. Дои:10.1053 / ajkd.2001.27689. PMID 11576875.
- ^ Heberden W. Commentarii Di Morborium Historia et Curatione. Лондон: Пейн, 1801.
- ^ Бергер Дж, Хинглэйс Н. (1968). "Les Depots Intercapillaires d'IgA-IgG". Дж Урол Нефрол. 74: 694–95.
внешняя ссылка
| Классификация | |
|---|---|
| Внешние ресурсы |