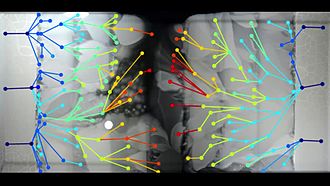
Список устойчивых к антибиотикам бактерий - Википедия - List of antibiotic-resistant bacteria
А список устойчивых к антибиотикам бактерий представлен ниже. Эти бактерии показали устойчивость к антибиотикам (или устойчивость к противомикробным препаратам ).
Фермент NDM-1 (металло-бета-лактамаза-1 Нью-Дели)
НДМ-1 является фермент что делает бактерии устойчив к широкому спектру бета-лактамные антибиотики.
NDM-1 (металло-бета-лактамаза-1 из Нью-Дели) возник в Индии. В индийских больницах внутрибольничные инфекции распространены, и с появлением новых супер-ошибок в Индии это может сделать их опасными.[2] Картирование проб сточных вод и водоснабжения, которые были положительными по NDM-1, указывает на широкое распространение инфекции в Нью-Дели еще в 2011 году.[2]
NDM-1 был впервые обнаружен в Клебсиелла пневмонии изолировать от Шведский пациент Индийский происхождения в 2008 году. Позже он был обнаружен у бактерий в Индия, Пакистан, то объединенное Королевство, Соединенные Штаты,[3] Канада[4] и Япония.[5]
Грамм положительный
Clostridium difficile
Clostridium difficile это нозокомиальный возбудитель, вызывающий диарейные заболевания во всем мире.[6][7] Диарея, вызванная C. difficile может быть опасным для жизни. Инфекции чаще всего встречаются у людей, которые недавно прошли курс лечения и / или антибиотиками. C. difficile инфекции обычно возникают во время госпитализации.[8]
Согласно отчету CDC за 2015 год, C. difficile вызвала почти 500 000 случаев заражения в Соединенных Штатах за год. По оценкам, с этими инфекциями было связано 15 000 смертей. По оценке CDC, C. difficile Стоимость заражения может составить 3,8 миллиарда долларов в течение 5 лет.[9]
C. difficile колит наиболее сильно связан с фторхинолоны, цефалоспорины, карбапенемы, и клиндамицин.[10][11][12]
Некоторые исследования показывают, что чрезмерное использование антибиотиков в животноводстве способствует вспышкам бактериальных инфекций, таких как C. difficile.[16]
Антибиотики, особенно с широким спектром действия (например, клиндамицин), нарушают нормальную кишечную флору. Это может привести к чрезмерному росту C. difficile, который процветает в этих условиях. За этим может последовать псевдомембранозный колит, вызывающий генерализованное воспаление толстой кишки и развитие «псевдомембраны», вязкого скопления воспалительных клеток, фибрина и некротических клеток [4]. Клиндамицин -устойчивый C. difficile был зарегистрирован как возбудитель крупных вспышек диарейных заболеваний в больницах Нью-Йорка, Аризоны, Флориды и Массачусетса в период с 1989 по 1992 год.[13] Географически рассредоточенные вспышки C. difficile штаммы, устойчивые к фторхинолон антибиотики, такие как ципрофлоксацин и левофлоксацин, также были зарегистрированы в Северной Америке в 2005 году.[14]
Энтерококк
С множественной лекарственной устойчивостью Enterococcus faecalis и Enterococcus faecium связаны с нозокомиальные инфекции.[15] Эти штаммы включают: пенициллин -устойчивый Энтерококк, устойчивый к ванкомицину Энтерококк, и линезолид -устойчивый Энтерококк.[16]
Микобактерии туберкулеза
Туберкулез (ТБ), устойчивый к антибиотикам, называется МЛУ ТБ (ТБ с множественной лекарственной устойчивостью). Ежегодно во всем мире от МЛУ-ТБ умирает 150 000 человек.[17] Этому способствовал рост эпидемии ВИЧ / СПИДа.[18]
Mycobacterium tuberculosis - облигатный патоген, который эволюционировал, чтобы обеспечить его постоянство в популяциях людей.[19] Это очевидно из того факта, что Mycobacterium tuberculosis должна вызывать заболевание легких, чтобы успешно передаваться от одного человека к другому. Туберкулез, более известный как туберкулез, имеет один из самых высоких показателей смертности среди патогенов в мире. Смертность не претерпела значительного снижения из-за растущей устойчивости к определенным антибиотикам.[17] Несмотря на то, что на создание вакцины были потрачены годы исследований и много рабочих часов, такой вакцины до сих пор не существует. Туберкулез имеет очень высокий уровень вирулентности, что отчасти связано с тем, что он чрезвычайно передается. Туберкулез считался одним из самых распространенных заболеваний, от которого не было лекарства до открытия стрептомицин к Селман Ваксман в 1943 г.[20] Однако вскоре у бактерий появилась устойчивость. С тех пор такие препараты, как изониазид и рифампицин был использован. М. туберкулез развивает устойчивость к лекарствам за счет спонтанных мутаций в геномах. Эти типы мутаций могут приводить к изменениям генотипа и фенотипа, которые могут способствовать репродуктивному успеху, поэтому они могут передаваться и превращаться в устойчивые бактерии. Устойчивость к одному препарату является обычным явлением, и поэтому лечение обычно проводится более чем одним препаратом. ТБ с широкой лекарственной устойчивостью (ШЛУ-ТБ) - это ТБ, устойчивый к препаратам второго ряда.[18][21]
Сопротивление Микобактерии туберкулеза к изониазид, рифампицин, и другие распространенные методы лечения становятся все более актуальной клинической проблемой. Доказательств наличия плазмид у этих бактерий нет.[22] М. туберкулез не имеют возможности взаимодействовать с другими бактериями для обмена плазмидами.[22][23]
Mycoplasma genitalium
Mycoplasma genitalium это небольшая патогенная бактерия, которая живет на мерцательных эпителиальных клетках мочевыводящих и половых путей человека. До сих пор остается спорным вопрос о том, следует ли признать эту бактерию возбудителем, передающимся половым путем. Заражение Mycoplasma genitalium иногда проявляется клиническими симптомами или комбинацией симптомов, но иногда может протекать бессимптомно. Это вызывает воспаление в уретра (уретрит ) как у мужчин, так и у женщин, что связано с слизисто-гнойные выделения в мочевыводящих путях и жжение при мочеиспускании.
Лечение Mycoplasma genitalium инфекции становятся все труднее из-за быстрого развития множественной лекарственной устойчивости, а диагностика и лечение еще больше затрудняются тем фактом, что М. genitalium инфекции обычно не обнаруживаются.[24] Азитромицин является наиболее распространенным лечением первой линии, но обычно применяемое лечение азитромицином разовой дозой в 1 грамм может привести к развитию устойчивости бактерий к азитромицину.[25] Альтернативное пятидневное лечение азитромицином не показало развития устойчивости к противомикробным препаратам.[26] Эффективность азитромицина против М. genitalium существенно снизился, что, как считается, происходит за счет SNP в гене 23S рРНК. Считается, что одни и те же SNP ответственны за устойчивость к джозамицин который прописан в некоторых странах.[27] Моксифлоксацин может использоваться в качестве лечения второй линии, если азитромицин не может уничтожить инфекцию. Однако резистентность к моксифлоксацину наблюдается с 2007 г., предположительно, из-за парк SNP.[27][28] Тетрациклины, включая доксициклин, имеют низкий уровень клинической эрадикации М. genitalium инфекции.[29] Было описано несколько случаев, когда доксициклин, азитромицин и моксифлоксацин не помогли, но пристинамицин все еще смог искоренить инфекцию.[27]
Золотистый стафилококк
Золотистый стафилококк является одним из основных резистентных патогенов. Найдено на слизистые оболочки и человеческая кожа Примерно у трети населения он чрезвычайно легко адаптируется к давлению антибиотиков. Это была одна из первых бактерий, у которых пенициллин резистентность была обнаружена - в 1947 году, всего через четыре года после начала массового производства препарата. Метициллин был тогда предпочтительным антибиотиком, но с тех пор был заменен на оксациллин из-за значительной токсичности для почек. Метициллин-устойчивый Золотистый стафилококк (MRSA) был впервые обнаружен в Великобритании в 1961 году и сейчас «довольно распространен» в больницах.[нужна цитата ]. MRSA стал причиной 37% смертельных случаев сепсис в Великобритания в 1999 г. по сравнению с 4% в 1991 г. Половина всех S. aureus инфекции в нас устойчивы к пенициллину, метициллину, тетрациклин и эритромицин.
Стрептококк
Streptococcus pyogenes (Группа А Стрептококк: GAS) инфекции обычно можно лечить разными антибиотиками. Штаммы S. pyogenes устойчивы к макролид появились антибиотики; однако все штаммы остаются одинаково восприимчивыми к пенициллин.[30]
Сопротивление Пневмококк до пенициллина и других бета-лактамов растет во всем мире. Основной механизм устойчивости включает введение мутаций в гены, кодирующие пенициллин-связывающие белки. Считается, что избирательное давление играет важную роль, а использование бета-лактамных антибиотиков считается фактором риска инфицирования и колонизации. S. pneumoniae Ответственный за пневмония, бактериемия, средний отит, менингит, синусит, перитонит и артрит.[30]
Грамотрицательный
Campylobacter
Campylobacter вызывает диарею (часто с кровью), лихорадку и спазмы в животе. Также могут возникнуть серьезные осложнения, такие как временный паралич. Врачи полагаются на ципрофлоксацин и азитромицин для лечения пациентов с тяжелым заболеванием, хотя Campylobacter проявляет устойчивость к этим антибиотикам.[8]
Neisseria gonorrhoeae
Neisseria gonorrhoeae - возбудитель, передающийся половым путем, вызывающий гонорея, заболевание, передающееся половым путем, которое может привести к выделениям и воспалению в уретре, шейке матки, глотке или прямой кишке.[8] Это может вызвать боль в области таза, боль при мочеиспускании, выделения из полового члена и влагалища, а также системные симптомы. Это также может вызвать серьезные репродуктивные осложнения.[8]
Гамма-протеобактерии
Энтеробактерии
По данным на 2013 г., трудноизлечимые или неизлечимые инфекции устойчивые к карбапенемам Enterobacteriaceae (CRE), также известная как Enterobacteriaceae, продуцирующая карбапенемазу (CPE), растет среди пациентов в медицинских учреждениях. CRE устойчивы почти ко всем доступным антибиотикам. Почти половина пациентов больниц, которые заражаются CRE-инфекцией кровотока, умирают от инфекции.[8]
Клебсиелла пневмонии
Klebsiella pneumoniae карбапенемаза (КПК ) -продуцирующие бактерии представляют собой группу новых высокоустойчивых к лекарственным средствам грамотрицательных бацилл, вызывающих инфекции, связанные со значительной заболеваемостью и смертностью, заболеваемость которой быстро растет в различных клинических условиях по всему миру. Клебсиелла пневмонии включает многочисленные механизмы устойчивости к антибиотикам, многие из которых расположены на высокомобильных генетических элементах.[31] Карбапенем антибиотики (до сих пор часто применяемые в качестве последнего средства для лечения устойчивых инфекций), как правило, неэффективны против организмов, продуцирующих KPC.[32]
Сальмонелла и Кишечная палочка
Заражение кишечная палочка и Сальмонелла может возникнуть в результате употребления зараженной пищи и загрязненная вода. Обе эти бактерии хорошо известны тем, что вызывают внутрибольничные (связанные с больницей) инфекции, и часто эти штаммы, обнаруживаемые в больницах, устойчивы к антибиотикам из-за адаптации к широкому распространению антибиотиков.[33] Когда обе бактерии распространяются, возникают серьезные проблемы со здоровьем. Многие люди попадают в больницу каждый год после заражения, в результате чего некоторые умирают. С 1993 года некоторые штаммы Кишечная палочка стали устойчивыми ко многим типам фторхинолоновые антибиотики.[нужна цитата ]
Хотя одна мутация играет огромную роль в развитии устойчивости к антибиотикам, исследование 2008 года показало, что высокая выживаемость после воздействия антибиотиков не может быть объяснена одной мутацией.[34] Это исследование было сосредоточено на развитии резистентности у Кишечная палочка к трем антибиотическим препаратам: ампициллину, тетрациклину и налидиксовой кислоте. Исследователи обнаружили, что некоторая устойчивость к антибиотикам у Кишечная палочка возникло в результате эпигенетического наследования, а не прямого наследования мутировавшего гена. Это было дополнительно подтверждено данными, показывающими, что возвращение к чувствительности к антибиотикам также было относительно частым. Это можно было объяснить только эпигенетикой.[34] Эпигенетика это тип наследования, при котором изменяется экспрессия генов, а не сам генетический код. Это изменение экспрессии генов может происходить многими способами, в том числе: метилирование ДНК и гистон модификация; однако важным моментом является то, что как наследование случайных мутаций, так и эпигенетических маркеров может привести к экспрессии генов устойчивости к антибиотикам.[34]
Устойчивость к полимиксины впервые появился в 2011 году.[35] Более простой способ распространения этого сопротивления - плазмида известный как MCR-1 был обнаружен в 2015 году.[35]
Pseudomonadales
Acinetobacter
Acinetobacter представляет собой грамотрицательные бактерии, вызывающие пневмонию или инфекции кровотока у тяжелобольных. С множественной лекарственной устойчивостью Acinetobacter стали очень устойчивы к антибиотикам.[8]
5 ноября 2004 г. Центры по контролю и профилактике заболеваний (CDC) сообщил о росте числа Acinetobacter baumannii инфекции кровотока у пациентов в военных медицинских учреждениях, в которых военнослужащие получили ранения в Ирак /Кувейт регион во время Операция иракская свобода И в Афганистан в течение Операция "Несокрушимая свобода" были обработаны. Большинство из них показали множественная лекарственная устойчивость (MRAB), с несколькими изолятами, устойчивыми ко всем протестированным препаратам.[36][37]
Синегнойная палочка
Синегнойная палочка очень распространен условно-патогенный микроорганизм. Одна из наиболее тревожных характеристик P. aeruginosa его низкая чувствительность к антибиотикам, что объясняется согласованным действием насосы для оттока нескольких лекарственных препаратов с хромосомно-кодируемыми генами устойчивости к антибиотикам (например, МЕКСАБ-ОПРМ, mexXY) и низкая проницаемость клеточных оболочек бактерий.[38] P. aeruginosa обладает способностью продуцировать 4-гидрокси-2-алкилхинолины (HAQ), и было обнаружено, что HAQ обладают прооксидантным действием и сверхэкспрессируют умеренно повышенную чувствительность к антибиотикам. В исследовании экспериментировали с P. aeruginosa биопленки и обнаружили, что нарушение работы генов relA и spoT вызывает инактивацию строгого ответа (SR) в клетках с ограничением питательных веществ, что делает клетки более восприимчивыми к антибиотикам.[39]
Смотрите также
Рекомендации
- ^ Байм, Михаил; Либерман, Тами Д .; Келсич, Эрик Д .; Чайт, Реми; Гросс, Ротем; Елин, Идан; Кишони, Рой (09.09.2016). «Пространственно-временная микробная эволюция на антибиотических ландшафтах». Наука. 353 (6304): 1147–1151. Bibcode:2016Научный ... 353.1147B. Дои:10.1126 / science.aag0822. ISSN 0036-8075. ЧВК 5534434. PMID 27609891.
- ^ а б Уолш, Тимоти Р.; Недели, Янис; Ливермор, Дэвид М; Толеман, Марк А (2011). «Распространение NDM-1-положительных бактерий в окружающей среде Нью-Дели и его последствия для здоровья человека: исследование точечной распространенности в окружающей среде». Ланцетные инфекционные болезни. 11 (5): 355–362. Дои:10.1016 / с 1473-3099 (11) 70059-7. PMID 21478057.
- ^ Мэрилин Маркионе (13 сентября 2010 г.). «Новые лекарственно-устойчивые супербактерии обнаружены в 3 штатах». Бостон Глобус.
- ^ Мадлен Уайт (21 августа 2010 г.). «В GTA обнаружен супербак». Торонто Стар.
- ^ Юаса, Шино (8 сентября 2010 г.). «Япония подтверждает первый случай гена супербактерии». Бостонский глобус.
- ^ Гердинг Д. Н., Джонсон С., Петерсон Л. Р., Маллиган М. Е., Сильва Дж. (1995). «Диарея и колит, связанные с Clostridium difficile». Заразить. Control Hosp. Эпидемиол. 16 (8): 459–477. Дои:10.1086/648363. PMID 7594392.
- ^ McDonald LC (2005). "Clostridium difficile: ответ на новую угрозу от старого врага ". Заразить. Control Hosp. Эпидемиол. 26 (8): 672–5. Дои:10.1086/502600. PMID 16156321.
- ^ а б c d е ж «Наибольшие угрозы - устойчивость к антибиотикам / противомикробным препаратам - CDC». www.cdc.gov. Получено 2016-05-05.
- ^ "Пресс-релизы CDC". CDC. Январь 2016. Получено 2016-05-05.
- ^ Baxter R, Ray GT, Fireman BH (январь 2008 г.). «Исследование случай-контроль использования антибиотиков и последующей диареи, связанной с Clostridium difficile, у госпитализированных пациентов». Инфекционный контроль и больничная эпидемиология. 29 (1): 44–50. Дои:10.1086/524320. PMID 18171186.
- ^ Гиффорд А.Х., Киркланд КБ (декабрь 2006 г.). «Факторы риска диареи, связанной с Clostridium difficile, в онкологическом отделении для взрослых». Европейский журнал клинической микробиологии и инфекционных заболеваний. 25 (12): 751–5. Дои:10.1007 / s10096-006-0220-1. PMID 17072575. S2CID 23822514.
- ^ Палмор Т.Н., Сон С., Малак С.Ф., Иган Дж., Сепковиц К.А. (август 2005 г.). «Факторы риска приобретения диареи, связанной с Clostridium difficile, среди амбулаторных пациентов онкологической больницы». Инфекционный контроль и больничная эпидемиология. 26 (8): 680–4. Дои:10.1086/502602. ЧВК 5612438. PMID 16156323.
- ^ Джонсон С., Самор М.Х., Фэрроу К.А., Киллгор Г.Е., Теновер ФК, Лира Д., Руд Джи, ДеГиролами П., Балч А.Л., Рафферти М.Э., Груш С.М., Гердинг Д.Н. (1999). "Эпидемии диареи, вызванные устойчивым к клиндамицину штаммом Clostridium difficile в четырех больницах ». Медицинский журнал Новой Англии. 341 (23): 1645–1651. Дои:10.1056 / NEJM199911253412203. PMID 10572152.
- ^ Лу В.Г., Пуарье Л., Миллер М.А., Огтон М., Либман, доктор медицины, Мишо С., Бурголт А.М., Нгуен Т., Френетт С., Келли М., Вибьен А., Брассард П., Фенн С., Дьюар К., Хадсон Т.Дж., Хорн Р., Рене П. , Мончак Y, Даскаль А (2005). «Преимущественно клональная мультиинституциональная вспышка диареи, связанной с Clostridium difficile, с высокой заболеваемостью и смертностью». N Engl J Med. 353 (23): 2442–9. Дои:10.1056 / NEJMoa051639. PMID 16322602.
- ^ Хидрон А.И., Эдвардс-младший, Патель Дж., Хоран Т.С., Сиверт Д.М., Поллок Д.А., Фридкин С.К. (ноябрь 2008 г.). Группа национальной сети безопасности здравоохранения; Участвующие объекты национальной сети безопасности здравоохранения. «Ежегодное обновление NHSN: устойчивые к противомикробным препаратам патогены, связанные с инфекциями, связанными со здравоохранением: годовой сводный отчет по данным, переданным в Национальную сеть безопасности здравоохранения в Центрах контроля и профилактики заболеваний, 2006–2007 гг.» Инфекционный контроль Hosp Epidemiol. 29 (11): 996–1011. Дои:10.1086/591861. PMID 18947320.
- ^ Кристич, Кристофер Дж .; Райс, Луи Б .; Ариас, Сезар А. (01.01.2014). Гилмор, Майкл С .; Clewell, Don B .; Айк, Ясуёси; Шанкар, Натан (ред.). Энтерококковая инфекция - лечение и устойчивость к антибиотикам. Бостон: Массачусетский глазной и ушной лазарет. PMID 24649502.
- ^ а б «Устойчивость к противомикробным препаратам по-прежнему представляет угрозу общественному здоровью: беседа с Эдвардом Дж. Септимусом, доктором медицины, FIDSA, FACP, FSHEA, клиническим профессором внутренней медицины Техасского центра медицинских наук A&M». Агентство медицинских исследований и качества. 2013-04-17. Получено 2013-09-26.
- ^ а б LoBue P (2009). «Туберкулез с широкой лекарственной устойчивостью». Современное мнение об инфекционных заболеваниях. 22 (2): 167–73. Дои:10.1097 / QCO.0b013e3283229fab. PMID 19283912. S2CID 24995375.
- ^ Brites, D; Gagneux, S (17 апреля 2013 г.). «Совместная эволюция Mycobacterium tuberculosis и Homo sapiens, Brites, D., & Gagneux, S. (2015)». Иммунол Рев. 264 (1): 6–24. Дои:10.1111 / imr.12264. ЧВК 4339235. PMID 25703549.
- ^ Герцог Х (1998). «История туберкулеза». Дыхание. 65 (1): 5–15. Дои:10.1159/000029220. PMID 9523361.
- ^ Гао, Цянь; Ли, Ся (2010). «Передача туберкулеза с множественной лекарственной устойчивостью». Открытие лекарств сегодня: механизмы болезни. 7: e61 – e65. Дои:10.1016 / j.ddmec.2010.09.006.
- ^ а б Зайнуддин З.Ф., Дейл Дж.В. (1990). «Есть ли у Mycobacterium tuberculosis плазмиды?». Бугорок. 71 (1): 43–9. Дои:10.1016 / 0041-3879 (90) 90060-л. PMID 2115217.
- ^ Louw GE, Уоррен RM, Гей ван Питтиус NC, McEvoy CR, Van Helden PD, Victor TC (2009). «Акт баланса: отток / приток при устойчивости микобактериальных препаратов». Противомикробные препараты и химиотерапия. 53 (8): 3181–9. Дои:10.1128 / AAC.01577-08. ЧВК 2715638. PMID 19451293.
- ^ Сунета, Сони; Паркхаус, Энди; Джиллиан, Дин (24 апреля 2017 г.). «Макролидная и хинолонорезистентная Mycoplasma genitalium у мужчины с хроническим уретритом: верхушка британского айсберга? ". Инфекции, передающиеся половым путем. 93 (8): 556–557. Дои:10.1136 / sextrans-2016-053077. PMID 28438948. S2CID 9178150. Получено 6 октября 2017.
- ^ Yew, H. S .; Андерсон, Т .; Coughlan, E .; Верно, А. (2011). "Индуцированная устойчивость к макролидам у Mycoplasma genitalium изоляты от пациентов с рецидивирующим негонококковым уретритом ». Журнал клинической микробиологии. 49 (4): 1695–1696. Дои:10.1128 / JCM.02475-10. ЧВК 3122813. PMID 21346049.
- ^ Анагриус, Карин; Лоре, Бритта; Йенсен, Йорген Сков; Коенье, Том (2013). "Лечение Mycoplasma genitalium. Наблюдения в шведской клинике ЗППП ». PLOS ONE. 8 (4): e61481. Bibcode:2013PLoSO ... 861481A. Дои:10.1371 / journal.pone.0061481. ЧВК 3620223. PMID 23593483.
- ^ а б c Унемо, Магнус; Йенсен, Йорген С. (10 января 2017 г.). «Устойчивые к противомикробным препаратам инфекции, передаваемые половым путем: гонорея и Mycoplasma genitalium". Обзоры природы Урология. 14 (3): 139–125. Дои:10.1038 / nrurol.2016.268. PMID 28072403. S2CID 205521926.
- ^ «Варианты лечения Mycoplasma Genitalium». www.theonlineclinic.co.uk.
- ^ Jensen, J.S .; Cusini, M .; Gomberg, M .; Мои, М. (9 августа 2016 г.). "Европейские директивы по Mycoplasma genitalium инфекции ". Журнал Европейской академии дерматологии и венерологии. 30 (10): 1650–1656. Дои:10.1111 / jdv.13849. PMID 27505296.
- ^ а б Альбрих В.К., Монне Д.Л., Харбарт С. (2004). «Давление выбора антибиотиков и устойчивость к Streptococcus pneumoniae и Streptococcus pyogenes». Emerg. Заразить. Дис. 10 (3): 514–7. Дои:10.3201 / eid1003.030252. ЧВК 3322805. PMID 15109426.
- ^ Хадсон, Кори; Бент, Захари; Мигер, Роберт; Уильямс, Келли (7 июня 2014 г.). «Детерминанты устойчивости и мобильные генетические элементы штамма Klebsiella pneumoniae, кодирующего NDM-1». PLOS ONE. 9 (6): e99209. Bibcode:2014PLoSO ... 999209H. Дои:10.1371 / journal.pone.0099209. ЧВК 4048246. PMID 24905728.
- ^ Арнольд Р.С., Том К.А., Шарма С., Филлипс М., Кристи Джонсон Дж., Морган Диджей (2011). «Появление бактерий, продуцирующих карбапенемазу Klebsiella pneumoniae». Южный медицинский журнал. 104 (1): 40–5. Дои:10.1097 / SMJ.0b013e3181fd7d5a. ЧВК 3075864. PMID 21119555.
- ^ Дэвис Дж, Дэвис Д. (2010). «Истоки и эволюция устойчивости к антибиотикам». Микробиол Мол Биол Рев. 74 (3): 417–433. Дои:10.1128 / MMBR.00016-10. ЧВК 2937522. PMID 20805405.
- ^ а б c Адам М, Мурали Б., Гленн Н.О., Поттер СС (2008). «Развитие устойчивости бактерий к антибиотикам на основе эпигенетического наследования». BMC Evol. Биол. 8: 52. Дои:10.1186/1471-2148-8-52. ЧВК 2262874. PMID 18282299.
- ^ а б Рирдон, Сара (21 декабря 2015 г.). «Распространение гена устойчивости к антибиотикам еще не означает бактериального апокалипсиса». Природа. Дои:10.1038 / природа.2015.19037. S2CID 182042290.
- ^ Центры по профилактике заболеваний (CDC). (2004). «Инфекции Acinetobacter baumannii среди пациентов в военных медицинских учреждениях, лечящих раненых военнослужащих США, 2002–2004 годы». MMWR Morb. Смертный. Wkly. Представитель. 53 (45): 1063–6. PMID 15549020.
- ^ «Реферат по болезни Acinetobacter baumannii: Acinetobacter baumannii: новая угроза с множественной лекарственной устойчивостью».
сайт только для членства
- ^ Пул К. (2004). «Опосредованная оттоком множественная резистентность у грамотрицательных бактерий». Клиническая микробиология и инфекции. 10 (1): 12–26. Дои:10.1111 / j.1469-0691.2004.00763.x. PMID 14706082.
- ^ Nguyen D, Joshi-Datar A, Lepine F, Bauerle E, Olakanmi O, Beer K, McKay G, Siehnel R, Schafhauser J, Wang Y, Britigan BE, Singh PK (2011). «Активное голодание опосредует толерантность к антибиотикам в биопленках и бактериях с ограниченным содержанием питательных веществ». Наука. 334 (6058): 982–6. Bibcode:2011Наука ... 334..982N. Дои:10.1126 / science.1211037. ЧВК 4046891. PMID 22096200.
внешняя ссылка
- Список устойчивых к антибиотикам бактерий в Керли
- Анимация устойчивости к антибиотикам
- Рекомендации CDC «Управление микроорганизмами с множественной лекарственной устойчивостью в медицинских учреждениях, 2006 г.»
- Проект управления противомикробными препаратами, на Центр исследований и политики в области инфекционных заболеваний (CIDRAP), Университет Миннесоты