RHEB - RHEB
RHEB также известен как Гомолог Ras обогащен в мозге (RHEB) - это GTP-связывающий белок который повсеместно экспрессируется у людей и других млекопитающих. Белок в значительной степени участвует в путь mTOR и регуляция клеточного цикла.[5]
RHEB - недавно обнаруженный член суперсемейства Ras. Будучи родственником Рас сверхэкспрессия RHEB может наблюдаться во многих карциномах человека.[6] По этой причине способы ингибирования RHEB для контроля пути mTOR изучаются как возможные способы лечения неконтролируемого роста опухолевых клеток при некоторых заболеваниях, особенно при туберозный склероз.[7]
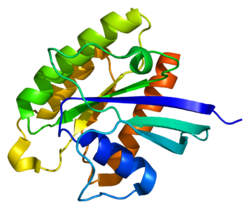
Структура


Rheb представляет собой белковый мономер массой 21 кДа, состоящий из 184 аминокислот.[5] Первые 169 аминокислот на N-конце составляют домен GTPase, а остальные аминокислоты являются частью гипервариабельной области, заканчивающейся на C-конце в мотиве CAAX (C - цистеин, A - алифатическая аминокислота, X - С-концевая аминокислота).[8]
Белок - это липидно-заякоренный, белок клеточной мембраны с пятью повторами GTP-связывающей области, связанной с RAS.[5] Также присутствуют «переключающие» области I и II, которые претерпевают конформационные изменения при перемещении между GTP-связанными (активированными) и GDP-связанными (неактивными) формами.[8]
RHEB выражается RHEB ген у человека.[9] Было нанесено на карту три псевдогена, два на хромосоме 10 и один на хромосоме 22.[5]
Функция
Активация mTORC1
RHEB жизненно важен для регулирования роста и клеточный цикл прогрессирование из-за его роли в инсулине / TOR /S6K сигнальный путь.[10] Механистическая мишень комплекса рапамицина 1 (mTORC1 ) представляет собой серин / треониновая киназа, активация которой приводит к каскадам фосфорилирования внутри клетки, которые приводят к росту и пролиферации клеток.[11] RHEB располагается на лизосома для активации mTORC1 и Rag7 белки локализуют mTORC1 в лизосоме и Комплекс Рагулятор-Тряпка, позволяя RHEB активировать белок.[12] RHEB действует как активатор mTORC1 в его GTP-связанной форме, поэтому GTP Связанный RHEB активирует рост и пролиферацию клеток внутри клетки.
Независимые функции mTORC1
RHEB может служить регулятором для других белков, независимых от mTORC1. Например, RHEB является активатором синтеза нуклеотидов, связывая карбамоилфосфатсинтетазу 2, аспартат-транскарбамилазу и дигидрооротазу (CAD ), фермент, необходимый для de novo синтез пиримидиновых нуклеотидов.[13] Увеличенный пул нуклеотидов в клетке может привести к увеличению пролиферации клеток. mTORC1 также является регулятором CAD, поэтому и RHEB, и mTORC1 участвуют в контроле уровня нуклеотидов в клетке.[13] 5 'аденозин-монофосфат-активированная протеинкиназа (AMPK) также оказался эффектором для RHEB.[14] AMPK - это протеинкиназа, которая запускает каскад фосфорилирования, ведущий к аутофагии. В исследованиях на крысах RHEB активирует AMPK.[14] Также было обнаружено, что RHEB взаимодействует с эффекторами выше по пути mTOR. Фосфолипаза D1 (PLD1) находится выше по пути mTOR и служит положительным эффектором для mTORC1.[15]
Прочие функции
RHEB может участвовать в нейрональной пластичности. Эта функция является новой и обычно не связана с белками Ras. Дефицит RHEB в переднем мозге эмбрионов мышей связан с уменьшением миелинизация из-за уменьшения зрелых олигодендроциты.[8]
В исследованиях мышей с нокаутом RHEB с помощью окрашивания гематоксилин-эозином было показано, что развитие сердца сильно нарушено. Сердечные миоциты не увеличиваются в размерах в достаточной степени, что указывает на необходимость функции RHEB mTOR. Это предполагает, что RHEB и активация пути mTOR необходимы для правильного сердечного развития у эмбрионов мышей.[16]

Отличия от суперсемейства Ras
RHEB функционирует иначе, чем другие белки суперсемейства Ras.[8] Подобно белкам суперсемейства Ras, этот белок обладает ГТФазной активностью и перемещается между GDP-связанной формой и GTP-связанной формой, и для этой активности требуется фарнезилирование белка. Однако, в отличие от таковых в суперсемействе Ras, конформационное изменение при перемещении между формами влияет только на переключатель I, тогда как переключатель II остается относительно стабильным из-за различий во вторичной структуре. Переключатель Ras II образует длинную α-спиральную структуру между челночными перемещениями, в то время как переключатель RHEB II имеет более нетипичную конструкцию, позволяющую выполнять новые функции.[17] Такая конформация вызывает снижение собственной скорости гидролиза GTP по сравнению с РАН из-за того, что каталитический Asp65 в области переключателя II RHEB блокируется от активного центра.[11]
Регулирование
Активность RHEB по гидролизу GTP по своей сути медленная, и форма, связанная с GTP, более распространена, поэтому RHEB скорее активен, чем неактивен в клетке.[11] Его активность строго регулируется внутри клетки белками, подавляющими опухоль, которые образуют комплекс TSC. В частности, TSC2 субъединица, туберин комплекса взаимодействует с RHEB и ингибирует его, регулируя белок. Туберин стимулирует RHEB гидролизовать GTP, тем самым инактивируя его.[18]
Туберозный склероз
Туберозный склероз представляет собой аутосомно-доминантное заболевание, при котором гены, необходимые для экспрессии белков, подавляющих опухоль, которые образуют комплекс TSC, мутированы или отсутствуют, поэтому комплекс TSC не может функционировать должным образом.[19] Это может привести к нарушению регуляции многих сигнальных белков и эффекторов внутри клетки, включая RHEB. Нерегулируемая активность RHEB может привести к неконтролируемому росту и делению клеток, что в конечном итоге может привести к образованию опухолей.[8]
Взаимодействия
RHEB был показан взаимодействовать с:
- Атаксия телеангиэктазия мутировала (Банкомат )[20]
- Атаксия, телеангиэктазия и Rad3-связанные (ATR )[20]
- 5 'AMP-активированная протеинкиназа (АМПК )[14]
- RAF протоонкоген серин / треонин-протеинкиназа (C-Raf )[20][21][22]
- Мишень рапамицинового комплекса 1 для млекопитающих (mTORC1 ),[20][23][24][25]
- Фосфолипаза D1 (PLD1 )[15]
- Регулирующий белок mTOR (RPTOR )[20]
- Комплекс туберозного склероза (TSC )[18][20][26][27][28][29] и
- Карбамоил-фосфатсинтетаза 2, аспартат-транскарбамоилаза, дигидрооротаза (CAD)[13]
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000106615 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000028945 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ а б c d «Гомолог RHEB Ras, обогащенный в мозге [Homo sapiens (человек)]». Джин - NCBI. Национальный центр биотехнологической информации, Национальные институты здравоохранения США.
- ^ Лу Чж, Шварцман МБ, Ли А.Ю., Шао Дж. М., Мюррей М. М., Кладни Р. Д., Фан Д., Краевски С., Чан Дж. Г., Миллс, Великобритания, Арбейт Дж. М. (апрель 2010 г.). «У млекопитающих мишень активатора рапамицина RHEB часто сверхэкспрессируется в карциномах человека и является критической и достаточной для канцерогенеза эпителия кожи». Исследования рака. 70 (8): 3287–98. Дои:10.1158 / 0008-5472.CAN-09-3467. ЧВК 2855737. PMID 20388784.
- ^ Сугиура Х, Ясуда С., Кацурабаяси С., Кавано Х, Эндо К., Такасаки К., Ивасаки К., Итикава М., Кобаяси Т., Хино О, Ямагата К. (01.01.2015). «Активация Rheb нарушает формирование синапсов позвоночника из-за накопления синтенина в комплексе туберозного склероза». Nature Communications. 6: 6842. Дои:10.1038 / ncomms7842. PMID 25880340.
- ^ а б c d е Heard JJ, Fong V, Bathaie SZ, Tamanoi F (сентябрь 2014 г.). «Недавний прогресс в изучении GTPases семейства Rheb». Сотовая связь. 26 (9): 1950–7. Дои:10.1016 / j.cellsig.2014.05.011. ЧВК 4134338. PMID 24863881.
- ^ Мизуки Н., Кимура М., Оно С., Мията С., Сато М., Андо Х, Исихара М., Гото К., Ватанабэ С., Ямадзаки М., Оно А., Тагучи С., Окумура К., Ногами М., Тагучи Т., Андо А., Иноко Х. (Май 1996 г.). «Выделение кДНК и геномных клонов гена человеческого Ras-связанного GTP-связывающего белка и его хромосомная локализация в длинном плече хромосомы 7, 7q36». Геномика. 34 (1): 114–8. Дои:10.1006 / geno.1996.0248. PMID 8661031.
- ^ Patel PH, Thapar N, Guo L, Martinez M, Maris J, Gau CL, Lengyel JA, Tamanoi F (сентябрь 2003 г.). «ГТФаза Rheb дрозофилы необходима для развития клеточного цикла и роста клеток». Журнал клеточной науки. 116 (Pt 17): 3601–10. Дои:10.1242 / jcs.00661. PMID 12893813.
- ^ а б c Mazhab-Jafari MT, Marshall CB, Ishiyama N, Ho J, Di Palma V, Stambolic V, Ikura M (сентябрь 2012 г.). «Автоингибируемый неканонический механизм гидролиза GTP посредством Rheb поддерживает гомеостаз mTORC1». Структура. 20 (9): 1528–39. Дои:10.1016 / j.str.2012.06.013. PMID 22819219.
- ^ Groenewoud MJ, Zwartkruis FJ (август 2013 г.). «Реб и Рэгс объединяются в лизосоме, чтобы активировать mTORC1». Сделки Биохимического Общества. 41 (4): 951–5. Дои:10.1042 / BST20130037. PMID 23863162.
- ^ а б c Сато Т., Акасу Х., Шимоно В., Мацу К., Фудзивара Й., Шибагаки Ю., Херд Дж. Дж., Таманой Ф, Хаттори С. (январь 2015 г.). «Белок Rheb связывает белок CAD (карбамоилфосфатсинтетаза 2, аспартаттранскарбамоилаза и дигидрооротаза) GTP- и эффекторным доменом и влияет на его клеточную локализацию и активность карбамоилфосфатсинтетазы (CPSase)». Журнал биологической химии. 290 (2): 1096–105. Дои:10.1074 / jbc.M114.592402. ЧВК 4294477. PMID 25422319.
- ^ а б c Lacher MD, Pincheira R, Zhu Z, Camoretti-Mercado B, Matli M, Warren RS, Castro AF (декабрь 2010 г.). «Rheb активирует AMPK и снижает уровни p27Kip1 в Tsc2-нулевых клетках посредством mTORC1-независимых механизмов: последствия для пролиферации клеток и туморогенеза». Онкоген. 29 (50): 6543–56. Дои:10.1038 / onc.2010.393. PMID 20818424. S2CID 205531885.
- ^ а б Sun Y, Fang Y, Yoon MS, Zhang C, Roccio M, Zwartkruis FJ, Armstrong M, Brown HA, Chen J (июнь 2008 г.). «Фосфолипаза D1 является эффектором Rheb в пути mTOR». Труды Национальной академии наук Соединенных Штатов Америки. 105 (24): 8286–91. Дои:10.1073 / pnas.0712268105. ЧВК 2448829. PMID 18550814.
- ^ Тамай Т., Ямагути О, Хикосо С., Такеда Т., Танейке М, Ока Т, Оябу Дж., Муракава Т., Накаяма Х, Уно Й, Хори К., Нисида К., Соненберг Н., Шах А.М., Такеда Дж., Комуро И., Оцу К. (Апрель 2013 г.). «Rheb (гомолог Ras, обогащенный в головном мозге) -зависимая мишень для активации рапамицинового комплекса 1 (mTORC1) млекопитающих становится незаменимой для гипертрофического роста сердца после раннего постнатального периода». Журнал биологической химии. 288 (14): 10176–87. Дои:10.1074 / jbc.M112.423640. ЧВК 3617260. PMID 23426372.
- ^ Aspuria PJ, Tamanoi F (октябрь 2004 г.). «Семейство Rheb GTP-связывающих белков». Сотовая связь. 16 (10): 1105–12. Дои:10.1016 / j.cellsig.2004.03.019. PMID 15240005.
- ^ а б Кастро А.Ф., Ребхун Дж. Ф., Кларк Дж. Дж., Куиллиам Лос-Анджелес (август 2003 г.). «Rheb связывает комплекс 2 туберозного склероза (TSC2) и способствует активации киназы S6 в зависимости от рапамицина и фарнезилирования». Журнал биологической химии. 278 (35): 32493–6. Дои:10.1074 / jbc.C300226200. PMID 12842888.
- ^ Чидл Дж. П., Рив депутат, Сэмпсон Дж. Р., Квятковски Д. Д. (август 2000 г.). «Молекулярно-генетические достижения в туберозном склерозе». Генетика человека. 107 (2): 97–114. Дои:10.1007 / s004390000348. PMID 11030407. S2CID 10960505.
- ^ а б c d е ж Long X, Lin Y, Ortiz-Vega S, Yonezawa K, Avruch J (апрель 2005 г.). «Rheb связывает и регулирует киназу mTOR». Текущая биология. 15 (8): 702–13. Дои:10.1016 / j.cub.2005.02.053. PMID 15854902. S2CID 3078706.
- ^ Karbowniczek M, Cash T, Cheung M, Robertson GP, Astrinidis A, Henske EP (июль 2004 г.). «Регулирование активности киназы B-Raf с помощью туберина и Rheb является мишенью млекопитающих для рапамицина (mTOR) -независимого». Журнал биологической химии. 279 (29): 29930–7. Дои:10.1074 / jbc.M402591200. PMID 15150271.
- ^ Йи В.М., Уорли П.Ф. (февраль 1997 г.). «Rheb взаимодействует с киназой Raf-1 и может функционировать для интеграции сигналов, зависимых от фактора роста и протеинкиназы A». Молекулярная и клеточная биология. 17 (2): 921–33. Дои:10.1128 / mcb.17.2.921. ЧВК 231818. PMID 9001246.
- ^ Long X, Ortiz-Vega S, Lin Y, Avruch J (июнь 2005 г.). «Связывание Rheb с мишенью рапамицина у млекопитающих (mTOR) регулируется достаточностью аминокислот». Журнал биологической химии. 280 (25): 23433–6. Дои:10.1074 / jbc.C500169200. PMID 15878852.
- ^ Смит Е.М., Финн С.Г., Ти А.Р., Браун Г.Дж., Гордость К.Г. (май 2005 г.). «Белок туберозного склероза TSC2 не требуется для регуляции рапамицина-мишени млекопитающих с помощью аминокислот и определенных клеточных стрессов». Журнал биологической химии. 280 (19): 18717–27. Дои:10.1074 / jbc.M414499200. PMID 15772076.
- ^ Бернарди Р., Герна И., Джин Д., Гризенди С., Алимонти А., Теруя-Фельдштейн Дж., Кордон-Кардо С., Саймон М. К., Рафии С., Пандольфи П. П. (август 2006 г.). «ПМЛ ингибирует трансляцию HIF-1альфа и неоангиогенез посредством репрессии mTOR». Природа. 442 (7104): 779–85. Дои:10.1038 / природа05029. PMID 16915281. S2CID 4427427.
- ^ Иноки К., Ли И, Сюй Т., Гуань К.Л. (август 2003 г.). «Rheb GTPase является прямой мишенью для активности TSC2 GAP и регулирует передачу сигналов mTOR». Гены и развитие. 17 (15): 1829–34. Дои:10.1101 / gad.1110003. ЧВК 196227. PMID 12869586.
- ^ Garami A, Zwartkruis FJ, Nobukuni T, Joaquin M, Roccio M, Stocker H, Kozma SC, Hafen E, Bos JL, Thomas G (июнь 2003 г.). «Активация инсулином Rheb, медиатора передачи сигналов mTOR / S6K / 4E-BP, ингибируется TSC1 и 2» (PDF). Молекулярная клетка. 11 (6): 1457–66. Дои:10.1016 / с1097-2765 (03) 00220-х. PMID 12820960.
- ^ Чжан И, Гао Х, Соседо Л.Дж., Ру Б., Эдгар Б.А., Пан Д. (июнь 2003 г.). «Rheb является прямой мишенью белков-супрессоров опухоли туберозного склероза». Природа клеточной биологии. 5 (6): 578–81. Дои:10.1038 / ncb999. PMID 12771962. S2CID 13451385.
- ^ Цао Й, Камиока Й, Ёкои Н., Кобаяши Т., Хино О, Онодера М., Мотидзуки Н., Накаэ Дж. (Декабрь 2006 г.). «Взаимодействие FoxO1 и TSC2 индуцирует инсулинорезистентность через активацию млекопитающего-мишени пути рапамицина / p70 S6K». Журнал биологической химии. 281 (52): 40242–51. Дои:10.1074 / jbc.M608116200. PMID 17077083.
дальнейшее чтение
- Ямагата К., Сандерс Л.К., Кауфманн В.Е., Йи В., Барнс, Калифорния, Натанс Д., Уорли П.Ф. (июнь 1994 г.). «rheb, ген, регулируемый факторами роста и синаптической активностью, кодирует новый Ras-родственный белок». Журнал биологической химии. 269 (23): 16333–9. PMID 8206940.
- Громов П.С., Мадсен П., Томеруп Н., Селис Дж. Э. (декабрь 1995 г.). «Новый подход к клонированию экспрессии малых GTPases: идентификация, распределение в тканях и картирование хромосом человеческого гомолога rheb». Письма FEBS. 377 (2): 221–6. Дои:10.1016/0014-5793(95)01349-0. PMID 8543055. S2CID 23656670.
- Боналду М.Ф., Леннон Г., Соарес МБ (сентябрь 1996 г.). «Нормализация и вычитание: два подхода для облегчения открытия генов». Геномные исследования. 6 (9): 791–806. Дои:10.1101 / гр.6.9.791. PMID 8889548.
- Кларк Г.Дж., Кинч М.С., Роджерс-Грэм К., Себти С.М., Гамильтон А.Д., Der CJ (апрель 1997 г.). «Связанный с Ras белок Rheb является фарнезилированным и противодействует передаче сигналов и трансформации Ras». Журнал биологической химии. 272 (16): 10608–15. Дои:10.1074 / jbc.272.16.10608. PMID 9099708.
- Инохара Н., Динг Л., Чен С., Нуньес Дж. (Апрель 1997 г.). «Харакири, новый регулятор гибели клеток, кодирует белок, который активирует апоптоз и селективно взаимодействует с белками, способствующими выживанию, Bcl-2 и Bcl-X (L)». Журнал EMBO. 16 (7): 1686–94. Дои:10.1093 / emboj / 16.7.1686. ЧВК 1169772. PMID 9130713.
- Центр Сангера, The; Центр секвенирования генома Вашингтонского университета, The (ноябрь 1998 г.). «К полной последовательности человеческого генома». Геномные исследования. 8 (11): 1097–108. Дои:10.1101 / гр. 8.11.1097. PMID 9847074.
- Кита К., Ву Ю.П., Сугая С., Мория Т., Номура Дж., Такахаши С., Ямамори Х., Накадзима Н., Судзуки Н. (август 2000 г.). «Поиск генов, чувствительных к УФ-излучению в клетках человека с помощью дифференциального отображения мРНК: участие человеческого ras-связанного GTP-связывающего белка, Rheb, в восприимчивости к УФ». Сообщения о биохимических и биофизических исследованиях. 274 (3): 859–64. Дои:10.1006 / bbrc.2000.3220. PMID 10924367.
- Hanzal-Bayer M, Renault L, Roversi P, Wittinghofer A, Hillig RC (май 2002 г.). «Комплекс Arl2-GTP и PDE дельта: от структуры к функции». Журнал EMBO. 21 (9): 2095–106. Дои:10.1093 / emboj / 21.9.2095. ЧВК 125981. PMID 11980706.
- Табанкай А.П., Гау К.Л., Мачадо И.М., Ульманн Э.Дж., Гутманн Д.Х., Го Л., Таманой Ф. (октябрь 2003 г.). «Идентификация доминантно-отрицательных мутантов Rheb GTPase и их использование для выявления участия человеческого Rheb в активации p70S6K». Журнал биологической химии. 278 (41): 39921–30. Дои:10.1074 / jbc.M306553200. PMID 12869548.
- Tee AR, Manning BD, Roux PP, Cantley LC, Blenis J (август 2003 г.). «Генные продукты комплекса туберозного склероза, туберин и хамартин, контролируют передачу сигналов mTOR, действуя как белковый комплекс, активирующий GTPase, по отношению к Rheb». Текущая биология. 13 (15): 1259–68. Дои:10.1016 / S0960-9822 (03) 00506-2. PMID 12906785. S2CID 6519150.
внешняя ссылка
- RHEB + белок, + человек в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
Эта статья включает текст из Национальная медицинская библиотека США, который находится в всеобщее достояние.