Сверхкритическая жидкость - Supercritical fluid
А сверхкритическая жидкость (SCF[1]) представляет собой любое вещество на температура и давление выше его критическая точка, где отчетливо жидкость и газ фаз не существует, но ниже давления, необходимого для сжатия его в твердый.[2] Может изливаться сквозь пористые твердые тела, подобные газу, преодолевая массообмен ограничения, которые замедляют перенос жидкости через такие материалы. СКФ значительно превосходят газы по способности растворяться материалы, такие как жидкости или твердые тела. Кроме того, вблизи критической точки небольшие изменения давления или температуры приводят к большим изменениям в плотность, позволяя «настраивать» многие свойства сверхкритической жидкости.
Сверхкритические жидкости встречаются в атмосферы из газовые гиганты Юпитер и Сатурн, и, вероятно, в тех из ледяные гиганты Уран и Нептун. Вода в сверхкритическом состоянии находится на земной шар, например, вода, вытекающая из черные курильщики, вид подводного гидротермальный источник.[3] В ряде промышленных и лабораторных процессов они используются в качестве замены органический растворители. Углекислый газ и воды являются наиболее часто используемыми сверхкритическими жидкостями, которые используются для декафеинация и выработка энергии, соответственно.
Характеристики
В общих чертах, сверхкритические жидкости обладают свойствами между газом и жидкостью. В таблице 1 показаны критические свойства некоторых веществ, которые обычно используются в качестве сверхкритических жидкостей.
| Растворитель | Молекулярная масса | Критическая температура | Критическое давление | Критическая плотность |
|---|---|---|---|---|
| г / моль | K | МПа (банкомат ) | г / см3 | |
| Углекислый газ (CO2) | 44.01 | 304.1 | 7.38 (72.8) | 0.469 |
| Вода (ЧАС2O)† | 18.015 | 647.096 | 22.064 (217.755) | 0.322 |
| Метан (CH4) | 16.04 | 190.4 | 4.60 (45.4) | 0.162 |
| Этан (C2ЧАС6) | 30.07 | 305.3 | 4.87 (48.1) | 0.203 |
| Пропан (C3ЧАС8) | 44.09 | 369.8 | 4.25 (41.9) | 0.217 |
| Этилен (C2ЧАС4) | 28.05 | 282.4 | 5.04 (49.7) | 0.215 |
| Пропилен (C3ЧАС6) | 42.08 | 364.9 | 4.60 (45.4) | 0.232 |
| Метанол (CH3ОЙ) | 32.04 | 512.6 | 8.09 (79.8) | 0.272 |
| Этиловый спирт (C2ЧАС5ОЙ) | 46.07 | 513.9 | 6.14 (60.6) | 0.276 |
| Ацетон (C3ЧАС6O) | 58.08 | 508.1 | 4.70 (46.4) | 0.278 |
| Оксид азота (N2O) | 44.013 | 306.57 | 7.35 (72.5) | 0.452 |
† Источник: Международная ассоциация свойств воды и пара (IAPWS )[5]
Таблица 2 показывает плотность, коэффициент диффузии и вязкость для типичных жидкостей, газов и сверхкритических жидкостей.
| Плотность (кг / м3) | Вязкость (мкПа · с ) | Коэффициент диффузии (мм2/ с) | |
|---|---|---|---|
| Газы | 1 | 10 | 1–10 |
| Сверхкритические жидкости | 100–1000 | 50–100 | 0.01–0.1 |
| Жидкости | 1000 | 500–1000 | 0.001 |
Кроме того, нет поверхностное натяжение в сверхкритическом флюиде, так как нет границы раздела фаз жидкость / газ. Изменяя давление и температуру текучей среды, ее свойства можно «настроить» так, чтобы они стали более похожими на жидкость или более газообразными. Одно из наиболее важных свойств - растворимость материала в жидкости. Растворимость в сверхкритической жидкости имеет тенденцию увеличиваться с увеличением плотности жидкости (при постоянной температуре). Поскольку плотность увеличивается с давлением, растворимость имеет тенденцию к увеличению с давлением. Взаимосвязь с температурой немного сложнее. При постоянной плотности растворимость увеличивается с температурой. Однако вблизи критической точки плотность может резко упасть при небольшом повышении температуры. Поэтому вблизи критической температуры растворимость часто падает с повышением температуры, а затем снова возрастает.[7]
Смеси
Обычно сверхкритические жидкости полностью смешивающийся друг с другом, так что бинарная смесь образует единую газовую фазу, если критическая точка смеси превышена. Однако известны исключения в системах, в которых один компонент намного более летуч, чем другой, которые в некоторых случаях образуют две несмешивающиеся газовые фазы при высоком давлении и температурах выше критических точек компонентов. Такое поведение было обнаружено, например, в системах N2-NH3, NH3-CH4, ТАК2-N2 и н-бутан-H2О.[8]
Критическую точку бинарной смеси можно оценить как среднее арифметическое критических температур и давлений двух компонентов,
Для большей точности критическую точку можно рассчитать с помощью уравнения состояния, такой как Пенг-Робинсон, или же методы группового взноса. Другие свойства, такие как плотность, также можно рассчитать с помощью уравнений состояния.[9]
Фазовая диаграмма

На рисунках 1 и 2 показаны двумерные проекции фазовая диаграмма. На фазовой диаграмме давление-температура (рис.1) величина кипячение кривая разделяет газ и жидкая область и заканчивается в критической точке, где жидкая и газовая фазы исчезают, становясь единой сверхкритической фазой.
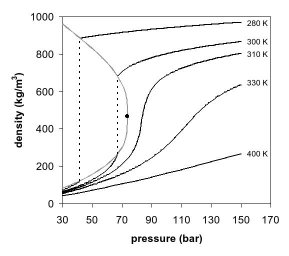
Появление единой фазы можно наблюдать и на фазовой диаграмме плотность - давление для диоксида углерода (рис. 2). При температуре значительно ниже критической, например 280 K, по мере увеличения давления газ сжимается и в конечном итоге (при температуре чуть более 40 бар ) конденсируется в более плотную жидкость, что приводит к разрыву линии (вертикальная пунктирная линия). Система состоит из 2-х фаз в равновесие, плотная жидкость и газ низкой плотности. По мере приближения к критической температуре (300 К) плотность газа в состоянии равновесия становится выше, а жидкости - ниже. В критической точке (304,1 К и 7,38 МПа (73,8 бар)) нет разницы в плотности, и две фазы становятся одной жидкой фазой. Таким образом, выше критической температуры газ нельзя сжижать под давлением. При температуре чуть выше критической (310 К), вблизи критического давления линия почти вертикальна. Небольшое увеличение давления вызывает большое увеличение плотности сверхкритической фазы. Многие другие физические свойства также показывают большие градиенты давления вблизи критической точки, например вязкость, то относительная диэлектрическая проницаемость и сила растворителя, которые все тесно связаны с плотностью. При более высоких температурах жидкость начинает вести себя больше как идеальный газ с более линейным соотношением плотность / давление, как видно на рисунке 2. Для двуокиси углерода при 400 К плотность увеличивается почти линейно с давлением.
Многие газы под давлением на самом деле являются сверхкритическими жидкостями. Например, у азота есть критическая точка 126,2 К (-147 ° C) и 3,4 МПа (34 бар). Следовательно, азот (или сжатый воздух) в газовом баллоне с давлением выше этого давления на самом деле является сверхкритической жидкостью. Их чаще называют постоянными газами. При комнатной температуре они намного выше своей критической температуры и, следовательно, ведут себя как почти идеальный газ, подобно CO.2 при 400 К. выше. Однако они не могут быть сжижены механическим давлением, если не охлаждаются ниже их критической температуры, требующей гравитационного давления, например, внутри газовые гиганты для получения жидкости или твердого вещества при высоких температурах.[нужна цитата ] Выше критической температуры повышенное давление может увеличить плотность настолько, чтобы SCF показывал плотность и поведение, подобные жидкости. При очень высоких давлениях SCF может быть сжат в твердое тело, потому что кривая плавления простирается вправо от критической точки на фазовой диаграмме P / T. В то время как давление, необходимое для сжатия сверхкритического CO2 в твердое тело может быть, в зависимости от температуры, до 570 МПа,[10] необходимое для затвердевания воды в сверхкритическом состоянии составляет 14 000 МПа.[11]
В Линия Fisher-Widom, то Widom line, или Линия Френкеля представляют собой термодинамические концепции, которые позволяют различать жидкоподобные и газоподобные состояния в сверхкритической жидкости.
В последние годы значительные усилия были посвящены исследованию различных свойств сверхкритических жидкостей. Это захватывающая область с долгой историей с 1822 года, когда барон Шарль Каньяр де ла Тур обнаружил сверхкритические жидкости, проводя эксперименты по изучению неоднородностей звука в герметичном стволе пистолета, заполненном различными жидкостями при высокой температуре.[12] В последнее время сверхкритические жидкости нашли применение в самых разных областях, от экстракции цветочного аромата из цветов до приложений в пищевой науке, таких как создание кофе без кофеина, функциональных пищевых ингредиентов, фармацевтических препаратов, косметики, полимеров, порошков, био- и функциональных продуктов. материалы, наносистемы, натуральные продукты, биотехнологии, ископаемое и биотопливо, микроэлектроника, энергия и окружающая среда. Во многом ажиотаж и интерес последнего десятилетия вызваны огромным прогрессом, достигнутым в увеличении мощности соответствующих экспериментальных инструментов. Разработка новых экспериментальных методов и улучшение существующих продолжает играть важную роль в этой области, при этом недавние исследования сосредоточены на динамических свойствах жидкостей.
Естественное явление
Гидротермальная циркуляция

Гидротермальная циркуляция происходит в земной коре там, где жидкость нагревается и начинает конвекцию. Считается, что эти жидкости достигают сверхкритических условий при различных условиях, таких как образование медно-порфировых отложений или высокотемпературная циркуляция морской воды на морском дне. На срединно-океанических хребтах эта циркуляция наиболее очевидна по появлению гидротермальных источников, известных как «черные курильщики». Это большие (метровые) дымовые трубы из сульфидных и сульфатных минералов, которые выводят флюиды до 400 ° C. Жидкости выглядят как большие черные клубящиеся облака дыма из-за осаждения растворенных металлов в жидкости. Вполне вероятно, что на глубине многие из этих выходных участков достигают сверхкритических условий, но большинство из них достаточно охлаждается к тому времени, когда они достигают морского дна, чтобы стать докритическими. Одно конкретное место выхода, Turtle Pits, показало короткий период сверхкритичности в месте выхода. Еще один сайт, Beebe в Каймановом желобе, как полагают, демонстрирует устойчивую сверхкритичность в вентиляционном отверстии.[13]
Планетарные атмосферы
Атмосфера Венера 96,5% углекислого газа и 3,5% азота. Поверхностное давление составляет 9,3 МПа (93 бара), а температура поверхности составляет 735 К, что выше критических точек обоих основных компонентов и делает приземную атмосферу сверхкритической жидкостью.
Внутренняя атмосфера Солнечной системы газовый гигант планеты состоят в основном из водорода и гелия при температурах значительно выше их критических точек. Газообразная внешняя атмосфера Юпитер и Сатурн плавно переходят в плотное жидкое внутреннее пространство, при этом характер переходных зон Нептун и Уран неизвестно. Теоретические модели внесолнечная планета Gliese 876 d создали океан сверхкритической жидкой воды под давлением со слоем твердого водяного льда под высоким давлением на дне.
Приложения
Извлечение сверхкритических жидкостей
Преимущества сверхкритическая флюидная экстракция (по сравнению с жидкостной экстракцией) заключаются в том, что она является относительно быстрой из-за низкой вязкости и высокой диффузионной способности, связанной со сверхкритическими жидкостями. Экстракция может быть до некоторой степени избирательной, контролируя плотность среды, и экстрагированный материал легко извлекается путем простого сброса давления, позволяя сверхкритической жидкости вернуться в газовую фазу и испариться, оставляя мало остатков растворителя или не оставляя их совсем. Двуокись углерода - самый распространенный сверхкритический растворитель. Он широко используется для декафеинация зеленых кофейных зерен, экстракция хмель для производства пива,[14] и производство эфирные масла и фармацевтическая продукция из растений.[15] Немного лаборатория методы испытаний включать использование сверхкритическая флюидная экстракция как метод экстракции вместо использования традиционных растворители.[16][17][18]
Разложение сверхкритической жидкости
Сверхкритическая вода может использоваться для разложения биомассы посредством сверхкритической водной газификации биомассы.[19] Этот тип газификации биомассы может использоваться для производства углеводородного топлива для использования в эффективном устройстве для сжигания или для производства водорода для использования в топливном элементе. В последнем случае выход водорода может быть намного выше, чем содержание водорода в биомассе из-за парового риформинга, когда вода является участником, обеспечивающим водород в общей реакции.
Сухая чистка
Сверхкритический диоксид углерода (SCD) можно использовать вместо PERC (перхлорэтилен ) или другие нежелательные растворители для сухая чистка. Иногда сверхкритический диоксид углерода вставки на кнопки, и, когда SCD разгерметизирован, кнопки лопаются или ломаются. Моющие средства, растворимые в диоксиде углерода, улучшают сольватирующую способность растворителя.[20] CO2в оборудовании для химической чистки используется жидкий CO2, не сверхкритический CO2, чтобы не повредить кнопки.
Сверхкритическая жидкостная хроматография
Сверхкритическая жидкостная хроматография (SFC) можно использовать в аналитическом масштабе, где он сочетает в себе многие преимущества высокоэффективная жидкостная хроматография (ВЭЖХ) и газовая хроматография (GC). Его можно использовать с нелетучими и термолабильными аналитами (в отличие от ГХ), а также с универсальным пламенно-ионизационный детектор (в отличие от ВЭЖХ), а также дает более узкие пики из-за быстрой диффузии. На практике преимуществ, предлагаемых SFC, было недостаточно, чтобы заменить широко используемые ВЭЖХ и ГХ, за исключением нескольких случаев, таких как хиральный разделение и анализ высокомолекулярных углеводородов.[21] Для изготовления эффективных препаративных имитация движущейся кровати единицы доступны.[22] Чистота конечных продуктов очень высока, но стоимость делает их пригодными только для очень ценных материалов, таких как фармацевтические препараты.
Химические реакции
Изменение условий реакционного растворителя может позволить разделение фаз для удаления продукта или однофазное для реакции. Быстрая диффузия ускоряет контролируемые диффузией реакции. Температура и давление могут регулировать реакцию по предпочтительным направлениям, например, для повышения выхода определенного хиральный изомер.[23] Есть также значительные экологические преимущества по сравнению с обычными органическими растворителями. Промышленные синтезы, которые выполняются в сверхкритических условиях, включают: полиэтилен из сверхкритических этен, изопропиловый спирт из сверхкритических пропен, 2-бутанол из сверхкритических бутен, и аммиак из сверхкритической смеси азот и водород.[12] Другие реакции в прошлом проводились в промышленных масштабах в сверхкритических условиях, включая синтез метанол и термический (некаталитический) крекинг масла. Из-за разработки эффективных катализаторы, требуемые температуры этих двух процессов были снижены и больше не являются сверхкритическими.[12]
Пропитка и крашение
Пропитка - это, по сути, обратная экстракция. Вещество растворяется в сверхкритической жидкости, раствор протекает мимо твердой подложки и осаждается на подложке или растворяется в ней. Окрашивание, которое легко выполняется на полимерных волокнах, таких как полиэфир, с использованием дисперсных (неионных) красители, является частным случаем этого. Углекислый газ также растворяется во многих полимерах, значительно набухая и пластифицируя их, что еще больше ускоряет процесс диффузии.
Формирование нано- и микрочастиц
Образование мелких частиц вещества с узким гранулометрическим составом - важный процесс в фармацевтической и других отраслях промышленности. Сверхкритические жидкости предоставляют несколько способов достижения этого путем быстрого превышения точка насыщения растворенного вещества путем разбавления, сброса давления или их комбинации. Эти процессы происходят быстрее в сверхкритических жидкостях, чем в жидкостях, что способствует зарождение или же спинодальный распад над рост кристаллов и дает очень мелкие частицы правильного размера. Последние сверхкритические жидкости показали способность уменьшать частицы размером до 5-2000 нм.[24]
Создание фармацевтических сокристаллов
Сверхкритические жидкости действуют как новые среды для генерации новых кристаллических форм API (активных фармацевтических ингредиентов), называемых фармацевтическими сокристаллами. Технология сверхкритических жидкостей предлагает новую платформу, которая позволяет за один этап генерировать частицы, которые трудно или даже невозможно получить традиционными методами. Создание чистых и высушенных новых сокристаллов (кристаллических молекулярных комплексов, содержащих API и один или несколько конформеров в кристаллической решетке) может быть достигнуто благодаря уникальным свойствам SCF за счет использования различных свойств сверхкритических флюидов: сверхкритического CO2 растворяющая способность, эффект антирастворителя и усиление его распыления.[1][25]
Сверхкритическая сушка
Сверхкритическая сушка это метод удаления растворителя без эффектов поверхностного натяжения. По мере высыхания жидкости поверхностное натяжение распространяется на небольшие структуры в твердом теле, вызывая деформацию и усадку. В сверхкритических условиях поверхностное натяжение отсутствует, и сверхкритическая жидкость может быть удалена без искажения. Сверхкритическая сушка используется для производства аэрогели и сушка хрупких материалов, таких как археологические образцы и биологические образцы для электронная микроскопия.
Сверхкритическое водное окисление
Сверхкритическое водное окисление использует сверхкритическую воду в качестве среды для окисления опасных отходов, что исключает образование токсичных продуктов сгорания, которые могут образовываться при горении.
Окисляемые отходы растворяются в сверхкритической воде вместе с молекулярным кислородом (или окислителем, который отдает кислород при разложении, например пероксид водорода ), в этот момент происходит реакция окисления.[нужна цитата ]
Сверхкритический водный гидролиз
Сверхкритический гидролиз представляет собой метод преобразования всех полисахаридов биомассы, а также связанного лигнина в низкомолекулярные соединения путем контактирования только с водой в сверхкритических условиях. Сверхкритическая вода действует как растворитель, поставщик тепловой энергии, разрушающей связи, теплоноситель и источник атомов водорода. Все полисахариды превращаются в простые сахара с почти количественным выходом за секунду или меньше. Алифатические межкольцевые связи лигнина также легко расщепляются на свободные радикалы, которые стабилизируются водородом из воды. Ароматические кольца лигнина не подвергаются влиянию при коротком времени реакции, так что производные лигнина продукты представляют собой смешанные фенолы с низкой молекулярной массой. Чтобы воспользоваться преимуществом очень короткого времени реакции, необходимого для расщепления, необходимо разработать систему непрерывной реакции. Тем самым сводится к минимуму количество воды, нагретой до сверхкритического состояния.
Сверхкритическая водная газификация
Сверхкритическая водная газификация представляет собой процесс использования положительного эффекта сверхкритической воды для преобразования водных потоков биомассы в чистую воду и газы, такие как H2, CH4, CO2, CO и т. Д.[26]
Сверхкритическая жидкость в энергетике
В эффективность из Тепловой двигатель в конечном итоге зависит от разницы температур между источником тепла и поглотителем (Цикл Карно ). Для повышения эффективности энергостанции то Рабочая Температура должен быть поднят. Используя воду в качестве рабочей жидкости, это переводит ее в сверхкритические условия.[27] Эффективность может быть повышена с 39% для субкритических режимов до 45% с использованием современных технологий.[28] Реакторы со сверхкритической водой (SCWR) - это перспективные передовые ядерные системы, обеспечивающие аналогичный прирост теплового КПД. Двуокись углерода также может использоваться на атомных электростанциях сверхкритического цикла с аналогичным увеличением эффективности.[29] Многие угольные сверхкритические парогенераторы работают по всему миру и повысили эффективность традиционных паровых электростанций.
Производство биодизеля
Превращение растительного масла в биодизель через переэтерификация реакция, где триглицерид превращается в метиловый эфир плюс глицерин. Обычно это делается с помощью метанол и едкий или кислотные катализаторы, но могут быть получены с использованием сверхкритического метанола без катализатора. Метод использования сверхкритического метанола для производства биодизеля был впервые изучен Сакой и его сотрудниками. Это имеет то преимущество, что позволяет использовать большее количество воды в сырье (в частности, в использованном кулинарном масле), продукт не нужно промывать для удаления катализатора, и его легче спроектировать как непрерывный процесс.[30]
Повышение нефтеотдачи, улавливания и хранения углерода
Сверхкритический диоксид углерода используется для усилить масло добыча на зрелых месторождениях нефти. При этом есть возможность использования "чистая угольная технология "сочетать улучшенные методы восстановления с связывание углерода. Сотрудничество2 отделен от других дымовые газы, сжимается до сверхкритического состояния и закачивается в геологическое хранилище, возможно, в существующие нефтяные месторождения для повышения добычи.
В настоящее время только схемы выделения ископаемого CO2 из природного газа фактически используют хранение углерода (например, Газовое месторождение Слейпнера ),[31] но есть много планов относительно будущих схем CCS с использованием CO до или после сжигания.2.[32][33][34][35] Также есть возможность уменьшить количество CO.2 в атмосфере с помощью биомасса для выработки энергии и изоляции CO2 произведено.
Усовершенствованная геотермальная система
Использование сверхкритического диоксида углерода вместо воды было исследовано в качестве геотермальной рабочей жидкости.
Холодильное оборудование
Сверхкритический диоксид углерода также становится полезным высокотемпературным хладагент, используется в новых, CFC /HFC -бесплатный домашний тепловые насосы используя транскритический цикл.[36] Эти системы постоянно развиваются, и тепловые насосы для сверхкритического диоксида углерода уже успешно продаются в Азии. В EcoCute системы из Японии - одни из первых коммерчески успешных высокотемпературных тепловых насосов для бытовой воды.
Осаждение сверхкритической жидкости
Сверхкритические жидкости можно использовать для осаждения функциональных наноструктурированных пленок и наноразмерных частиц металлов на поверхности. Высокая диффузионная способность и концентрация прекурсора в жидкости по сравнению с вакуумными системами, используемыми в химическое осаждение из паровой фазы позволяют осаждению происходить в режиме с ограниченной скоростью реакции на поверхности, обеспечивая стабильный и равномерный межфазный рост.[37] Это имеет решающее значение при разработке более мощных электронных компонентов, а осажденные таким образом частицы металла также являются мощными катализаторами химического синтеза и электрохимических реакций. Кроме того, из-за высокой скорости транспорта прекурсора в растворе можно покрывать частицы с большой площадью поверхности, которые химическое осаждение из паровой фазы будет демонстрировать истощение около выхода из системы, а также может привести к нестабильным поверхностным особенностям роста, таким как дендриты. В результате получаются очень тонкие и однородные пленки, осаждаемые со скоростью намного быстрее, чем осаждение атомного слоя, лучший другой инструмент для покрытия частиц в этой шкале размеров.[38]
Антимикробные свойства
CO2 при высоких давлениях имеет противомикробный характеристики.[39] Хотя его эффективность была продемонстрирована для различных применений, механизмы инактивации до конца не изучены, хотя их исследовали более 60 лет.[40]
История
В 1822 году барон Шарль Каньяр де ла Тур открыл критическую точку вещества в своем знаменитом пушка бочковые эксперименты. Прослушивание разрывов в звуке качения кремень мяч в герметичной пушке, наполненной жидкостями при различных температурах, он наблюдал критическую температуру. Выше этой температуры плотности жидкости и газа фазы становятся равными, и различие между ними исчезает, что приводит к единой сверхкритической жидкой фазе.[41]
Смотрите также
- Сверхкритическая адсорбция
- Транскритический цикл
- Критическая точка (термодинамика)
- Проект глубокого бурения в Исландии
Рекомендации
- ^ а б Padrela, L .; Rodrigues, M.A .; Velaga, S.P .; Matos, H.A .; Азеведо, Э. (2009). «Формирование сокристаллов индометацина-сахарина с использованием технологии сверхкритических жидкостей». Европейский журнал фармацевтических наук. 38 (1): 9–17. Дои:10.1016 / j.ejps.2009.05.010. PMID 19477273.
- ^ Шлоски, Кевин (1989). «Сверхкритические фазовые переходы при очень высоком давлении». J. Chem. Эд. 66 (12): 989. Дои:10.1021 / ed066p989.
- ^ Кощинский, Андреа (2008). «Гидротермальная вентиляция в условиях давления и температуры выше критической точки морской воды, 5 ° ю.ш. на Срединно-Атлантическом хребте». Геология. 36 (8): 615. Дои:10.1130 / G24726A.1.
- ^ Рид, Роберт С .; Шервуд, Томас Килгор; Prasnitz, J.M; Полинг, Брюс Э. (1987). Свойства газов и жидкостей (4-е изд.). Макгроу-Хилл. ISBN 9780070517998.
- ^ «Международная ассоциация свойств воды и пара». www.iapws.org. Получено 2020-01-20.
- ^ Отредактируйте Székely. "Что такое сверхкритическая жидкость?". Будапештский технологический и экономический университет. Архивировано из оригинал на 2016-01-08. Получено 2014-06-26.
- ^ «Сверхкритическая экстракция флюидов, соображения плотности». Получено 2007-11-20.
- ^ Гордон, Р. П. (1972). «Сверхкритическое разделение фаз». Журнал химического образования. 49 (4): 249–252. Дои:10.1021 / ed049p249.
- ^ А. А. Клиффорд (2007-12-04). «Расчет термодинамических свойств CO.2 с использованием уравнения состояния Пенга – Робинсона ". ООО "Критические процессы". оригинал на 2008-05-05. Получено 2007-11-20.
- ^ Бриджмен, П. (1914). «Изменение фазы под давлением. I. Фазовая диаграмма одиннадцати веществ с особым упором на кривую плавления». Phys. Rev. 3 (2): 126. Дои:10.1103 / PhysRev.3.126.
- ^ Мисима, О. (1978). «Кривая плавления льда VII». J. Chem. Phys. 68 (10): 4417. Дои:10.1063/1.435522.
- ^ а б c Лейтнер, Вальтер (2010). Сверхкритические жидкости, Vol. 4 Справочника по зеленой химии. Wiley-VCH.
- ^ Уэббер, А.П .; Murton, B .; Робертс, С .; Ходжкинсон, М. «Сверхкритический сброс и образование ВМС на гидротермальном поле Биби, Центр распространения Каймановых островов». Тезисы конференции Гольдшмидта 2014. Геохимическое общество. Архивировано из оригинал 29 июля 2014 г.. Получено 29 июля 2014.
- ^ "Интервью обнаженного ученого". 15 июля 2007 г.. Получено 2007-11-20.
- ^ Айзпуруа-Олайзола, Ойер; Ормазабал, Маркел; Вальехо, Азиер; Оливарес, Майтан; Наварро, Патрисия; Etxebarria, Нестор; Усобиага, Аресац (01.01.2015). «Оптимизация последовательного извлечения жирных кислот и полифенолов из отходов винограда Vitis Vinifera в сверхкритических жидкостях». Журнал пищевой науки. 80 (1): E101 – E107. Дои:10.1111/1750-3841.12715. ISSN 1750-3841. PMID 25471637.
- ^ U.S.EPA Method 3560 Сверхкритическая флюидная экстракция всех извлекаемых углеводородов. https://www.epa.gov/sites/production/files/2015-12/documents/3560.pdf
- ^ USEPA Method 3561 Сверхкритическая жидкостная экстракция полиядерных ароматических углеводородов. https://www.epa.gov/sites/production/files/2015-12/documents/3561.pdf
- ^ Использование озоноразрушающих веществ в лабораториях. ТемаНорд 2003: 516. «Архивная копия» (PDF). Архивировано из оригинал (PDF) на 2008-02-27. Получено 2011-03-28.CS1 maint: заархивированная копия как заголовок (связь)
- ^ «Сверхкритическая водная газификация биом». Архивировано из оригинал на 2009-03-23. Получено 2011-11-17.
- ^ "Новости науки онлайн". Получено 2007-11-20.
- ^ Барт, К. Дж. (2005). «Глава 4: Методы разделения». Добавки в полимеры: промышленный анализ и применение. Джон Уайли и сыновья. п. 212. Дои:10.1002 / 0470012064.ch4. ISBN 978-0-470-01206-2.
- ^ "Теория имитации движущейся кровати" (PDF). Архивировано из оригинал (PDF) на 2004-08-29. Получено 2007-11-20.
- ^ Р. Скотт Оукс; Энтони А. Клиффорд; Кейт Д. Бартл; Марк Торнтон Петт и Кристофер М. Рейнер (1999). «Окисление серы в сверхкритическом диоксиде углерода: резкое зависящее от давления усиление диастереоселективности сульфокисления производных цистеина». Химические коммуникации. 44 (3): 247–248. Дои:10.1039 / a809434i.
- ^ Санг-До Йео и Эрдоган Киран (2005).«Формирование полимерных частиц в сверхкритических жидкостях: обзор». Журнал сверхкритических жидкостей. 34 (3): 287–308. Дои:10.1016 / j.supflu.2004.10.006.
- ^ Падрела, Луис (2010). «Скрининг фармацевтических сокристаллов с использованием процесса распыления в сверхкритической жидкости». Журнал сверхкритических жидкостей. 53 (1–3): 156–164. Дои:10.1016 / j.supflu.2010.01.010.
- ^ «Риформинг в сверхкритической воде». Получено 16 мая 2017.
- ^ Малхотра, Ашок и Сатьякам Р., 2000, Влияние климатических параметров на оптимальную конструкцию сверхкритических электростанций, IECEC, Конференция по преобразованию энергии, стр. 1053–1058,
- ^ «Сверхкритические паровые циклы для электроэнергетики» (PDF). Архивировано из оригинал (PDF) 17 декабря 2008 г.. Получено 2007-11-20.
- ^ В. Досталь; М.Дж. Дрисколл; П. Гейзлар. «Цикл сверхкритического диоксида углерода для ядерных реакторов нового поколения» (PDF). MIT-ANP-TR-100. MIT-ANP-серия. Получено 2007-11-20.
- ^ Кунчана Буньякиат; Сукуня Макми; Руенгвит Савангкоу и Сомкиат Нгампрасертсит (2006). «Непрерывное производство биодизеля путем переэтерификации из растительных масел в сверхкритическом метаноле». Энергия и топливо. 20 (2): 812–817. Дои:10.1021 / ef050329b.
- ^ "Соленый водоносный горизонт CO2 Место хранения". Получено 2007-12-10.
- ^ «Водородная экономика: возможности, затраты, препятствия и потребности в исследованиях и разработках», с. 84 (2004)
- ^ FutureGen Technology В архиве 2008-01-01 на Wayback Machine
- ^ Эйвинд Вессия: «Реактор Фишера-Тропша, питаемый синтез-газом» В архиве 2007-09-29 на Wayback Machine
- ^ межправительственная комиссия по изменению климата Специальный отчет МГЭИК об улавливании и хранении диоксида углерода.
- ^ Часто задаваемые вопросы - сверхкритический CO2 в тепловых насосах и других приложениях В архиве 2007-10-06 на Wayback Machine
- ^ Е, Сян-Жун; Лин, Ю. Х. и Вай, С. М. (2003). "Производство сверхкритических жидкостей металлических нанопроволок и наностержней, созданных на основе многослойных углеродных нанотрубок". Современные материалы. 15 (4): 316–319. Дои:10.1002 / adma.200390077.
- ^ «ЮФО в сравнении с ССЗ». navolta.com. Наволта. Архивировано из оригинал 5 октября 2014 г.. Получено 3 октября 2014.
- ^ Cinquemani, C; Бойл, К; Бах, Э. и Шоллмейер, Э (2007). «Инактивация микробов с помощью сжатого углекислого газа - экологически безопасный процесс дезинфекции медицинских тканей». Журнал сверхкритических жидкостей. 42 (3): 392–397. Дои:10.1016 / j.supflu.2006.11.001.
- ^ Фрейзер, Д. (1951). «Разрушение бактерий путем сброса давления газа». Природа. 167 (4236): 33–34. Bibcode:1951 г., природа, 167 ... 33F. Дои:10.1038 / 167033b0. PMID 14796728. S2CID 8130763.
- ^ Берш, Бертран; Хенкель, Мальте; Кенна, Ральф (2009). «Критические явления: 150 лет со дня Каньяр де ла Тур». Журнал физических исследований. 13 (3): 3001–1–3001–4. arXiv:0905.1886. Bibcode:2009arXiv0905.1886B. Дои:10.1590 / S1806-11172009000200015. S2CID 5153362.
дальнейшее чтение
- Бруннер, Г. (2010). «Применение сверхкритических жидкостей». Ежегодный обзор химической и биомолекулярной инженерии. 1: 321–342. Дои:10.1146 / annurev-chembioeng-073009-101311. PMID 22432584.
внешняя ссылка
- Удобный калькулятор для плотности, энтальпии, энтропии и других термодинамических данных сверхкритического CO2 / воды и др.
- видеоролики, чтобы представить критическую точку сверхкритической жидкости и растворимость в сверхкритической жидкости
- ОБНАРУЖЕН NewScientist Environment: самая горячая вода на Земле
- Поляков, Мартын (28 апреля 2008 г.). «Сверхкритические жидкости». Пробирка. Брэди Харан для Ноттингемский университет.

