Асимметричный диметиларгинин - Asymmetric dimethylarginine
 | |
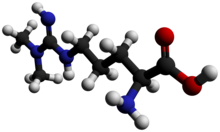 | |
| Имена | |
|---|---|
| Название ИЮПАК 2-амино-5 - [[амино (диметиламино) метилиден] амино] пентановая кислота | |
| Другие имена N (G), N (G ') - диметиларгинин | |
| Идентификаторы | |
3D модель (JSmol ) | |
| 3DMet | |
| 2261521 S | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| DrugBank | |
| КЕГГ | |
| MeSH | N, N-диметиларгинин |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C8ЧАС18N4О2 | |
| Молярная масса | 202.258 г · моль−1 |
| бревно п | −0.716 |
| Кислотность (пKа) | 2.497 |
| Основность (пKб) | 11.500 |
| Родственные соединения | |
Родственные алкановые кислоты | |
Родственные соединения | |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Асимметричный диметиларгинин (ADMA) - это природное химическое вещество, обнаруженное в плазма крови. Это метаболический побочный продукт постоянного белок процессы модификации в цитоплазма всех клеток человека. Это тесно связано с L-аргинин, условно необходимое аминокислота. ADMA мешает L-аргинин в производстве оксид азота (NO), ключевое химическое вещество, участвующее в нормальном эндотелиальный функция и, в более широком смысле, сердечно-сосудистый здоровье.
Открытие
Патрик Валланс и его Лондон коллеги впервые отметили роль асимметричного диметиларгинина в качестве помех в начале 1990-х годов.[1]Сегодня продолжаются биохимические и клинические исследования роли ADMA в сердечно-сосудистые заболевания, сахарный диабет, Эректильная дисфункция и некоторые формы почка болезнь.
Синтез и регулирование в организме
Асимметричный диметиларгинин создается в белке. метилирование, общий механизм посттрансляционной модификации белков. Эта реакция катализируется фермент набор называется S-аденозилметиониновый белок N-метилтрансферазы (протеинметилазы I и II).[2]Метильные группы, переданные для создания ADMA, происходят из метил групповой донор S-аденозилметионин, промежуточное звено в метаболизме гомоцистеин. (Гомоцистеин является важным химическим веществом в крови, потому что он также маркер сердечно-сосудистых заболеваний). После синтез, ADMA переносится в внеклеточный пространство и оттуда в плазму крови. Асимметричный диметиларгинин измеряется с использованием высокоэффективная жидкостная хроматография.
Концентрации АДМА существенно повышаются природными или окисленными ЛПНП холестерин.[3]Таким образом, происходит спиралевидный эффект с высокими уровнями эндотелиальных ЛПНП, вызывающих более высокие значения ADMA, которые, в свою очередь, ингибируют продукцию NO, необходимую для стимулирования расширение сосудов. Выведение АДМА происходит путем выведения с мочой и метаболизма ферментом. диметиларгинин диметиламиногидролаза (DDAH). Предполагается, что роль гомоцистеина как фактора риска сердечно-сосудистых заболеваний опосредована подавлением гомоцистеином продукции DDAH в организме. Полифенольные антиоксиданты также играют роль в подавлении гомоцистеина.
ADMA и предлагаемые направления терапевтических исследований

Поскольку повышенные уровни ADMA, по-видимому, связаны с неблагоприятными последствиями для здоровья человека, такими как сердечно-сосудистые заболевания, нарушения обмена веществ, а также широкий спектр заболеваний пожилых людей, возможное снижение уровней ADMA может иметь важные терапевтические эффекты. Однако еще предстоит установить, можно ли управлять уровнями ADMA и, что более важно, дает ли это полезные клинические преимущества.
Связь ADMA с нарушениями регуляции липидов предполагает, что добавки свободные жирные кислоты может манипулировать уровнями ADMA. Однако исследования не показали, что они имеют эффект.[4][5]
Роль ADMA связана с повышенным уровнем гомоцистеин.[6][7][8] Хотя подходы к модификации последнего пероральными добавками фолиевая кислота были настоятельно рекомендованы, исследования показали, что это не дает какой-либо клинической пользы, и предположили, что витамины группы В могут вместо этого увеличивать некоторые сердечно-сосудистые риски.[9][10][11]
Прямое изменение уровней ADMA с добавками L-аргинин.[12][13]Есть надежда, что такое вмешательство может не только улучшить функцию эндотелия, но и уменьшить клинические симптомы явного сердечно-сосудистого заболевания.[14][15]Однако исследования показывают несоответствие результатов в клиническом контексте.[16]и недавние результаты манипулирования уровнями гомоцистеина требуют особой осторожности в отношении того, какие клинические исходы могут возникнуть в результате этого подхода.
Статины Помимо воздействия на уровень циркулирующего холестерина, он также увеличивает уровень оксида азота и, таким образом, оказывает прямое влияние на кровоснабжение сердца. Повышенные уровни ADMA, по-видимому, изменяют этот эффект и, следовательно, могут иметь последствия для реакции пациентов на прием статинов.[17]
Повторное введение d-амфетамина может снизить ADMA.[18]
Смотрите также
Рекомендации
- ^ Vallance, P .; Leone, A .; Calver, A .; Collier, J .; Монкада, С. (1992). «Эндогенный диметиларгинин как ингибитор синтеза оксида азота». Журнал сердечно-сосудистой фармакологии. 20 Дополнение 12: S60 – S62. Дои:10.1097/00005344-199204002-00018. PMID 1282988. S2CID 38113918.
- ^ Равал Н., Раджпурохит Р., Лишве М.А., Уильямс К.Р., Пайк В.К., Ким С. (1995). «Структурная специфика субстрата для S-аденозилметионин: протеин аргинин N-метилтрансферазы ». Biochim Biophys Acta. 1248 (1): 11–8. Дои:10.1016 / 0167-4838 (94) 00213-Z. PMID 7536038.
- ^ Богер Р., Сюдов К., Борлак Дж., Тум Т., Ленцен Х., Шуберт Б., Цикас Д., Боде-Богер С.М. (21 июля 2000 г.). «Холестерин ЛПНП стимулирует синтез асимметричного диметиларгинина в эндотелиальных клетках человека: участие S-аденозилметионин-зависимых метилтрансфераз». Circ Res. 87 (2): 99–105. Дои:10.1161 / 01.RES.87.2.99. PMID 10903992.
- ^ Eid HM, Arnesen H, Hjerkinn EM, Lyberg T, Ellingsen I, Seljeflot I (2006). «Влияние диеты и воздействия жирных кислот омега-3 на асимметричный диметиларгинин». Нутр Метаб (Лондон). 3 (1): 4. Дои:10.1186/1743-7075-3-4. ЧВК 1343562. PMID 16396682.
- ^ Намиранян К., Миттермайер Ф, Артвол М., Плейнер Дж., Шаллер Дж., Майер Б.Х., Байерле-Эдер М., Роден М., Баумгартнер-Парцер С., Вольц М. (2005). «Свободные жирные кислоты не увеличивают резко асимметричные концентрации диметиларгинина». Horm Metab Res. 37 (12): 768–72. Дои:10.1055 / с-2005-921100. PMID 16372232.
- ^ Krzyzanowska K, Mittermayer F, Krugluger W, Schnack C, Hofer M, Wolzt M, Schernthaner G (2006). «Асимметричный диметиларгинин связан с макрососудистыми заболеваниями и общим гомоцистеином у пациентов с диабетом 2 типа». Атеросклероз. 189 (1): 236–40. Дои:10.1016 / j.atherosclerosis.2005.12.007. PMID 16414052.
- ^ Дайал С., Ленц С.Р. (2005). «АДМА и гипергомоцистеинемия». Vasc Med. 10 Дополнение 1 (2): S27–33. Дои:10.1191 / 1358863x05vm599oa. PMID 16444866.
- ^ Stuhlinger MC, Stanger O (2005). «Асимметричный диметил-L-аргинин (ADMA): возможная связь между гомоцист (е) ином и эндотелиальной дисфункцией». Curr Drug Metab. 6 (1): 3–14. Дои:10.2174/1389200052997393. PMID 15720202.
- ^ Зунгас С., МакГрат Б.П., Бранли П., Керр П.Г., Маске К., Вулф Р., Аткинс Р.К., Николлс К., Френкель М., Хатчисон Б.Г., Уокер Р., Макнил Дж.Дж. (2006). «Сердечно-сосудистая заболеваемость и смертность в исследовании атеросклероза и добавок фолиевой кислоты (ASFAST) при хронической почечной недостаточности: многоцентровое рандомизированное контролируемое исследование». J Am Coll Cardiol. 47 (6): 1108–16. Дои:10.1016 / j.jacc.2005.10.064. PMID 16545638.
- ^ Lonn, E; Юсуф, S; Арнольд, MJ; Шеридан, П; Пог, Дж; Микс, М; Маккуин, MJ; Пробстфилд, Дж; и другие. (2006). «Снижение уровня гомоцистеина с помощью фолиевой кислоты и витаминов группы В при сосудистых заболеваниях». N Engl J Med. 354 (15): 1567–77. Дои:10.1056 / NEJMoa060900. PMID 16531613. S2CID 21790155.
- ^ Bonaa KH, Njolstad I, Ueland PM, Schirmer H, Tverdal A, Steigen T, Wang H, Nordrehaug JE, Arnesen E, Rasmussen K (2006). «Снижение уровня гомоцистеина и сердечно-сосудистые события после острого инфаркта миокарда». N Engl J Med. 354 (15): 1578–88. Дои:10.1056 / NEJMoa055227. PMID 16531614.
- ^ Боде-Богер С.М., Мук Дж., Сурдацкий А., Брабант Г., Богер Р. Х., Фролих Дж. К. (2003). «Пероральный L-аргинин улучшает функцию эндотелия у здоровых людей старше 70 лет». Vasc Med. 8 (2): 77–81. Дои:10.1191 / 1358863x03vm474oa. PMID 14518608.
- ^ Джон П. Кук (2002). Сердечно-сосудистое лечение. Случайный дом. ISBN 0-7679-0881-3.
- ^ Ректор Т.С., Банк А.Дж., Маллен К.А., Чумперлин Л.К., Сих Р., Пиллай К., Кубо С.Х. (15 июня 1996 года). «Рандомизированное двойное слепое плацебо-контролируемое исследование дополнительного перорального приема L-аргинина у пациентов с сердечной недостаточностью». Тираж. 93 (12): 2135–41. Дои:10.1161 / 01.CIR.93.12.2135. PMID 8925582.
- ^ Ceremuzynski L, Chamiec T, Herbaczynska-Cedro K (1997). «Влияние перорального L-аргинина на переносимость физической нагрузки у пациентов со стабильной стенокардией». Am J Cardiol. 80 (3): 331–3. Дои:10.1016 / S0002-9149 (97) 00354-8. PMID 9264427.
- ^ Лоскальцо Дж. (2004). «L-аргинин и атеротромбоз». J Nutr. 134 (10 Прил.): 2798S – 2800S, обсуждение 2818S – 2819S. Дои:10.1093 / jn / 134.10.2798S. PMID 15465788.
- ^ Джанатуинен Т., Лааксо Дж., Лааксонен Р., Весалайнен Р., Нуутила П., Лехтимаки Т., Райтакари О. Т., Кнуути Дж. (2003). «Асимметричный диметиларгинин в плазме изменяет действие правастатина на кровоток в миокарде у молодых людей». Vasc Med. 8 (3): 185–9. Дои:10.1191 / 1358863x03vm490oa. PMID 14989559. S2CID 36938530.
- ^ Ванавески, Таави; Нарвик, Джейн; Иннос, Юрген; Филипс, Мари-Энн; Оттас, Айгар; Плаас, Марио; Харинг, Лийна; Зилмер, Михкель; Вазар, Ээро (12.06.2018). «Повторное введение D-амфетамина вызывает отчетливые изменения в поведении и уровнях метаболитов у мышей линии 129Sv и Bl6». Границы неврологии. 12: 399. Дои:10.3389 / фнинс.2018.00399. ISSN 1662-4548. ЧВК 6005828. PMID 29946233.
