Рак печени - Liver cancer
| Рак печени | |
|---|---|
| Другие имена | Рак печени, первичное злокачественное новообразование печени, первичный рак печени |
 | |
| компьютерная томография из печень с холангиокарцинома | |
| Специальность | Гастроэнтерология Гепатология Онкология |
| Симптомы | Шишка или боль в правой части под грудная клетка, вздутие живота, желтоватая кожа, легкие синяки, похудание, слабость[1] |
| Обычное начало | От 55 до 65 лет[2] |
| Причины | Цирроз из-за гепатит Б, гепатит С, или же алкоголь, афлатоксин, неалкогольная жировая болезнь печени, печеночные двуустки[3][4] |
| Диагностический метод | Анализы крови, медицинская визуализация, биопсия ткани[1] |
| Профилактика | Иммунизация против гепатита В, лечение инфицированных гепатитом B или C[3] |
| Уход | Хирургия, таргетная терапия, радиационная терапия[1] |
| Прогноз | Пятилетняя выживаемость ~ 18% (США);[2] 40% (Япония)[5] |
| Частота | 618 700 (на момент 2015 года)[6] |
| Летальные исходы | 782,000 (2018)[7] |
Рак печени, также известный как рак печени и первичный рак печени, является рак что начинается в печень.[1] Рак, который распространился на печень откуда-то еще, известен как метастазы в печень, встречается чаще, чем то, что начинается в печени.[3] Симптомы рака печени могут включать уплотнение или боль в правом боку ниже грудная клетка, вздутие живота, желтоватая кожа, легкие синяки, похудание и слабость.[1]
Основная причина рака печени: цирроз из-за гепатит Б, гепатит С или же алкоголь.[4] Другие причины включают: афлатоксин, неалкогольная жировая болезнь печени и печеночные двуустки.[3] Наиболее распространенные типы: гепатоцеллюлярная карцинома (ГЦК), что составляет 80% случаев, и холангиокарцинома.[3] Менее распространенные типы включают муцинозное кистозное новообразование и внутрипротоковое папиллярное новообразование желчных путей.[3] Диагноз может быть подтвержден анализы крови и медицинская визуализация, с подтверждением биопсия ткани.[1]
Профилактические меры включают: иммунизация против гепатита В и лечение инфицированных гепатитом В или С.[3] Скрининг рекомендуется тем, у кого хроническое заболевание печени.[3] Варианты лечения могут включать: хирургия, таргетная терапия и радиационная терапия.[1] В некоторых случаях абляционная терапия, эмболизирующая терапия или же трансплантация печени может быть использовано.[1] Можно внимательно следить за небольшими образованиями в печени.[1]
Первичный рак печени во всем мире занимает шестое место по частоте возникновения рака (6%) и второе место среди причин смерти от рака (9%).[3][8] В 2018 году это произошло у 841 тысячи человек и привело к 782 тысячам смертей.[7] В 2015 году 263 000 смертей от рака печени были вызваны гепатитом B, 245 000 - алкоголем и 167 000 - гепатитом C.[9] Более высокие показатели рака печени встречаются там, где распространены гепатиты B и C, в том числе в Азии и К югу от Сахары.[3] Мужчины чаще поражаются ГЦК, чем женщины.[3] Диагноз чаще всего ставится в возрасте от 55 до 65 лет.[2] Пятилетняя выживаемость составляет 18,4% в США,[2] и 40,4% в Японии.[5] Слово «печеночный» происходит от Греческий Hêpar, что означает «печень».[10]
Признаки и симптомы
Поскольку рак печени - это Обобщающий термин для многих типов рака признаки и симптомы зависят от того, какой тип рака присутствует. Холангиокарцинома связана с потливость, желтуха, боль в животе, потеря веса и увеличение печени.[11] Гепатоцеллюлярная карцинома связана с брюшная масса, боль в животе, рвота, анемия, боль в спине, желтуха, зуд, потеря веса и высокая температура.[12]
Причины
Вирусная инфекция

Вирусная инфекция либо гепатит С вирус (HCV) или Гепатит Б вирус (HBV) является сегодня основной причиной рака печени в мире, составляя 80% гепатоцеллюлярная карцинома (HCC).[13][14][15] Вирусы вызывают ГЦК, потому что массивные воспаление, фиброз, и в конечном итоге цирроз происходит в печени. ГЦК обычно возникает после цирроза, с ежегодной заболеваемостью 1,7% у лиц с циррозом, инфицированных ВГС.[16] Около 5-10% людей, инфицированных HBV, становятся хроническими носителями, и около 30% из них приобретают хроническое заболевание печени, которое может привести к ГЦК.[13] Инфекция HBV также связана с холангиокарцинома.[17] Роль вирусов, отличных от HCV или HBV, в развитии рака печени гораздо менее ясна, хотя есть некоторые доказательства того, что коинфекция HBV и гепатит D вирус может увеличить риск ГЦК.[18]
Много генетический и эпигенетический При инфицировании ВГС и ВГВ в клетках печени образуются изменения, которые являются основным фактором образования опухолей печени. Вирусы вызывают злокачественные изменения в клетках, изменяя метилирование гена, влияя на экспрессию генов и стимулируя или подавляя клеточные пути передачи сигналов. Таким образом, вирусы могут предотвратить запрограммированную форму гибели клеток (апоптоз ) и способствуют репликации и устойчивости вируса.[13][16]
HBV и HCV также вызывают злокачественные изменения, вызывая повреждение ДНК и геномная нестабильность. Это путем создания активные формы кислорода, экспрессируют белки, которые мешают ферментам репарации ДНК, а HCV вызывает активацию фермент-мутатор.[19][20]
Цирроз
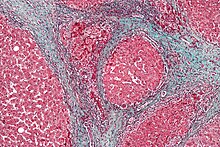
Помимо вирусных цирроз Как описано выше, другие причины цирроза печени могут привести к ГЦК. Прием алкоголя коррелирует с риском ГЦК, и этот риск намного выше у людей с вызванным алкоголем циррозом печени. Известно несколько заболеваний, которые вызывают цирроз и приводят к раку, в том числе наследственные. гемохроматоз и первичный билиарный цирроз.[21]
Афлатоксин
Афлатоксин воздействие может привести к развитию ГЦК. Афлатоксины - это группа химических веществ, вырабатываемых грибами. Aspergillus flavus (название происходит от A. flavus токсин) и A. parasiticus. Загрязнение пищевых продуктов грибами приводит к попаданию в организм химических веществ, очень токсичных для печени. Обычные продукты питания, загрязненные токсинами, - это злаки, арахис и другие овощи. Загрязнение пищевых продуктов распространено в Африке, Юго-Восточной Азии и Китае. Сопутствующая инфекция HBV и воздействие афлатоксина увеличивают риск рака печени более чем в три раза по сравнению с инфицированными HBV людьми без воздействия афлатоксина. Афлатоксины вызывают рак через мутации и эпигенетические изменения. Афлатоксины вызывают целый спектр мутаций[22][23] включая очень частую мутацию в p53 подавитель опухолей ген.[22] Мутация в p53, предположительно в сочетании с другими мутациями, индуцированными афлатоксином, и эпигенетический переделки,[24] вероятно является частой причиной индуцированного афлатоксином канцерогенез.
Другие причины у взрослых
- Диспластические узелки высокой степени - это предраковые поражения печени. В течение двух лет риск рака, вызванного этими узелками, составляет 30–40%.[25]
- Ожирение превратился в важный фактор риска, поскольку он может привести к стеатогепатит.[15][26]
- Сахарный диабет увеличивает риск ГЦК.[26]
- Курение увеличивает риск ГЦК по сравнению с некурящими и бывшими курильщиками.[26]
- Риск холангиокарциномы в течение жизни составляет около 5-10% у людей с первичный склерозирующий холангит.[27]
- Печеночная двуустка инфекция увеличивает риск холангиокарциномы, и это причина, по которой Таиланд имеет особенно высокие показатели этого рака.[28]
Дети
Повышенный риск рака печени у детей может быть вызван: Синдром Беквита – Видемана (связанный с гепатобластомой),[29][30] семейный аденоматозный полипоз (связанный с гепатобластомой),[30] низкий вес при рождении (связанный с гепатобластомой),[31] Прогрессирующий семейный внутрипеченочный холестаз (связанный с ГЦК)[32] и Трисомия 18 (связанный с гепатобластомой).[30]
Диагностика
Много методы визуализации используются для диагностики первичного рака печени. Для HCC они включают медицинский ультразвук, компьютерная томография (CT) и магнитно-резонансная томография (МРТ). При визуализации печени с помощью ультразвука вероятность того, что опухоль превышает 2 см, является ГЦК, более 95%. Большинство холангиокарцим возникает в веселый области печени и часто проявляется обструкцией желчных протоков. Если предполагается, что причина непроходимости злокачественная, эндоскопическая ретроградная холангиопанкреатография (ЭРХПГ), УЗИ, КТ, МРТ и магнитно-резонансная холангиопанкреатография (MRCP).[33]
Онкомаркеры, химические вещества, которые иногда обнаруживаются в крови больных раком, могут быть полезны при диагностике и контроле за течением рака печени. Высокий уровень альфа-фетопротеин (AFP) в крови может быть обнаружен во многих случаях HCC и внутрипеченочной холангиокарциномы. Холангиокарциному можно обнаружить с помощью этих обычно используемых онкомаркеров: углеводный антиген 19-9 (CA 19-9), карциноэмбриональный антиген (CEA) и раковый антиген 125 (CA125 ). Эти опухолевые маркеры обнаруживаются при первичном раке печени, а также при других формах рака и некоторых других заболеваниях.[34][35]
Классификация

Наиболее частым раком печени, составляющим примерно 75% всех первичных раковых заболеваний печени, является гепатоцеллюлярная карцинома (HCC) (также называемый гепатома, что неверно, потому что аденомы обычно доброкачественные). ГЦК - это рак, образованный клетками печени, известный как гепатоциты, которые становятся злокачественными. Другой тип рака, образованный клетками печени, - это гепатобластома, который, в частности, образуется незрелыми клетками печени.[37] Это редкая злокачественная опухоль, которая в основном развивается у детей и составляет примерно 1% всех онкологических заболеваний у детей и 79% всех первичных раковых заболеваний печени в возрасте до 15 лет. Большинство гепатобластом формируется в правой доле.[31]
Рак печени также может исходить из других структур в печени, таких как желчный проток, кровеносный сосуд и иммунные клетки. Рак желчного протока (холангиокарцинома и холангиоцеллюлярный цистаденокарцинома ) составляют примерно 6% первичных раковых заболеваний печени.[37] Существует также вариантный тип ГЦК, включающий как ГЦК, так и холангиокарциному.[38] Опухоли кровеносных сосудов (ангиосаркома и гемангиоэндотелиома, эмбриональная саркома и фибросаркома производятся из соединительной ткани, известной как мезенхима. Раковые образования, вызванные мышцами печени, лейомиосаркома и рабдомиосаркома. Другие менее распространенные виды рака печени включают: карциносаркомы, тератомы, опухоли желточного мешка, карциноидные опухоли и лимфомы.[37] Лимфомы обычно имеют диффузную инфильтрацию в печень, но в редких случаях они также могут образовывать массу печени.
Многие виды рака, обнаруженные в печени, не являются истинным раком печени, а являются раком из других участков тела, который распространился на печень (известный как метастазы ). Часто сайт происхождения желудочно-кишечный тракт, так как печень находится рядом со многими из этих метаболически активных, богатых кровью органов, рядом с кровеносными сосудами и лимфатическими узлами (такими как панкреатический рак, рак желудка, рак толстой кишки и карциноидные опухоли в основном из приложение ), но и из рак молочной железы, рак яичников, рак легких, рак почек, рак простаты.
Профилактика
Профилактику рака можно разделить на первичную, вторичную и третичную. Первичная профилактика превентивно снижает воздействие фактора риска рака печени. Одним из наиболее эффективных способов первичной профилактики рака печени является вакцинация против гепатита В. Вакцинация против гепатит С вирус в настоящее время недоступен. Другие формы первичной профилактики направлены на ограничение передачи этих вирусов путем пропаганды безопасных инъекций, скрининга. донорство крови продукты, а также скрининг бессимптомных лиц из группы высокого риска. Афлатоксин воздействия можно избежать с помощью послеуборочных мероприятий для предотвращения появления плесени, которые оказались эффективными в Западная Африка. Сокращение злоупотребление алкоголем, ожирение, и сахарный диабет также снизит уровень заболеваемости раком печени. Контроль диеты в гемохроматоз может снизить риск железная перегрузка, снижая риск рака.[39]
Вторичная профилактика включает в себя лечение агента, участвующего в образовании рака (канцерогенез ) и предотвращение канцерогенеза, если это невозможно. Вылечить инфицированных вирусом людей невозможно, но лечение противовирусными препаратами, такими как интерферон, может снизить риск рака печени. Хлорофиллин может иметь потенциал в снижении эффектов афлатоксина.[39]
Третичная профилактика включает лечение для предотвращения рецидива рака печени. К ним относятся использование химиотерапевтических и противовирусных препаратов.[39]
Уход
Гепатоцеллюлярная карцинома
Этот раздел должен быть обновлено. (Июнь 2017 г.) |

Частичное хирургическая резекция оптимальное лечение гепатоцеллюлярная карцинома (ГЦК) у пациентов с достаточным резервом функции печени. Повышенный риск осложнений, таких как печеночная недостаточность, может возникать при резекции цирротической (т.е. менее чем оптимально функциональной) печени. 5-летняя выживаемость после резекции значительно улучшились за последние несколько десятилетий и теперь могут превышать 50%. Однако частота рецидивов после резекции может превышать 70%, будь то из-за распространения исходной опухоли или образования новых опухолей.[40] Трансплантация печени также может рассматриваться в случаях ГЦК, когда эта форма лечения может переноситься и опухоль соответствует определенным критериям (таким как Миланские критерии ). Как правило, пациенты, которым предстоит трансплантация печени, имеют множественные поражения печени, тяжелую базовую дисфункцию печени или и то, и другое. Менее 30–40% людей с ГЦК имеют право на операцию и трансплантацию, поскольку рак часто выявляется на поздней стадии. Кроме того, ГЦК может прогрессировать во время ожидания трансплантации печени, что может предотвратить трансплантацию из-за строгих критериев.
Чрескожная абляция - единственное нехирургическое лечение, которое может предложить излечение. Существует много форм чрескожной абляции, которые состоят из инъекций химических веществ в печень (этиловый спирт или же уксусная кислота ) или создание экстремальных температур с помощью радиочастотная абляция, микроволны, лазеры или же криотерапия. Из них радиочастотная абляция имеет одну из лучших репутаций при ГЦК, но ограничения включают невозможность лечения опухолей вблизи других органов и кровеносных сосудов из-за тепловыделения и эффекта теплоотвода соответственно.[41][42] Кроме того, отдаленные результаты процедур чрескожной аблации при ГЦК изучены недостаточно. В общем, хирургическое вмешательство является предпочтительным методом лечения, когда это возможно.
Системный химиотерапия обычно не используются при ГЦК, хотя местная химиотерапия может использоваться в процедуре, известной как трансартериальная химиоэмболизация. В этой процедуре цитотоксические препараты, такие как доксорубицин или же цисплатин с липиодол вводятся, а артерии, снабжающие печень, блокируются желатиновой губкой или другими частицами. Поскольку большинство системных лекарств неэффективны при лечении ГЦК, исследования молекулярных путей, участвующих в образовании рака печени, привели к сорафениб, а таргетная терапия препарат, препятствующий пролиферации клеток и рост клеток крови. Сорафениб получил одобрение FDA для лечения запущенной гепатоцеллюлярной карциномы в ноябре 2007 года.[43] Этот препарат обеспечивает выживаемость при запущенном ГЦК.[42]
Лучевая терапия не часто используется при ГЦК, потому что печень не переносит облучение. Хотя с помощью современных технологий можно обеспечить целенаправленное облучение опухоли, минимизируя дозу для остальной части печени. Двойное лечение - лучевая терапия плюс химиоэмболизация, местная химиотерапия, системная химиотерапия или лекарственные препараты таргетной терапии - может дать преимущество перед одной лучевой терапией.[44]

Холангиокарцинома
Резекция - это вариант при холангиокарциноме, но менее 30% случаев холангиокарциномы являются операбельными при постановке диагноза. После операции частота рецидивов достигает 60%.[45][46] Трансплантат печени может быть использован там, где частичная резекция не является вариантом, и адъювант химиолучевая терапия может принести пользу в некоторых случаях.[27]
60% холангиокарцином формируются в перихилярный регион и фотодинамическая терапия можно использовать для улучшения качество жизни и время выживания в этих неоперабельных случаях. Фотодинамическая терапия - это новое лечение, при котором для лечения опухоли используются молекулы, активируемые светом. Соединения активируются в области опухоли лазерным светом, который вызывает высвобождение токсичных активных форм кислорода, убивающих опухолевые клетки.[45][47]
Системные химиотерапии, такие как гемцитабин и цисплатин иногда используются в неоперабельных случаях холангиокарциномы.[27]
Радиочастотная абляция, трансартериальная химиоэмболизация и внутренняя лучевая терапия (брахитерапия ) все перспективны в лечении холангиокарциномы.[46]
Лучевая терапия может использоваться в качестве адъюванта или для паллиативного лечения холангиокарциномы.[48]
Гепатобластома
Удаление опухоли либо хирургическая резекция или же пересадка печени может использоваться при лечении гепатобластомы. В некоторых случаях лечение может помочь хирургическое вмешательство. Химиотерапию можно использовать до и после операции и трансплантации.[49]
Химиотерапия, включая цисплатин, винкристин, циклофосфамид, и доксорубицин используются для системного лечения гепатобластомы. Из этих препаратов цисплатин кажется наиболее эффективным.[50]
Эпидемиология

В мире, по состоянию на 2010 г.[Обновить]рак печени стал причиной 754 000 смертей по сравнению с 460 000 в 1990 г., что делает его третьей по значимости причиной смерти от рака после легких и желудка.[51] В 2012 году на него приходилось 7% диагнозов рака у мужчин, что стало 5-м местом среди наиболее диагностируемых онкологических заболеваний в этом году.[52] Из этих смертей 340 000 были вторичными по отношению к гепатиту B, 196 000 были вторичными по отношению к гепатиту C и 150 000 были вторичными по отношению к алкоголю.[51] ГЦК, самая распространенная форма рака печени, имеет поразительное географическое распространение. В Китае зарегистрировано 50% случаев ГЦК во всем мире, и более 80% всех случаев приходится на страны Африки к югу от Сахары или в Восточной Азии из-за гепатит Б вирус.[28][53] Холангиокарцинома также имеет значительное географическое распространение, причем Таиланд показывает самые высокие показатели в мире из-за присутствия печеночной двуустки.[28][54]
Индия
Число новых случаев гепатоцеллюлярной карциномы в год в Индии у мужчин составляет около 4,1, а у женщин - 1,2 на 100 000 человек. Обычно это происходит в возрасте от 40 до 70 лет.[55]
объединенное Королевство
Рак печени является восемнадцатым по распространенности раком в Великобритании (в 2011 году в Великобритании был диагностирован рак печени около 4300 человек) и двенадцатым по частоте причиной смерти от рака (в 2012 году от этого заболевания умерло около 4500 человек).[56]
Соединенные Штаты
Смертность от рака печени среди взрослых в возрасте 25 лет и старше увеличилась на 43 процента с 7,2 на 100 000 стандартного населения США в 2000 году до 10,3 в 2016 году. Показатели смертности от рака печени увеличились на 43 процента с 10,5 в 2000 году до 15,0 в 2016 году для мужчин и на 40 процентов с 4,5 до 6.3 для женщин. Уровень смертности мужчин был в 2,0–2,5 раза выше уровня смертности женщин на протяжении всего этого периода.[57]
Исследование
Гепкортеспенлизимут-L представляет собой пероральную иммунотерапию, которая проходит фазу 3 клинических испытаний по поводу ГЦК.[58]
Смотрите также
Рекомендации
- ^ а б c d е ж грамм час я «Первичное лечение рака печени у взрослых (PDQ®) - версия для пациентов». NCI. 6 июля 2016 г. В архиве из оригинала 2 октября 2016 г.. Получено 29 сентября 2016.
- ^ а б c d "Информационные бюллетени SEER Stat: рак печени и внутрипеченочных желчных протоков". NCI. В архиве из оригинала от 28.07.2017.
- ^ а б c d е ж грамм час я j k Всемирный доклад о раке, 2014 г.. Всемирная организация здоровья. 2014. С. Глава 5.6. ISBN 978-9283204299.
- ^ а б ГББ 2013 Смертность и причины смерти, соавторы (17 декабря 2014 г.). «Глобальная, региональная и национальная смертность от всех причин и причин смерти с разбивкой по возрасту и полу от 240 причин смерти, 1990–2013 гг .: систематический анализ для исследования глобального бремени болезней 2013 г.». Ланцет. 385 (9963): 117–71. Дои:10.1016 / S0140-6736 (14) 61682-2. ЧВК 4340604. PMID 25530442.
- ^ а б «が ん 診療 連 携 拠 点 生存率 集 計 : [国立 が ん 研究 セ ン タ ー 統計]». ganjoho.jp. Получено 2 февраля 2020.
- ^ ГББ 2015 Заболеваемость и травматизм, частота и распространенность, соавторы. (8 октября 2016 г.). «Глобальная, региональная и национальная заболеваемость, распространенность и годы, прожитые с инвалидностью для 310 заболеваний и травм, 1990–2015 гг .: систематический анализ для исследования глобального бремени болезней 2015 г.». Ланцет. 388 (10053): 1545–1602. Дои:10.1016 / S0140-6736 (16) 31678-6. ЧВК 5055577. PMID 27733282.
- ^ а б Брей, Ф; Ферли, Дж; Сурджоматарам, я; Сигель, Р.Л .; Торре, Луизиана; Джемаль, А (ноябрь 2018 г.). «Глобальная статистика рака 2018: оценки GLOBOCAN заболеваемости и смертности от 36 раковых заболеваний в 185 странах во всем мире». КА: Журнал онкологических заболеваний для клиницистов. 68 (6): 394–424. Дои:10.3322 / caac.21492. PMID 30207593. S2CID 52188256.
- ^ Всемирный доклад о раке, 2014 г.. Всемирная организация здоровья. 2014. С. Глава 1.1. ISBN 978-9283204299.
- ^ ГББ 2015 Смертность и причины смерти, соавторы. (8 октября 2016 г.). «Ожидаемая продолжительность жизни на глобальном, региональном и национальном уровнях, смертность от всех причин и смертность от конкретных причин для 249 причин смерти, 1980–2015 гг .: систематический анализ для исследования глобального бремени болезней 2015 г.». Ланцет. 388 (10053): 1459–1544. Дои:10.1016 / с0140-6736 (16) 31012-1. ЧВК 5388903. PMID 27733281.
- ^ "Гепато- Этимология". Dictionary.com. В архиве из оригинала 10 октября 2015 г.. Получено 24 октября 2015.
- ^ Холангиокарцинома в eMedicine
- ^ «Опухоли печени у детей». Бостонская детская больница. Архивировано из оригинал на 2011-06-04.
- ^ а б c Арзуманян А; Рейс, HM; Фейтельсон, Массачусетс (февраль 2013 г.). «Патогенетические механизмы гепатоцеллюлярной карциномы, ассоциированной с HBV и HCV». Обзоры природы. Рак. 13 (2): 123–35. Дои:10.1038 / nrc3449. PMID 23344543. S2CID 29447705.
- ^ Розен, HR (23 июня 2011 г.). «Клиническая практика. Хроническая инфекция гепатита С». Медицинский журнал Новой Англии. 364 (25): 2429–38. Дои:10.1056 / NEJMcp1006613. PMID 21696309. S2CID 19755395.
- ^ а б «Общая информация о первичном раке печени у взрослых». Национальный институт рака. 1980-01-01. В архиве из оригинала от 2 января 2013 г.. Получено 13 января 2013.
- ^ а б Jeong, SW; Джанг, JY; Чанг, RT (декабрь 2012 г.). «Вирус гепатита С и гепатоканцерогенез». Клиническая и молекулярная гепатология. 18 (4): 347–56. Дои:10.3350 / см · ч. 2012.18.4.347. ЧВК 3540370. PMID 23323249.
- ^ Ральфс, S; Хан, С.А. (май 2013 г.). «Роль вирусов гепатита в холангиокарциноме». Журнал вирусных гепатитов. 20 (5): 297–305. Дои:10.1111 / jvh.12093. PMID 23565610.
- ^ Кью, MC (март 2013 г.). «Вирусы гепатита (кроме вирусов гепатита B и C) как причины гепатоцеллюлярной карциномы: обновленная информация». Журнал вирусных гепатитов. 20 (3): 149–57. Дои:10.1111 / jvh.12043. PMID 23383653.
- ^ Такеда Х, Такай А, Инузука Т, Марусава Х (2017). «Генетическая основа гепатоцеллюлярной карциномы, связанной с вирусом гепатита: связь между инфекцией, воспалением и онкогенезом». J. Гастроэнтерол. 52 (1): 26–38. Дои:10.1007 / s00535-016-1273-2. PMID 27714455.
- ^ Ян, SF; Чанг, CW; Wei, RJ; Shiue, YL; Wang, SN; Да, Ю.Т. (2014). «Вовлечение путей ответа на повреждение ДНК в гепатоцеллюлярной карциноме». BioMed Research International. 2014: 153867. Дои:10.1155/2014/153867. ЧВК 4022277. PMID 24877058.
- ^ Фаттович, Г; Строффолини, Т; Загни, я; Донато, Ф (ноябрь 2004 г.). «Гепатоцеллюлярная карцинома при циррозе: частота и факторы риска». Гастроэнтерология. 127 (5 Приложение 1): S35–50. Дои:10.1053 / j.gastro.2004.09.014. PMID 15508101.
- ^ а б Смела М.Э., Карриер С.С., Бейли Е.А., Эссигманн Дж.М. (апрель 2001 г.). «Химия и биология афлатоксина B (1): от мутационной спектрометрии к канцерогенезу». Канцерогенез. 22 (4): 535–45. Дои:10.1093 / carcin / 22.4.535. PMID 11285186.
- ^ Perduca V, Omichessan H, Baglietto L, Severi G (январь 2018 г.). «Мутационные и эпигенетические признаки в раковой ткани, связанные с воздействием окружающей среды и образом жизни». Curr Opin Oncol. 30 (1): 61–67. Дои:10.1097 / CCO.0000000000000418. PMID 29076965. S2CID 20842446.
- ^ Дай И, Хуан К., Чжан Б., Чжу Л., Сюй В. (ноябрь 2017 г.). «Афлатоксин B1-индуцированные эпигенетические изменения: обзор». Food Chem. Токсикол. 109 (Pt 1): 683–689. Дои:10.1016 / j.fct.2017.06.034. PMID 28645871.
- ^ Ди Томмазо, L; Сангиованни, А; Борцио, М; Парк, Ю.Н. Farinati, F; Ронкалли, М. (апрель 2013 г.). «Распространенные предраковые поражения печени». Лучшие практики и исследования. Клиническая гастроэнтерология. 27 (2): 269–84. Дои:10.1016 / j.bpg.2013.03.015. PMID 23809245.
- ^ а б c Chuang SC, La Vecchia C, Boffetta P (1 декабря 2009 г.). «Рак печени: описательная эпидемиология и факторы риска, кроме инфекции HBV и HCV». Письма о раке. 286 (1): 9–14. Дои:10.1016 / j.canlet.2008.10.040. PMID 19091458.
- ^ а б c Разумилава, N; Горс, GJ (январь 2013 г.). «Классификация, диагностика и лечение холангиокарциномы». Клиническая гастроэнтерология и гепатология. 11 (1): 13–21.e1, викторина e3–4. Дои:10.1016 / j.cgh.2012.09.009. ЧВК 3596004. PMID 22982100.
- ^ а б c Джемал, А; Брей, Ф; Центр, ММ; Ферли, Дж; Уорд, E; Форман, Д. (март – апрель 2011 г.). «Глобальная статистика рака». КА: Журнал онкологических заболеваний для клиницистов. 61 (2): 69–90. Дои:10.3322 / caac.20107. PMID 21296855. S2CID 30500384.
- ^ ДеБаун, MR; Такер, Массачусетс (март 1998 г.). «Риск рака в течение первых четырех лет жизни у детей из Регистра синдрома Беквита-Видемана». Журнал педиатрии. 132 (3, Пет 1): 398–400. Дои:10.1016 / S0022-3476 (98) 70008-3. PMID 9544889.
- ^ а б c Спектор, LG; Берч, Дж (ноябрь 2012 г.). «Эпидемиология гепатобластомы». Детская кровь и рак. 59 (5): 776–9. Дои:10.1002 / pbc.24215. PMID 22692949. S2CID 65545.
- ^ а б Эмре, S; McKenna, GJ (декабрь 2004 г.). «Опухоли печени у детей». Детская трансплантация. 8 (6): 632–8. Дои:10.1111 / j.1399-3046.2004.00268.x. PMID 15598339.
- ^ Давид-Спраул, А; Gonzales, E; Бауссан, С; Jacquemin, E (8 января 2009 г.). «Прогрессирующий семейный внутрипеченочный холестаз». Журнал редких заболеваний Orphanet. 4: 1. Дои:10.1186/1750-1172-4-1. ЧВК 2647530. PMID 19133130.
- ^ Арифф, Б; Ллойд, CR; Хан, S; Шариф, М; Thillainayagam, AV; Bansi, DS; Хан, SA; Тейлор-Робинсон, SD; Лим, AK (21 марта 2009 г.). «Визуализация рака печени». Всемирный журнал гастроэнтерологии. 15 (11): 1289–300. Дои:10.3748 / wjg.15.1289. ЧВК 2658841. PMID 19294758.
- ^ Малагуарнера, G; Паладина, I; Джордано, М; Малагуарнера, М; Бертино, G; Берретта, М. (2013). «Сывороточные маркеры внутрипеченочной холангиокарциномы». Маркеры заболеваний. 34 (4): 219–28. Дои:10.1155/2013/196412. ЧВК 3809974. PMID 23396291.
- ^ Чжао YJ, Цзюй Q, Ли GC (2013). «Онкомаркеры гепатоцеллюлярной карциномы». Мол Клин Онкол. 1 (4): 593–598. Дои:10.3892 / mco.2013.119. ЧВК 3915636. PMID 24649215.
- ^ Таблица 37.2 в: Штернберг, Стивен (2012). Диагностическая хирургическая патология Штернберга. Место публикации не указано: LWW. ISBN 978-1-4511-5289-0. OCLC 953861627.
- ^ а б c Ахмед, Ахмед, я; Лобо Д.Н .; Лобо, Дилип Н. (январь 2009 г.). «Злокачественные опухоли печени». Хирургия (Оксфорд). 27 (1): 30–37. Дои:10.1016 / j.mpsur.2008.12.005.
- ^ Хан С.А., Дэвидсон Б.Р., Голдин Р.Д., Хитон Н., Карани Дж., Перейра С.П., Розенберг В.М., Тейт П., Тейлор-Робинсон С.Д., Тиллайнаягам А.В., Томас ХК, Васан Х. (2012). «Рекомендации по диагностике и лечению холангиокарциномы: обновленная информация». Кишечник. 61 (12): 1657–69. Дои:10.1136 / gutjnl-2011-301748. PMID 22895392.
- ^ а б c Хошида, Y; Fuchs, BC; Танабе, К.К. (1 ноября 2012 г.). «Профилактика гепатоцеллюлярной карциномы: потенциальные цели, экспериментальные модели и клинические проблемы». Текущие мишени противораковых препаратов. 12 (9): 1129–59. Дои:10.2174/156800912803987977. ЧВК 3776581. PMID 22873223.
- ^ Брюикс Дж., Шерман М., Американская ассоциация по изучению заболеваний печени (март 2011 г.). «Лечение гепатоцеллюлярной карциномы: обновленная информация». Гепатология. 53 (3): 1020–2. Дои:10.1002 / hep.24199. ЧВК 3084991. PMID 21374666.
- ^ Wang, ZG; Чжан, Г.Ф .; Wu, JC; Цзя, МК (август 2013 г.). «Адъювантная терапия гепатоцеллюлярной карциномы: современное состояние и перспективы». Открытия лекарств и терапия. 7 (4): 137–143. Дои:10.5582 / ddt.2013.v7.4.137. PMID 24071575.
- ^ а б де Лопе, CR; Tremosini, S; Форнер, А; Рейг, М; Bruix, J (2012). «Управление ГЦК». Журнал гепатологии. 56 Приложение 1: S75–87. Дои:10.1016 / S0168-8278 (12) 60009-9. PMID 22300468.
- ^ Китинг GM, Санторо А (2009). «Сорафениб: обзор его использования при запущенной гепатоцеллюлярной карциноме». Наркотики. 69 (2): 223–40. Дои:10.2165/00003495-200969020-00006. PMID 19228077.
- ^ Фэн, М; Бен-Йозеф, Э (октябрь 2011 г.). «Лучевая терапия гепатоцеллюлярной карциномы». Семинары по радиационной онкологии. 21 (4): 271–7. Дои:10.1016 / j.semradonc.2011.05.002. PMID 21939856.
- ^ а б Ulstrup, T; Педерсен, FM (25 февраля 2013 г.). «[Фотодинамическая терапия холангиокарциномы]». Ugeskrift для Laeger. 175 (9): 579–82. PMID 23608009.
- ^ а б Kuhlmann, JB; Блюм, HE (май 2013 г.). «Локорегиональная терапия холангиокарциномы». Текущее мнение в гастроэнтерологии. 29 (3): 324–8. Дои:10.1097 / MOG.0b013e32835d9dea. PMID 23337933. S2CID 37403999.
- ^ Ортнер, Массачусетс (сентябрь 2011 г.). «Фотодинамическая терапия холангиокарциномы». Лазеры в хирургии и медицине. 43 (7): 776–80. Дои:10.1002 / кв.м.21106. PMID 22057505.
- ^ Валеро V, 3-й; Косгроув, Д; Герман, JM; Павлик, TM (август 2012 г.). «Ведение перихилярной холангиокарциномы в эпоху мультимодальной терапии». Экспертный обзор гастроэнтерологии и гепатологии. 6 (4): 481–95. Дои:10.1586 / egh.12.20. ЧВК 3538366. PMID 22928900.
- ^ Мейерс, Р.Л .; Czauderna, P; Отте, Дж. Б. (ноябрь 2012 г.). «Хирургическое лечение гепатобластомы». Детская кровь и рак. 59 (5): 800–8. Дои:10.1002 / pbc.24220. PMID 22887704.
- ^ Перилонго, G; Малоголовкин, М; Feusner, J (ноябрь 2012 г.). «Клинические исследования гепатобластомы: извлеченные уроки и будущие задачи». Детская кровь и рак. 59 (5): 818–21. Дои:10.1002 / pbc.24217. PMID 22678761.
- ^ а б Lozano, R; Нагави, М; Бригадир, К; Lim, S; Сибуя, К; Aboyans, V; Авраам, Дж; Adair, T; Aggarwal, R; Ahn, S. Y .; Альварадо, М; Anderson, H.R .; Андерсон, Л. М .; Andrews, K. G .; Аткинсон, К; Baddour, L.M .; Баркер-Колло, S; Бартельс, Д. Х .; Bell, M. L .; Бенджамин, Э. Дж .; Bennett, D; Bhalla, K; Бикбов, Б; Бин Абдулхак, А; Бирбек, G; Blyth, F; Боллигер, I; Boufous, S; Бучелло, С; и другие. (15 декабря 2012 г.). «Глобальная и региональная смертность от 235 причин смерти для 20 возрастных групп в 1990 и 2010 годах: систематический анализ для исследования глобального бремени болезней 2010 года». Ланцет. 380 (9859): 2095–128. Дои:10.1016 / S0140-6736 (12) 61728-0. HDL:10536 / DRO / DU: 30050819. PMID 23245604. S2CID 1541253.
- ^ Всемирный доклад о раке, 2014 г.. Международное агентство по изучению рака, Всемирная организация здравоохранения. 2014 г. ISBN 978-92-832-0432-9.
- ^ Эль-Сераг, HB; Рудольф, К.Л. (июнь 2007 г.). «Гепатоцеллюлярная карцинома: эпидемиология и молекулярный канцерогенез». Гастроэнтерология. 132 (7): 2557–76. Дои:10.1053 / j.gastro.2007.04.061. PMID 17570226.
- ^ Хан, SA; Толедано, МБ; Тейлор-Робинсон, SD (2008). «Эпидемиология, факторы риска и патогенез холангиокарциномы». Е.П.Б.. 10 (2): 77–82. Дои:10.1080/13651820801992641. ЧВК 2504381. PMID 18773060.
- ^ «Обзор гепатоцеллюлярной карциномы». Рак печени. В архиве из оригинала 18 марта 2017 г.. Получено 18 марта 2017.
- ^ «Статистика рака печени». Cancer Research UK. В архиве из оригинала 17 октября 2014 г.. Получено 28 октября 2014.
- ^ Сюй, Цзяцюань (июль 2018 г.). Тенденции смертности от рака печени среди взрослых в возрасте 25 лет и старше в США, 2000–2016 гг.. Хяттсвилл, Мэриленд: Министерство здравоохранения и социальных служб США, Центры по контролю и профилактике заболеваний, Национальный центр статистики здравоохранения.. Получено 17 сентября 2018.
- ^ Испытание фазы 3 иммунной системы гепкортеспенлизимута-L, иммунотерапии рака печени «Архивная копия». В архиве из оригинала 30.05.2015. Получено 2015-05-29.CS1 maint: заархивированная копия как заголовок (связь)
внешняя ссылка
| Классификация | |
|---|---|
| Внешние ресурсы |
