Газовая хроматография - Gas chromatography
Эта статья нужны дополнительные цитаты для проверка. (Ноябрь 2020) (Узнайте, как и когда удалить этот шаблон сообщения) |
 Газовый хроматограф с пробоотборником | |
| Акроним | GC |
|---|---|
| Классификация | Хроматография |
| Аналиты | Органический Неорганический Должно быть летучий |
| Другие техники | |
| Связанный | Тонкослойная хроматография Высокоэффективная жидкостная хроматография |
| С переносом | Газовая хроматография-масс-спектрометрия |
Газовая хроматография (GC) - распространенный тип хроматография используется в аналитическая химия за разделение и анализ соединений, которые могут быть испарился без разложение. Типичные применения ГХ включают проверку чистоты конкретного вещества или разделение различных компонентов смеси (также можно определить относительные количества таких компонентов). В некоторых ситуациях ГХ может помочь в идентификации соединения. В препаративная хроматография, ГХ может использоваться для получения чистых соединений из смеси.[1][2]
В газовой хроматографии Мобильная фаза (или «движущаяся фаза») - носитель газ, обычно инертный газ Такие как гелий или инертный газ, такой как азот. Гелий остается наиболее часто используемым газом-носителем примерно в 90% приборов, хотя водород предпочтительнее для улучшенного разделения.[3] В стационарная фаза представляет собой микроскопический слой жидкость или же полимер на инертном твердый опора, внутри части стекло или же металл трубку, названную колонной (дань уважения колонна фракционирования используется в перегонке). Прибор, используемый для газовой хроматографии, называется газовый хроматограф (или «аэрограф», «газоотделитель»).
Анализируемые газообразные соединения взаимодействуют со стенками колонки, покрытой неподвижной фазой. Это заставляет каждое соединение элюировать в другое время, известное как время удерживания соединения. Сравнение времен удерживания - вот что придает ГХ аналитическую ценность.
Газовая хроматография в принципе аналогична колоночная хроматография (а также другие формы хроматографии, такие как ВЭЖХ, TLC ), но имеет несколько заметных отличий. Во-первых, процесс разделения соединений в смеси осуществляется между жидкой неподвижной фазой и подвижной газовой фазой, тогда как в колоночной хроматографии неподвижная фаза является твердой, а подвижная фаза - жидкостью. (Отсюда полное название процедуры «Газожидкостная хроматография», относящаяся к подвижной и неподвижной фазам соответственно.) Во-вторых, колонка, через которую проходит газовая фаза, расположена в печи, где температура газа может быть контролируемый, тогда как колоночная хроматография (обычно) не имеет такого контроля температуры. Наконец, концентрация соединения в газовой фазе - это исключительно функция из давление газа газа.[1]
Газовую хроматографию также иногда называют парофазная хроматография (VPC) или газожидкостная распределительная хроматография (GLPC). Эти альтернативные названия, а также их соответствующие сокращения часто используются в научной литературе. Строго говоря, GLPC - наиболее правильная терминология, поэтому многие авторы предпочитают ее.[1]
История
Хроматография датируется 1903 годом в работе русского ученого, Михаил Семенович Цветт,[4] которые разделяли растительные пигменты с помощью жидкостной колоночной хроматографии. Немецкий физический химик Эрика Кремер в 1947 г. вместе с Австрийский аспирант Фриц Приор разработала теоретические основы ГХ и построила первый жидкостно-газовый хроматограф, но ее работа считалась неуместной и долгое время игнорировалась.[5] Арчер Джон Портер Мартин, который был награжден Нобелевская премия за его работу по развитию жидкостно-жидкостной (1941 г.) и бумажной (1944 г.) хроматографии, поэтому ему приписывают основание газовой хроматографии. Популярность газовой хроматографии быстро возросла после разработки пламенно-ионизационного детектора.[6]
ГХ анализ
А газовый хроматограф прибор химического анализа для разделения химикатов в сложной пробе. В газовом хроматографе используется проточная узкая трубка, известная как столбец, через которую проходят различные химические составляющие образца в потоке газа (газ-носитель, Мобильная фаза) с разной скоростью в зависимости от их различных химических и физических свойств и их взаимодействия с определенным заполнением колонки, называемой стационарная фаза. Когда химические вещества выходят из конца колонки, они обнаруживаются и идентифицируются электронным способом. Функция стационарной фазы в столбце заключается в разделении различных компонентов, заставляя каждый из них выходить из столбца в разное время (время удерживания). Другие параметры, которые можно использовать для изменения порядка или времени удерживания, - это скорость потока газа-носителя, длина колонки и температура.
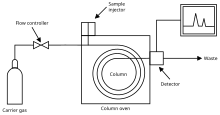
В ГХ-анализе известный объем газообразного или жидкого аналит вводится во «вход» (головку) колонны, обычно с помощью микропроцессора.шприц (или твердофазные волокна микроэкстракции, или система переключения источника газа). Когда газ-носитель перемещает молекулы аналита через колонку, это движение тормозится адсорбция аналита молекулы либо на стенки колонки, либо на упаковочные материалы в колонке. Скорость, с которой молекулы продвигаются по колонке, зависит от силы адсорбция, что, в свою очередь, зависит от типа молекулы и материалов неподвижной фазы. Поскольку каждый тип молекулы имеет разную скорость развития, различные компоненты смеси аналитов разделяются по мере их продвижения вдоль колонки и достижения конца колонки в разное время (время удерживания). Детектор используется для контроля потока на выходе из колонны; таким образом, можно определить время, когда каждый компонент достигает выхода, и количество этого компонента. Обычно вещества идентифицируются (качественно) по порядку, в котором они выходят (элюируются) из колонки, и по времени удерживания анализируемого вещества в колонке.
Физические компоненты
Автосэмплеры
Автоматический пробоотборник обеспечивает средства для автоматической подачи пробы во входные отверстия. Ручное введение образца возможно, но уже не является обычным явлением. Автоматическая установка обеспечивает лучшую воспроизводимость и оптимизацию времени.

Существуют разные виды автосэмплеров. Автосэмплеры можно классифицировать в зависимости от емкости образца (авто-инжекторы и автосэмплеры, где авто-инжекторы могут обрабатывать небольшое количество образцов), а также роботизированных технологий (робот XYZ[7] против вращающегося робота - наиболее распространенный), или для анализа:
- Жидкость
- Статическое пространство над головой благодаря шприцевой технологии
- Динамическое свободное пространство за счет технологии Transfer-Line
- Твердофазная микроэкстракция (SPME)
Входы

Вход колонки (или инжектор) обеспечивает средства для ввода пробы в непрерывный поток газа-носителя. Впускное отверстие - это часть оборудования, прикрепленная к головке колонки.
Общие типы входных отверстий:
- Инжектор S / SL (split / splitless); образец вводится в небольшую обогреваемую камеру шприцем через перегородку - тепло способствует улетучивание образца и матрицы образцов. Затем газ-носитель перемещает либо всю (режим без разделения), либо часть (режим разделения) пробы в колонку. В режиме разделения часть смеси пробы и газа-носителя в камере инжекции выпускается через разделенное вентиляционное отверстие. Разделенная инъекция предпочтительна при работе с образцами с высокими концентрациями аналитов (> 0,1%), тогда как без разделения лучше всего подходит для анализа следовых количеств с небольшими количествами аналитов (<0,01%). В режиме без разделения разделительный клапан открывается по прошествии заданного времени для продувки более тяжелых элементов, которые в противном случае могли бы загрязнить систему. Это предварительно установленное (без разделения) время должно быть оптимизировано, более короткое время (например, 0,2 мин) обеспечивает меньшее отставание, но потери в ответе, более длительное время (2 мин) увеличивает задержку, но также и сигнал.[8]
- Впуск на колонке; здесь проба вводится непосредственно в колонку целиком без нагрева или при температуре ниже точки кипения растворителя. Низкая температура конденсирует образец в узкую зону. Затем колонку и вход можно нагреть, выпуская образец в газовую фазу. Это обеспечивает минимально возможную температуру для хроматографии и предохраняет образцы от разложения выше их точки кипения.
- Инжектор ПТВ; Впервые ввод образца с программированием температуры был описан Фогтом в 1979 году.[нужна цитата ] Первоначально Фогт разработал эту технику как метод введения больших объемов образца (до 250 мкл) в капиллярную ГХ. Фогт вводил образец в лайнер с контролируемой скоростью впрыска. Температура лайнера была выбрана немного ниже точки кипения растворителя. Растворитель с низкой температурой кипения непрерывно выпаривали и выпускали через разделительную линию. Основываясь на этой методике, Пой разработал инжектор испарения с программируемой температурой; PTV. Путем введения образца при низкой начальной температуре футеровки можно обойти многие недостатки классических методов горячего вдувания.[нужна цитата ]
- Вход источника газа или газовый переключающий клапан; газовые пробы в сборных бутылях подключены к тому, что чаще всего является переключающим клапаном с шестью портами. Поток газа-носителя не прерывается, в то время как образец может быть расширен в ранее откачанный контур для образца. После переключения содержимое петли для отбора проб вводится в поток газа-носителя.
- Система P / T (Purge-and-Trap); Через водный образец барботируют инертный газ, в результате чего из матрицы удаляются нерастворимые летучие химические вещества. Летучие вещества «улавливаются» абсорбирующей колонкой (известной как ловушка или концентратор) при температуре окружающей среды. Затем ловушка нагревается, и летучие вещества направляются в поток газа-носителя. Образцы, требующие предварительного концентрирования или очистки, могут быть введены через такую систему, обычно подключенную к порту S / SL.
Выбор газа-носителя (подвижной фазы) важен. Водород имеет диапазон скоростей потока, сравнимый по эффективности с гелием. Однако гелий может быть более эффективным и обеспечивать лучшее разделение, если скорость потока оптимизирована. Гелий негорючий и работает с большим количеством детекторов и старых инструментов. Поэтому гелий является наиболее распространенным газом-носителем. Однако цена гелия за последние годы значительно выросла, в результате чего все большее количество хроматографов переходят на газообразный водород. Историческое использование, а не рациональное рассмотрение, может способствовать дальнейшему предпочтительному использованию гелия.
Детекторы
Наиболее часто используемые детекторы - это пламенно-ионизационный детектор (FID) и детектор теплопроводности (TCD). Оба чувствительны к широкому спектру компонентов, и оба работают в широком диапазоне концентраций. Хотя TCD по сути универсальны и могут использоваться для обнаружения любого компонента, кроме газа-носителя (при условии, что их теплопроводность отличается от теплопроводности газа-носителя при температуре детектора), FID чувствительны в первую очередь к углеводородам и более чувствительны. им, чем TCD. Однако FID не может обнаружить воду. Оба детектора также довольно прочные. Поскольку TCD является неразрушающим, его можно использовать последовательно перед FID (деструктивным), что обеспечивает дополнительное обнаружение одних и тех же аналитов.[9] Другие детекторы чувствительны только к определенным типам веществ или хорошо работают только в более узких диапазонах концентраций.
Детектор теплопроводности (TCD) основывается на теплопроводности вещества, проходящего вокруг вольфрам-рениевой нити с током, проходящим через нее.[10] В этой установке гелий или азот служат в качестве газа-носителя из-за их относительно высокой теплопроводности, которая обеспечивает охлаждение нити и поддерживает равномерное удельное сопротивление и электрический КПД нити.[10][11] Однако, когда молекулы аналита элюируются из колонки в смеси с газом-носителем, теплопроводность уменьшается, и это вызывает отклик детектора.[11] Отклик происходит из-за пониженной теплопроводности, вызывающей повышение температуры и удельного сопротивления нити накала, что приводит к колебаниям напряжения.[10] Чувствительность детектора пропорциональна току нити накала, в то время как она обратно пропорциональна непосредственной температуре окружающей среды этого детектора, а также скорости потока газа-носителя.[10]
В пламенно-ионизационный детектор (ПИД) электроды размещаются рядом с пламенем, подпитываемым водородом / воздухом, рядом с выходом из колонны, и когда углеродсодержащие соединения выходят из колонны, они подвергаются пиролизу пламенем.[10][11] Этот детектор работает только для органических / углеводородных соединений из-за способности углерода образовывать катионы и электроны при пиролизе, который генерирует ток между электродами.[10][11] Увеличение тока преобразуется и появляется на хроматограмме в виде пика. ПИД имеют низкие пределы обнаружения (несколько пикограммов в секунду), но они не могут генерировать ионы из карбонил содержащие углерод.[10] Газы-носители, совместимые с FID, включают гелий, водород, азот и аргон.[10][11]
Детектор щелочного пламени (AFD) или детектор ионизации щелочного пламени (AFID) имеет высокую чувствительность к азоту и фосфору, как и NPD. Однако ионы щелочного металла поставляются с газообразным водородом, а не с каплей над пламенем. По этой причине AFD не страдает «усталостью» от NPD, но обеспечивает постоянную чувствительность в течение длительного периода времени. Кроме того, когда в пламя не добавляются ионы щелочных металлов, AFD работает как стандартный FID. А каталитическое горение детектор (CCD) измеряет горючие углеводороды и водород. Детектор ионизации разряда (DID) использует высоковольтный электрический разряд для образования ионов.
В реактор полидуговой является дополнением к новым или существующим приборам GC-FID, которое преобразует все органические соединения в молекулы метана до их обнаружения FID. Этот метод может быть использован для улучшения отклика FID и позволяет обнаруживать гораздо больше углеродсодержащих соединений.[12] Полное преобразование соединений в метан и теперь эквивалентный отклик в детекторе также устраняет необходимость калибровки и стандартов, поскольку все факторы отклика эквивалентны показателям метана. Это позволяет проводить быстрый анализ сложных смесей, содержащих молекулы, где стандарты недоступны.
Пламенный фотометрический детектор (FPD) использует фотоэлектронный умножитель для обнаружения спектральных линий соединений, когда они горят в пламени. Соединения, элюированные из колонки, переносятся в пламя, питаемое водородом, которое возбуждает определенные элементы в молекулах, а возбужденные элементы (P, S, галогены, некоторые металлы) излучают свет с определенной характерной длиной волны.[11] Излучаемый свет фильтруется и детектируется фотоэлектронным умножителем.[10][11] В частности, эмиссия фосфора составляет около 510–536 нм, а эмиссия серы - 394 нм.[10][11] С помощью атомно-эмиссионного детектора (AED) образец, элюируемый из колонки, попадает в камеру, которая возбуждается микроволнами, индуцирующими плазму.[11] Плазма заставляет пробу аналита разлагаться, и некоторые элементы генерируют спектры атомной эмиссии.[11] Спектры атомной эмиссии дифрагируют на дифракционной решетке и регистрируют с помощью ряда фотоумножителей или фотодиодов.[11]
Детектор электронного захвата (ECD) использует радиоактивный бета-частица (электронный) источник для измерения степени захвата электронов. ECD используются для обнаружения молекул, содержащих электроотрицательные / отводящие элементы и функциональные группы, такие как галогены, карбонил, нитрилы, нитрогруппы и металлоорганические соединения.[10][11] В этом типе детектора в качестве газа-носителя подвижной фазы используется либо азот, либо 5% метана в аргоне.[10][11] Газ-носитель проходит между двумя электродами, расположенными на конце колонны, и рядом с катодом (отрицательный электрод) находится радиоактивная фольга, такая как 63Ni.[10][11] Радиоактивная фольга испускает бета-частицу (электрон), которая сталкивается с газом-носителем и ионизирует его, генерируя больше ионов, в результате чего возникает ток.[10][11] Когда молекулы аналита с электроотрицательными / отводящими элементами или функциональными группами захватываются электронами, что приводит к уменьшению тока, вызывая отклик детектора.[10][11]
Азотно-фосфорный детектор (NPD), форма термоэлектронный детектор, где азот и фосфор изменяют рабочая функция на валике со специальным покрытием и измеряется результирующий ток.
Детектор сухой электролитической проводимости (DELCD) использует воздушную фазу и высокую температуру (v. Coulsen) для измерения хлорированных соединений.
Масс-спектрометр (MS), также называемый ГХ-МС; высокоэффективный и чувствительный даже при небольшом количестве пробы. Этот детектор можно использовать для идентификации аналитов на хроматограммах по их масс-спектру.[13] Немного ГХ-МС связаны с ЯМР-спектрометр который действует как резервный детектор. Эта комбинация известна как ГХ-МС-ЯМР.[нужна цитата ] Немного ГХ-МС-ЯМР связаны с инфракрасный спектрофотометр который действует как резервный детектор. Эта комбинация известна как GC-MS-NMR-IR. Однако следует подчеркнуть, что это очень редко, поскольку большинство необходимых анализов можно сделать с помощью чисто ГХ-МС.[нужна цитата ]
Вакуумный ультрафиолет (VUV) представляет собой новейшую разработку детекторов для газовой хроматографии. Большинство химических веществ поглощают и имеют уникальные сечения поглощения газовой фазы в контролируемом диапазоне длин волн ВУФ около 120–240 нм. Если для аналитов известны поперечные сечения поглощения, детектор ВУФ позволяет абсолютное определение (без калибровки) количества молекул, присутствующих в проточной кювете, в отсутствие химических помех.[14]
Другие детекторы включают детектор электролитической проводимости Холла (ElCD), детектор ионизации гелия (HID), инфракрасный детектор (IRD), фотоионизационный детектор (PID), детектор ионизации импульсного разряда (PDD) и термоэлектронный ионизационный детектор (TID).[15]
Методы

Метод представляет собой совокупность условий, в которых ГХ работает для данного анализа. Разработка метода - это процесс определения того, какие условия являются адекватными и / или идеальными для требуемого анализа.
Условия, которые могут быть изменены для проведения необходимого анализа, включают температуру на входе, температуру детектора, температуру колонки и температурную программу, скорость потока газа-носителя и газа-носителя, стационарную фазу колонки, диаметр и длину, тип и скорость потока на входе, размер образца и ввод техника. В зависимости от детектора (ов) (см. Ниже), установленного на ГХ, может существовать ряд условий детектора, которые также можно изменять. Некоторые ГХ также включают клапаны, которые могут изменять направление потока пробы и носителя. Время открытия и закрытия этих клапанов может иметь важное значение при разработке метода.
Выбор газа-носителя и скорость потока
Типичные газы-носители включают гелий, азот, аргон, водород и воздуха. Какой газ использовать, обычно определяется используемым детектором, например, СДЕЛАЛ в качестве газа-носителя требуется гелий. Однако при анализе проб газа носитель иногда выбирают на основе матрицы пробы, например, при анализе смеси в аргоне, носитель аргона предпочтителен, поскольку аргон в пробе не отображается на хроматограмме. Безопасность и доступность также могут влиять на выбор носителя, например, водород воспламеняем, а гелий высокой чистоты может быть трудно получить в некоторых регионах мира. (Видеть: Гелий - возникновение и производство.) В результате того, что гелий становится все более дефицитным, водород часто заменяется гелием в качестве газа-носителя в нескольких приложениях.
Чистота газа-носителя также часто определяется детектором, хотя необходимый уровень чувствительности также может играть важную роль. Обычно используется чистота 99,995% или выше. Наиболее распространенными степенями чистоты, требуемыми современными приборами для большинства чувствительности, являются степени 5,0, или чистота 99,999%, что означает, что в газе-носителе содержится всего 10 ppm примесей, которые могут повлиять на результаты. Наиболее часто используемые классы чистоты - это 6,0, но потребность в обнаружении на очень низких уровнях в некоторых криминалистических и экологических приложениях вызвала потребность в газах-носителях с чистотой 7,0, и теперь они коммерчески доступны. Торговые наименования типичной чистоты включают «нулевой класс», «сверхвысокий уровень чистоты (UHP)», «класс 4,5» и «класс 5,0».
Линейная скорость газа-носителя влияет на анализ так же, как и температура (см. Выше). Чем выше линейная скорость, тем быстрее анализ, но меньше разделение между аналитами. Следовательно, выбор линейной скорости - это такой же компромисс между уровнем разделения и продолжительностью анализа, что и выбор температуры колонки. Линейная скорость будет реализована посредством расхода газа-носителя относительно внутреннего диаметра колонны.
В ГХ, выпущенных до 1990-х годов, скорость потока носителя контролировалась косвенно, путем регулирования давления на входе носителя или «давления в головке колонны». Фактический расход измерялся на выходе из колонки или детектора с помощью электронного расходомера или пузырькового расходомера, и это могло быть трудоемким, трудоемким и неприятным процессом. Невозможно было изменить настройку давления во время эксперимента, и, таким образом, поток был практически постоянным во время анализа. Связь между расходом и давлением на входе рассчитывается с помощью Уравнение Пуазейля для сжимаемых жидкостей.
Однако многие современные газовые хроматографы измеряют скорость потока электронным способом и регулируют давление газа-носителя, чтобы задать скорость потока. Следовательно, давление носителя и скорость потока можно регулировать во время цикла, создавая программы давления / расхода, аналогичные программам температуры.
Выбор стационарного соединения
В полярность растворенного вещества имеет решающее значение для выбора стационарного соединения, которое в оптимальном случае будет иметь такую же полярность, что и растворенное вещество. Обычными стационарными фазами в открытых трубчатых колоннах являются цианопропилфенилдиметилполисилоксан, карбовакс-полиэтиленгликоль, бисцианопропилцианопропилфенилполисилоксан и дифенилдиметилполисилоксан. Для насадочных колонн доступны другие варианты.[10]
Типы входов и скорости потока
Выбор типа впускного отверстия и техники впрыска зависит от того, находится ли образец в жидкой, газовой, адсорбированной или твердой форме, а также от того, присутствует ли матрица растворителя, которая должна быть испарена. Растворенные образцы можно вводить непосредственно в колонку через инжектор COC, если условия хорошо известны; если матрица растворителя должна быть испарена и частично удалена, используется инжектор S / SL (наиболее распространенный метод впрыска); газовые пробы (например, воздушные баллоны) обычно вводятся с использованием системы клапанов переключения газа; адсорбированные образцы (например, на трубках с адсорбентом) вводятся с использованием либо внешнего (оперативного или автономного) устройства десорбции, такого как система продувки и улавливания, либо десорбируются в инжекторе (приложения для ТФМЭ).
Размер образца и метод ввода
Ввод образца
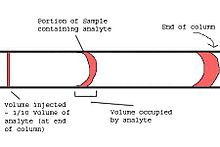
Настоящий хроматографический анализ начинается с введения образца в колонку. Развитие капиллярной газовой хроматографии привело к множеству практических проблем с техникой впрыска. Метод впрыска в колонку, часто используемый с насадочными колонками, обычно невозможен с капиллярными колонками. В системе впрыска в капиллярном газовом хроматографе впрыскиваемое количество не должно перегружать колонку, а ширина впрыскиваемой пробки должна быть небольшой по сравнению с разбрасыванием из-за хроматографического процесса. Несоблюдение этого последнего требования снизит разделительную способность колонки. Как правило, закачиваемый объем Vтравма, а объем ячейки детектора VDet, должна составлять около 1/10 объема, занятого частью образца, содержащей интересующие молекулы (аналиты), когда они выходят из колонки.
Некоторые общие требования, которым должна соответствовать хорошая методика впрыска, заключаются в том, чтобы можно было получить оптимальную эффективность разделения колонки, она должна позволять точные и воспроизводимые инъекции небольших количеств репрезентативных проб, она не должна вызывать изменений в составе пробы, она не должна демонстрировать различение, основанное на различиях в температуре кипения, полярности, концентрации или термической / каталитической стабильности, и его следует применять для анализа следов, а также для неразбавленных образцов.
Однако существует ряд проблем, связанных с использованием шприцев для инъекций. Даже самые лучшие шприцы утверждают, что точность составляет всего 3%, а в неквалифицированных руках ошибок намного больше. Игла может отрезать небольшие кусочки резины от перегородки, когда через нее вводится образец. Они могут заблокировать иглу и помешать наполнению шприца при следующем использовании. Может быть неочевидно, что это произошло. Часть пробы может попасть в резину и высвободиться во время последующих инъекций. Это может вызвать появление паразитных пиков на хроматограмме. Возможна избирательная потеря более летучих компонентов пробы за счет испарения с кончика иглы.[16]
Выбор столбца
Выбор колонки зависит от образца и активного измеряемого объекта. Основным химическим признаком, учитываемым при выборе колонки, является полярность смеси, но функциональные группы может играть большую роль при выборе столбца. Полярность образца должна точно соответствовать полярности неподвижной фазы колонки для увеличения разрешающая способность и разделение при сокращении времени работы. Разделение и время анализа также зависят от толщины пленки (неподвижной фазы), диаметра колонки и длины колонки.
Температура колонки и температурная программа

Колонка (и) в ГХ находится в термостате, температура которого точно регулируется электронным способом. (Обсуждая «температуру колонки», аналитик технически имеет в виду температуру термостата колонки. Однако это различие не имеет значения и не будет проводиться в этой статье.)
Скорость прохождения пробы через колонку прямо пропорциональна температуре колонки. Чем выше температура колонки, тем быстрее проба движется по колонке. Однако чем быстрее проба движется через колонку, тем меньше она взаимодействует с неподвижной фазой и тем меньше разделяются аналиты.
Обычно температура колонки выбирается так, чтобы обеспечить компромисс между продолжительностью анализа и уровнем разделения.
Метод, при котором колонка поддерживается при одной и той же температуре на протяжении всего анализа, называется «изотермическим». Однако в большинстве методов температура колонки повышается во время анализа, начальная температура, скорость повышения температуры (температурный «линейный рост») и конечная температура называются температурной программой.
Температурная программа позволяет анализируемым веществам, которые элюируются на ранней стадии анализа, адекватно разделяться, сокращая время, необходимое для прохождения поздно элюируемых аналитов через колонку.
Обработка и анализ данных
Качественный анализ
Как правило, хроматографические данные представлены в виде графика отклика детектора (ось y) от времени удерживания (ось x), который называется хроматограммой. Это обеспечивает спектр пиков для образца, представляющего аналиты присутствует в образце, элюируемом из колонки в разное время. Время удерживания можно использовать для идентификации аналитов, если условия метода постоянны. Кроме того, характер пиков будет постоянным для образца при постоянных условиях и может идентифицировать сложные смеси аналитов. Однако в большинстве современных приложений ГХ подключен к масс-спектрометр или аналогичный детектор, который способен идентифицировать аналиты, представленные пиками.
Количественный анализ
Площадь под пиком пропорциональна количеству анализируемого вещества, присутствующего на хроматограмме. Посчитав площадь пика с помощью математической функции интеграция можно определить концентрацию аналита в исходной пробе. Концентрацию можно рассчитать с помощью калибровочная кривая создается путем нахождения ответа на серию концентраций аналита или путем определения относительный коэффициент отклика аналита. Коэффициент относительного отклика - это ожидаемое отношение аналита к внутренний стандарт (или же внешний стандарт ) и рассчитывается путем нахождения отклика известного количества аналита и постоянного количества внутреннего стандарта (химического вещества, добавляемого в образец при постоянной концентрации с различным временем удерживания аналита).
В большинстве современных ГХ-МС системы, компьютер программного обеспечения используется для рисования и интегрирования пиков и сопоставления РС спектры в библиотеку спектров.
Приложения
Как правило, вещества, которые испаряются при температуре ниже 300 ° C (и, следовательно, стабильны до этой температуры), можно измерить количественно. Образцы также должны быть соль -свободный; они не должны содержать ионы. Можно измерить очень незначительные количества вещества, но часто требуется, чтобы образец измерялся по сравнению с образцом, содержащим чистое подозреваемое вещество, известное как эталонный стандарт.
Чтобы сделать показания более значимыми, можно использовать различные температурные программы; например, чтобы различать вещества, которые ведут себя одинаково во время процесса ГХ.
Специалисты, работающие с GC, анализируют содержание химического продукта, например, для проверки качества продуктов в химической промышленности; или измерения токсичных веществ в почве, воздухе или воде. ГХ очень точен при правильном использовании и может измерять пикомоли вещества в жидкой пробе объемом 1 мл, или частей на миллиард концентрации в газовых пробах.
На практических курсах в колледжах студенты иногда знакомятся с ГК, изучая содержание Лаванда масла или измерения этилен что секретируется Nicotiana benthamiana растения после искусственного повреждения их листьев. Эти ГХ анализируют углеводороды (C2-C40 +). В типичном эксперименте насадочная колонка используется для разделения легких газов, которые затем обнаруживаются с помощью TCD. В углеводороды отделяются с помощью капиллярной колонки и обнаруживаются с помощью FID. Сложность с анализами легких газов, которые включают H2 заключается в том, что He, который является наиболее распространенным и наиболее чувствительным инертным носителем (чувствительность пропорциональна молекулярной массе), имеет почти идентичную теплопроводность с водородом (разница в теплопроводности между двумя отдельными нитями в схеме типа моста Уитстона показывает когда компонент был элюирован). По этой причине широко используются приборы с двойным ТПД с отдельным каналом для водорода, в котором в качестве носителя используется азот. Аргон часто используется при анализе химических реакций газовой фазы, таких как синтез F-T, так что можно использовать один газ-носитель, а не два отдельных. Чувствительность снижена, но это компромисс в пользу простоты подачи газа.
Газовая хроматография широко используется в Криминалистика. Такие разнообразные дисциплины, как идентификация и количественная оценка твердой дозы наркотика (форма перед употреблением), расследование поджогов, анализ сколов краски и токсикологические исследования, используют GC для выявления и количественной оценки различных биологических образцов и улик с места преступления.
В популярной культуре
В этом разделе тон или стиль могут не отражать энциклопедический тон используется в Википедии. (Октябрь 2019) (Узнайте, как и когда удалить этот шаблон сообщения) |
Фильмы, книги и телешоу имеют тенденцию искажать возможности газовой хроматографии и работу, выполняемую с помощью этих инструментов.
В телешоу США CSI например, ГХ используются для быстрой идентификации неизвестных образцов. Например, аналитик может сказать через пятнадцать минут после получения образца: «Это бензин куплен в Шеврон станции за последние две недели ".
Фактически, типичный анализ газовой хроматографии занимает гораздо больше времени; иногда один образец необходимо запустить более часа в соответствии с выбранной программой; и еще больше времени необходимо, чтобы «нагреть» колонку, чтобы освободить ее от первого образца и использовать для следующего. В равной степени необходимо несколько прогонов, чтобы подтвердить результаты исследования - анализ ГХ одного образца может просто дать результат на случайность (см. Статистическая значимость ).
Кроме того, ГХ не позволяет точно идентифицировать большинство образцов; и не все вещества в образце обязательно будут обнаружены. Все, что вам действительно говорит ГХ, - это то, в какое относительное время компонент элюировался из колонки и что детектор был к нему чувствителен. Чтобы результаты были значимыми, аналитикам необходимо знать, какие компоненты при каких концентрациях следует ожидать; и даже в этом случае небольшое количество вещества может скрываться за веществом, имеющим как более высокую концентрацию, так и такое же относительное время элюирования. И последнее, но не менее важное: результаты пробы необходимо часто сравнивать с ГХ-анализом контрольной пробы, содержащей только предполагаемое вещество.
А ГХ-МС может устранить большую часть этой двусмысленности, поскольку масс-спектрометр определит молекулярную массу компонента. Но это все еще требует времени и навыков, чтобы сделать это правильно.
Точно так же большинство анализов ГХ не нажать кнопку операции. Вы не можете просто бросить пробирку с образцом в лоток автоматического пробоотборника, нажать кнопку и заставить компьютер сказать вам все, что вам нужно знать о пробе. Операционная программа должна быть тщательно выбрана в соответствии с ожидаемым составом пробы.
Кнопка может использоваться для многократного анализа аналогичных образцов, например, в химической производственной среде, или для сравнения 20 образцов из одного и того же эксперимента для расчета среднего содержания одного и того же вещества. Однако в отношении тех расследований, которые изображаются в книгах, фильмах и телешоу, это явно не так.
Газовый хроматограф и его изобретатель Арчер Мартин был кратко упомянут в Симпсоны Сезон 3, Эпизод 9 “Flaming Moe’s "В шоу-энд-рассказе в Барта учебный класс.
Смотрите также
- Аналитическая химия
- Хроматография
- Газовая хроматография – масс-спектрометрия
- Высокоэффективная жидкостная хроматография
- Обратная газовая хроматография
- Стандартное дополнение
- Тонкослойная хроматография
- Неразрешенная сложная смесь
- Вторичная ионизация электрораспылением
- Масс-спектрометрия реакции переноса протона
- Масс-спектрометрия с проточной трубкой для выбранных ионов
Рекомендации
- ^ а б c Павия, Л., Гэри М. Лэмпман, Джордж С. Криц, Рэндалл Г. Энгель (2006). Введение в органические лабораторные методы (4-е изд.). Томсон Брукс / Коул. С. 797–817. ISBN 978-0-495-28069-9.CS1 maint: несколько имен: список авторов (связь)
- ^ "Газовая хроматография". Linde AG. Архивировано из оригинал 3 марта 2012 г.. Получено 11 марта 2012.
- ^ Гроб, Конрад (1997). «Газы-носители для ГХ». Restek Advantage, Restek Corporation. Получено 9 марта, 2016.
- ^ "Berichte der Deutschen Botanischen Gesellschaft v.24 1906". HathiTrust. Получено 2019-04-19.
- ^ Эттре, Лесли С. (2008), Начало газовой адсорбционной хроматографии 60 лет назад, LCGC Северная Америка
- ^ Р. А. Дьюар; МакВИЛЬЯМ И.Г. (март 1958 г.). "Детектор ионизации пламенем для газовой хроматографии". Природа. 181 (4611): 760. Bibcode:1958Натура.181..760М. Дои:10.1038 / 181760a0. ISSN 1476-4687.
- ^ Карвалью, Матеус (2018). "Osmar, автоматический пробоотборник для микрошприцев с открытым исходным кодом". ОборудованиеX. 3: 10–38. Дои:10.1016 / j.ohx.2018.01.001.
- ^ Честин, Томас Г. «Сплит / без деления и колонные газовые хроматографические инжекторы». Получено 6 октября, 2019.
- ^ "Газовая хроматография". ACRF. Получено 11 марта 2012.
- ^ а б c d е ж грамм час я j k л м п о п Харрис, Дэниел С. (1999). «24. Газовая хроматография». Количественный химический анализ (Глава) (Пятое изд.). В. Х. Фриман и компания. С. 675–712. ISBN 978-0-7167-2881-8.
- ^ а б c d е ж грамм час я j k л м п о п Хигсон, С. (2004). Аналитическая химия. OXFORD University Press ISBN 978-0-19-850289-0
- ^ Дауэнхауэр, Пол (21 января 2015 г.). «Количественный детектор углерода (КХД) для определения характеристик сложных смесей с высоким разрешением без калибровки». Лабораторный чип. 15 (2): 440–7. Дои:10.1039 / c4lc01180e. PMID 25387003.
- ^ Скуг, Дуглас А .; West, Donald M .; Джеймс Холлер, Ф .; Крауч, Стэнли Р. (1 января 2013 г.). Основы аналитической химии. Скуг, Дуглас А., Уэст, Дональд М., Холлер, Ф. Джеймс, Крауч, Стэнли Р. (Девятое изд.). Бельмонт, Калифорния. ISBN 9780495558286. OCLC 824171785.
- ^ Schug, Kevin A .; Савицкий, Ян; Карлтон, Дуг Д .; Фань, Хуэй; Макнейр, Гарольд М .; Ниммо, Джон П .; Кролл, Питер; Смэтс, Джонатан; Уолш, Филипп; Харрисон, Дейл (1834). «Вакуумный ультрафиолетовый детектор для газовой хроматографии». Аналитическая химия. 86 (16): 8329–35. Дои:10.1021 / ac5018343. PMID 25079505.
- ^ «Детекторы на основе ионизации для газовой хроматографии». Журнал хроматографии А. 1421: 137–153. 2015-11-20. Дои:10.1016 / j.chroma.2015.02.061.
- ^ Grob, Robert L .; Барри, Юджин Ф. (2004). Современная практика газовой хроматографии (4-е изд.). Джон Вили и сыновья. ISBN 978-0-471-22983-4.
внешняя ссылка
![]() СМИ, связанные с Газовая хроматография в Wikimedia Commons
СМИ, связанные с Газовая хроматография в Wikimedia Commons
- Хроматографические колонки в библиотеке Chemistry LibreTexts
- Газовая хроматография в Керли
