Фосфорибулокиназа - Phosphoribulokinase
| фосфорибулокиназа | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 Трехмерное мультипликационное изображение протомера фосфорибулокиназы из Methanospirillum hungatei | |||||||||
| Идентификаторы | |||||||||
| Номер ЕС | 2.7.1.19 | ||||||||
| Количество CAS | 9030-60-8 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| БРЕНДА | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | AmiGO / QuickGO | ||||||||
| |||||||||
Фосфорибулокиназа (ФРК) (EC 2.7.1.19 ) является важным фотосинтетический фермент это катализирует то АТФ -зависимый фосфорилирование из рибулоза 5-фосфат (RuP) в рибулоза 1,5-бисфосфат (RuBP), оба промежуточные звенья в Цикл Кальвина. Его основная функция - регенерировать RuBP, который является исходным субстрат и CO2-акцепторная молекула цикла Кальвина.[1] ФРК принадлежит к семейству ферменты трансферазы, особенно те, которые переносят фосфорсодержащие группы (фосфотрансферазы ) к акцептору спиртовой группы. Вместе с рибулозо-1,5-бисфосфаткарбоксилаза / оксигеназа (RuBisCo) фосфорибулокиназа уникальна для цикла Кальвина.[2] Следовательно, активность ФРК часто определяет скорость метаболизма в организмах, для которых фиксация углерода ключ к выживанию.[3] Большая часть первоначальной работы по PRK была проделана с шпинат экстракты листьев в 1950-х годах; последующие исследования PRK в других фотосинтетических прокариотический и эукариотический организмы последовали. Возможность существования PRK была впервые признана Weissbach et al. в 1954 г .; например, группа отметила, что углекислый газ фиксация в сырых экстрактах шпината усиливалась добавлением АТФ.[3][4] Первая очистка PRK была проведена Гурвицем и его коллегами в 1956 году.[5][6][7]
АТФ + Mg2+ - D-рибулозо-5-фосфат АДФ + D-рибулоза 1,5-бисфосфат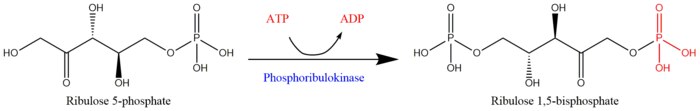 Схема реакции восстановления рибулозо-1,5-бисфосфата из рибулозо-5-фосфата фосфорибулокиназой[1]
Схема реакции восстановления рибулозо-1,5-бисфосфата из рибулозо-5-фосфата фосфорибулокиназой[1]
Два субстраты ФРК АТФ и D-рибулоза 5-фосфат, а его два продукты находятся ADP и D-рибулоза 1,5-бисфосфат. Деятельность ФРК требует наличия двухвалентный металл катион как Mg2+, как указано в приведенной выше реакции.[3]
Структура
Структура PRK различна у прокариот и эукариот. Прокариотические PRK обычно существуют как октамеры 32 кДа подразделения, в то время как эукариотические PRK часто димеры субъединиц 40 кДа.[8][9] Структурные определения для эукариотической PRK еще предстоит провести, но прокариотические структуры PRK все еще полезны для рационализации регуляции и механизма PRK. По состоянию на 2018 г. только две кристаллические структуры были разрешены для этого класса ферментов в Rhodobacter sphaeroides и Methanospirillum hungatei, с соответствующими PDB коды доступа 1A7J и 5B3F.

Rhodobacter sphaeroides
В Rhodobacter sphaeroides, PRK (или RsPRK) существует как гомооктомер с участием протомеры состоит из семи нитей смешанные β-листы, Семь α-спирали, и вспомогательная пара антипараллельных β-тяжи.[10] Субъединица РсПРК обнаруживает сворачивание белка аналогично складыванию нуклеотидмонофосфат (NMP) киназы.[3] Исследования мутагенеза предполагаю, что либо Asp 42 или Asp 169 действует как каталитический база это депротонирует O1 гидроксил кислород на RuP для нуклеофильная атака АТФ, а другой действует лиганд для катиона металла как Mg2+ (подробнее см. механизм ниже).[10] Другой остатки присутствует на активный сайт для РСПРК включают Его 45, Arg 49, Arg 168 и Arg 173, которые предположительно участвуют в связывании RuP.[10] (См. Изображение справа).
Methanospirillum hungatei
В архей ФРК Methanospirillum hungatei, ФРК (или МхПРК) существует как гомодимер из двух протомеры, каждый из которых состоит из восьмицепочечных смешанных β-листов, окруженных α-спиралями и β-цепями - аналогично структуре бактериальной PRK из Р. sphaeroides (см. информационное поле выше).[11] Хотя их четвертичные структуры отличаются и у них низкий идентичность аминокислотной последовательности, МхПРК и РспРК имеют сходные по конструкции N-концевые домены а также последовательно консервативные остатки, такие как His 55, Lys 151 и Arg 154.[11]
Механизм и деятельность
PRK катализирует фосфорилирование RuP в RuBP. Каталитический остаток в ферменте (т.е. аспартат в RsPRK) депротонирует кислород гидроксила O1 на RuP и активирует это для нуклеофильной атаки γ-фосфорильная группа АТФ.[10] Поскольку γ-фосфорильная группа переносится от АТФ к RuP, ее стереохимия инвертирует.[12] Чтобы учесть такую инверсию, каталитический механизм PRK не должен включать фосфорильный фермент. средний.[12]
Некоторые исследования предполагают, что оба субстрата (АТФ и RuP) одновременно связываются с PRK и образуют тройной комплекс. Другие предполагают, что добавление субстрата происходит последовательно; конкретный порядок, в котором добавляются субстраты, все еще оспаривается и может фактически различаться для разных организмов.[13][14] Помимо связывания субстратов, PRK также требует перевязка катионам двухвалентных металлов, например Mg2+ или Mn2+ для деятельности; Hg2+ было продемонстрировано, чтобы инактивировать фермент.[3][15]
Ферментная специфичность
ФРК показывает высокий специфичность для рибулозо-5-фосфата. Он не действует ни на одну из следующих поверхностей: D-ксилулоза 5-фосфат, фруктозо-6-фосфат, и седогептулоза 7-фосфат.[15] Однако при высоком концентрации, PRK может иногда фосфорилировать рибозо-5-фосфат, соединение перед Шаг регенерации RuBP в цикле Кальвина.[15] Кроме того, PRK, выделенный из Alcaligenes eutrophus было показано использовать уридинтрифосфат (UTP) и гуанозинтрифосфат (GTP) в качестве субстратов, альтернативных АТФ.[8][3]
эффекты pH
Реакция фосфорилирования протекает с максимальным скорость в pH 7,9, без обнаруживаемой активности при pH ниже 5,5 или выше 9,0.[15]
Регулирование
В механизмы с помощью которых прокариотические и эукариотические PRK регулируемый варьироваться. Прокариотические PRK обычно подвержены аллостерическая регуляция в то время как эукариотические PRK часто регулируются обратимый тиол /дисульфид обмен.[16] Эти различия, вероятно, связаны со структурными различиями в их С-концевые домены[11]
Аллостерическая регуляция прокариотической PRK
НАДН известно, что стимулирует активность PRK, в то время как AMP и фосфоенолпируват (PEP), как известно, подавляют активность.[3] Было показано, что AMP участвует в конкурентное торможение в Thiobacillus ferrooxidans ФРК.[17] С другой стороны, PEP действует как неконкурентный ингибитор ФРК.[18]
Регуляция эукариотической PRK
Эукариотическая PRK обычно регулируется через обратимый Снижение окисления своего цистеин сульфгидрил группы, но исследования показывают, что его деятельность может регулироваться другими белки или метаболиты в хлоропласт. Таких метаболитов, 6-фосфоглюконат Было показано, что он является наиболее эффективным ингибитором эукариотической PRK, конкурируя с RuP за активный сайт фермента.[19] Это явление может возникать из-за схожести молекулярная структура между 6-фосфоглюконатом и RuP.
Более поздняя работа по регуляции эукариотической PRK была сосредоточена на ее способности формировать мультиферментные комплексы с другими ферментами цикла Кальвина, такими как глицеральдегид-3-фосфатдегидрогеназа (G3PDH) или RuBisCo.[20] В Хламидомонада Reinhardtii, PRK хлоропласта и G3PDH существуют как биферментный комплекс из 2 молекул димерного PRK и 2 молекул тетрамерный Тщательная ассоциация G3PDH с помощью остатка Arg 64, который потенциально может также передавать информацию между двумя ферментами.[21]
Мультиферментные комплексы, вероятно, имеют более сложные регуляторные механизмы, и исследования уже исследовали такие процессы. Например, было показано, что комплексы PRK-глицеральдегид-3-фосфатдегидрогеназа в Scenedesmus obliquus диссоциировать только для высвобождения активированных форм составляющих его ферментов в присутствии НАДФН, дитиотреитол (DTT), и тиоредоксин.[22] Другой интересной темой было сравнение относительных уровней активности PRK в тех случаях, когда она комплексна, и когда это не так. Для различных фотосинтезирующих эукариот ферментативная активность комплексной PRK может быть усилена по сравнению со свободной PRK, и наоборот.[23][24]
Другие имена
В систематическое название этого класса ферментов является АТФ: D-рибулозо-5-фосфат-1-фосфотрансфераза. Другие широко используемые названия включают фосфопентокиназу, рибулозо-5-фосфаткиназу, фосфопентокиназу, фосфорибулокиназу (фосфорилирование), 5-фосфорибулозокиназу, рибулозофосфаткиназу, PKK, PRuK и PRK.
использованная литература
- ^ а б 1958-, Берг, Джереми М. (Джереми Марк) (2015-04-08). Биохимия. Тимочко, Джон Л., 1948-, Гатто, Грегори Дж., Младший (Грегори Джозеф), Страйер, Люберт. (Восьмое изд.). Нью-Йорк. ISBN 978-1464126109. OCLC 913469736.CS1 maint: числовые имена: список авторов (ссылка на сайт)
- ^ Марсден WJ (16 сентября 1983 г.). «Очистка и молекулярные и каталитические свойства фосфорибулокиназы из Cyanobacterium Chlorogloeopsis fritschii». Журнал общей микробиологии. 130 (4): 999–1006. Дои:10.1099/00221287-130-4-999.
- ^ а б c d е ж г Miziorko HM (2000). «Фосфорибулокиназа: современные взгляды на структуру / функциональную основу регуляции и катализа». В Purich DL (ред.). Достижения в энзимологии и смежных областях молекулярной биологии. Достижения в энзимологии и смежных областях молекулярной биологии. 74. John Wiley & Sons, Inc., стр. 95–127. Дои:10.1002 / 9780470123201.ch3. ISBN 9780470123201. PMID 10800594.
- ^ Вайсбах А., Смирниотис П.З., Хорекер Б.Л. (июль 1954 г.). «Фиксация пентозофосфата и СО2 экстрактами шпината». Журнал Американского химического общества. 76 (13): 3611–3612. Дои:10.1021 / ja01642a090.
- ^ Hurwitz J, Weissbach A, Horecker BL, Smyrniotis PZ (февраль 1956 г.). «Фосфорибулокиназа шпината». Журнал биологической химии. 218 (2): 769–83. PMID 13295229.
- ^ Ракер Э (июль 1957 г.). «Восстановительный пентозофосфатный цикл. I. Фосфорибулокиназа и рибулозодифосфаткарбоксилаза». Архивы биохимии и биофизики. 69: 300–10. Дои:10.1016/0003-9861(57)90496-4. PMID 13445203.
- ^ Якоби В. Б., Браммонд Д. О., Очоа С. (февраль 1956 г.). «Образование 3-фосфоглицериновой кислоты путем фиксации двуокиси углерода ферментами листьев шпината». Журнал биологической химии. 218 (2): 811–22. PMID 13295232.
- ^ а б Зиберт К., Шоберт П., Боуэн Б. (март 1981 г.). «Очистка, некоторые каталитические и молекулярные свойства фосфорибулокиназы из Alcaligenes eutrophus». Biochimica et Biophysica Acta (BBA) - Энзимология. 658 (1): 35–44. Дои:10.1016/0005-2744(81)90247-3. PMID 6260209.
- ^ Б. Бьюкенен, Боб (28 ноября 2003 г.). «Роль света в регуляции ферментов хлоропластов». Анну. Rev. Plant Physiol. 31: 341–374. Дои:10.1146 / annurev.pp.31.060180.002013.
- ^ а б c d Харрисон Д.Х., Ранквист Дж. А., Голуб А., Мизиорко Н. М. (апрель 1998 г.). «Кристаллическая структура фосфорибулокиназы из Rhodobacter sphaeroides обнаруживает складку, аналогичную структуре аденилаткиназы». Биохимия. 37 (15): 5074–85. Дои:10.1021 / bi972805y. PMID 9548738.
- ^ а б c Коно Т., Мехротра С., Эндо К., Кизу Н., Матусда М., Кимура Х., Мизохата Е., Иноуэ Т., Хасунума Т., Йокота А., Мацумура Х, Ашида Х (январь 2017 г.). «Путь метаболизма углерода, опосредованный RuBisCO, у метаногенных архей». Nature Communications. 8: 14007. Bibcode:2017НатКо ... 814007K. Дои:10.1038 / ncomms14007. ЧВК 5241800. PMID 28082747.
- ^ а б Miziorko HM, Eckstein F (ноябрь 1984 г.). «Стереохимический ход реакции, катализируемой рибулозо-5-фосфаткиназой». Журнал биологической химии. 259 (21): 13037–40. PMID 6490643.
- ^ Лебретон С., Гонтеро Б., Авилан Л., Рикар Дж. (Декабрь 1997 г.). «Передача информации в мультиферментных комплексах - 1. Термодинамика конформационных ограничений и эффектов памяти в биферментном глицеральдегид-3-фосфат-дегидрогеназно-фосфорибулокиназном комплексе хлоропластов Chlamydomonas reinhardtii». Европейский журнал биохимии. 250 (2): 286–95. Дои:10.1111 / j.1432-1033.1997.0286a.x. PMID 9428675.
- ^ Вадано А., Нисикава К., Хирахаси Т., Сато Р., Иваки Т. (1 апреля 1998 г.). «Механизм реакции фосфорибулокиназы из цианобактерии Synechococcus PCC7942». Фотосинтез Исследования. 56 (1): 27–33. Дои:10.1023 / А: 1005979801741. S2CID 21409736.
- ^ а б c d Гурвиц Дж (1962). [28c] Фосфорибулокиназа. Методы в энзимологии. 5. С. 258–261. Дои:10.1016 / с0076-6879 (62) 05214-3. ISBN 9780121818050.
- ^ Табита FR (сентябрь 1980 г.). «Контроль пиридиновых нуклеотидов и субъединичная структура фосфорибулокиназы фотосинтезирующих бактерий». Журнал бактериологии. 143 (3): 1275–80. Дои:10.1128 / JB.143.3.1275-1280.1980. ЧВК 294495. PMID 6251028.
- ^ Гейл Н.Л., Бек СП (сентябрь 1966 г.). «Конкурентное ингибирование фосфорибулокиназы AMP». Сообщения о биохимических и биофизических исследованиях. 24 (5): 792–6. Дои:10.1016 / 0006-291X (66) 90396-2. PMID 5970515.
- ^ Баллард Р. У., Макелрой Р. Д. (август 1971 г.). «Фосфоенолпируват, новый ингибитор фосфорибулокиназы в pseudomonas facilis». Сообщения о биохимических и биофизических исследованиях. 44 (3): 614–8. Дои:10.1016 / с0006-291x (71) 80127-4. PMID 4330777.
- ^ Gardemann, A .; Stitt, M .; Heldt, H.W. (1983-01-13). «Контроль фиксации СО2. Регулирование рибулозо-5-фосфаткиназы шпината с помощью уровней стромальных метаболитов». Biochimica et Biophysica Acta (BBA) - Биоэнергетика. 722 (1): 51–60. Дои:10.1016/0005-2728(83)90156-1.
- ^ Мюллер, Бруно (1972-08-01). «Лабильный комплекс ферментов, фиксирующих CO2, в хлоропластах шпината». Zeitschrift für Naturforschung B. 27 (8): 925–932. Дои:10.1515 / znb-1972-0814.
- ^ Авилан Л., Гонтеро Б., Лебретон С., Рикар Дж. (Декабрь 1997 г.). «Передача информации в мультиферментных комплексах - 2. Роль Arg64 фосфорибулокиназы Chlamydomonas reinhardtii в передаче информации между глицеральдегид-3-фосфатдегидрогеназой и фосфорибулокиназой». Европейский журнал биохимии. 250 (2): 296–302. Дои:10.1111 / j.1432-1033.1997.0296a.x. PMID 9428676.
- ^ Николсон С., Истерби Дж. С., Паулс Р. (январь 1987 г.). «Свойства мультимерного белкового комплекса из хлоропластов, обладающих потенциальной активностью НАДФН-зависимой глицеральдегид-3-фосфатдегидрогеназы и фосфорибулокиназы». Европейский журнал биохимии. 162 (2): 423–31. Дои:10.1111 / j.1432-1033.1987.tb10619.x. PMID 3026812.
- ^ Rault M, Gontero B, Ricard J (май 1991 г.). «Активация тиоредоксином фосфорибулокиназы в мультиферментном комплексе хлоропластов». Европейский журнал биохимии. 197 (3): 791–7. Дои:10.1111 / j.1432-1033.1991.tb15973.x. PMID 1851485.
- ^ Гонтеро Б., Муллиерт Дж., Ро М., Джудичи-Ортикони М. Т., Рикар Дж. (Ноябрь 1993 г.). «Структурно-функциональные свойства мультиферментного комплекса из хлоропластов шпината. 2. Модуляция кинетических свойств ферментов в агрегированном состоянии». Европейский журнал биохимии. 217 (3): 1075–82. Дои:10.1111 / j.1432-1033.1993.tb18339.x. PMID 8223631.


