Рибонуклеаза поджелудочной железы крупного рогатого скота - Bovine pancreatic ribonuclease
| Панкреатическая рибонуклеаза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
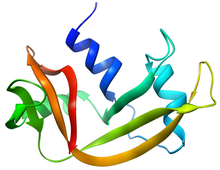 Структура РНКазы А | |||||||||
| Идентификаторы | |||||||||
| Номер ЕС | 3.1.27.5 | ||||||||
| Количество CAS | 9001-99-4 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| БРЕНДА | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | AmiGO / QuickGO | ||||||||
| |||||||||

Рибонуклеаза поджелудочной железы крупного рогатого скота, также часто называемый рибонуклеаза А поджелудочной железы крупного рогатого скота или просто РНКаза А, это панкреатическая рибонуклеаза фермент что раскалывает одноцепочечный РНК. Рибонуклеаза поджелудочной железы крупного рогатого скота - одна из классических модельных систем белок наука.[1] Два Нобелевские премии по химии были награждены за работы по рибонуклеазе поджелудочной железы крупного рогатого скота: в 1972 г. премия была присуждена Кристиан Анфинсен за его работу над сворачивание белка и чтобы Стэнфорд Мур и Уильям Штайн за их работу над взаимосвязью между белками структура и это химический механизм;[2] в 1984 г. премия была присуждена Роберт Брюс Меррифилд для развития химический синтез белков.[3]
История
Рибонуклеаза поджелудочной железы крупного рогатого скота стала обычной модельной системой при изучении белков в основном потому, что она была чрезвычайно стабильной и могла быть очищена в больших количествах. В 1940-е годы Броня и Компания очищенный килограмм белка - очень большое количество, особенно очистка белка стандарты того времени - и предлагали образцы по низкой цене заинтересованным ученым.[4] Возможность иметь одну партию очищенного фермент сделали его доминирующей модельной системой для изучения белков. Его обычно называют рибонуклеаза А или же РНКаза А как самый выдающийся член ее белковая семья, известный как панкреатическая рибонуклеаза, рибонуклеаза А или рибонуклеаза I.
Кристиан Анфинсен исследования окислительное сворачивание процесс рибонуклеазы поджелудочной железы крупного рогатого скота заложил основу для понимания взаимосвязи между аминокислотная последовательность и свернутый белок трехмерная структура и укрепил термодинамическая гипотеза сворачивания белка, согласно которому свернутая форма белка представляет его свободная энергия минимум.[4][5]
РНКаза А была первым ферментом, для которого правильный каталитический механизм был предложен еще до того, как стала известна его структура.[6] РНКаза А была первым белком, продемонстрировавшим эффекты неродных изомеры из пептидные связи предшествующий пролин остатки в сворачивании белка.[7]
Рибонуклеаза поджелудочной железы крупного рогатого скота также была модельным белком, используемым для разработки многих спектроскопических методов анализа структуры белка, включая поглощение, круговой дихроизм, Раман, электронный парамагнитный резонанс (EPR) и ядерный магнитный резонанс (ЯМР) спектроскопия. Это был первый модельный белок для разработки химических методов исследования белков, таких как химическая модификация открытых боковых цепей, антигенный признание и ограниченное протеолиз неупорядоченных сегментов. Рибонуклеаза S, которая представляет собой РНКазу А, обработанную протеаза субтилизин, был третьим белком, у которого кристаллографическая структура решена в 1967 г.[8]
Структура и свойства

РНКаза А - относительно небольшой белок (124 остатка, ~ 13,7 кДа). Его можно охарактеризовать как двухслойный белок с глубокой щелью для связывания субстрата РНК. Первый слой состоит из трех альфа спирали (остатки 3-13, 24-34 и 50-60) из N-концевой половины белка. Второй слой состоит из трех β-шпильки (остатки 61-74, 79-104 и 105-124 из С-концевой половины) расположены в два β-листы. Шпильки 61-74 и 105-124 образуют четырехцепочечный антипараллельный β-лист, который лежит на спираль 3 (остатки 50-60). Самая длинная β-шпилька 79-104 спаривается с короткой β-цепью (остатки 42-45) с образованием трехцепочечной антипараллельной β-лист что лежит на спираль 2 (остатки 24-34).
РНКаза A имеет четыре дисульфидные связи в своем нативном состоянии: Cys26-Cys84, Cys58-110, Cys40-95 и Cys65-72. Первые два (26-84 и 58-110) важны для конформационного сворачивания; каждый присоединяется к альфа спираль первого слоя до бета-лист второго слоя, образуя небольшое гидрофобное ядро поблизости. Две последние дисульфидные связи (40-95 и 65-72) менее важны для складывания; любой из них может быть уменьшен (но не оба сразу) без воздействия на нативную структуру в физиологических условиях. Эти дисульфидные связи соединяют сегменты петли и относительно подвержены воздействию растворителя. Дисульфидная связь 65-72 имеет чрезвычайно высокую склонность к образованию, значительно большую, чем можно было бы ожидать от ее петля энтропии, как в виде пептида, так и в виде полноразмерного белка. Это указывает на то, что β-шпилька 61-74 имеет высокую склонность к конформационному укладыванию.
РНКаза A - основной белок (pя = 9,63); его многочисленные положительные заряды согласуются с его привязкой к РНК (поли-анион ). В более общем плане РНКаза A необычно полярна или, скорее, необычно лишена гидрофобных групп, особенно алифатических. Это может объяснить потребность в четырех дисульфидных связях для стабилизации структуры. Низкое гидрофобное содержание может также служить для уменьшения физического отталкивания между высокозаряженными группами (собственными и их субстратной РНК) и областями с низким уровнем заряда. диэлектрическая постоянная (неполярные остатки).
N-терминал α-спираль РНКазы A (остатки 3-13) соединяется с остальной частью РНКазы A гибким линкером (остатки 16-23). Как показал Ф. М. Ричардс, этот линкер может расщепляться субтилизин между остатками 20 и 21, не вызывая диссоциации N-концевой спирали от остальной части РНКазы A. Комплекс пептид-белок называется «РНКаза S», пептид (остатки 1-20) называется «S-пептид» и остаток (остатки 21-124) называют «S-белком». В константа диссоциации S-пептида для S-белка составляет примерно 30 пМ; эта жесткая привязка может быть использована для очистка белка присоединением S-пептида к интересующему белку и пропусканием смеси через аффинную колонку со связанным S-белком. [Меньший С-пептид (остатки 1-13) также работают.] Модельная система РНКазы S также использовалась для изучения сворачивания белков путем сочетания сворачивания и ассоциации. S-пептид был первым пептидом из природного белка, который, как было показано, имеет (мерцающую) вторичную структуру изолированно (Кли и Браун в 1967 г.).
РНКаза А расщепляется после пиримидин нуклеотиды.[9] Расщепление происходит в два этапа: во-первых, 3 ’, 5’-фосфодиэфирная связь расщепляется с образованием 2’, 3’-циклического промежуточного фосфодиэфира; во-вторых, циклический фосфодиэфир гидролизуется до 3’-монофосфата.[10] Это может быть подавлено ингибитор рибонуклеазы белка, ионами тяжелых металлов и комплексами уридина с ванадатом.[10]
Ферментативный механизм
Положительные заряды РНКазы А лежат в основном в глубокой щели между двумя долями. Субстрат РНК находится в этой щели и расщепляется двумя каталитическими гистидин остатки His12 и His119 с образованием 2 ', 3'-циклического фосфатного промежуточного соединения, которое стабилизируется соседним Lys41.
Ферментативная регуляция
Этот белок может использовать морфеин модель аллостерическая регуляция.[11]
Смотрите также
Рекомендации
- ^ Рейнс RT (1998). «Рибонуклеаза А». Chem. Rev. 98 (3): 1045–1066. Дои:10.1021 / cr960427h. PMID 11848924.
- ^ "Нобелевская премия по химии 1972 г.". Nobelprize.org. Получено 10 февраля 2015.
- ^ "Нобелевская премия по химии 1984 г.". Nobelprize.org. Получено 10 февраля 2015.
- ^ а б Ричардс FM (1972). «Нобелевская премия 1972 года по химии». Наука. 178 (4060): 492–3. Дои:10.1126 / science.178.4060.492. PMID 17754377.
- ^ Marshall, G.R .; Feng, J. A .; Кустер, Д. Дж. (2008). «Назад в будущее: рибонуклеаза А». Биополимеры. 90 (3): 259–77. Дои:10.1002 / bip.20845. PMID 17868092.
- ^ Cuchillo CM, Nogués MV, Raines RT (2011). «Рибонуклеаза поджелудочной железы крупного рогатого скота: пятьдесят лет первому механизму ферментативной реакции». Биохимия. 50 (37): 7835–7841. Дои:10.1021 / bi201075b. ЧВК 3172371. PMID 21838247.
- ^ Шмид, FX; Болдуин, Р.Л. (октябрь 1978 г.). «Кислотный катализ образования медленно сворачивающихся видов РНКазы A: свидетельство того, что эта реакция является изомеризацией пролина». Труды Национальной академии наук Соединенных Штатов Америки. 75 (10): 4764–8. Дои:10.1073 / pnas.75.10.4764. ЧВК 336200. PMID 283390.
- ^ Wyckoff HW, Hardman KD, Allewell NM, Inagami T, Johnson LN, Richards FM (1967). «Структура рибонуклеазы-S при разрешении 3,5 А». J. Biol. Chem. 242 (17): 3984–8. PMID 6037556.
- ^ Волкин Э., Кон В.Е. (1953). «О строении рибонуклеиновых кислот. II. Продукты действия рибонуклеаз». J. Biol. Chem. 205 (2): 767–82. PMID 13129256.
- ^ а б Кристал Уортингтон. "Рибонуклеаза - Руководство по ферментам Уортингтона". Получено 2011-09-26.
- ^ Селвуд Т., Джаффе Э.К. (2012). «Динамические диссоциирующие гомоолигомеры и контроль функции белка». Arch. Biochem. Биофизы. 519 (2): 131–43. Дои:10.1016 / j.abb.2011.11.020. ЧВК 3298769. PMID 22182754.
дальнейшее чтение
- Kartha, G .; Bello, J .; Харкер, Д. (1967). Третичная структура рибонуклеазы. Бостон: Природа. ISBN 0-12-588945-3.
- Scheraga HA, Wedemeyer WJ, Welker E (2001). «Рибонуклеаза А поджелудочной железы крупного рогатого скота: исследования окислительного и конформационного фолдинга». Meth. Энзимол. 341: 189–221. Дои:10.1016 / S0076-6879 (01) 41153-0. PMID 11582778.
внешняя ссылка
- Рибонуклеаза + А в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)

