Паракринная передача сигналов - Paracrine signaling
Паракринная передача сигналов это форма передача сигналов от ячейки или от ячейки к ячейке в котором клетка выдает сигнал, чтобы вызвать изменения в соседних клетках, изменяя поведение этих клеток. Сигнальные молекулы, известные как паракринные факторы, распространяются на относительно короткие расстояния (местное действие), в отличие от клеточной передачи сигналов посредством эндокринные факторы, гормоны, которые перемещаются на значительно большие расстояния через сердечно-сосудистая система; юкстакриновые взаимодействия; и аутокринная сигнализация. Клетки, вырабатывающие паракринные факторы, секретируют их в непосредственное внеклеточный среда. Затем факторы перемещаются в соседние клетки, в которых полученный градиент фактора определяет результат. Однако точное расстояние, на которое могут пройти паракринные факторы, неизвестно.
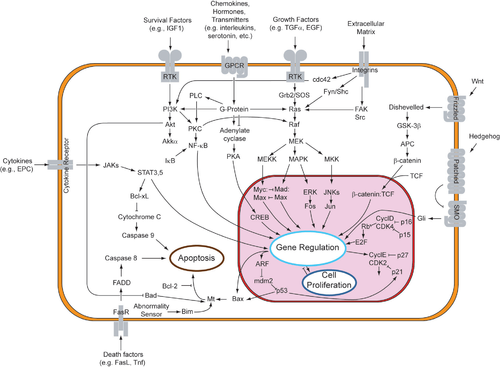
Хотя паракринная передача сигналов вызывает разнообразный набор ответов в индуцированных клетках, большинство паракринных факторов используют относительно упрощенный набор рецепторы и пути. На самом деле разные органы в организме - даже между разными видами - как известно, используют одинаковые наборы паракринных факторов в дифференциальном развитии.[1] Высококонсервативные рецепторы и пути могут быть организованы в четыре основных семейства на основе аналогичных структур: фактор роста фибробластов (FGF) семья, Ежик семья, Wnt семья и Суперсемейство TGF-β. Связывание паракринного фактора с его рецептором инициирует преобразование сигнала каскады, вызывающие разные ответы.
Паракринные факторы вызывают компетентных респондентов
Чтобы паракринные факторы успешно вызывали ответ в принимающей клетке, эта клетка должна иметь соответствующие рецепторы, доступные на клеточной мембране для приема сигналов, также известные как компетентный. Кроме того, отвечающая клетка также должна обладать способностью механически индуцироваться.
Семейство факторов роста фибробластов (FGF)
Хотя семейство паракринных факторов FGF выполняет широкий спектр функций, основные результаты подтверждают идею, что они в первую очередь стимулируют пролиферацию и дифференцировку.[2][3] Чтобы выполнять множество разнообразных функций, FGF могут быть альтернативно сплайсированы или даже иметь разные инициирующие кодоны для создания сотен различных FGF. изоформы.[4]
Одна из наиболее важных функций рецепторов FGF (FGFR) заключается в развитии конечностей. Эта сигнализация включает девять различных альтернативно сращенный изоформы рецептора.[5] Fgf8 и Fgf10 являются двумя ключевыми игроками в развитии конечностей. В инициировании передних конечностей и росте конечностей у мышей осевые (продольные) сигналы от промежуточных конечностей мезодерма производит Tbx5, что впоследствии сигнализирует о том же мезодерма производить Fgf10. Fgf10 затем сигнализирует эктодерма начать производство Fgf8, что также стимулирует выработку Fgf10. Исключение Fgf10 приводит к появлению мышей без конечностей.[6]
Кроме того, паракринная передача сигналов Fgf важна для развивающегося глаза цыплят. В fgf8 мРНК локализуется в том, что дифференцируется в нервной сетчатка из оптический стакан. Эти клетки контактируют с внешними клетками эктодермы, которые в конечном итоге станут линзами.[4]
Фенотип и выживаемость мышей после нокаута некоторых генов FGFR:[5]
| Ген нокаута FGFR | Выживание | Фенотип |
|---|---|---|
| Fgf1 | Жизнеспособный | Неясно |
| Fgf3 | Жизнеспособный | Внутреннее ухо, дифференциация скелета (хвоста) |
| Fgf4 | Смертельный | Разрастание внутренней клеточной массы |
| Fgf8 | Смертельный | Гаструляция дефект, развитие ЦНС, развитие конечностей |
| Fgf10 | Смертельный | Развитие нескольких органов (включая конечности, тимус, гипофиз) |
| Fgf17 | Жизнеспособный | Развитие мозжечка |
Путь рецепторной тирозинкиназы (RTK)
Паракринная передача сигналов через факторы роста фибробластов и его соответствующие рецепторы используют рецептор тирозин путь. Этот сигнальный путь хорошо изучен с использованием Дрозофила глаза и человеческий рак.[7]
Связывание FGF с FGFR фосфорилаты праздный киназа и активирует путь RTK. Этот путь начинается на поверхности клеточной мембраны, где лиганд связывается со своим специфическим рецептором. Лиганды, которые связываются с RTK, включают: факторы роста фибробластов, эпидермальные факторы роста, факторы роста тромбоцитов и фактор стволовых клеток.[7] Это димеризует трансмембранный рецептор к другому рецептору RTK, что вызывает аутофосфорилирование и последующее конформационное изменение из гомодимеризованный рецептор. Это конформационное изменение активирует спящую киназу каждой RTK на остатке тирозина. В связи с тем, что рецептор проходит через мембрану из внеклеточной среды через липидный бислой, и в цитоплазма связывание рецептора с лигандом также вызывает трансфосфорилирование цитоплазматического домена рецептора.[8]
An адаптерный белок (например, SOS) распознает фосфорилированный тирозин на рецепторе. Этот белок функционирует как мостик, который соединяет RTK с промежуточным белком (таким как GNRP), запуская внутриклеточный сигнальный каскад. В свою очередь, промежуточный белок стимулирует связанный с GDP Ras к активированному GTP-связанному Ras. GAP в конечном итоге возвращает Ras в неактивное состояние. Активация Рас может инициировать три сигнальных пути ниже Ras: Ras → Raf → MAP-киназный путь, PI3-киназный путь и Ral-путь. Каждый путь приводит к активации факторов транскрипции, которые проникают в ядро, чтобы изменить экспрессию генов.[9]

Рецептор RTK и рак
Было показано, что паракринная передача сигналов факторов роста между соседними клетками усугубляет канцерогенез. Фактически, мутантные формы одного RTK могут играть причинную роль в самых разных типах рака. Комплект протоонкоген кодирует рецептор тирозинкиназы, лиганд которого представляет собой паракринный белок, называемый фактором стволовых клеток (SCF), который важен для кроветворение (образование клеток в крови).[10] Рецептор Kit и родственные рецепторы тирозинкиназы на самом деле являются ингибирующими и эффективно подавляют активацию рецептора. Мутантные формы рецептора Kit, которые активируются конститутивно независимо от лигандов, обнаруживаются в разнообразном множестве злокачественных новообразований.[11]
Путь RTK и рак
Исследования по рак щитовидной железы выяснил теорию о том, что паракринная передача сигналов может помочь в создании микроокружения опухоли. Хемокин транскрипция активируется, когда Ras находится в GTP-связанном состоянии. Затем хемокины высвобождаются из клетки и могут свободно связываться с другой соседней клеткой. Паракринная передача сигналов между соседними клетками создает эту петлю положительной обратной связи. Таким образом, конститутивная транскрипция активированных белков формирует идеальную среду для возникновения опухолей.[12] Фактически, множественное связывание лигандов с рецепторами RTK чрезмерно стимулирует путь Ras-Raf-MAPK, который сверхэкспрессирует то митогенный и инвазивная способность клеток.[13]
Путь Jak-STAT
В дополнение к пути RTK, факторы роста фибробластов может также активировать сигнальный каскад Jak-STAT. Вместо того, чтобы нести ковалентно связанные домены тирозинкиназ, рецепторы Jak-STAT образуют нековалентные комплексы с тирозинкиназами Jak (Янус киназа ) учебный класс. Эти рецепторы связываются для эритропоэтин (важно для эритропоэз ), тромбопоэтин (важно для тромбоцит формирование), и интерферон (важно для обеспечения функции иммунных клеток).[14]
После димеризации рецепторов цитокинов после связывания лиганда Jaks трансфосфорилируют друг друга. Образующиеся фосфотирозины привлекают белки STAT. Белки STAT димеризуются и проникают в ядро, чтобы действовать как факторы транскрипции изменить экспрессию генов.[14] В частности, STATS транскрибируют гены, которые способствуют пролиферации и выживанию клеток, такие как myc.[15]
Фенотип и выживаемость мышей после нокаута некоторых генов Jak или STAT:[16]
| Нокаут-ген | Выживание | Фенотип |
|---|---|---|
| Jak1 | Смертельный | Неврологический дефицит |
| Jak2 | Смертельный | Нарушение эритропоэза |
| Stat1 | Жизнеспособный | Человеческая карликовость и краниосиностоз синдромы |
| Stat3 | Смертельный | Тканевые специфические фенотипы |
| Stat4 | Жизнеспособный | дефектная дифференцировка Th1, управляемая IL-12, повышенная чувствительность к внутриклеточным патогенам |
Аберрантный путь Jak-STAT и мутации костей
Путь Jak-STAT играет важную роль в развитии конечностей, в частности, в его способности регулировать рост костей посредством паракринной передачи сигналов цитокинов. Однако мутации в этом пути приводят к тяжелым формам карликовости: танатофорная дисплазия (летальный) и ахондроплазический карликовость (жизнеспособная).[17] Это связано с мутацией в Fgf ген, вызывающий преждевременную и постоянную активацию Stat1 фактор транскрипции. Хондроцитов деление клеток преждевременно прекращается, что приводит к летальной карликовости. Клетки пластинки роста костей ребер и конечностей не транскрибируются. Таким образом, неспособность грудной клетки расширяться препятствует дыханию новорожденного.[18]
Путь Jak-STAT и рак
Исследование паракринной передачи сигналов через путь Jak-STAT выявило его потенциал в активации инвазивного поведения яичников. эпителиальные клетки. Этот эпителиальный мезенхимальный переход очень очевиден в метастаз.[19] Паракринная передача сигналов через путь Jak-STAT необходима при переходе от стационарных эпителиальных клеток к мобильным мезенхимальным клеткам, которые способны проникать в окружающие ткани. Было обнаружено, что только путь Jak-STAT индуцирует мигрирующие клетки.[20]
Семья Ёжиков
В Семейство белков ежа участвует в индукции типов клеток и создании границ тканей и формирования паттерна и обнаруживается во всех двусторонних организмах. Белки ежа были впервые открыты и изучены в Дрозофила. Белки Hedgehog производят ключевые сигналы для формирования конечностей и план тела плодовых мух, а также гомеостаз взрослых тканей, вовлеченных в поздние эмбриогенез и метаморфоза. Не менее трех ежей "Дрозофилы" гомологи были обнаружены у позвоночных: звукового ежа, пустынного ежа и индийского ежа. Соник ёжик (SHH ) играет различные роли в развитии позвонков, опосредуя передачу сигналов и регулируя организацию центральной нервной системы, конечностей и сомит полярность. Ежик пустыни (DHH ) выражается в Клетки Сертоли участвует в сперматогенез. Индийский ёжик (IHH ) экспрессируется в кишечнике и хрящах, что важно для постнатального роста костей.[21][22][23]
Сигнальный путь ежа


Члены семейства белков Hedgehog действуют путем связывания с трансмембранный "Исправлено "рецептор, который связан с"Сглаженный "белок, с помощью которого сигнал Hedgehog может быть преобразованный. В отсутствие Hedgehog рецептор Patched подавляет действие Smoothened. Подавление Smoothened вызывает Кубитус прерывистый Белковые комплексы (Ci), Fused и Cos, прикрепленные к микротрубочкам, остаются неповрежденными. В этой конформации белок Ci расщепляется, так что часть белка может проникать в ядро и действовать как транскрипционный репрессор. При наличии Hedgehog Patched больше не запрещает Smoothened. Тогда активный сглаженный белок способен ингибировать PKA и Slimb, так что белок Ci не расщепляется. Этот интактный белок Ci может проникать в ядро, связываться с белком CPB и действовать как транскрипционный активатор, индуцируя экспрессию генов Hedgehog-response.[23][24][25]
Сигнальный путь ежа и рак
Путь передачи сигналов Hedgehog имеет решающее значение для правильного формирования паттерна и ориентации тканей во время нормального развития большинства животных. Белки ежа вызывают распространение клеток в одних клетках и дифференцировки в других. Аберрантная активация пути Hedgehog связана с несколькими типами раки, Базально-клеточная карцинома особенно. Эта неконтролируемая активация белков Hedgehog может быть вызвана мутациями сигнального пути, которые могут быть лиганд независимый, или мутация, вызывающая чрезмерное выражение белка Hedgehog, который будет зависеть от лиганда. Кроме того, было показано, что активация пути Hedgehog, индуцированная терапией, необходима для прогрессирования опухолей рака простаты после андрогенная депривационная терапия.[26] Эта связь между сигнальным путем Hedgehog и раком человека может обеспечить возможность терапевтического вмешательства в качестве лечения такого рака. Сигнальный путь Hedgehog также участвует в нормальной регуляции стволовая клетка популяций, и необходимы для нормального роста и регенерации поврежденных органов. Это может предоставить другой возможный путь для туморогенез по Ежовой тропе.[27][28][29]
Wnt семья

В Wnt белок семья включает в себя большое количество цистеин -богатые гликопротеины. Белки Wnt активируют преобразование сигнала каскадов тремя разными путями, канонический Wnt путь, неканонический путь планарной полярности клеток (PCP), а неканонический Wnt / Ca2+ путь. Белки Wnt, по-видимому, контролируют широкий спектр процессов развития и считаются необходимыми для контроля шпиндель ориентация, полярность клеток, адгезия, опосредованная кадгерином, и раннее развитие эмбрионов у многих различных организмов. Текущие исследования показали, что нарушение регуляции передачи сигналов Wnt играет роль в образовании опухоли, поскольку на клеточном уровне белки Wnt часто регулируются. распространение клеток, морфология клетки, клетка подвижность, и судьба клетки.[30]
Канонический путь передачи сигналов Wnt

в канонический путь, Белки Wnt связываются со своим трансмембранным рецептором Вьющиеся семейство белков. Связывание Wnt с белком Frizzled активирует Растрепанный белок. В активном состоянии белок Dishevelled подавляет активность киназы гликогенсинтазы 3 (GSK3 ) фермент. Обычно активный GSK3 предотвращает диссоциацию β-катенина на APC белок, что приводит к β-катенин деградация. Таким образом, ингибированный GSK3 позволяет β-катенину диссоциировать от APC, накапливаться и перемещаться в ядро. В ядре β-катенин связывается с Lef / Tcf фактор транскрипции, который уже работает с ДНК в качестве репрессора, подавляя транскрипцию генов, которые она связывает. Связывание β-катенина с Lef / Tcf работает как активатор транскрипции, активируя транскрипцию Wnt-чувствительных генов.[31][32][33]
Неканонические пути передачи сигналов Wnt
Неканонические пути Wnt обеспечивают путь передачи сигнала для Wnt, который не включает β-катенин. В неканонических путях Wnt влияет на актин и микротрубчатый цитоскелет а также транскрипция гена.
Путь неканонической планарной клеточной полярности (PCP)

Неканонический путь PCP регулирует клеточную морфология, разделение, и движение. И снова белки Wnt связываются и активируют Frizzled, так что Frizzled активирует белок Disheveled, который привязан к плазматической мембране через Колючий белок и трансмембранный белок Stbm. Активный Disheveled активирует RhoA GTPase через связанный активатор Disheveled морфогенез 1 (Daam1) и Rac белок. Активный RhoA способен вызывать изменения цитоскелета путем активации Roh-ассоциированной киназы (ROCK) и напрямую влиять на транскрипцию генов. Активный Rac может напрямую индуцировать изменения цитоскелета и влиять на транскрипцию генов через активацию JNK.[31][32][33]
Неканонический Wnt / Ca2+ путь
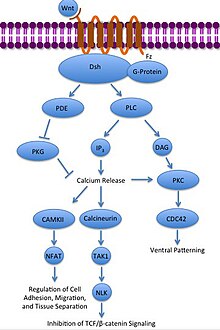
Неканонический Wnt / Ca2+ путь регулирует внутриклеточный кальций уровни. Wnt снова связывается и активируется с Frizzled. Однако в этом случае активированный Frizzled заставляет связанный G-белок активировать фосфолипаза (PLC), который взаимодействует и разделяет PIP2 в DAG и IP3. IP3 затем может связываться с рецептором на эндоплазматический ретикулум для высвобождения внутриклеточных запасов кальция, чтобы вызвать кальций-зависимую экспрессию генов.[31][32][33]
Сигнальные пути Wnt и рак
Сигнальные пути Wnt имеют решающее значение для передачи сигналов между клетками во время нормального развития и эмбриогенеза и необходимы для поддержания взрослой ткани, поэтому нетрудно понять, почему нарушение сигнальных путей Wnt может способствовать развитию человека. дегенеративное заболевание и рак.
Пути передачи сигналов Wnt сложны, в них задействовано множество различных элементов, и поэтому они имеют множество мишеней для неправильной регуляции. Мутации, которые вызывают конститутивную активацию сигнального пути Wnt, приводят к образованию опухоли и раку. Аберрантная активация пути Wnt может привести к увеличению пролиферации клеток. Текущие исследования сосредоточены на действии сигнального пути Wnt на регуляцию выбора стволовых клеток для пролиферации и самообновления. Это действие передачи сигналов Wnt по возможному контролю и поддержанию стволовых клеток может обеспечить возможное лечение рака, проявляющего аберрантную передачу сигналов Wnt.[34][35][36]
Суперсемейство TGF-β
"TGF "(Трансформирующий фактор роста) - это семейство белков, которое включает 33 члена, которые кодируют димерный, секретируемые полипептиды, регулирующие развитие.[37] Многие процессы развития находятся под его контролем, включая гаструляцию, симметрию оси тела, морфогенез органов и гомеостаз тканей у взрослых.[38] Все TGF-β лиганды связываются с рецепторами типа I или II с образованием гетеротетрамических комплексов.[39]
Путь TGF-β
В Путь TGF-β регулирует многие клеточные процессы в развивающихся эмбрионах и взрослых организмах, включая рост клеток, дифференциация, апоптоз, и гомеостаз. Существует пять типов рецепторов типа II и семь типов рецепторов типа I у людей и других млекопитающих. Эти рецепторы известны как «киназы двойной специфичности», потому что их цитоплазматический киназный домен обладает слабой тирозинкиназной активностью, но сильным. серин /треонин киназная активность.[40] Когда лиганд суперсемейства TGF-β связывается с рецептором типа II, он рекрутирует рецептор типа I и активирует его, фосфорилируя остатки серина или треонина его «GS» бокса.[41] Это формирует активационный комплекс, который затем может фосфорилировать белки SMAD.

Путь SMAD
Есть три класса SMAD:
Примеры SMAD в каждом классе:[42][43][44]
| Учебный класс | SMAD |
|---|---|
| R-SMAD | SMAD1, SMAD2, SMAD3, SMAD5 и SMAD8 / 9 |
| Со-SMAD | SMAD4 |
| I-SMAD | SMAD6 и SMAD7 |
Суперсемейство TGF-β активирует членов группы SMAD семьи, которые действуют как факторы транскрипции. В частности, рецептор типа I, активируемый рецептором типа II, фосфорилирует R-SMAD которые затем связываются с co-SMAD, SMAD4. R-SMAD / Co-SMAD образует комплекс с импортин и попадает в ядро, где действуют как факторы транскрипции и либо активируют, либо подавляют экспрессию целевого гена.
Специфические лиганды TGF-β приведут к активации либо SMAD2 / 3, либо SMAD1 / 5. R-SMAD. Например, когда активин, Узловой, или же Лиганд TGF-β связывается с рецепторами, фосфорилированный рецепторный комплекс может активировать SMAD2 и SMAD3 через фосфорилирование. Однако, когда лиганд BMP связывается с рецепторами, фосфорилированный рецепторный комплекс активирует SMAD1 и SMAD5. Тогда комплексы Smad2 / 3 или Smad1 / 5 образуют димерный комплекс с SMAD4 и стать факторы транскрипции. Хотя есть много R-SMAD участвует в пути, существует только один со-SMAD, SMAD4.[45]
Не-SMAD путь
Сигнальные белки, не относящиеся к Smad, вносят вклад в ответы пути TGF-β тремя способами. Во-первых, сигнальные пути, отличные от Smad, фосфорилируют Smads. Во-вторых, Smads напрямую передает сигналы другим путям, напрямую связываясь с другими сигнальными белками, такими как киназы. Наконец, рецепторы TGF-β напрямую фосфорилируют не-Smad белки.[46]
Члены суперсемейства TGF-β
1. Семейство TGF-β
В эту семью входят TGF-β1, TGF-β2, TGF-β3 и TGF-β5. Они участвуют в положительном и отрицательном регулировании деление клеток, формирование внеклеточный матрикс между ячейками, апоптоз, и эмбриогенез. Они привязаны к Рецептор TGF-β типа II (TGFBRII).
TGF-β1 стимулирует синтез коллаген и фибронектин и препятствует деградации внеклеточный матрикс. В конечном итоге он увеличивает производство внеклеточного матрикса за счет эпителиальные клетки.[39]Белки TGF-β регулируют эпителий, контролируя, где и когда они разветвляются с образованием протоков почек, легких и слюнных желез.[39]
2. Семейство костных морфогенетических белков (BMP)
Первоначально было обнаружено, что члены семейства BMP вызывают формирование кости, как следует из их названия. Однако BMP очень многофункциональны и также могут регулировать апоптоз, миграция клеток, деление клеток, и дифференциация. Они также определяют переднюю / заднюю ось, вызывают рост и регулируют гомеостаз.[37]
BMP привязаны к рецептор костного морфогенетического белка II типа (БМПР2). Некоторые из белков BMP семья BMP4 и BMP7. BMP4 способствует образованию костей, вызывает гибель клеток или сигнализирует об образовании эпидермис, в зависимости от ткани, на которую он действует. BMP7 имеет решающее значение для развития почек, синтеза сперматозоидов и поляризации нервной трубки. Обе BMP4 и BMP7 регулируют стабильность и процессинг зрелого лиганда, включая деградирующие лиганды в лизосомах.[37] BMP действуют путем диффузии из клеток, которые их создают.[47]
Другие члены суперсемейства TFG-β
- Семья Vg1
- Семья Activin
- Участвует в эмбриогенез и остеогенез
- Регулировать инсулин и гипофиз, гонад и гипоталамический гормоны
- Факторы выживания нервных клеток
- 3 Активина: Активин А, Активин B и Activin AB.
- Глиальный нейротрофический фактор (GDNF)
- Нужен для почек и кишечный нейрон дифференциация
- Мюллеровский ингибирующий фактор
- Участвует в определении пола у млекопитающих
- Узловой
- Связывается с Рецептор активина А типа 2В
- Образует рецепторный комплекс с Рецептор активина A типа 1B или с Рецептор активина А типа 1С.[48]
- Факторы роста и дифференциации (GDF)
Сводная таблица сигнального пути TFG-β
| Лиганд суперсемейства TGF Beta | Рецептор II типа | Рецептор I типа | R-SMAD | Со-SMAD | Ингибиторы лигандов |
|---|---|---|---|---|---|
| Активин А | ACVR2A | ACVR1B (ALK4) | SMAD2, SMAD3 | SMAD4 | Фоллистатин |
| GDF1 | ACVR2A | ACVR1B (ALK4) | SMAD2, SMAD3 | SMAD4 | |
| GDF11 | ACVR2B | ACVR1B (ALK4), TGFβRI (ALK5) | SMAD2, SMAD3 | SMAD4 | |
| Костные морфогенетические белки | BMPR2 | BMPR1A (ALK3), BMPR1B (ALK6) | SMAD1 SMAD5, SMAD8 | SMAD4 | Noggin, Chordin, ДАН |
| Узловой | ACVR2B | ACVR1B (ALK4), ACVR1C (ALK7) | SMAD2, SMAD3 | SMAD4 | Левша |
| TGFβs | TGFβRII | TGFβRI (ALK5) | SMAD2, SMAD3 | SMAD4 | LTBP1, THBS1, Декорин |
Примеры
Фактор роста и факторы свертывания являются паракринными сигнальными агентами. Местное действие передачи сигналов фактора роста играет особенно важную роль в развитии тканей. Также, ретиноевая кислота, активная форма витамин А, функционирует паракринным образом, регулируя экспрессию генов во время эмбрионального развития у высших животных.[49] У насекомых, Аллатостатин контролирует рост за счет паракринного воздействия на все тела.[нужна цитата ]
У зрелых организмов паракринная передача сигналов участвует в ответах на аллергены, восстановление тканей, формирование рубцовая ткань и кровь свертывание.[нужна цитата ]
Смотрите также
- цАМФ-зависимый путь
- Сотовая связь (биология)
- Перекрестные помехи (биология)
- Сигнальный путь JAK-STAT
- Липидная сигнализация
- Местный гормон - либо паракринный гормон, либо гормон, действующий как паракринным, так и эндокринным образом
- Путь передачи сигналов MAPK
- Netpath - Кураторский ресурс путей передачи сигналов у людей
- Паракринный регулятор
Рекомендации
- ^ «Паракринные факторы». Получено 27 июля 2018.
- ^ Gospodarowicz, D .; Феррара, штат Нью-Йорк; Schweigerer, L .; Нойфельд, Г. (1987). «Структурная характеристика и биологические функции фактора роста фибробластов». Эндокринные обзоры. 8 (2): 95–114. Дои:10.1210 / едрв-8-2-95. PMID 2440668.
- ^ Рифкин, Дэниел Б .; Москателли, Дэвид (1989). «Последние разработки в клеточной биологии основного фактора роста фибробластов». Журнал клеточной биологии. 109 (1): 1–6. Дои:10.1083 / jcb.109.1.1. JSTOR 1613457. ЧВК 2115467. PMID 2545723.
- ^ а б Лаппи, Дуглас А. (1995). «Нацеливание на опухоль через рецепторы фактора роста фибробластов». Семинары по биологии рака. 6 (5): 279–88. Дои:10.1006 / scbi.1995.0036. PMID 8562905.
- ^ а б Xu, J .; Сюй, Дж; Colvin, JS; McEwen, DG; Макартур, Калифорния; Coulier, F; Gao, G; Гольдфарб, М. (1996). «Рецепторная специфичность семейства факторов роста фибробластов». Журнал биологической химии. 271 (25): 15292–7. Дои:10.1074 / jbc.271.25.15292. PMID 8663044.
- ^ Логан, М. (2003). «Палец или палец ноги: молекулярная основа идентичности конечностей». Разработка. 130 (26): 6401–10. Дои:10.1242 / dev.00956. PMID 14660539.
- ^ а б Фантл, Венди Дж; Джонсон, Дэниел Э; Уильямс, Льюис Т (1993). «Передача сигналов рецепторными тирозинкиназами». Ежегодный обзор биохимии. 62: 453–81. Дои:10.1146 / annurev.bi.62.070193.002321. PMID 7688944.
- ^ Ярден, Йосеф; Ульрих, Аксель (1988). "Тирозинкиназы рецепторов фактора роста". Ежегодный обзор биохимии. 57: 443–78. Дои:10.1146 / annurev.bi.57.070188.002303. PMID 3052279.
- ^ Кац, Майкл Э; Маккормик, Фрэнк (1997). «Передача сигнала от нескольких эффекторов Ras». Текущее мнение в области генетики и развития. 7 (1): 75–9. Дои:10.1016 / S0959-437X (97) 80112-8. PMID 9024640.
- ^ Zsebo, Krisztina M .; Уильямс, Дэвид А .; Geissler, Edwin N .; Броуди, Вирджиния С .; Мартин, Фрэнсис Х .; Аткинс, Гарри L .; Сюй, Роу-Инь; Birkett, Neal C .; Окино, Кеннет Х .; Мердок, Дуглас С.; Якобсен, Фредерик В .; Langley, Keith E .; Smith, Kent A .; Такейш, Такаши; Каттанах, Брюс М .; Галли, Стивен Дж .; Саггс, Сидней В. (1990). «Фактор стволовых клеток кодируется в локусе SI мыши и является лигандом для рецептора тирозинкиназы c-kit». Клетка. 63 (1): 213–24. Дои:10.1016 / 0092-8674 (90) 90302-У. PMID 1698556.
- ^ Рённстранд, Л. (2004). «Передача сигнала через рецептор фактора стволовых клеток / c-Kit». Клеточные и молекулярные науки о жизни. 61 (19–20): 2535–48. Дои:10.1007 / s00018-004-4189-6. PMID 15526160.
- ^ Мелилло, Роза Марина; Кастеллоне, Мария Доменика; Гуарино, Валентина; Де Фалько, Валентина; Чирафики, Анна Мария; Сальваторе, Джулиана; Каяццо, Фиорина; Басоло, Фульвио; Джаннини, Риккардо; Крухоффер, Могенс; Ортофт, Торбен; Фуско, Альфредо; Санторо, Массимо (2005). «Линейный сигнальный каскад RET / PTC-RAS-BRAF опосредует подвижный и митогенный фенотип клеток рака щитовидной железы». Журнал клинических исследований. 115 (4): 1068–81. Дои:10.1172 / JCI22758. ЧВК 1062891. PMID 15761501.
- ^ Колч, Вальтер (2000). «Значимые отношения: регуляция пути Ras / Raf / MEK / ERK посредством белковых взаимодействий». Биохимический журнал. 351 (2): 289–305. Дои:10.1042/0264-6021:3510289. ЧВК 1221363. PMID 11023813.
- ^ а б Ааронсон, Дэвид С .; Хорват, Курт М. (2002). «Дорожная карта для тех, кто не знает JAK-STAT». Наука. 296 (5573): 1653–5. Bibcode:2002Наука ... 296.1653A. Дои:10.1126 / science.1071545. PMID 12040185.
- ^ Роулингс, Джейсон С .; Рослер, Кристин М .; Харрисон, Дуглас А. (2004). «Путь передачи сигналов JAK / STAT». Журнал клеточной науки. 117 (8): 1281–3. Дои:10.1242 / jcs.00963. PMID 15020666.
- ^ О'Ши, Джон Дж; Гадина, Массимо; Шрайбер, Роберт Д. (2002). «Цитокиновая передача сигналов в 2002 году: новые сюрпризы в пути Jak / Stat». Клетка. 109 (2): S121–31. Дои:10.1016 / S0092-8674 (02) 00701-8. PMID 11983158.
- ^ Шианг, Рита; Томпсон, Лесли М .; Чжу, Я-Чжэнь; Церковь, Дина М .; Филдер, Томас Дж .; Босиан, Морин; Винокур, Сара Т .; Васмут, Джон Дж. (1994). «Мутации в трансмембранном домене FGFR3 вызывают наиболее распространенную генетическую форму карликовости, ахондроплазию». Клетка. 78 (2): 335–42. Дои:10.1016/0092-8674(94)90302-6. PMID 7913883.
- ^ Каллури, Рагху; Вайнберг, Роберт А. (2009). «Основы эпителиально-мезенхимального перехода». Журнал клинических исследований. 119 (6): 1420–8. Дои:10.1172 / JCI39104. ЧВК 2689101. PMID 19487818.
- ^ Silver, Debra L .; Монтелл, Дениз Дж. (2001). «Передача паракринных сигналов по пути JAK / STAT активирует инвазивное поведение эпителиальных клеток яичников у дрозофилы». Клетка. 107 (7): 831–41. Дои:10.1016 / S0092-8674 (01) 00607-9. PMID 11779460.
- ^ Ingham, P.W .; МакМахон, AP (2001). «Передача сигналов ежа в развитии животных: парадигмы и принципы». Гены и развитие. 15 (23): 3059–87. Дои:10.1101 / gad.938601. PMID 11731473.
- ^ Bitgood, Mark J .; МакМэхон, Эндрю П. (1995). "Ежик и BMP Гены коэкспрессируются во многих различных участках межклеточного взаимодействия в эмбрионе мыши ». Биология развития. 172 (1): 126–38. Дои:10.1006 / dbio.1995.0010. PMID 7589793.
- ^ а б Jacob, L .; Лум, Л. (2007). «Сигнальный путь ежа». STKE науки. 2007 (407): см6. Дои:10.1126 / стке. 4072007см6. PMID 17925577.
- ^ Джонсон, Рональд Л; Скотт, Мэтью П. (1998). «Новые игроки и головоломки на сигнальном пути Ежика». Текущее мнение в области генетики и развития. 8 (4): 450–6. Дои:10.1016 / S0959-437X (98) 80117-2. PMID 9729722.
- ^ Нюбаккен, К; Перримон, Н. (2002). «Передача сигнала ежа: последние открытия». Текущее мнение в области генетики и развития. 12 (5): 503–11. Дои:10.1016 / S0959-437X (02) 00333-7. PMID 12200154.
- ^ Любик А.А., Нури М., Чыонг С., Гаффари М., Адомат Х.Х., Кори Э., Кокс М.Э., Ли Н., Ганз Э.С., Йенки П., Фам С., Буттян Р. (2016). «Паракринная передача сигналов Sonic Hedgehog значительно способствует приобретенному стероидогенезу в микросреде опухоли простаты». Международный журнал рака. 140 (2): 358–369. Дои:10.1002 / ijc.30450. PMID 27672740.
- ^ Collins, R.T .; Коэн, С.М. (2005). «Генетический экран у дрозофилы для выявления новых компонентов сигнального пути ежа». Генетика. 170 (1): 173–84. Дои:10.1534 / генетика.104.039420. ЧВК 1449730. PMID 15744048.
- ^ Евангелиста, М .; Tian, H .; Де Соваж, Ф. Дж. (2006). "Сигнальный путь ежа при раке". Клинические исследования рака. 12 (20): 5924–8. Дои:10.1158 / 1078-0432.CCR-06-1736. PMID 17062662.
- ^ Тайпале, Юсси; Бичи, Филип А. (2001). «Пути передачи сигналов Hedgehog и Wnt при раке». Природа. 411 (6835): 349–54. Bibcode:2001Натура.411..349Т. Дои:10.1038/35077219. PMID 11357142.
- ^ Cadigan, K. M .; Нуссе Р. (1997). «Передача сигналов Wnt: общая тема в развитии животных». Гены и развитие. 11 (24): 3286–305. Дои:10.1101 / gad.11.24.3286. PMID 9407023.
- ^ а б c Дейл, Тревор С. (1998). "Передача сигнала семейством лигандов Wnt". Биохимический журнал. 329 (Pt 2): 209–23. Дои:10.1042 / bj3290209. ЧВК 1219034. PMID 9425102.
- ^ а б c Чен, Си; Ян, июнь; Эванс, Пол М; Лю, Чуньмин (2008). «Сигнализация Wnt: хорошее и плохое». Acta Biochimica et Biophysica Sinica. 40 (7): 577–94. Дои:10.1111 / j.1745-7270.2008.00440.x. ЧВК 2532600. PMID 18604449.
- ^ а б c Комия, Юко; Хабас, Раймонд (2008). «Пути передачи сигнала Wnt». Органогенез. 4 (2): 68–75. Дои:10.4161 / org.4.2.5851. ЧВК 2634250. PMID 19279717.
- ^ Логан, Катриона Й .; Нуссе, Роэль (2004). «Путь передачи сигналов Wnt в развитии и болезни». Ежегодный обзор клеточной биологии и биологии развития. 20: 781–810. CiteSeerX 10.1.1.322.311. Дои:10.1146 / annurev.cellbio.20.010403.113126. PMID 15473860.
- ^ Люстиг, В; Беренс, Дж (2003). «Путь передачи сигналов Wnt и его роль в развитии опухолей». Журнал исследований рака и клинической онкологии. 129 (4): 199–221. Дои:10.1007 / s00432-003-0431-0. PMID 12707770.
- ^ Нет, Питер; Райс, Кристиан; Каров, Мариса; Эгея, Вирджиния; Ильмер, Матиас; Йохум, Марианна (2007). «Путь передачи сигнала Wnt в стволовых и раковых клетках: влияние на клеточную инвазию». Стволовые клетки. 3 (1): 18–29. Дои:10.1007 / s12015-007-0001-y. PMID 17873378.
- ^ а б c Бандйопадхьяй, Амитабха; Цудзи, Куниказу; Кокс, Карен; Харф, Брайан Д .; Розен, Вики; Табин, Клиффорд Дж. (2006). «Генетический анализ роли BMP2, BMP4 и BMP7 в формировании паттерна конечностей и скелетогенезе». PLOS Genetics. 2 (12): e216. Дои:10.1371 / journal.pgen.0020216. ЧВК 1713256. PMID 17194222.
- ^ Аттисано, Лилиана; Врана, Джеффри Л. (2002). «Передача сигнала суперсемейством TGF-β». Наука. 296 (5573): 1646–7. Bibcode:2002Наука ... 296.1646A. Дои:10.1126 / science.1071809. PMID 12040180.
- ^ а б c Wrana, Jeffrey L .; Оздамар, Бариш; Ле Рой, Кристина; Бенчабейн, Хассина (2008). «Сигнальные рецепторы семейства TGF-β». В Деринке, Рик; Миязоно, Кохей (ред.). Семейство TGF-β. С. 151–77. ISBN 978-0-87969-752-5.
- ^ тен Дийке, Питер; Хелдин, Карл-Хенрик (2006). "Семья Смад". В десять Дайке, Питер; Хелдин, Карл-Хенрик (ред.). Передача сигналов Smad: распространение, дифференциация и болезнь Smads. Белки и регуляция клеток. 5. Дордрехт: Спрингер. С. 1–13. ISBN 978-1-4020-4709-1.
- ^ Мустакас, Аристидис (01.09.2002). «Сеть сигнализации Smad». Журнал клеточной науки. 115 (17): 3355–6. PMID 12154066.
- ^ Ву, Цзя-Вэй; Ху, Мин; Чай, Джиджи; Сеоан, Жанна; Хьюз, Морган; Ли, Кэри; Риготти, Дэниел Дж .; Кьин, Пила; Muir, Tom W .; Фэрман, Роберт; Массаге, Жанна; Ши, Игун (2001). «Кристаллическая структура фосфорилированного Smad2». Молекулярная клетка. 8 (6): 1277–89. Дои:10.1016 / S1097-2765 (01) 00421-X. PMID 11779503.
- ^ Павлетич, Никола П .; Хата, Игун; Ло, Акико; Massagué, Roger S .; Павлетич, Жанна (1997). «Структурная основа мутационной инактивации опухолевого супрессора Smad4». Природа. 388 (6637): 87–93. Bibcode:1997Натура.388Р..87С. Дои:10.1038/40431. PMID 9214508.
- ^ Ито, Фумико; Асао, Хиронобу; Сугамура, Кадзуо; Хельдин, Карл-Хенрик; Тен Дийке, Питер; Ито, Сусуму (2001). «Содействие передаче сигналов костного морфогенетического белка посредством отрицательной регуляции ингибирующих Smads». Журнал EMBO. 20 (15): 4132–42. Дои:10.1093 / emboj / 20.15.4132. ЧВК 149146. PMID 11483516.
- ^ Шмирер, Бернхард; Хилл, Кэролайн С. (2007). «Передача сигнала TGFβ – SMAD: молекулярная специфичность и функциональная гибкость». Обзоры природы Молекулярная клеточная биология. 8 (12): 970–82. Дои:10.1038 / nrm2297. PMID 18000526.
- ^ Мустакас, Аристидис; Хелдин, Карл-Хенрик (2005). «Сигналы Non-Smad TGF-β». Журнал клеточной науки. 118 (16): 3573–84. Дои:10.1242 / jcs.02554. PMID 16105881.
- ^ Окавара, Бисей; Иемура, Шун-Ичиро; Тен Дийке, Питер; Уэно, Наото (2002). «Диапазон действия BMP определяется его N-концевым основным аминокислотным ядром». Текущая биология. 12 (3): 205–9. Дои:10.1016 / S0960-9822 (01) 00684-4. PMID 11839272.
- ^ Мунир, Садия; Сюй, Гуосюн; У, Яоцзюн; Ян, Бертон; Lala, Peeyush K .; Пэн, Чун (2004). «Nodal и ALK7 ингибируют пролиферацию и индуцируют апоптоз в клетках трофобласта человека». Журнал биологической химии. 279 (30): 31277–86. Дои:10.1074 / jbc.M400641200. PMID 15150278.
- ^ Дестер, Грегг (сентябрь 2008 г.). «Синтез ретиноевой кислоты и передача сигналов во время раннего органогенеза». Клетка. 134 (6): 921–31. Дои:10.1016 / j.cell.2008.09.002. ЧВК 2632951. PMID 18805086.
внешняя ссылка
- Паракрин + сигнализация в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- "паракринный " в Медицинский словарь Дорланда
