Вирус гепатита В - Hepatitis B virus
| Вирус гепатита В | |
|---|---|
 | |
| Просвечивающая электронная микроскопия микрофотография показывая Вирус гепатита В вирионы | |
| Классификация вирусов | |
| (без рейтинга): | Вирус |
| Область: | Рибовирия |
| Королевство: | Парарнавиры |
| Тип: | Artverviricota |
| Учебный класс: | Revtraviricetes |
| Заказ: | Blubervirales |
| Семья: | Hepadnaviridae |
| Род: | Ортогепаднавирус |
| Разновидность: | Вирус гепатита В |
Вирус гепатита В (HBV), является частично двухцепочечным ДНК-вирус,[1] вид рода Ортогепаднавирус и член Hepadnaviridae семейство вирусов.[2] Этот вирус вызывает болезнь гепатит Б.[3]
Болезнь
Несмотря на то, что существует вакцина для предотвращения гепатита B, HBV остается глобальной проблемой здравоохранения. Гепатит B может быть острым, а затем перейти в хронический, приводя к другим заболеваниям и состояниям здоровья.[4] Помимо гепатита, инфекция HBV может привести к цирроз и гепатоцеллюлярная карцинома.[5]
Также было высказано предположение, что это может увеличить риск панкреатический рак.[3]
Роли в болезни
Вирусная инфекция от Вирус гепатита В (HBV) вызывает многие гепатоцит изменения из-за прямого действия белка, кодируемого вирусом, HBx, и косвенным изменениям из-за большого увеличения внутриклеточный активные формы кислорода (ROS) после заражения. HBx, по-видимому, нарушает регуляцию ряда клеточных путей. HBx вызывает нарушение регуляции частично путем связывания с геномными ДНК, изменяя паттерны экспрессии miRNAs, влияя на гистоновые метилтрансферазы, связываясь с SIRT1 белок для активации транскрипция, и сотрудничая с гистон метилазы и деметилазы для изменения паттернов клеточной экспрессии.[6] HBx частично ответственен за приблизительно 10 000-кратное увеличение внутриклеточных ROS при хронической инфекции HBV.[7] Увеличение ROS может быть частично вызвано локализацией HBx в митохондрии где HBx снижает потенциал митохондриальной мембраны.[8] Кроме того, еще один HBV белок, HBsAg, также увеличивает ROS за счет взаимодействия с эндоплазматический ретикулум.[8]
Увеличение активные формы кислорода (АФК) после инфицирования ВГВ вызывает воспаление, которое приводит к дальнейшему увеличению АФК.[7] АФК вызывают более 20 типов повреждений ДНК.[9] Окислительное повреждение ДНК является мутагенным.[10] Кроме того, восстановление повреждений ДНК может вызвать эпигенетические изменения в месте повреждения во время восстановления ДНК.[11] Эпигенетический изменения и мутации могут вызывать дефекты клеточного аппарата, которые затем способствуют болезнь печени. К тому времени, когда накапливающиеся эпигенетические и мутационные изменения в конечном итоге вызывают прогрессирование рак, эпигенетические изменения, по-видимому, играют большую роль в этом канцерогенез чем мутации. Только один или два гена, TP53[12] и, возможно ARID1A,[13] мутировали более чем в 20% рак печени в то время как 41 ген имеет гиперметилированные промоторы (подавление экспрессии гена) более чем в 20% случаев рака печени, причем семь из этих генов гиперметилированы более чем в 75% случаев рака печени.[12] Помимо изменений в участках репарации ДНК, эпигенетические изменения также вызваны тем, что HBx рекрутирует ДНК-метилтрансфераза ферменты, DNMT1 и / или DNMT3A к определенным локусам генов, чтобы изменить их метилирование уровни и экспрессия генов.[14] HBx тоже переделывает ацетилирование гистонов которые могут повлиять на экспрессию генов.[14]
Несколько тысяч генов, кодирующих белок, по-видимому, имеют сайты связывания HBx.[6][15] Помимо генов, кодирующих белки, около 15 микроРНК и 16 Длинные некодирующие РНК также зависят от связывания HBx со своими промоторами.[15] Каждая измененная микроРНК может влиять на экспрессию нескольких сотен матричных РНК (см. микроРНК ).
Классификация
Вирус гепатита В классифицируется как типовой вид из Ортогепаднавирус, который содержит восемь других видов.[16] Род классифицируется как часть Hepadnaviridae семейство, которое содержит еще один род, Авихепаднавирус.[16] Это семейство вирусов не было отнесено к вирусному ряду.[17] Вирусы, похожие на гепатит В, обнаружены во всех обезьяны (орангутаны, гиббоны, гориллы и шимпанзе ), в Обезьяны Старого Света,[18] И в Новый мир шерстистые обезьяны (в вирус гепатита В шерстистой обезьяны ), что предполагает древнее происхождение этого вируса у приматов.
Вирус делится на четыре основных серотипы (adr, adw, ayr, ayw) на основе антигенных эпитопы присутствует на его белки оболочки. Эти серотипы основаны на общем детерминанте (а) и двух взаимоисключающих парах детерминант (d / y и w / r). Вирусные штаммы также были разделены на десять генотипов (A – J) и сорок субгенотипов в соответствии с общими вариациями нуклеотидной последовательности генома.[19] Генотипы имеют четкое географическое распределение и используются для отслеживания эволюции и передачи вируса. Различия между генотипами влияют на тяжесть заболевания, течение и вероятность осложнений, а также реакцию на лечение и, возможно, вакцинацию.[20][21] Серотипы и генотипы не обязательно совпадают.
Генотип D имеет 10 подгенотипов.[22][19]
Неклассифицированные виды
От летучих мышей был выделен ряд еще не классифицированных разновидностей гепатита B.[23]
Морфология
Структура
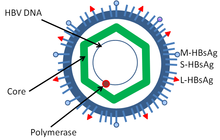
Вирус гепатита В является членом Семья гепаднавирусов.[24] Вирусная частица, называемая частица Дэйна[25] (вирион ), состоит из внешнего липид конверт и икосаэдр нуклеокапсид ядро состоит из белок. Нуклеокапсид включает вирусную ДНК и ДНК-полимеразу, которая имеет обратная транскриптаза активность аналогична ретровирусам.[26] Внешняя оболочка содержит встроенные белки, которые участвуют в связывании вируса и проникновении в чувствительные клетки. Вирус является одним из самых маленьких оболочечных вирусов животных с диаметром вириона 42 нм, но плеоморфный существуют формы, в том числе нитевидные и сферические тела без ядра. Эти частицы не являются инфекционными и состоят из липидов и белков, которые образуют часть поверхности вириона, которая называется поверхностным антигеном (HBsAg ), и вырабатывается в избытке в течение жизненного цикла вируса.[27]
Составные части
Это состоит из:
- HBsAg - Поверхностный гепатит В антиген (HBsAg) был первым обнаруженным белком вируса гепатита В.[28] Он состоит из малого (S), среднего (M) и большого (L) белка.[29]
- HBcAg (HBeAg вариант сплайсинга) - HBcAg является основным структурный белок HBV икосаэдр нуклеокапсид и он имеет функцию в репликация из вирус.[30] Образование капсида антигена HBV (HBcAg) является основным фактором инфекционное заболевание ячейки.[31] HBcAg способствует клиренсу HBV in vivo, но неизвестно, должен ли HBcAg находиться в капсидной форме, чтобы способствовать выведению вируса.[32]
- ДНК-полимераза вируса гепатита B
- HBx. Белок вируса гепатита B HBx мал,[33] 154 аминокислота длинный, неструктурный и играет важную роль в HBV-ассоциированном заболевании печени и HBV репликация в HepG2 клетки. Многие активности были связаны с экспрессией HBx. Однако молекулярные механизмы многих из этих активностей неизвестны.[34] Этот белок многофункциональный, он активирует клеточные сигнальные пути и необходим для вирусной инфекционное заболевание.[35]
Вирус гепатита D требует, чтобы частицы оболочки HBV стали вирулентными.[36]
Эволюция
Трудно установить раннюю эволюцию гепатита B, как и всех вирусов.
Расхождение ортогепаднавирус и авихепаднавирус произошло ~ 125 000 лет назад (интервал 95% 78 297–313 500).[37] Вирусы Avihepadnavirus и Orthohepadna начали диверсифицироваться около 25 000 лет назад.[37] Ветвление в это время привело к появлению генотипов Orthohepadna A – H. У человеческих штаммов самый недавний общий предок датируется от 7000 (интервал 95%: 5 287–9 270) до 10 000 (интервал 95%: 6 305–16 681) лет назад.
У Avihepadnavirus отсутствует X-белок, но в геноме гепаднавируса уток присутствует рудиментарная рамка считывания X.[38] Белок X, возможно, произошел от ДНК гликозилаза.
Частота несинонимичных мутаций в этом вирусе оценивается примерно в 2 × 10−5 замен аминокислот на сайт в год.[39] Среднее количество замен нуклеотидов на сайт в год составляет ~ 7,9×10−5.
Вторая оценка происхождения этого вируса предполагает, что он был самым последним общим предком человеческих штаммов, появившихся около 1500 лет назад.[40] Самый недавний общий предок птичьих штаммов был установлен 6000 лет назад. Частота мутаций составила ~ 10−6 замен / сайт / год.
Другой анализ с большим набором данных предполагает, что гепатит B инфицировал людей 33 600 лет назад (на 95% выше плотность в задней части тела 22 000-47 100 лет назад.[41] Расчетная скорость замещения составила 2,2 × 10−6 замен / сайт / год. Значительный рост населения отмечен за последние 5000 лет. Межвидовое заражение орангутангов и гиббонов произошло за последние 6 100 лет.
Изучение последовательностей зебровых вьюрков отодвинуло происхождение этого рода, по крайней мере, до 40 миллион лет назад и, возможно, чтобы 80 миллион лет назад.[42] Шимпанзе, горилла, орангутанг, и группа видов гиббонов с человеческими изолятами. К неприматам относятся вирус гепатита сурков, вирус гепатита сусликов и вирус гепатита арктических белок. Также был описан ряд видов, заражающих летучих мышей. Было высказано предположение, что вид летучих мышей Нового Света может быть источником вида приматов.[43]
Исследование изолятов из циркумполярной арктической популяции человека показало, что предок субгенотипа B5 ( эндемический тип обнаружено в этой популяции), что предковый вирус возник в Азии около 2000 лет назад (95% HPD 900 г. до н.э. - 830 г. н.э.).[44] Слияние произошло около 1000 г. н.э. Первоначально этот субгенотип распространился из Азии в Гренландия а затем распространились на запад за последние 400 лет.
Самое старое свидетельство инфекции гепатита B датируется Бронзовый век.[45][46] Доказательства были получены из человеческих останков возрастом 4500 лет.[46] Согласно исследованию 2018 г., вирусный геномы получено секвенирование дробовика стал самым старым из когда-либо извлеченных из образцов позвоночных.[46] Также было обнаружено, что некоторые древние вирусные гепатиты напряжения до сих пор заражают людей, а другие вымерли.[46] Это опровергло мнение о том, что гепатит B возник в Новом Свете и распространился в Европе примерно в 16 веке.[46]
Геном
Размер
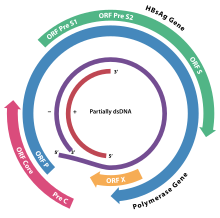
В геном HBV изготавливается из круглого ДНК, но это необычно, потому что ДНК не является полностью двухцепочечной. Один конец полноразмерной цепи связан с вирусным ДНК-полимераза. Геном 3020–3320 нуклеотиды длинная (для полной цепи) и 1700–2800 нуклеотидов (для короткой цепи).[47]
Кодирование
Негативная (некодирующая) цепь комплементарна вирусной мРНК. Вирусная ДНК обнаруживается в ядре вскоре после заражения клетки. Частично двухцепочечная ДНК становится полностью двухцепочечной за счет завершения (+) смысловой цепи клеточным ДНК-полимеразы (на более поздней стадии используется вирусная ДНК-полимераза) и удаление белка вирусной полимеразы (P) из (-) смысловой цепи и короткой последовательности РНК из (+) смысловой цепи. Некодирующие основания удаляют с концов (-) смысловой цепи, и концы соединяют заново.
Вирусные гены транскрибируются клеточными РНК-полимераза II в ядре клетки из матрицы ковалентно замкнутой кольцевой ДНК (cccDNA). Два энхансера, обозначенные как энхансер I (EnhI) и энхансер II (EnhII), были идентифицированы в геноме HBV. Оба энхансера проявляют большую активность в клетках печеночного происхождения, и вместе они управляют и регулируют экспрессию полных вирусных транскриптов.[48][49][50] Существует четыре известных гена, кодируемых геномом, которые называются C, P, S и X. Основной белок кодируется геном C (HBcAg), и его стартовому кодону предшествует запуск AUG в рамке выше. кодон из которого производится pre-core белок. HBeAg продуцируется протеолитическим процессингом пре-корового белка. ДНК-полимераза кодируется геном P. Ген S - это ген, кодирующий поверхностный антиген (HBsAg). Ген HBsAg представляет собой одну длинную открытую рамку считывания, но содержит три кодона в «стартовой» рамке (ATG), которые делят ген на три части: пре-S1, пре-S2 и S. Из-за множественных стартовых кодонов полипептиды трех производятся разные размеры, называемые большим, средним и малым (pre-S1 + pre-S2 + S, pre-S2 + S или S).[51] Функция белка, кодируемого геном X, полностью не изучена,[52] но некоторые данные свидетельствуют о том, что он может действовать как транскрипционный трансактиватор.
Несколько некодирующая РНК элементы были идентифицированы в геноме HBV. К ним относятся: HBV PREalpha, HBV PREbeta и Эпсилон сигнала инкапсидации РНК HBV.[53][54]
Генотипы
Генотипы различаются по крайней мере на 8% последовательности и имеют четкое географическое распределение, что было связано с антропологической историей. Внутри генотипов были описаны подтипы: они различаются на 4–8% генома.
Известно восемь генотипы помечены от A до H.[20]
Описан возможный новый генотип "I",[55] но принятие этого обозначения не универсально.[56]
С тех пор были признаны еще два генотипа.[57] В текущем (2014 г.) листинге от A до J. Также распознаются несколько подтипов.
Есть как минимум 24 подтипа.
Различные генотипы могут по-разному реагировать на лечение.[58][59]
- Индивидуальные генотипы
Тип F, который отличается от других геномов на 14%, является наиболее дивергентным из известных типов. Тип А преобладает в Европа, Африка и Юго-Восточная Азия, в том числе Филиппины. Тип B и C преобладают в Азия; тип D распространен в Средиземноморье, Средний Восток и Индия; тип E локализован в Африке к югу от Сахары; тип F (или H) ограничен центральным и Южная Америка. Тип G был обнаружен в Франция и Германия. Генотипы A, D и F преобладают в Бразилия и все генотипы встречаются в Соединенные Штаты с частотами, зависящими от этнической принадлежности.
Штаммы E и F, по-видимому, произошли от коренного населения Африки и Нового Света соответственно.
Тип A имеет два подтипа: Aa (A1) в Африке / Азии и на Филиппинах и Ae (A2) в Европе / США.
Тип B имеет два различных географических распределения: Bj / B1 ('j' - Япония) и Ba / B2 ('a' - Азия). Тип Ba был далее подразделен на четыре клады (B2 – B4).
Тип C имеет два географических подтипа: Cs (C1) в Юго-Восточной Азии и Ce (C2) в Восточной Азии. Подтипы C были разделены на пять клад (C1 – C5). Шестая клада (C6) была описана на Филиппинах, но на сегодняшний день только в одном изоляте.[60] Тип C1 связан с Вьетнам, Мьянма и Таиланд; тип C2 с Япония, Корея и Китай; тип C3 с Новая Каледония и Полинезия; C4 с Австралия; и C5 с Филиппины. Еще один подтип описан в Папуа, Индонезия.[61]
Тип D разделен на 7 подтипов (D1 – D7).
Тип F подразделяется на 4 подтипа (F1 – F4). F1 был дополнительно разделен на 1a и 1b. В Венесуэла подтипы F1, F2 и F3 встречаются у американских индейцев востока и запада. Среди южноамериканских индейцев был обнаружен только F3. Подтипы Ia, III и IV имеют ограниченное географическое распространение (Центральная Америка, Север и Юг Южной Америки соответственно), в то время как клады Ib и II встречаются во всех Америках, за исключением Северной Южной Америки и Северной Америки соответственно.
Жизненный цикл

Жизненный цикл Вирус гепатита В сложный. Гепатит B - один из немногих известных не ретровирусный вирусы, которые используют обратная транскрипция как часть процесса репликации.
- Вложение
- Вирус проникает в клетку, связываясь с рецепторами на поверхности клетки и проникая в нее посредством эндоцитоз при посредничестве либо клатрин или же кавеолин-1.[62] HBV изначально связывается с гепарин сульфат протеогликан. Затем пре-S1-сегмент белка L HBV плотно связывается с рецептором клеточной поверхности. котранспортный полипептид тауроколата натрия (NTCP), закодированный SLC10A1gene.[63] NTCP в основном встречается в синусоидальная мембрана из клетки печени. Присутствие NTCP в клетках печени коррелирует с тканевой специфичностью инфекции HBV.[62]
- Проникновение
- После эндоцитоза вирусная мембрана сливается с мембраной клетки-хозяина, высвобождая нуклеокапсид в цитоплазму.[64]
- Без покрытия
- Поскольку вирус размножается с помощью РНК, созданной ферментом-хозяином, вирусная геномная ДНК должна быть перенесена в ядро клетки. Считается, что капсид транспортируется на микротрубочки к ядерная пора. Основные белки диссоциируют от частично двухцепочечной вирусной ДНК, которая затем становится полностью двухцепочечной (ДНК-полимеразами хозяина) и трансформируется в ковалентно замкнутую кольцевую ДНК (cccDNA ), который служит шаблоном для транскрипции четырех вирусных мРНК.
- Репликация
- Самая большая мРНК (которая длиннее вирусного генома) используется для создания новых копий генома и создания капсид основной белок и вирусная РНК-зависимаяДНК-полимераза.
- сборка
- Эти четыре вирусных транскрипта подвергаются дополнительной обработке и продолжают формировать вирионы потомства, которые высвобождаются из клетки или возвращаются в ядро и рециклируются, чтобы произвести еще больше копий.[51][65]
- Релиз
- Затем длинная мРНК транспортируется обратно в цитоплазму, где белок Р вириона синтезирует ДНК за счет своей активности обратной транскриптазы.
Трансактивированные гены
HBV обладает способностью трансактивировать FAM46A.[66]
Смотрите также
Рекомендации
- ^ Рю В. (2017). Молекулярная вирусология патогенных вирусов человека. Академическая пресса. С. 247–260. ISBN 978-0-12-800838-6.
- ^ Hunt R (21 ноября 2007 г.). «Вирусы гепатита». Университет Южной Калифорнии, факультет патологии и микробиологии. Получено 13 марта 2008.
- ^ а б Hassan MM, Li D, El-Deeb AS, Wolff RA, Bondy ML, Davila M, Abbruzzese JL (октябрь 2008 г.). «Связь между вирусом гепатита В и раком поджелудочной железы». Журнал клинической онкологии. 26 (28): 4557–62. Дои:10.1200 / JCO.2008.17.3526. ЧВК 2562875. PMID 18824707.
- ^ «Возвращаясь к вирусу гепатита B: проблемы лечебной терапии».
- ^ Schwalbe M, Ohlenschläger O, Marchanka A, Ramachandran R, Häfner S, Heise T, Görlach M (март 2008 г.). «Структура раствора альфа-стебель-петля посттранскрипционного регуляторного элемента вируса гепатита В». Исследования нуклеиновых кислот. 36 (5): 1681–9. Дои:10.1093 / nar / gkn006. ЧВК 2275152. PMID 18263618.
- ^ а б Балакришнан Л., Милавец Б. (ноябрь 2017 г.). «Эпигенетическая регуляция вирусных биологических процессов». Вирусы. 9 (11): 346. Дои:10.3390 / v9110346. ЧВК 5707553. PMID 29149060.
- ^ а б Иванов А.В., Валуев-Эллистон В.Т., Тюрина Д.А., Иванова О.Н., Кочетков С.Н., Бартош Б., Исагулянц М.Г. (январь 2017). «Окислительный стресс, триггер канцерогенеза печени, вызванного вирусами гепатита С и В». Oncotarget. 8 (3): 3895–3932. Дои:10.18632 / oncotarget.13904. ЧВК 5354803. PMID 27965466.
- ^ а б Хиггс MR, Chouteau P, Lerat H (май 2014 г.). "'Печень дала умереть: окислительное повреждение ДНК и гепатотропные вирусы » (PDF). Журнал общей вирусологии. 95 (Pt 5): 991–1004. Дои:10.1099 / vir.0.059485-0. PMID 24496828.
- ^ Ю Й, Цуй Й, Нидернхофер Л. Дж., Ван И (декабрь 2016 г.). "Возникновение, биологические последствия и значимость для здоровья человека повреждения ДНК, вызванного окислительным стрессом". Химические исследования в токсикологии. 29 (12): 2008–2039. Дои:10.1021 / acs.chemrestox.6b00265. ЧВК 5614522. PMID 27989142.
- ^ Диздароглу М (декабрь 2012). «Окислительное повреждение ДНК: механизмы, восстановление и болезнь». Письма о раке. 327 (1–2): 26–47. Дои:10.1016 / j.canlet.2012.01.016. PMID 22293091.
- ^ Нисида Н, Кудо М (2013). «Окислительный стресс и эпигенетическая нестабильность в гепатоканцерогенезе человека». Пищеварительные заболевания. 31 (5–6): 447–53. Дои:10.1159/000355243. PMID 24281019.
- ^ а б Озен С., Йылдыз Дж., Дагкан А.Т., Чевик Д., Орс А., Келес У. и др. (Май 2013). «Генетика и эпигенетика рака печени». Новая биотехнология. 30 (4): 381–4. Дои:10.1016 / j.nbt.2013.01.007. HDL:11693/20956. PMID 23392071.
- ^ Шибата Т., Абуратани Х. (июнь 2014 г.). «Исследование геномов рака печени». Обзоры природы. Гастроэнтерология и гепатология. 11 (6): 340–9. Дои:10.1038 / nrgastro.2014.6. PMID 24473361.
- ^ а б Тиан И, Ян В., Сон Дж, Ву И, Ни Би (август 2013 г.). «Вызванные белком Х гепатита В аберрантные эпигенетические модификации, способствующие патогенезу гепатоцеллюлярной карциномы человека». Молекулярная и клеточная биология. 33 (15): 2810–6. Дои:10.1128 / MCB.00205-13. ЧВК 3719687. PMID 23716588.
- ^ а б Герриери Ф., Беллони Л., Д'Андреа Д., Педикони Н., Ле Пера Л., Тестони Б. и др. (Февраль 2017). «Полногеномная идентификация прямых геномных мишеней HBx». BMC Genomics. 18 (1): 184. Дои:10.1186 / s12864-017-3561-5. ЧВК 5316204. PMID 28212627.
- ^ а б «Таксономия вирусов: выпуск 2018b». Международный комитет по таксономии вирусов (ICTV). Февраль 2019 г.. Получено 14 марта 2019.
- ^ Mason, W.S .; и другие. (8 июля 2008 г.). «00.030. Hepadnaviridae». Индекс вирусов ICTVdB. Международный комитет по таксономии вирусов. Получено 13 марта 2009.
- ^ Dupinay T, et al. (Ноябрь 2013). «Обнаружение естественной трансмиссивной хронической вирусной инфекции гепатита B среди Macaca fascicularis с острова Маврикий». Гепатология. 58 (5). С. 1610–1620. Дои:10.1002 / hep.26428. PMID 23536484.
- ^ а б Хунди Г.Б., Сталин Радж V, Гебре Майкл Д., Па С.Д., Купманс депутат, Остерхаус А.Д. и др. (Февраль 2017). «Новый вирус гепатита B субгенотипа D10, циркулирующий в Эфиопии». Журнал вирусных гепатитов. 24 (2): 163–173. Дои:10.1111 / jvh.12631. PMID 27808472.
- ^ а б Крамвис А., Кью М., Франсуа Г. (март 2005 г.). «Генотипы вируса гепатита В». Вакцина. 23 (19): 2409–23. Дои:10.1016 / j.vaccine.2004.10.045. PMID 15752827.
- ^ Магниус ЛО, Нордер Х (1995). «Подтипы, генотипы и молекулярная эпидемиология вируса гепатита В, отраженные вариабельностью последовательности S-гена». Интервирология. 38 (1–2): 24–34. Дои:10.1159/000150411. PMID 8666521.
- ^ Гош С., Банерджи П., Дени П., Мондал Р.К., Нанди М., Ройчоудхури А. и др. (Март 2013 г.). «Новый субгенотип HBV D9, новый рекомбинант D / C, выявленный у пациентов с хронической HBeAg-отрицательной инфекцией в Восточной Индии». Журнал вирусных гепатитов. 20 (3): 209–18. Дои:10.1111 / j.1365-2893.2012.01655.x. PMID 23383660.
- ^ Дрекслер Дж. Ф., Гейпель А., Кениг А., Корман В. М., ван Риель Д., Лейтен Л. М. и др. (Октябрь 2013). «Летучие мыши являются носителями патогенных гепаднавирусов, антигенно связанных с вирусом гепатита В и способных инфицировать гепатоциты человека». Труды Национальной академии наук Соединенных Штатов Америки. 110 (40): 16151–6. Bibcode:2013PNAS..11016151D. Дои:10.1073 / pnas.1308049110. ЧВК 3791787. PMID 24043818.
- ^ Цукерман AJ (1996). «Глава 70: Вирусы гепатита». В Baron S; и другие. (ред.). Медицинская микробиология Барона (4-е изд.). Univ Техасского медицинского отделения. ISBN 978-0-9631172-1-2. Получено 11 апреля 2018.
- ^ «ВОЗ | Гепатит В». www.who.int. Архивировано из оригинал 10 июля 2015 г.. Получено 12 июля 2015.
- ^ Локарнини S (2004). «Молекулярная вирусология вируса гепатита В». Семинары по заболеванию печени. 24 Дополнение 1 (Дополнение 1): 3–10. CiteSeerX 10.1.1.618.7033. Дои:10.1055 / с-2004-828672. PMID 15192795.
- ^ Говард CR (июль 1986 г.). «Биология гепаднавирусов». Журнал общей вирусологии. 67 (7): 1215–35. Дои:10.1099/0022-1317-67-7-1215. PMID 3014045.
- ^ Jaroszewicz J, Calle Serrano B, Wursthorn K, Deterding K, Schlue J, Raupach R и др. (Апрель 2010 г.). "Уровни поверхностного антигена гепатита B (HBsAg) в естественной истории инфекции вирусом гепатита B (HBV): европейская перспектива". Журнал гепатологии. 52 (4): 514–22. Дои:10.1016 / j.jhep.2010.01.014. PMID 20207438.
- ^ Сигер С., Мейсон В.С. (март 2000 г.). «Биология вируса гепатита В». Обзоры микробиологии и молекулярной биологии. 64 (1): 51–68. Дои:10.1128 / ммбр.64.1.51-68.2000. ЧВК 98986. PMID 10704474.
- ^ Линь Ю.Дж., Ву Х.Л., Чен Д.С., Чен П.Дж. (сентябрь 2012 г.). «Нуклеокапсид вируса гепатита В, но не свободный ядерный антиген, контролирует клиренс вируса у мышей». Журнал вирусологии. 86 (17): 9266–73. Дои:10.1128 / JVI.00608-12. ЧВК 3416136. PMID 22718814.
- ^ Lin YJ, Huang LR, Yang HC, Tzeng HT, Hsu PN, Wu HL, et al. (Май 2010 г.). «Корневой антиген вируса гепатита B определяет персистентность вируса в модели мышей C57BL / 6». Труды Национальной академии наук Соединенных Штатов Америки. 107 (20): 9340–5. Дои:10.1073 / pnas.1004762107. ЧВК 2889105. PMID 20439715.
- ^ Борн ЧР, Катен С.П., Фулц М.Р., Пакианатан С., Злотник А. (март 2009 г.). «Мутантный коровый белок вируса гепатита B имитирует ингибиторы самосборки икосаэдрического капсида». Биохимия. 48 (8): 1736–42. Дои:10.1021 / bi801814y. ЧВК 2880625. PMID 19196007.
- ^ Тан Х, Оиси Н., Канеко С., Мураками С. (октябрь 2006 г.). «Молекулярные функции и биологические роли белка x вируса гепатита В». Наука о раке. 97 (10): 977–83. Дои:10.1111 / j.1349-7006.2006.00299.x. PMID 16984372.
- ^ Макклейн С.Л., Клиппингер А.Дж., Лиццано Р., Бушар М.Дж. (ноябрь 2007 г.). «Репликация вируса гепатита B связана с HBx-зависимым митохондриями-регулируемым увеличением уровней цитозольного кальция». Журнал вирусологии. 81 (21): 12061–5. Дои:10.1128 / JVI.00740-07. ЧВК 2168786. PMID 17699583.
- ^ Бушар М.Дж., Пуро Р.Дж., Ван Л., Шнайдер Р.Дж. (июль 2003 г.). «Активация и ингибирование клеточных путей передачи сигналов кальция и тирозинкиназы позволяет идентифицировать мишени белка HBx, участвующего в репликации вируса гепатита B». Журнал вирусологии. 77 (14): 7713–9. Дои:10.1128 / JVI.77.14.7713-7719.2003. ЧВК 161925. PMID 12829810.
- ^ Чай Н., Чанг Х.Э., Николас Э., Хан З., Ярник М., Тейлор Дж. (Август 2008 г.). «Свойства субвирусных частиц вируса гепатита В». Журнал вирусологии. 82 (16): 7812–7. Дои:10.1128 / JVI.00561-08. ЧВК 2519590. PMID 18524834.
- ^ а б ван Хемерт Ф.Дж., ван де Клундерт М.А., Лукашов В.В., Коотстра Н.А., Беркхаут Б., Заайер Х.Л. (2011). «Белок X вируса гепатита B: происхождение и сходство структуры с центральным доменом ДНК-гликозилазы». PLOS ONE. 6 (8): e23392. Bibcode:2011PLoSO ... 623392V. Дои:10.1371 / journal.pone.0023392. ЧВК 3153941. PMID 21850270.
- ^ Линь Б., Андерсон Д.А. (2000). «Рудиментарная открытая рамка считывания X в вирусе гепатита В уток». Интервирология. 43 (3): 185–90. Дои:10.1159/000025037. PMID 11044813.
- ^ Osiowy C, Giles E, Tanaka Y, Mizokami M, Minuk GY (ноябрь 2006 г.). «Молекулярная эволюция вируса гепатита В за 25 лет». Журнал вирусологии. 80 (21): 10307–14. Дои:10.1128 / JVI.00996-06. ЧВК 1641782. PMID 17041211.
- ^ Чжоу Y, Холмс EC (август 2007 г.). «Байесовские оценки скорости эволюции и возраста вируса гепатита B». Журнал молекулярной эволюции. 65 (2): 197–205. Bibcode:2007JMolE..65..197Z. Дои:10.1007 / s00239-007-0054-1. PMID 17684696.
- ^ Параскевис Д., Магиоркинис Г., Магиоркинис Э., Хо С.Ю., Белшоу Р., Аллен Дж. П., Хатзакис А. (март 2013 г.). «Датирование происхождения и распространения инфекции вируса гепатита В у людей и приматов». Гепатология. 57 (3): 908–16. Дои:10.1002 / hep.26079. PMID 22987324.
- ^ Литтлджон М., Локарнини С., Юэнь Л. (январь 2016 г.). «Происхождение и эволюция вируса гепатита B и вируса гепатита D». Перспективы Колд-Спринг-Харбор в медицине. 6 (1): a021360. Дои:10.1101 / cshperspect.a021360. ЧВК 4691804. PMID 26729756.
- ^ Раше А., Соуза Б.Ф., Дрекслер Дж. Ф. (февраль 2016 г.). «Гепаднавирусы летучих мышей и происхождение вирусов гепатита В приматов». Текущее мнение в вирусологии. 16: 86–94. Дои:10.1016 / j.coviro.2016.01.015. PMID 26897577.
- ^ Bouckaert R, Simons BC, Krarup H, Friesen TM, Osiowy C (2017). «Отслеживание эволюционной истории генотипа B5 (ранее B6) вируса гепатита B (HBV) в циркумполярной Арктике с помощью филогеографического моделирования». PeerJ. 5: e3757. Дои:10.7717 / peerj.3757. ЧВК 5581946. PMID 28875087.
- ^ Мюлеманн Б., Джонс Т.К., Дамгаард ПБ, Аллентофт М.Э., Шевнина И., Логвин А. и др. (Май 2018). «Древние вирусы гепатита В от бронзового века до средневековья». Природа. 557 (7705): 418–423. Bibcode:2018Натура.557..418M. Дои:10.1038 / s41586-018-0097-z. PMID 29743673.
- ^ а б c d е Бен Гуарино (9 мая 2018 г.). «В останках древних людей обнаружены новые штаммы вируса гепатита В». Вашингтон Пост. Получено 9 января 2018.
- ^ Кей А., Зулим Ф (август 2007 г.). «Генетическая изменчивость и эволюция вируса гепатита В». Вирусные исследования. 127 (2): 164–76. Дои:10.1016 / j.virusres.2007.02.021. PMID 17383765.
- ^ Дойч Г., Шауль Ю. (февраль 2004 г.). «Преобладание энхансера I в экспрессии гена вируса гепатита В». Молекулярная и клеточная биология. 24 (4): 1799–808. Дои:10.1128 / mcb.24.4.1799-1808.2004. ЧВК 344184. PMID 14749394.
- ^ Антонуччи Т.К., Раттер В.Дж. (февраль 1989 г.). «Промоторы вируса гепатита B (HBV) регулируются усилителем HBV тканеспецифическим образом». Журнал вирусологии. 63 (2): 579–83. ЧВК 247726. PMID 2536093.
- ^ Хуан Б., Сиддики А. (1993). «Регулирование экспрессии гена вируса гепатита В». Журнал гепатологии. 17 Дополнение 3: S20-3. Дои:10.1016 / s0168-8278 (05) 80419-2. PMID 8509635.
- ^ а б Бек Дж., Нассал М. (январь 2007 г.). «Репликация вируса гепатита В». Всемирный журнал гастроэнтерологии. 13 (1): 48–64. Дои:10.3748 / wjg.v13.i1.48. ЧВК 4065876. PMID 17206754.
- ^ Бушар MJ, Шнайдер RJ (декабрь 2004 г.). «Загадочный ген X вируса гепатита В». Журнал вирусологии. 78 (23): 12725–34. Дои:10.1128 / JVI.78.23.12725-12734.2004. ЧВК 524990. PMID 15542625.
- ^ Смит Дж., Донелло Дж., Люк Р., Стегер Дж., Надежда Т. Дж. (Ноябрь 1998 г.). «Посттранскрипционный регуляторный элемент вируса гепатита В содержит две консервативные стебли-петли РНК, которые необходимы для функционирования». Исследования нуклеиновых кислот. 26 (21): 4818–27. Дои:10.1093 / nar / 26.21.4818. ЧВК 147918. PMID 9776740.
- ^ Flodell S, Schleucher J, Cromsigt J, Ippel H, Kidd-Ljunggren K, Wijmenga S (ноябрь 2002 г.). «Апикальный стержень-петля сигнала инкапсидации вируса гепатита B складывается в стабильную тройную петлю с двумя лежащими под ней пиримидиновыми выступами». Исследования нуклеиновых кислот. 30 (21): 4803–11. Дои:10.1093 / нар / gkf603. ЧВК 135823. PMID 12409471.
- ^ Olinger CM, Jutavijittum P, Hübschen JM, Yousukh A, Samountry B, Thammavong T. и др. (Ноябрь 2008 г.). «Возможный новый генотип вируса гепатита В, Юго-Восточная Азия». Возникающие инфекционные заболевания. 14 (11): 1777–80. Дои:10.3201 / eid1411.080437. ЧВК 2630741. PMID 18976569.
- ^ Курбанов Ф., Танака Ю., Крамвис А., Симмондс П., Мизоками М. (август 2008 г.). «Когда я должен« рассматривать новый генотип вируса гепатита В? ». Журнал вирусологии. 82 (16): 8241–2. Дои:10.1128 / JVI.00793-08. ЧВК 2519592. PMID 18663008.
- ^ Эрнандес С., Венегас М., Брам Дж., Вильянуэва Р.А. (октябрь 2014 г.). «Полногеномная последовательность клона вируса гепатита B генотипа f1b от хронически инфицированного чилийского пациента». Анонсы генома. 2 (5): e01075–14. Дои:10.1128 / genomeA.01075-14. ЧВК 4208329. PMID 25342685.
- ^ Паламбо Э (2007). «Генотипы гепатита В и ответ на противовирусную терапию: обзор». Американский журнал терапии. 14 (3): 306–9. Дои:10.1097 / 01.pap.0000249927.67907.eb. PMID 17515708.
- ^ Махтаб М.А., Рахман С., Хан М., Карим Ф. (октябрь 2008 г.). «Генотипы вируса гепатита В: обзор». Международная организация по заболеваниям печени и желчевыводящих путей и поджелудочной железы. 7 (5): 457–64. PMID 18842489.
- ^ Кавинта Л., Сун Дж., Май А., Инь Дж., Фон Мельцер М., Радтке М. и др. (Июнь 2009 г.). «Новый изолят вируса гепатита B из Филиппин, возможно, представляющий новый субгенотип C6». Журнал медицинской вирусологии. 81 (6): 983–7. Дои:10.1002 / jmv.21475. PMID 19382274.
- ^ Лусида М.И., Нуграапутра В.Е., Хандаджани Р., Нагано-Фуджи М., Сасаяма М., Утсуми Т., Хотта Х. (июль 2008 г.). «Новые субгенотипы генотипов вируса гепатита B C и D в Папуа, Индонезия». Журнал клинической микробиологии. 46 (7): 2160–6. Дои:10.1128 / JCM.01681-07. ЧВК 2446895. PMID 18463220.
- ^ а б Чжан З., Зендер Б., Дамрау С., Урбан С. (июль 2016 г.). «Визуализация проникновения вируса гепатита В - новые инструменты и подходы для непосредственного отслеживания проникновения вируса в гепатоциты». Письма FEBS. 590 (13): 1915–26. Дои:10.1002/1873-3468.12202. PMID 27149321.
- ^ Янь Х, Лю И, Суй Дж, Ли В. (сентябрь 2015 г.). «NTCP открывает двери для заражения вирусом гепатита B». Антивирусные исследования. 121: 24–30. Дои:10.1016 / j.antiviral.2015.06.002. PMID 26071008.
- ^ Ваташи К., Вакита Т. (август 2015 г.). "Вирус гепатита B и проникновение вируса гепатита D, видовая специфичность и тропизм тканей". Перспективы Колд-Спринг-Харбор в медицине. 5 (8): a021378. Дои:10.1101 / cshperspect.a021378. ЧВК 4526719. PMID 26238794.
- ^ Брюсс V (январь 2007 г.). «Морфогенез вируса гепатита В». Всемирный журнал гастроэнтерологии. 13 (1): 65–73. Дои:10.3748 / wjg.v13.i1.65. ЧВК 4065877. PMID 17206755.
- ^ «Fam46A (кодирование белков)». Генные Карты. Генные Карты. Получено 18 февраля 2015.
