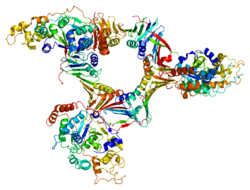
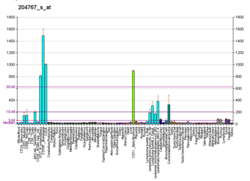
Эндонуклеаза 1, специфичная для структуры лоскута - Википедия - Flap structure-specific endonuclease 1
Эндонуклеаза лоскута 1 является фермент что у людей кодируется FEN1 ген.[5][6]
Функция
Белок, кодируемый этим геном, удаляет 5 'выступающих «створок» (или коротких участков одноцепочечной ДНК, которые «свисают», потому что их нуклеотидные основания не могут связываться с их комплементарной парой оснований - несмотря на любое спаривание оснований ниже по течению) при репарации ДНК и обрабатывает 5 'концы Фрагменты Окадзаки в синтезе отстающей цепи ДНК. Прямое физическое взаимодействие между этим белком и AP-эндонуклеазой 1 во время длинного патча. базовая эксцизионная пластика обеспечивает скоординированную загрузку белков на субстрат, таким образом передавая субстрат от одного фермента к другому. Белок является членом семейства эндонуклеаз XPG / RAD2 и является одним из десяти белков, необходимых для внеклеточной репликации ДНК. Вторичная структура ДНК может ингибировать обработку лоскута при определенных тринуклеотидные повторы зависимым от длины способом, скрывая 5'-конец лоскута, который необходим как для связывания, так и для расщепления белком, кодируемым этим геном. Следовательно, вторичная структура может препятствовать защитной функции этого белка, приводя к сайт-специфическим расширениям тринуклеотидов.[6]
Взаимодействия
Эндонуклеаза 1, специфичная для структуры лоскута, может взаимодействовать с:
Избыточная экспрессия FEN1 при раке
FEN1 чрезмерно экспрессируется при большинстве случаев рака груди,[17] предстательная железа,[18] желудок,[19][20] нейробластомы,[21] поджелудочная,[22] и легкое.[23]
FEN1 является важным ферментом неточного пути восстановления двухцепочечных разрывов ДНК, называемого микрогомологически зависимым альтернативным соединением концов или соединение концов, опосредованное микрогомологией (MMEJ).[24] MMEJ всегда включает в себя хотя бы небольшую делецию, так что это мутагенный путь.[25] Несколько других путей также могут восстанавливать двухцепочечные разрывы в ДНК, включая менее неточный путь негомологичное соединение концов (NHEJ) и точные пути с использованием гомологичный рекомбинационный ремонт (HRR).[26] Различные факторы определяют, какой путь будет использоваться для восстановления двухцепочечных разрывов ДНК.[25] Когда FEN1 сверхэкспрессируется (это происходит, когда его промотор гипометилирован[17]) может быть предпочтительнее крайне неточный путь MMEJ, вызывающий более высокую частоту мутаций и повышенный риск рака.
Ракам очень часто не хватает экспрессии одного или нескольких генов репарации ДНК, но сверхэкспрессия гена репарации ДНК необычна при раке. Например, по крайней мере 36 ферментов репарации ДНК при мутационном дефекте в клетках зародышевой линии вызывают повышенный риск рака (наследственный онкологические синдромы ).[нужна цитата ] Точно так же по крайней мере 12 генов репарации ДНК часто оказывались эпигенетически репрессированными при одном или нескольких раках.[нужна цитата ] (Смотрите также Эпигенетически уменьшенная репарация ДНК и рак.) Обычно недостаточная экспрессия фермента репарации ДНК приводит к увеличению нереставрированных повреждений ДНК, которые из-за ошибок репликации (транслезионный синтез ), приводят к мутациям и раку. Однако репарация MMEJ, опосредованная FEN1, очень неточна, поэтому в этом случае чрезмерная экспрессия, а не недостаточная экспрессия приводит к раку.
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000168496 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000024742 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ «Ссылка на Mouse PubMed:». Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Хираока Л.Р., Харрингтон Дж. Дж., Герхард Д.С., Либер М.Р., Хсие С.Л. (июль 1995 г.). «Последовательность человеческого FEN-1, структурно-специфической эндонуклеазы, и хромосомная локализация гена (FEN1) у мыши и человека». Геномика. 25 (1): 220–5. Дои:10.1016 / 0888-7543 (95) 80129-А. PMID 7774922.
- ^ а б «Ген Entrez: эндонуклеаза 1, специфичная для структуры лоскута FEN1».
- ^ а б Дианова И.И., Бор В.А., Дианов Г.Л. (октябрь 2001 г.). «Взаимодействие человеческой AP-эндонуклеазы 1 с эндонуклеазой 1 лоскута и ядерным антигеном пролиферирующих клеток, участвующих в репарации эксцизионного основания длинного пятна». Биохимия. 40 (42): 12639–44. Дои:10.1021 / bi011117i. PMID 11601988.
- ^ а б Шарма С., Соммерс Дж. А., Ву Л., Бор В. А., Хиксон И. Д., Брош Р. М. (март 2004 г.). «Стимуляция эндонуклеазы-1 лоскута белком синдрома Блума». J. Biol. Chem. 279 (11): 9847–56. Дои:10.1074 / jbc.M309898200. PMID 14688284.
- ^ а б c Henneke G, Koundrioukoff S, Hübscher U (июль 2003 г.). «Фосфорилирование человеческого Fen1 циклин-зависимой киназой модулирует его роль в регуляции репликационной вилки». Онкоген. 22 (28): 4301–13. Дои:10.1038 / sj.onc.1206606. PMID 12853968.
- ^ а б Хасан С., Штуки М., Хасса П.О., Имхоф Р., Гериг П., Хунцикер П., Хюбшер Ю., Хоттигер, Миссури (июнь 2001 г.). «Регулирование активности эндонуклеазы-1 лоскута человека путем ацетилирования через транскрипционный коактиватор p300». Мол. Клетка. 7 (6): 1221–31. Дои:10.1016 / с1097-2765 (01) 00272-6. PMID 11430825.
- ^ Чай Кью, Чжэн Л., Чжоу М., Турчи Дж.Дж., Шен Б. (декабрь 2003 г.). «Взаимодействие и стимуляция нуклеазной активности человеческого FEN-1 с помощью гетерогенного ядерного рибонуклеопротеина A1 в процессинге альфа-сегмента во время созревания фрагмента Окадзаки». Биохимия. 42 (51): 15045–52. Дои:10.1021 / bi035364t. PMID 14690413.
- ^ Jónsson ZO, Hindges R, Hübscher U (апрель 1998 г.). «Регулирование репликации ДНК и репарации белков посредством взаимодействия с лицевой стороной ядерного антигена пролиферирующих клеток». EMBO J. 17 (8): 2412–25. Дои:10.1093 / emboj / 17.8.2412. ЧВК 1170584. PMID 9545252.
- ^ Гэри Р., Людвиг Д.Л., Корнелиус Х.Л., Макиннес М.А., Парк М.С. (сентябрь 1997 г.). «Эндонуклеаза репарации ДНК XPG связывается с ядерным антигеном пролиферирующих клеток (PCNA) и разделяет элементы последовательности с PCNA-связывающими областями FEN-1 и ингибитором циклин-зависимой киназы p21». J. Biol. Chem. 272 (39): 24522–9. Дои:10.1074 / jbc.272.39.24522. PMID 9305916.
- ^ Чен У, Чен С., Саха П, Датта А. (октябрь 1996 г.). «p21Cip1 / Waf1 нарушает рекрутирование человеческого Fen1 ядерным антигеном пролиферирующих клеток в комплекс репликации ДНК». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 93 (21): 11597–602. Bibcode:1996PNAS ... 9311597C. Дои:10.1073 / пнас.93.21.11597. ЧВК 38103. PMID 8876181.
- ^ Ю П, Хуан Б., Шен М., Лау Ц., Чан Э, Мишель Дж., Сюн Й., Паян Д. Г., Ло И (январь 2001 г.). «p15 (PAF), новый фактор, связанный с PCNA, с повышенной экспрессией в опухолевых тканях». Онкоген. 20 (4): 484–9. Дои:10.1038 / sj.onc.1204113. PMID 11313979.
- ^ Брош Р.М., фон Коббе С., Соммерс Дж. А., Кармакар П., Опреско П. Л., Пиотровски Дж., Дианова И., Дианов Г. Л., Бор В. А. (октябрь 2001 г.). «Белок синдрома Вернера взаимодействует с эндонуклеазой 1 лоскута человека и стимулирует его активность по расщеплению». EMBO J. 20 (20): 5791–801. Дои:10.1093 / emboj / 20.20.5791. ЧВК 125684. PMID 11598021.
- ^ а б Сингх П., Ян М., Дай Х, Ю Д., Хуанг Ц., Тан В., Кернстин К. Х., Лин Д., Шен Б. (2008). «Сверхэкспрессия и гипометилирование гена эндонуклеазы 1 лоскута при раке груди и других формах рака». Мол. Рак Res. 6 (11): 1710–7. Дои:10.1158 / 1541-7786.MCR-08-0269 (неактивно 11.10.2020). ЧВК 2948671. PMID 19010819.CS1 maint: DOI неактивен по состоянию на октябрь 2020 г. (связь)
- ^ Лам Дж. С., Селигсон Д. Б., Ю Х, Ли А., Ива М., Пантак А. Дж., Зенг Г., Хорват С., Беллдегрун А. С. (2006). «Эндонуклеаза лоскута 1 сверхэкспрессируется при раке простаты и связана с высоким показателем Глисона». BJU Int. 98 (2): 445–51. Дои:10.1111 / j.1464-410X.2006.06224.x. PMID 16879693. S2CID 22165252.
- ^ Kim JM, Sohn HY, Yoon SY, Oh JH, Yang JO, Kim JH, Song KS, Rho SM, Yoo HS, Yoo HS, Kim YS, Kim JG, Kim NS (2005). «Идентификация генов, связанных с раком желудка, с использованием микроматрицы кДНК, содержащей новые метки экспрессированной последовательности, экспрессируемые в клетках рака желудка». Clin. Рак Res. 11 (2 Pt 1): 473–82. PMID 15701830.
- ^ Ван К., Се С, Чен Д. (2014). «Эндонуклеаза лоскута 1 является многообещающим кандидатом в биомаркеры рака желудка и участвует в пролиферации клеток и апоптозе». Int. J. Mol. Med. 33 (5): 1268–74. Дои:10.3892 / ijmm.2014.1682. PMID 24590400.
- ^ Краузе А., Комбаре V, Яконо I, Лакруа Б, Компаньон С, Бержерон С., Вальсезия-Виттманн С., Лейсснер П., Мужен Б., Пюизье А. (2005). «Полногеномный анализ экспрессии генов в нейробластомах, обнаруженных массовым скринингом» (PDF). Рак Lett. 225 (1): 111–20. Дои:10.1016 / j.canlet.2004.10.035. PMID 15922863.
- ^ Якобузио-Донахью, Калифорния, Майтра А., Олсен М., Лоу А.В., ван Хик Н.Т., Рости С., Уолтер К., Сато Н., Паркер А., Ашфак Р., Джаффи Э., Рю Б., Джонс Дж., Эшлеман Дж. Р., Йео Си Джей, Кэмерон Дж. Л. , Керн С.Е., Хрубан Р.Х., Браун П.О., Гоггинс М. (2003). «Исследование глобальных паттернов экспрессии генов в аденокарциноме поджелудочной железы с использованием микрочипов кДНК». Являюсь. Дж. Патол. 162 (4): 1151–62. Дои:10.1016 / S0002-9440 (10) 63911-9. ЧВК 1851213. PMID 12651607.
- ^ Николова Т, Кристманн М, Кайна Б (2009). «FEN1 сверхэкспрессируется в опухолях яичек, легких и головного мозга». Противораковый Res. 29 (7): 2453–9. PMID 19596913.
- ^ Шарма С., Джавадекар С.М., Пандей М., Шривастава М., Кумари Р., Рагхаван С.К. (2015). «Гомология и ферментативные требования к альтернативному соединению концов в зависимости от микрогомологии». Cell Death Dis. 6 (3): e1697. Дои:10.1038 / cddis.2015.58. ЧВК 4385936. PMID 25789972.
- ^ а б Лян Л., Дэн Л., Чен Й, Ли Г.К., Шао С., Тишфилд Дж. А. (2005). «Модуляция присоединения концов ДНК ядерными белками». J. Biol. Chem. 280 (36): 31442–9. Дои:10.1074 / jbc.M503776200. PMID 16012167.
- ^ Оттавиани Д., Лекейн М., Шир Д. (2014). «Роль микрогомологии в структурной изменчивости генома». Тенденции Genet. 30 (3): 85–94. Дои:10.1016 / j.tig.2014.01.001. PMID 24503142.
дальнейшее чтение
- Фингер Л.Д., Бланшар М.С., Таймер К.А., Сенгерова Б., Сингх П., Чавес В., Лю Ф., Грасби Дж. А., Шен Б. (2009). «Карман 3'-лоскута эндонуклеазы 1 лоскута человека имеет решающее значение для связывания субстрата и катализа». J. Biol. Chem. 284 (33): 22184–94. Дои:10.1074 / jbc.M109.015065. ЧВК 2755943. PMID 19525235.
- Кемени М.М., Алава Г., Оливер Дж. М. (1993). «Улучшение ответов при гепатомах с инфузиями в печеночную артерию с циркадным ритмом рекомбинантного интерлейкина-2». J. Immunother. 12 (4): 219–23. Дои:10.1097/00002371-199211000-00001. PMID 1477073.
- Ли Х, Ли Дж, Харрингтон Дж, Либер М.Р., Бургерс П.М. (1995). «Синтез запаздывающей нити ДНК в репликационной вилке эукариот включает связывание и стимуляцию FEN-1 ядерным антигеном пролиферирующих клеток». J. Biol. Chem. 270 (38): 22109–12. Дои:10.1074 / jbc.270.38.22109. PMID 7673186.
- Робинс П., Паппин Д. Д., Вуд Р. Д., Линдал Т. (1994). «Структурная и функциональная гомология между ДНКазой IV млекопитающих и 5'-нуклеазным доменом ДНК-полимеразы I. Escherichia coli». J. Biol. Chem. 269 (46): 28535–8. PMID 7961795.
- Мюррей Дж. М., Тавассоли М., аль-Харити Р., Шелдрик К. С., Леманн А. Р., Карр А. М., Уоттс Ф.З. (1994). «Структурная и функциональная консервация человеческого гомолога гена Schizosaccharomyces pombe rad2, который необходим для сегрегации хромосом и восстановления после повреждения ДНК». Мол. Клетка. Биол. 14 (7): 4878–88. Дои:10.1128 / MCB.14.7.4878. ЧВК 358860. PMID 8007985.
- Харрингтон Дж. Дж., Либер М. Р. (1994). «Характеристика эндонуклеазы, специфичной для структуры ДНК млекопитающих». EMBO J. 13 (5): 1235–46. Дои:10.1002 / j.1460-2075.1994.tb06373.x. ЧВК 394933. PMID 8131753.
- Шен Б., Нолан Дж. П., Скляр Л. А., Парк М. С. (1996). «Незаменимые аминокислоты для связывания субстрата и катализа эндонуклеазы 1 лоскута человека». J. Biol. Chem. 271 (16): 9173–6. Дои:10.1074 / jbc.271.16.9173. PMID 8621570.
- Чен У, Чен С., Саха П, Датта А (1996). «p21Cip1 / Waf1 нарушает рекрутирование человеческого Fen1 ядерным антигеном пролиферирующих клеток в комплекс репликации ДНК». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 93 (21): 11597–602. Bibcode:1996PNAS ... 9311597C. Дои:10.1073 / пнас.93.21.11597. ЧВК 38103. PMID 8876181.
- Варбрик Э., Лейн Д.П., Гловер Д.М., Кокс Л.С. (1997). «Гомологичные области Fen1 и p21Cip1 конкурируют за связывание с одним и тем же сайтом на PCNA: потенциальный механизм для координации репликации и репарации ДНК». Онкоген. 14 (19): 2313–21. Дои:10.1038 / sj.onc.1201072. PMID 9178907.
- Клунгланд А., Линдал Т. (1997). «Второй путь завершения эксцизионной репарации оснований ДНК человека: восстановление очищенными белками и потребность в ДНКазе IV (FEN1)». EMBO J. 16 (11): 3341–8. Дои:10.1093 / emboj / 16.11.3341. ЧВК 1169950. PMID 9214649.
- Гэри Р., Людвиг Д.Л., Корнелиус Г.Л., Макиннес Массачусетс, Парк М.С. (1997). «Эндонуклеаза репарации ДНК XPG связывается с ядерным антигеном пролиферирующих клеток (PCNA) и разделяет элементы последовательности с PCNA-связывающими областями FEN-1 и ингибитором циклин-зависимой киназы p21». J. Biol. Chem. 272 (39): 24522–9. Дои:10.1074 / jbc.272.39.24522. PMID 9305916.
- Stöhr H, Marquardt A, Rivera A, Cooper PR, Nowak NJ, Shows TB, Gerhard DS, Weber BH (1998). «Генная карта области желточной макулярной дистрофии Беста в хромосоме 11q12-q13.1». Genome Res. 8 (1): 48–56. Дои:10.1101 / гр.8.1.48. ЧВК 310689. PMID 9445487.
- Jónsson ZO, Hindges R, Hübscher U (1998). «Регулирование репликации ДНК и репарации белков посредством взаимодействия с лицевой стороной ядерного антигена пролиферирующих клеток». EMBO J. 17 (8): 2412–25. Дои:10.1093 / emboj / 17.8.2412. ЧВК 1170584. PMID 9545252.
- Warbrick E, Heatherington W, Lane DP, Glover DM (1998). «PCNA-связывающие белки в Drosophila melanogaster: анализ консервативного связывающего домена PCNA». Нуклеиновые кислоты Res. 26 (17): 3925–32. Дои:10.1093 / nar / 26.17.3925. ЧВК 147798. PMID 9705499.
- Хосфилд ди-джей, Мол CD, Шен Б., Тайнер Дж. А. (1998). «Структура репарации и репликации эндонуклеазы и экзонуклеазы FEN-1 ДНК: связывание ДНК и связывания PCNA с активностью FEN-1». Клетка. 95 (1): 135–46. Дои:10.1016 / S0092-8674 (00) 81789-4. PMID 9778254. S2CID 8283941.
- Дианов Г.Л., Дженсен Б.Р., Кенни М.К., Бор В.А. (1999). «Репликационный белок А стимулирует ядерную антиген-зависимую репарацию абазических участков в ДНК пролиферирующих клеток экстрактами клеток человека». Биохимия. 38 (34): 11021–5. Дои:10.1021 / bi9908890. PMID 10460157.
- Грин А.Л., Снайп-младший, Горденин Д.А., Резник М.А. (1999). «Функциональный анализ человеческого FEN1 в Saccharomyces cerevisiae и его роль в стабильности генома». Гм. Мол. Genet. 8 (12): 2263–73. Дои:10.1093 / hmg / 8.12.2263. PMID 10545607.
- Мацумото Ю., Ким К., Гурвиц Дж., Гэри Р., Левин Д.С., Томкинсон А.Э., Парк М.С. (1999). «Восстановление ядерной антиген-зависимой репарации апуриновых / апиримидиновых участков пролиферирующих клеток очищенными белками человека». J. Biol. Chem. 274 (47): 33703–8. Дои:10.1074 / jbc.274.47.33703. PMID 10559261.
- Спиро С., Пеллетье Р., Рольфсмайер М.Л., Диксон М.Дж., Лауэ Р.С., Гупта Г., Парк М.С., Чен Х, Мариаппан С.В., МакМюррей СТ (2000). «Ингибирование процессинга FEN-1 вторичной структурой ДНК в тринуклеотидных повторах». Мол. Клетка. 4 (6): 1079–85. Дои:10.1016 / S1097-2765 (00) 80236-1. PMID 10635332.
- Хасан С., Штуки М., Хасса П.О., Имхоф Р., Гериг П., Хунцикер П., Хюбшер Ю., Хоттигер МО (2001). «Регулирование активности эндонуклеазы-1 лоскута человека путем ацетилирования через транскрипционный коактиватор p300». Мол. Клетка. 7 (6): 1221–31. Дои:10.1016 / S1097-2765 (01) 00272-6. PMID 11430825.
- Caldwell RB, Braselmann H, Schoetz U, Heuer S, Scherthan H, Zitzelsberger H (4 июля 2016 г.). «Положительный кофактор 4 (PC4) имеет решающее значение для изменения маршрута пути репарации ДНК в клетках DT40». Sci. Представитель. 6: 28890. Bibcode:2016НатСР ... 628890C. Дои:10.1038 / srep28890. ЧВК 4931448. PMID 27374870.