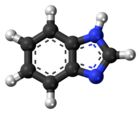
Бензимидазол - Benzimidazole
 | |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC 1ЧАС-1,3-бензимидазол | |||
| Другие имена 1ЧАС-Benzo [d] имидазол | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| 109682 | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.000.075 | ||
| Номер ЕС |
| ||
| 3106 | |||
| КЕГГ | |||
PubChem CID | |||
| UNII | |||
| |||
| |||
| Характеристики | |||
| C7ЧАС6N2 | |||
| Молярная масса | 118.139 г · моль−1 | ||
| Температура плавления | От 170 до 172 ° C (от 338 до 342 ° F, от 443 до 445 K) | ||
| Кислотность (пKа) | 12,8 (для бензимидазола) и 5,6 (для конъюгированной кислоты) [1] | ||
| Опасности | |||
| Паспорт безопасности | Внешний паспорт безопасности материалов | ||
| Пиктограммы GHS |  | ||
| Сигнальное слово GHS | Предупреждение | ||
| H302, H315, H319, H335 | |||
| P261, P264, P270, P271, P280, P301 + 312, P302 + 352, P304 + 340, P305 + 351 + 338, P312, P321, P330, P332 + 313, P337 + 313, P362, P403 + 233, P405, P501 | |||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Бензимидазол это гетероциклический ароматный органическое соединение. Это бициклическое соединение состоит из слияния бензол и имидазол. Это бесцветное твердое вещество.
Подготовка
Бензимидазол получают конденсацией о-фенилендиамин с муравьиная кислота,[2] или эквивалент триметилортоформиат:
- C6ЧАС4(NH2)2 + HC (OCH3)3 → С6ЧАС4N (NH) CH + 3 CH3ОЙ
2-замещенные производные получают, когда проводят конденсацию с альдегидами вместо муравьиной кислоты с последующим окислением. Этот метод дает 2-замещенные бензимидазолы.[3]
Реакции
Бензимидазол - это основа:
- C6ЧАС4N (NH) CH + H+ → [C6ЧАС4(NH)2CH]+
Его также можно депротонировать с помощью более сильных оснований:
- C6ЧАС4N (NH) CH + LiH → Li [C6ЧАС4N2CH] + H2
Имин может быть алкилирован и также служит лигандом в координационная химия. Наиболее характерные особенности бензимидазольного комплекса N-рибозил-диметилбензимидазол, как обнаружено в витамин B12.[4]
N,N '-Соли диалкилбензимидазолия являются предшественниками некоторых N-гетероциклические карбены.[5][6]
Приложения
Бензимидазолы часто биоактивны. Много антигельминтные препараты (альбендазол, мебендазол, триклабендазол и др.) относятся к классу соединений бензимидазола. Бензимидазольные фунгициды коммерциализируются. Они действуют, связываясь с микротрубочками грибов и останавливая рост гиф. Он также связывается с микротрубочками веретена и блокирует деление ядра.

В ингибиторы протонной помпы (антациды ) омепразол, лансопразол, пантопразол, рабепразол, и тенатопразол все содержат бензимидазольную группу. Другие фармацевтические препараты, содержащие бензимидазольную группу, включают: этонитазен, галетерон, маватреп, и довитиниб. Производные бензимидазола входят в число наиболее часто используемых кольцевых систем для низкомолекулярных лекарств, перечисленных FDA США. [7]
При производстве печатных плат бензимидазол можно использовать в качестве органический консервант паяемости.[нужна цитата ]
Некоторые красители являются производными бензимидазолов.[8]
Смотрите также
- Бензимидазолин
- Полибензимидазол, волокно с высокими характеристиками
Рекомендации
- ^ Walba, H. & Isensee, R. W. Константы кислотности некоторых арилимидазолов и их катионов. J. Org. Chem. 26, 2789-2791 (1961).
- ^ Э. К. Вагнер и В. Х. Миллетт (1943). «Бензимидазол». Органический синтез.; Коллективный объем, 2, п. 65.
- ^ Роберт А. Смайли «Фенилен- и толуендиамины» в Энциклопедии промышленной химии Ульмана 2002, Wiley-VCH, Weinheim. Дои:10.1002 / 14356007.a19_405
- ^ Х. А. Баркер; Р. Д. Смит; Х. Вайсбах; Дж. И. Тухи; Дж. Н. Лэдд и Б. Э. Вулкани (1 февраля 1960 г.). «Выделение и свойства кристаллических коферментов кобамида, содержащих бензимидазол или 5,6-диметилбензимидазол». Журнал биологической химии. 235 (2): 480–488. PMID 13796809.
- ^ Р. Джекстелл; А. Фриш; М. Беллер; Д. Роттгер; М. Малаун; Б. Бильдштейн (2002). «Эффективная теломеризация 1,3-бутадиена со спиртами в присутствии карбеновых комплексов палладия (0), образующихся in situ». Журнал молекулярного катализа A: химический. 185 (1–2): 105–112. Дои:10.1016 / S1381-1169 (02) 00068-7.
- ^ Х. В. Хюинь; Дж. Х. Х. Хо; Т. С. Нео; Л. Л. Кох (2005). «Управляемый растворителем селективный синтез транс-сконфигурированного комплекса бензимидазолин-2-илиденпалладий (II) и исследования его каталитической активности типа Хека». Журнал металлоорганической химии. 690 (16): 3854–3860. Дои:10.1016 / j.jorganchem.2005.04.053.
- ^ Taylor, R.D .; MacCoss, M .; Лоусон, А. Д. Дж. Мед. Хим. 2014, 57, 5845.>
- ^ Хорст Бернет "Метиновые красители и пигменты" в Энциклопедия промышленной химии Ульмана, 2008, Wiley-VCH, Weinheim. Дои: 10.1002 / 14356007.a16_487.pub2
дальнейшее чтение
- Гримметт М. Р. (1997). Синтез имидазола и бензимидазола. Бостон: Academic Press. ISBN 0-12-303190-7.