Развитие нервной системы - Development of the nervous system
| Эта статья является частью серии статей о |
| Развитие системы органов |
|---|
| Нервная система |
| Пищеварительная система |
| Репродуктивная система |
| Мочеиспускательная система |
| Эндокринная система |
| Развитие человека |
| Сердечно-сосудистая система |
В развитие нервной системы, или же нейронное развитие, или же развитие нервной системы, относится к процессам, которые создают, формируют и изменяют форму нервная система животных, с самых ранних стадий эмбриональное развитие к взрослой жизни. Область нейронного развития опирается на оба нейробиология и биология развития для описания и понимания клеточных и молекулярных механизмов развития сложных нервных систем. нематоды и плодовые мошки к млекопитающие.
Дефекты нервного развития могут привести к таким порокам развития, как: голопрозэнцефалия, и широкий выбор неврологические расстройства в том числе парез конечностей и паралич, нарушения равновесия и зрения, и припадки,[1] И в люди другие расстройства, такие как Синдром Ретта, Синдром Дауна и Интеллектуальная недееспособность.[2]
Обзор развития мозга позвоночных
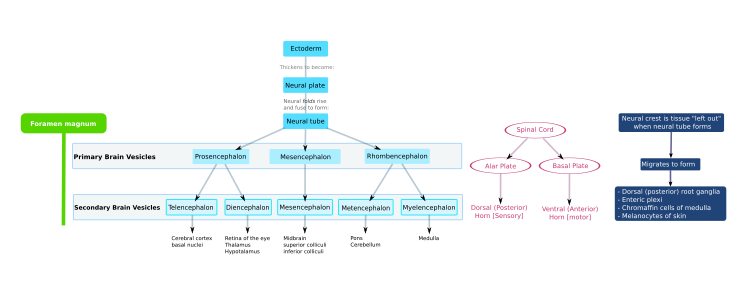
В позвоночное животное Центральная нервная система (CNS) происходит от эктодерма - самый внешний зародышевый лист эмбриона. Часть дорсальной эктодермы становится специфицированной нервной эктодермой - нейроэктодерма что формирует нервная пластинка по спинной стороне эмбриона.[3] Это часть раннего формирования паттерна эмбриона (включая эмбрион беспозвоночных), который также устанавливает передне-заднюю ось.[4] Нервная пластинка является источником большинства нейронов и глиальных клеток ЦНС. В нервная борозда формируется вдоль длинной оси нервной пластинки, и нервная пластинка складывается, давая начало нервная трубка.[5] Когда трубка закрыта с обоих концов, она заполнена эмбриональной спинномозговой жидкостью.[6] По мере развития эмбриона передняя часть нервной трубки расширяется и образует три первичные мозговые пузырьки, которые стали передний мозг (передний мозг ), средний мозг (средний мозг ), и задний мозг (ромбовидный мозг ). Эти простые, ранние пузырьки увеличиваются и далее делятся на конечный мозг (будущее кора головного мозга и базальный ганглий ), промежуточный мозг (будущее таламус и гипоталамус ), средний мозг (будущее колликулы ), мозговой мозг (будущее мосты и мозжечок ), и продолговатый мозг (будущее мозговое вещество ).[7] Центральная камера, заполненная спинномозговой жидкостью, проходит непрерывно от конечного мозга до центральный канал из спинной мозг, и представляет собой развивающийся желудочковая система ЦНС. Эмбриональный спинномозговая жидкость отличается от образовавшейся на более поздних стадиях развития и от спинномозговой жидкости взрослых; он влияет на поведение нейронных предшественников.[6] Поскольку нервная трубка дает начало головному и спинному мозгу, любые мутации на этом этапе развития могут привести к фатальным деформациям, таким как анэнцефалия или пожизненная инвалидность, например расщелина позвоночника. За это время стенки нервной трубки содержат нервные стволовые клетки, которые стимулируют рост мозга при многократном делении. Постепенно некоторые клетки перестают делиться и дифференцируются на нейроны и глиальные клетки, которые являются основными клеточными компонентами ЦНС. Вновь сгенерированные нейроны мигрировать в разные части развивающегося мозга, чтобы самоорганизоваться в разные мозговые структуры. Как только нейроны достигают своих региональных позиций, они расширяются. аксоны и дендриты, которые позволяют им общаться с другими нейронами через синапсы. Синаптическая связь между нейронами приводит к установлению функциональной нейронные цепи которые опосредуют сенсорную и моторную обработку и лежат в основе поведения.[8]
Аспекты
Некоторые ориентиры нейронного развития включают рождение и дифференциация из нейроны из стволовая клетка предшественники, миграция незрелых нейронов от мест их рождения в эмбрионе до их конечных положений, рост аксоны и дендриты от нейронов, руководство подвижного конус роста через эмбрион к постсинаптическим партнерам, поколение синапсы между этими аксонами и их постсинаптическими партнерами, и, наконец, пожизненное изменения в синапсах, которые, как считается, лежат в основе обучения и памяти.
Обычно эти процессы развития нервной системы можно разделить на два класса: независимые от активности механизмы и зависимые от активности механизмы. Обычно считается, что независимые от активности механизмы происходят как зашитые процессы, определяемые генетическими программами, исполняемыми внутри отдельных нейронов. К ним относятся дифференциация, миграция и управление аксоном к их первоначальным целевым областям. Эти процессы считаются независимыми от нервной активности и сенсорного опыта. Один раз аксоны достигают своих целевых областей, в игру вступают механизмы, зависящие от деятельности. Хотя образование синапсов не зависит от активности, модификация синапсов и устранение синапсов требует нейронной активности.
Нейробиология развития использует множество животные модели включая мышь Mus musculus плодовая муха Drosophila melanogaster, данио Данио Рерио, лягушка Xenopus laevis, а аскарида Caenorhabditis elegans.
Миелинизация, формирование липидно-миелиновой оболочки вокруг аксонов нейронов, является процессом, который необходим для нормальной функции мозга. Миелиновая оболочка обеспечивает изоляцию нервного импульса при коммуникации между нейронными системами. Без этого импульс был бы нарушен, и сигнал не достиг бы своей цели, что нарушило бы нормальное функционирование. Поскольку большая часть развития мозга происходит на пренатальной стадии и в младенчестве, крайне важно, чтобы миелинизация и развитие коры головного мозга происходили должным образом. Магнитно-резонансная томография (МРТ) - это неинвазивный метод, используемый для исследования миелинизации и созревания коры (кора - это внешний слой головного мозга, состоящий из серое вещество ). Вместо того, чтобы показывать реальный миелин, МРТ учитывает водную фракцию миелина, меру содержания миелина. Многокомпонентная релаксометрия (MCR) позволяет визуализировать и количественно оценить содержание миелина. MCR также полезен для отслеживания созревания белого вещества, которое играет важную роль в когнитивном развитии. Было обнаружено, что в младенчестве миелинизация происходит по типу задне-переднего отдела. Поскольку существует мало доказательств связи между миелинизацией и толщиной коры, было обнаружено, что толщина коры не зависит от белого вещества. Это позволяет различным аспектам мозга расти одновременно, что приводит к более полноценному развитию мозга.[9]
Нейронная индукция
В начале эмбриональное развитие позвоночного, дорсальная эктодерма становится специфицированной, чтобы дать начало эпидермис и нервная система; часть дорсальной эктодермы уточняется нервная эктодерма сформировать нервная пластинка что дает начало нервной системе.[3][10] Превращение недифференцированной эктодермы в нейроэктодерму требует сигналов от мезодерма. В начале гаструляции презумптивные мезодермальные клетки перемещаются через дорсальную губу бластопора и образуют слой мезодермы между ними. энтодерма и эктодерма. Мезодермальные клетки мигрируют по дорсальной средней линии, давая начало нотохорд что превращается в позвоночник. Нейроэктодерма, покрывающая хорду, развивается в нервную пластинку в ответ на диффузный сигнал, производимый хордой. Остальная часть эктодермы дает начало эпидермису. Способность мезодермы преобразовывать вышележащую эктодерму в нервную ткань называется нервная индукция.
У раннего эмбриона нервная пластинка складывается наружу, образуя нервная борозда. Начиная с области будущей шеи, нервные складки этой канавки близко, чтобы создать нервная трубка. Образование нервной трубки из эктодермы называется нейруляция. Брюшная часть нервной трубки называется базальная пластинка; спинная часть называется сигнальная пластина. Полый интерьер называется нервный канал, а открытые концы нервной трубки, называемые нейропорами, закрываются.[11]
Пересаженная губа бластопора может преобразовывать эктодерму в нервную ткань и, как говорят, обладает индуктивным эффектом. Нейронные индукторы - это молекулы, которые могут индуцировать экспрессию нервных генов в эктодерме. эксплантаты без индукции мезодермальных генов. Нейронную индукцию часто изучают в Xenopus эмбрионы, поскольку они имеют простой план тела и есть хорошие маркеры, позволяющие отличить нервную ткань от не нервной. Примерами нервных индукторов являются молекулы голова и хордин.
Когда эмбриональные эктодермальные клетки культивируются при низкой плотности в отсутствие мезодермальных клеток, они претерпевают нейральную дифференцировку (экспрессируют нервные гены), предполагая, что нейральная дифференцировка является судьбой эктодермальных клеток по умолчанию. В культуры эксплантатов (которые позволяют прямые межклеточные взаимодействия) одни и те же клетки дифференцируются в эпидермис. Это связано с действием BMP4 (а TGF-β семейный белок), который индуцирует дифференцировку эктодермальных культур в эпидермис. Во время нейральной индукции ноггин и хордин продуцируются дорсальной мезодермой (хордой) и диффундируют в вышележащую эктодерму, подавляя активность BMP4. Это ингибирование BMP4 заставляет клетки дифференцироваться в нервные клетки. Ингибирование передачи сигналов TGF-β и BMP (костный морфогенетический белок) может эффективно индуцировать нервную ткань из плюрипотентные стволовые клетки.[12]
Регионализация
На более поздней стадии развития верхняя часть нервной трубки изгибается на уровне будущего среднего мозга - средний мозг, в мезэнцефалическом изгибе или головной изгиб. Выше средний мозг это передний мозг (будущий передний мозг), а под ним - ромбовидный мозг (будущий задний мозг).
Крыловая пластинка переднего мозга расширяется, образуя конечный мозг что порождает полушария головного мозга, а его базальная пластина становится промежуточный мозг. В оптический пузырь (который в конечном итоге становится зрительным нервом, сетчаткой и радужной оболочкой) формируется на базальной пластинке переднего мозга.
Моделирование нервной системы
В хордовые, дорсальная эктодерма формирует всю нервную ткань и нервную систему. Узор происходит из-за специфических условий окружающей среды - разных концентраций сигнальных молекул
Дорсовентральная ось
Вентральная половина нервная пластинка контролируется нотохорд, который действует как «организатор». Спинная половина контролируется эктодерма пластина, которая образует обе стороны нервной пластинки.[13]
Эктодерма по умолчанию превращается в нервную ткань. Доказательства этого исходят от единичных культивируемых клеток эктодермы, которые продолжают формировать нервную ткань. Постулируется это из-за отсутствия БМП, которые заблокированы организатором. Организатор может производить такие молекулы, как фоллистатин, голова и хордин которые ингибируют BMP.
Вентральная нервная трубка имеет рисунок звуковой еж (Shh) от хорды, которая действует как индуцирующая ткань. Полученные из нотохорды сигналы Shh для плита пола, и вызывает выражение Shh на полу. Shh, происходящий из донной пластинки, впоследствии передает сигналы другим клеткам нервной трубки и важен для правильной спецификации доменов предшественников вентральных нейронов. Потеря Shh из хорды и / или пластинки дна препятствует правильной спецификации этих доменов-предшественников. Шш связывает Исправлено1, снимая патч-опосредованное ингибирование Сглаженный, что привело к активации семейства Gli факторы транскрипции (GLI1, GLI2, и GLI3 ).
В этом контексте Shh действует как морфоген - он вызывает дифференцировку клеток в зависимости от его концентрации. При низких концентрациях образует вентральную интернейроны, при более высоких концентрациях вызывает двигательный нейрон развития, и в самых высоких концентрациях он вызывает дифференциацию пластин пола. Отсутствие причин дифференцировки, модулируемой Shh голопрозэнцефалия.
Дорсальная нервная трубка формируется с помощью BMP из эпидермальной эктодермы, фланкирующей нервную пластинку. Они вызывают сенсорные интернейроны, активируя Sr / Thr киназы и изменение SMAD уровни фактора транскрипции.
Рострокаудальная (переднезадняя) ось
Сигналы, которые контролируют переднезаднее нервное развитие, включают: FGF и ретиноевая кислота, которые действуют на задний и спинной мозг.[14] Например, задний мозг формируется Hox-гены, которые экспрессируются в перекрывающихся доменах вдоль переднезадней оси под контролем ретиноевой кислоты. В 3′ (3 простых конца) гены в Hox-кластере индуцируются ретиноевой кислотой в заднем мозге, тогда как 5′ (5 простых концов) Hox-гены не индуцируются ретиноевой кислотой и экспрессируются более кзади в спинном мозге. Hoxb-1 выражается в ромбомере 4 и дает начало лицевой нерв. Без этого выражения Hoxb-1 нерв, похожий на тройничный нерв возникает.
Нейрогенез
Нейрогенез это процесс, при котором нейроны генерируются из нервные стволовые клетки и клетки-предшественники. Нейроны являются «постмитотическими», что означает, что они никогда больше не будут делиться на протяжении всей жизни организма.[8]
Эпигенетические модификации играют ключевую роль в регулировании экспрессия гена в различении нервные стволовые клетки и имеют решающее значение для определения судьбы клеток в мозге развивающихся и взрослых млекопитающих. Эпигенетические модификации включают: Метилирование цитозина ДНК формировать 5-метилцитозин и Деметилирование 5-метилцитозина.[15][16] Метилирование цитозина ДНК катализируется ДНК-метилтрансферазы (ДНМТ). Деметилирование метилцитозина катализируется в несколько последовательных стадий посредством Ферменты TET которые проводят окислительные реакции (например, 5-метилцитозин к 5-гидроксиметилцитозин ) и ферменты ДНК базовая эксцизионная пластика (BER) путь.[15]
Нейрональная миграция
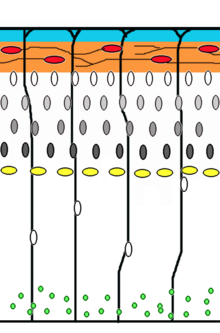
Нейронный миграция это метод, с помощью которого нейроны перемещаются от своего источника или места рождения к своему конечному положению в мозгу. Есть несколько способов сделать это, например путем радиальной миграции или тангенциальной миграции. Последовательности радиальной миграции (также известной как глиальное наведение) и транслокации сомов были захвачены покадровая микроскопия.[17]

Радиальная миграция
Клетки-предшественники нейронов пролиферируют в желудочковая зона развивающихся неокортекс, где основной нервной стволовой клеткой является радиальная глиальная клетка. Первый постмитотический клетки должны покинуть нишу стволовых клеток и мигрировать наружу, чтобы сформировать препланшет, которому суждено стать Клетки Кахаля-Ретциуса и плита нейроны. Эти клетки делают это путем транслокации сомов. Нейроны, мигрирующие с этим способом передвижения, биполярны и прикрепляют передний край процесса к пиа. В сома затем переносится на поверхность пиала нуклеокинез, процесс, посредством которого микротрубочка «клетка» вокруг ядра удлиняется и сжимается вместе с центросома чтобы направить ядро к его конечному пункту назначения.[18] Радиальные глиальные клетки волокна которого служат каркасом для мигрирующих клеток и средством радиальной коммуникации, опосредованной кальциевой динамической активностью,[19][20] действуют как основная возбуждающая нейрональная стволовая клетка коры головного мозга[21][22] или переместиться в кортикальную пластинку и дифференцироваться в астроциты или нейроны.[23] Сомальная транслокация может произойти в любой момент развития.[17]
Последующие волны нейронов расщепляют предварительную пластину, перемещаясь по ней. лучевая глия волокна для формирования корковой пластинки. Каждая волна мигрирующих клеток проходит мимо своих предшественников, образуя слои наизнанку, а это означает, что самые молодые нейроны находятся ближе всего к поверхности.[24][25] Подсчитано, что управляемая глиями миграция составляет 90% мигрирующих нейронов у человека и около 75% у грызунов.[26]
Тангенциальная миграция
Большинство интернейронов перемещаются по касательной через несколько способов миграции, чтобы достичь своего соответствующего местоположения в коре головного мозга. Примером тангенциальной миграции является перемещение интернейронов из ганглиозное возвышение к коре головного мозга. Одним из примеров продолжающейся тангенциальной миграции в зрелом организме, наблюдаемой у некоторых животных, является ростральный миграционный поток соединение субвентрикулярная зона и обонятельная луковица.
Аксофильная миграция
Многие нейроны, мигрирующие вдоль передне-задней оси тела, используют существующие аксон участки для миграции; это называется аксофильной миграцией. Пример этого режима миграции приведен в ГнРГ-экспрессирующие нейроны, которые проделывают долгий путь от места своего рождения через нос, через передний мозг и в гипоталамус.[27] Многие механизмы этой миграции были разработаны, начиная с внеклеточных ориентиров.[28] которые запускают внутриклеточную передачу сигналов. Эти внутриклеточные сигналы, такие как кальциевая сигнализация, привести к актин [29] и микротрубочка[30] цитоскелет динамики, которые производят клеточные силы, которые взаимодействуют с внеклеточной средой через белки клеточной адгезии [31] вызвать движение этих клеток.
Многополярная миграция
Существует также метод миграции нейронов, называемый многополярная миграция.[32][33] Это наблюдается в мультиполярных клетках, которые у человека в изобилии присутствуют в корковая промежуточная зона. Они не похожи на клетки, мигрирующие посредством локомоции или сомальной транслокации. Вместо этого эти мультиполярные клетки экспрессируют нейрональные маркеры и распространяют множество тонких отростков в различных направлениях независимо от радиальных глиальных волокон.[32]
Нейротрофические факторы
Выживание нейронов регулируется факторами выживания, называемыми трофическими факторами. Нейротрофическая гипотеза была сформулирована Виктором Гамбургером и Рита Леви Монтальчини на основе исследований развивающейся нервной системы. Виктор Гамбургер обнаружил, что имплантация дополнительной конечности развивающемуся цыпленку приводит к увеличению количества спинномозговых мотонейронов. Первоначально он думал, что дополнительная конечность вызывает пролиферацию двигательных нейронов, но позже он и его коллеги показали, что во время нормального развития наблюдается значительная гибель двигательных нейронов, а дополнительная конечность предотвращает гибель клеток. Согласно нейротрофической гипотезе, растущие аксоны конкурируют за ограниченное количество трофических факторов, производных от мишени, и аксоны, которые не получают достаточной трофической поддержки, погибают в результате апоптоза. Теперь ясно, что факторы, производимые рядом источников, способствуют выживанию нейронов.
- Фактор роста нервов (NGF): Рита Леви Монтальчини и Стэнли Коэн очистили первый трофический фактор, фактор роста нервов (NGF), за что они получили Нобелевскую премию. Существует три связанных с NGF трофических фактора: BDNF, NT3 и NT4, которые регулируют выживание различных популяций нейронов. Белки Trk действуют как рецепторы для NGF и родственных факторов. Trk - рецепторная тирозинкиназа. Димеризация и фосфорилирование Trk приводит к активации различных внутриклеточных сигнальных путей, включая пути киназы MAP, Akt и PKC.
- CNTF: ресничный нейротрофический фактор - еще один белок, который действует как фактор выживания мотонейронов. CNTF действует через рецепторный комплекс, который включает CNTFRα, GP130 и LIFRβ. Активация рецептора приводит к фосфорилированию и привлечению киназы JAK, которая, в свою очередь, фосфорилирует LIFR β. LIFRβ действует как стыковочный сайт для факторов транскрипции STAT. Киназа JAK фосфорилирует белки STAT, которые отделяются от рецептора и перемещаются в ядро для регулирования экспрессии генов.
- GDNF: нейротрофический фактор глиального происхождения является членом TGFb семейство белков и является мощным трофическим фактором для нейронов полосатого тела. Функциональный рецептор представляет собой гетеродимер, состоящий из рецепторов типа 1 и типа 2. Активация рецептора типа 1 приводит к фосфорилированию белков Smad, которые перемещаются в ядро для активации экспрессии генов.
Формирование синапсов
Нервно-мышечное соединение
Большая часть нашего понимания формирования синапсов происходит из исследований нервно-мышечного соединения. Передатчик в этом синапсе - ацетилхолин. Рецептор ацетилхолина (AchR) присутствует на поверхности мышечных клеток до образования синапсов. Прибытие нерва вызывает скопление рецепторов в синапсе. McMahan и Sanes показали, что синаптогенный сигнал концентрируется в базальная пластинка. Они также показали, что синаптогенный сигнал вырабатывается нервом, и определили этот фактор как Усмешка. Агрин индуцирует кластеризацию AchR на поверхности мышц, и образование синапсов нарушается у мышей с нокаутом агрина. Агрин передает сигнал через рецептор MuSK в рапсин. Фишбах и его коллеги показали, что субъединицы рецептора избирательно транскрибируются из ядер, расположенных рядом с синаптическим сайтом. Это опосредуется нейрегулином.
В зрелом синапсе каждое мышечное волокно иннервируется одним двигательным нейроном. Однако во время развития многие волокна иннервируются множеством аксонов. Лихтман и его коллеги изучили процесс удаления синапсов.[34] Это событие зависит от активности. Частичная блокада рецептора приводит к втягиванию соответствующих пресинаптических окончаний.
Синапсы ЦНС
Агрин, по-видимому, не является центральным медиатором образования синапсов в ЦНС, и существует активный интерес к идентификации сигналов, которые опосредуют синаптогенез в ЦНС. Нейроны в культуре развивают синапсы, подобные тем, которые образуются in vivo, что позволяет предположить, что синаптогенные сигналы могут правильно функционировать in vitro. Исследования синаптогенеза ЦНС сосредоточены в основном на глутаматергических синапсах. Эксперименты по визуализации показывают, что дендриты очень динамичны во время развития и часто инициируют контакт с аксонами. За этим следует привлечение постсинаптических белков к месту контакта. Стивен Смит и его коллеги показали, что контакт, инициированный дендритные филоподии могут развиваться в синапсы.
Индукция образования синапсов глиальными факторами: Баррес и его коллеги сделали наблюдение, что факторы в глиальных кондиционированных средах индуцируют образование синапсов в культурах ганглиозных клеток сетчатки. Формирование синапсов в ЦНС коррелирует с дифференцировкой астроцитов, предполагая, что астроциты могут обеспечивать синаптогенный фактор. Идентичность астроцитарных факторов пока неизвестна.
Нейролигины и SynCAM в качестве синаптогенных сигналов: Sudhof, Serafini, Scheiffele и др. показали, что нейролигины и SynCAM могут действовать как факторы, вызывающие пресинаптическую дифференцировку. Нейролигины концентрируются в постсинаптическом участке и действуют через нейрексины, сконцентрированные в пресинаптических аксонах. SynCAM - это молекула клеточной адгезии, которая присутствует как в пре-, так и в постсинаптических мембранах.
Зависимые от активности механизмы в сборке нейронных цепей
Процессы миграция нейронов, дифференциация и управление аксоном обычно считаются механизмами, независимыми от активности, и полагаются на жестко запрограммированные генетические программы в самих нейронах. Однако результаты исследований показали, что зависимые от активности механизмы в посредничестве некоторых аспектов этих процессов, таких как скорость миграции нейронов,[35] аспекты нейрональной дифференциации[36] и поиск пути аксонов.[37] Механизмы, зависящие от активности, влияют на развитие нейронных цепей и имеют решающее значение для построения ранних карт связности и постоянного уточнения синапсов, которое происходит во время развития.[38] В развивающихся цепях мы наблюдаем два различных типа нейронной активности - ранняя спонтанная активность и сенсорно-вызванная активность. Спонтанная активность возникает в начале нейронная цепь развитие даже при отсутствии сенсорного ввода и наблюдается во многих системах, таких как развивающаяся зрительная система,[39][40] слуховая система,[41][42] двигательная система,[43] гиппокамп,[44] мозжечок[45] и неокортекс.[46]
Экспериментальные методы, такие как прямая электрофизиологическая запись, флуоресцентная визуализация с использованием индикаторов кальция и оптогенетические методы, пролили свет на природу и функцию этих ранних всплесков активности.[47][48] У них есть четкие пространственные и временные модели во время развития.[49] и их устранение во время развития, как известно, приводит к дефициту уточнения сети в зрительной системе.[50] В незрелом сетчатка, волны спонтанных потенциалов действия возникают из ганглиозные клетки сетчатки и сканирование по поверхности сетчатки в первые несколько послеродовых недель.[51] Эти волны опосредуются нейротрансмиттер ацетилхолин на начальном этапе, а затем глутамат.[52] Считается, что они инструктируют формирование двух сенсорных карт - ретинотопный сегрегация по карте и глазам.[53] Уточнение ретинотопной карты происходит в нижележащих визуальных целях в головном мозге. верхний холмик (SC) и дорсальный латеральное коленчатое ядро (LGN).[54] Фармакологическое нарушение и мышиные модели, лишенные β2-субъединицы никотиновый ацетилхолиновый рецептор показал, что отсутствие спонтанной активности приводит к заметным дефектам в ретинотопия и специфическая для глаз сегрегация.[53]
В развивающихся слуховая система, развивающиеся улитка генерировать всплески активности, которые распространяются по всему внутренние волосковые клетки и спиральный узел нейроны, которые передают слуховую информацию в мозг.[55] АТФ высвобождение из поддерживающих клеток запускает потенциалы действия в внутренние волосковые клетки.[56] В слуховой системе считается, что спонтанная активность участвует в формировании тонотопической карты путем разделения аксонов кохлеарных нейронов, настроенных на высокие и низкие частоты.[55] В двигательной системе периодические всплески спонтанной активности вызываются возбуждающим действием. ГАМК и глутамат на ранних стадиях и ацетилхолин и глутамат на более поздних этапах.[57] В развивающихся данио спинной мозг ранняя спонтанная активность необходима для формирования все более синхронных чередующихся всплесков между ипсилатеральными и контралатеральными областями спинного мозга и для интеграции новых клеток в цепь.[58] в кора, ранние волны активности наблюдались в мозжечок и корковые срезы.[59] Как только сенсорный стимул становится доступным, окончательная тонкая настройка карт сенсорного кодирования и уточнение схемы начинают все больше и больше полагаться на сенсорно-вызванную активность, что продемонстрировано классическими экспериментами с эффектами сенсорной депривации во время критические периоды.[59]
Современный диффузионный вес МРТ методы могут также раскрыть макроскопический процесс развития аксонов. В коннектом может быть построен из диффузная МРТ данные: вершины графа соответствуют анатомически размеченным областям серого вещества, и две такие вершины, скажем, ты и v, соединены ребром, если трактография На этапе обработки данных обнаруживается аксональное волокно, которое соединяет две области, соответствующие ты и v.
Многочисленные брайнграфы, вычисленные из Проект Human Connectome можно скачать с http://braingraph.org сайт. Consensus Connectome Dynamics (CCD) - это замечательное явление, которое было обнаружено путем постоянного уменьшения минимального параметра достоверности в графическом интерфейсе Будапешт Справочный Коннектом Сервер.[60][61] Будапештский эталонный сервер Connectome (http://connectome.pitgroup.org ) изображает церебральные связи n = 418 испытуемых с частотным параметром k: для любого k = 1,2, ..., n можно просмотреть граф ребер, которые присутствуют как минимум в k коннектомах. Если параметр k уменьшается один за другим с k = n до k = 1, то в графе появляется все больше и больше ребер, так как условие включения ослабляется. Удивительное наблюдение заключается в том, что появление краев далеко не случайно: они напоминают растущую сложную структуру, такую как дерево или куст (визуализировано на анимации слева).
Предполагается, что [62] что растущая структура копирует аксональный развитие человеческого мозга: самые ранние развивающиеся связи (аксональные волокна) характерны для большинства субъектов, а развивающиеся впоследствии связи имеют все большую и большую дисперсию, потому что их вариации накапливаются в процессе развития аксонов.
Устранение синапсов
За каждое нервно-мышечное соединение соревнуются несколько мотонейронов, но доживает только один.[34] Соревнование in vitro Было показано, что в ней участвует ограниченное количество выделяемого нейротрофического вещества или что нервная активность дает преимущество сильным постсинаптическим связям, давая устойчивость к токсину, также высвобождающемуся при нервной стимуляции. В естественных условияхПредполагается, что мышечные волокна выбирают самый сильный нейрон посредством ретроградного сигнала.
Взрослый нейрогенез
Нейрогенез также встречается в определенных частях мозга взрослого человека.
Смотрите также
Рекомендации
- ^ «Неврологические признаки и болезни». 2 ноября 2016 г. Архивировано с оригинал на 2016-11-02. Получено 1 мая 2020.
- ^ "Дефекты нервной трубки". Получено 6 декабря 2011.
- ^ а б Гилберт, Скотт (2006). Биология развития (8-е изд.). Издательство Sinauer Associates. стр.373 –379. ISBN 9780878932504.
- ^ Вольперт, Льюис (2015). Принципы развития (Пятое изд.). С. 522–526. ISBN 9780199678143.
- ^ Саладин, Кеннет (2011). Анатомия и физиология Единство формы и функции. Нью-Йорк: Макгроу Хилл. п. 514. ISBN 9780073378251.
- ^ а б Гато, А; Алонсо, Мичиган; Martín, C .; и другие. (28 августа 2014 г.). «Эмбриональная спинномозговая жидкость в развитии мозга: контроль нервных предшественников». Хорватский медицинский журнал. 55 (4): 299–305. Дои:10.3325 / cmj.2014.55.299. ЧВК 4157377. PMID 25165044.
- ^ Гилберт, Скотт (2013). Биология развития (Десятое изд.). Sinauer Associates Inc. ISBN 978-1605351926.[страница нужна ]
- ^ а б Кандел, Эрик Р. (2006). Принципы нейронауки (5. изд.). Эпплтон и Ланге: Макгроу Хилл. ISBN 978-0071390118.[страница нужна ]
- ^ Croteau-Chonka, Elise C .; Дин, Дуглас К., III; Ремер, Джастин; Диркс, Холли; О'Мюрчартей, Джонатан; Деони, Шон К.Л. (15 октября 2015 г.). «Изучение взаимосвязи между созреванием коры и миелинизацией белого вещества в раннем детстве». NeuroImage. 125: 413–421. Дои:10.1016 / j.neuroimage.2015.10.038. ЧВК 4691410. PMID 26499814.

- ^ Вольперт, Льюис (2015). Принципы развития (Пятое изд.). п. 163. ISBN 9780199678143.
- ^ Estomih Mtui; Грегори Грюнер (2006). Клиническая нейроанатомия и неврология. Филадельфия: Сондерс. п. 1. ISBN 978-1-4160-3445-2.
- ^ Чемберс, С. М .; Fasano, C.A .; Papapetrou, E.P .; Tomishima, M .; Sadelain, M .; Студер, Л. (2009). «Высокоэффективное нейронное преобразование человеческих ES- и iPS-клеток путем двойного ингибирования передачи сигналов SMAD». Природа Биотехнологии. 27 (3): 275–280. Дои:10.1038 / nbt.1529. ЧВК 2756723. PMID 19252484.
- ^ Джесселл, Томас М .; Кандел, Эрик Р .; Шварц, Джеймс Х. (2000). «Глава 55». Принципы нейронауки (4-е изд.). Нью-Йорк: Макгроу-Хилл. ISBN 978-0838577011.
- ^ Дестер, Дж. (Сентябрь 2008 г.). «Синтез ретиноевой кислоты и передача сигналов во время раннего органогенеза». Клетка. 134 (6): 921–31. Дои:10.1016 / j.cell.2008.09.002. ЧВК 2632951. PMID 18805086.
- ^ а б Ван, Чжицинь; Тан, Бейша; Он, Юйцюань; Цзинь, Пэн (март 2016 г.). «Динамика метилирования ДНК в нейрогенезе». Эпигеномика. 8 (3): 401–414. Дои:10.2217 / epi.15.119. ЧВК 4864063. PMID 26950681.
- ^ Ноак, Флориан; Патаскар, Абхиджит; Шнайдер, Мартин; Бухгольц, Франк; Тивари, Виджай К.; Калегари, Федерико (27 февраля 2019 г.). «Оценка и сайт-специфическая манипуляция (гидрокси-) метилирования ДНК во время кортикогенеза мышей». Альянс наук о жизни. 2 (2): e201900331. Дои:10.26508 / lsa.201900331. ЧВК 6394126. PMID 30814272.
- ^ а б Надараджа Б., Брюнстрем Дж., Груцендлер Дж., Вонг Р., Перлман А. (2001). «Два режима радиальной миграции в раннем развитии коры головного мозга». Nat Neurosci. 4 (2): 143–50. Дои:10.1038/83967. PMID 11175874.
- ^ Сэмюэлс Б., Цай Л. (2004). «Нуклеокинез освещенный». Nat Neurosci. 7 (11): 1169–70. Дои:10.1038 / нн1104-1169. PMID 15508010.
- ^ Ракич, П. (май 1972 г.). «Способ миграции клеток к поверхностным слоям неокортекса эмбриона обезьяны». Журнал сравнительной неврологии. 145 (1): 61–83. Дои:10.1002 / cne.901450105. PMID 4624784.
- ^ Сыпь, БГ; Акман, JB; Ракич, П. (февраль 2016 г.). «Двунаправленная радиальная активность Са (2+) регулирует нейрогенез и миграцию во время раннего формирования кортикального столба». Достижения науки. 2 (2): e1501733. Bibcode:2016SciA .... 2E1733R. Дои:10.1126 / sciadv.1501733. ЧВК 4771444. PMID 26933693.
- ^ Noctor, SC; Флинт, AC; Weissman, TA; Даммерман, RS; Кригштейн, АР (8 февраля 2001 г.). «Нейроны, происходящие из радиальных глиальных клеток, устанавливают радиальные единицы в неокортексе». Природа. 409 (6821): 714–20. Bibcode:2001Натура.409..714Н. Дои:10.1038/35055553. PMID 11217860.
- ^ Тамамаки Н., Накамура К., Окамото К., Канеко Т. (сентябрь 2001 г.). «Радиальная глия является предшественником нейронов неокортекса в развивающейся коре головного мозга». Neurosci. Res. 41 (1): 51–60. Дои:10.1016 / S0168-0102 (01) 00259-0. PMID 11535293.
- ^ Мията Т., Кавагути А., Окано Х., Огава М. (сентябрь 2001 г.). «Асимметричное наследование радиальных глиальных волокон корковыми нейронами». Нейрон. 31 (5): 727–41. Дои:10.1016 / S0896-6273 (01) 00420-2. PMID 11567613.
- ^ Надараджа Б., Парнавелас Дж. (2002). «Способы миграции нейронов в развивающейся коре головного мозга». Обзоры природы Неврология. 3 (6): 423–32. Дои:10.1038 / nrn845. PMID 12042877.
- ^ Ракич П. (1972). «Способ миграции клеток к поверхностным слоям неокортекса эмбриона обезьяны». Журнал сравнительной неврологии. 145 (1): 61–83. Дои:10.1002 / cne.901450105. PMID 4624784.
- ^ Летинич К., Зонджу Р., Ракич П. (июнь 2002 г.). «Происхождение ГАМКергических нейронов в неокортексе человека». Природа. 417 (6889): 645–9. Bibcode:2002Натурал.417..645Л. Дои:10.1038 / природа00779. PMID 12050665.
- ^ Рэй S (2010). «Из носа в мозг: развитие нейронов гонадотропин-рилизинг-гормона-1». Журнал нейроэндокринологии. 22 (7): 743–753. Дои:10.1111 / j.1365-2826.2010.02034.x. ЧВК 2919238. PMID 20646175.
- ^ Джакобини П., Мессина А., Рэй С., Джампьетро С., Крепальди Т., Кармелье П., Фасоло А. (2007). «Фактор роста гепатоцитов действует как мотор и направляющий сигнал для миграции нейронов гонадотропинового гормона-рилизинг-гормона-1» (PDF). Журнал неврологии. 27 (2): 431–445. Дои:10.1523 / JNEUROSCI.4979-06.2007. ЧВК 6672060. PMID 17215404.
- ^ Хатчинс Б.И., Кленке Ю., Рэй С. (2013). «Зависимый от высвобождения кальция поток актина в ведущем процессе опосредует миграцию аксофилов». Журнал неврологии. 33 (28): 11361–71. Дои:10.1523 / JNEUROSCI.3758-12.2013. ЧВК 3724331. PMID 23843509.
- ^ Хатчинс, Б. Ян; Рэй, Сьюзен (2014). «Захват плюсовых концов микротрубочек актиновой корой способствует миграции аксофильных нейронов за счет увеличения натяжения микротрубочек в ведущем процессе». Границы клеточной неврологии. 8: 400. Дои:10.3389 / fncel.2014.00400. ЧВК 4245908. PMID 25505874.
- ^ Паркаш Дж, Чимино I, Феррарис Н, Касони Ф, Рэй С, Кэппи Х, Превот В, Джакобини П (2012). «Подавление β1-интегрина в клетках гонадотропин-рилизинг-гормона нарушает миграцию и удлинение аксонов, что приводит к серьезным репродуктивным изменениям». Журнал неврологии. 32 (47): 16992–7002. Дои:10.1523 / JNEUROSCI.3057-12.2012. ЧВК 5238668. PMID 23175850.
- ^ а б Табата Х., Накадзима К. (5 ноября 2003 г.). «Мультиполярная миграция: третий способ миграции радиальных нейронов в развивающейся коре головного мозга». Журнал неврологии. 23 (31): 9996–10001. Дои:10.1523 / JNEUROSCI.23-31-09996.2003. ЧВК 6740853. PMID 14602813.
- ^ Надараджа Б., Алифрагис П., Вонг Р., Парнавелас Дж. (2003). «Миграция нейронов в развивающейся коре головного мозга: наблюдения на основе изображений в реальном времени». Кора головного мозга. 13 (6): 607–11. Дои:10.1093 / cercor / 13.6.607. PMID 12764035.
- ^ а б Терни, Стивен Дж .; Lichtman, Jeff W .; Харрис, Уильям А. (26 июня 2012 г.). «Изменение результатов устранения синапсов при развитии нервно-мышечных соединений in vivo: доказательства синаптической конкуренции и ее механизма». PLOS Биология. 10 (6): e1001352. Дои:10.1371 / journal.pbio.1001352. ЧВК 3383738. PMID 22745601.
- ^ Комуро, Хитоши; Ракич, Пасько (август 1996 г.). «Внутриклеточные колебания Ca2 + модулируют скорость миграции нейронов». Нейрон. 17 (2): 275–285. Дои:10.1016 / s0896-6273 (00) 80159-2. PMID 8780651.
- ^ Гу, Х; Олсон, E.C; Спитцер, Северная Каролина (1994). «Спонтанные выбросы и волны кальция в нейронах во время ранней дифференцировки». Журнал неврологии. 14 (11): 6325–35. Дои:10.1523 / JNEUROSCI.14-11-06325.1994.
- ^ Hanson, M.G; Милнер, Л.Д .; Ландмессер, Л.Т. (2008). «Спонтанная ранняя активность в спинном мозге цыплят влияет на решения о поиске пути моторных аксонов». Brain Res. Rev. 57 (1): 77–85. Дои:10.1016 / j.brainresrev.2007.06.021. ЧВК 2233604. PMID 17920131.
- ^ Киркби, Л.А.; Sack, G.S; Фирл, А; Феллер, М.Б. (4 декабря 2013 г.). «Роль коррелированной спонтанной активности в сборке нейронных цепей». Нейрон. 80 (5): 1129–44. Дои:10.1016 / j.neuron.2013.10.030. ЧВК 4560201. PMID 24314725.
- ^ Хуберман, А.Д. (2007). «Механизмы развития глазных зрительных цепей». Текущее мнение в нейробиологии. 17 (1): 73–80. Дои:10.1016 / j.conb.2007.01.005. PMID 17254766.
- ^ Мейстер, М; Wong, R.O.L; Бейлор, Д.А.; Шац, К.Дж. (1991). «Синхронные всплески потенциалов действия в ганглиозных клетках развивающейся сетчатки». Наука. 252 (5008): 939–43. Bibcode:1991Научный ... 252..939М. Дои:10.1126 / science.2035024. PMID 2035024.
- ^ Липпе, W.R (1994). «Ритмичная спонтанная активность в развивающейся слуховой системе птиц». Журнал неврологии. 14 (3): 1486–95. Дои:10.1523 / JNEUROSCI.14-03-01486.1994.
- ^ Джонс, Т.А.; Джонс, S.M; Паггетт, К.С. (15 октября 2001 г.). «Изначальный ритмический взрыв в эмбриональных ганглиозных клетках улитки». Журнал неврологии. 21 (20): 8129–35. Дои:10.1523 / JNEUROSCI.21-20-08129.2001. ЧВК 6763868. PMID 11588185.
- ^ О'Донован, М.Дж. (1999). «Происхождение спонтанной активности в развивающихся сетях нервной системы позвоночных». Текущее мнение в нейробиологии. 9 (1): 94–104. Дои:10.1016 / s0959-4388 (99) 80012-9. PMID 10072366.
- ^ Крепель, V; Аронов Д; Хоркера, я; Represa, A; Бен-Ари, Й; Коссарт, Р. (2007). «Связанный с родами несинаптический когерентный паттерн активности в развивающемся гиппокампе». Нейрон. 54 (1): 105–120. Дои:10.1016 / j.neuron.2007.03.007. PMID 17408581.
- ^ Ватт, А.Дж .; Cuntz, H; Мори, М; Нуссер, Z; Sjostrom, P.J; Хауссер, М (2009). «Бегущие волны в развивающейся коре мозжечка, опосредованные асимметричным соединением клеток Пуркинье». Природа Неврологии. 12 (4): 463–73. Дои:10.1038 / №2285. ЧВК 2912499. PMID 19287389.
- ^ Корлью, Ревекка; Bosma, Martha M .; Муди, Уильям Дж. (Октябрь 2004 г.). «Спонтанная синхронная электрическая активность корковых нейронов новорожденных мышей». Журнал физиологии. 560 (2): 377–390. Дои:10.1113 / jphysiol.2004.071621. ЧВК 1665264. PMID 15297578.
- ^ Феллер, Марла Б. (апрель 1999 г.). «Спонтанная коррелированная активность в развивающихся нервных цепях». Нейрон. 22 (4): 653–656. Дои:10.1016 / s0896-6273 (00) 80724-2. PMID 10230785.
- ^ О'Донован, Майкл Дж .; Чуб Николай; Веннер, Питер (октябрь 1998 г.). «Механизмы спонтанной активности в развитии спинномозговых сетей». Журнал нейробиологии. 37 (1): 131–145. Дои:10.1002 / (sici) 1097-4695 (199810) 37: 1 <131 :: aid-neu10> 3.0.co; 2-h. PMID 9777737.
- ^ Стаффорд, Бен К .; Шер, Александр; Литке, Алан М .; Фельдхейм, Дэвид А. (октябрь 2009 г.). «Пространственно-временные паттерны волн сетчатки, лежащие в основе зависимого от активности уточнения ретинофугальных проекций». Нейрон. 64 (2): 200–212. Дои:10.1016 / j.neuron.2009.09.021. ЧВК 2771121. PMID 19874788.
- ^ Торборг, Кристина Л .; Феллер, Марла Б. (июль 2005 г.). «Спонтанная узорчатая активность сетчатки и уточнение проекций сетчатки». Прогресс в нейробиологии. 76 (4): 213–235. Дои:10.1016 / j.pneurobio.2005.09.002. PMID 16280194.
- ^ Галли, L; Маффеи, Л. (7 октября 1988 г.). «Спонтанная импульсная активность ганглиозных клеток сетчатки крыс в пренатальной жизни». Наука. 242 (4875): 90–91. Bibcode:1988Научный ... 242 ... 90Г. Дои:10.1126 / science.3175637. PMID 3175637.
- ^ Форд, Кевин Дж .; Феллер, Марла Б. (26 июля 2011 г.). «Сборка и разборка холинергической сети сетчатки». Визуальная неврология. 29 (1): 61–71. Дои:10.1017 / S0952523811000216. ЧВК 3982217. PMID 21787461.
- ^ а б Киркби, Лоури А .; Sack, Georgeann S .; Фирл, Алана; Феллер, Марла Б. (декабрь 2013 г.). «Роль коррелированной спонтанной активности в сборке нейронных цепей». Нейрон. 80 (5): 1129–1144. Дои:10.1016 / j.neuron.2013.10.030. ЧВК 4560201. PMID 24314725.
- ^ Акман, Джеймс Б.; Бербридж, Тимоти Дж .; Крейр, Майкл С. (10 октября 2012 г.). «Волны сетчатки координируют структурированную активность всей развивающейся зрительной системы». Природа. 490 (7419): 219–225. Bibcode:2012Натура.490..219A. Дои:10.1038 / природа11529. ЧВК 3962269. PMID 23060192.
- ^ а б Кандлер, Карл; Клаус, Аманда; Но, Джихён (10 мая 2009 г.). «Тонотопическая реорганизация развивающихся слуховых контуров ствола мозга». Природа Неврологии. 12 (6): 711–717. Дои:10.1038 / номер 2332. ЧВК 2780022. PMID 19471270.
- ^ Тритч, Николас X; Родригес-Контрерас, Адриан; Кринс, Том Т. Н; Ван, Хан Чин; Борст, Дж. Джерард Дж. Берглес, Дуайт Э. (1 августа 2010 г.). «Потенциалы действия кальция в волосковых клетках определяют активность слуховых нейронов до появления слуха». Природа Неврологии. 13 (9): 1050–1052. Дои:10.1038 / №2604. ЧВК 2928883. PMID 20676105.
- ^ Момосе-Сато, Йоко; Сато, Кацусигэ (2013). «Масштабная синхронизированная деятельность в стволе мозга и спинном мозге эмбриона». Границы клеточной неврологии. 7: 36. Дои:10.3389 / fncel.2013.00036. ЧВК 3625830. PMID 23596392.
- ^ Деформация, Эрика; Агарвал, Гаутам; Вайарт, Клэр; Фридманн, Дрю; Oldfield, Claire S .; Коннер, Олден; Дель Бене, Филиппо; Arrenberg, Aristides B .; Байер, Хервиг; Исаков, Эхуд Ю. (январь 2012 г.). «Появление паттерновой активности в развивающемся спинном мозге рыбок данио». Текущая биология. 22 (2): 93–102. Дои:10.1016 / j.cub.2011.12.002. ЧВК 3267884. PMID 22197243.
- ^ а б Санес, Дэн; Рех, Томас; Харрис, Уильям. Развитие нервной системы (Третье изд.). Эльзевир.[страница нужна ]
- ^ Салкаи, Балаж; Керепеси, Чаба; Варга, Балинт; Гролмуш, Винс (май 2015 г.). "Будапештский эталонный сервер Connectome v2.0". Письма о неврологии. 595: 60–62. arXiv:1412.3151. Дои:10.1016 / j.neulet.2015.03.071. PMID 25862487.
- ^ Салкаи, Балаж; Керепеси, Чаба; Варга, Балинт; Гролмуш, Винс (15 сентября 2016 г.). «Параметризуемые консенсусные коннектомы из проекта Human Connectome: Будапештский эталонный сервер коннектома v3.0». Когнитивная нейродинамика. 11 (1): 113–116. arXiv:1602.04776. Дои:10.1007 / s11571-016-9407-z. ЧВК 5264751. PMID 28174617.
- ^ Керепеси, Чаба; Салкаи, Балаж; Варга, Балинт; Гролмуш, Винс; Ши, Юнтан (30 июня 2016 г.). «Как направить границы коннектомов: динамика консенсусных коннектомов и развитие связей в человеческом мозгу». PLOS ONE. 11 (6): e0158680. arXiv:1509.05703. Bibcode:2016PLoSO..1158680K. Дои:10.1371 / journal.pone.0158680. ЧВК 4928947. PMID 27362431.
внешняя ссылка
| Библиотечные ресурсы около Развитие нервной системы |
- Нейронное развитие (рецензируемый журнал открытого доступа).
- Перенос времени нейроразвития у видов млекопитающих
- Развивающийся мозг ребенка
- Развитие мозга
- Как бедность может изменить мозг
- Подростковый мозг


