Синдром аспирации мекония - Meconium aspiration syndrome
| Синдром аспирации мекония | |
|---|---|
| Другие имена | Неонатальная аспирация мекония |
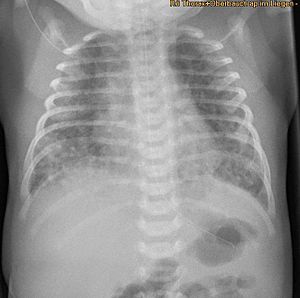 | |
| Рентгеновский снимок, показывающий степень повреждения эпителия легких в ответ на меконий у новорожденных с синдромом аспирации мекония. | |
| Специальность | Неонатология |
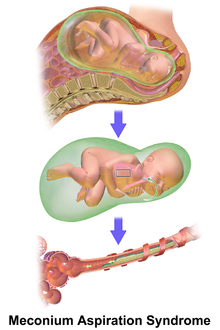
Синдром аспирации мекония (МАС) также известный как неонатальная аспирация мекония заболевание новорожденных. В нем описывается спектр заболеваний и патофизиология новорожденных, рожденных в околоплодных водах, окрашенных меконием (MSAF) и имеющих меконий в их легких. Таким образом, MAS имеет широкий диапазон степени тяжести в зависимости от того, какие состояния и осложнения развиваются после родов. Более того, патофизиология MAS многофакторна и чрезвычайно сложна, поэтому она является ведущей причиной заболеваемости и смертности доношенных детей.[1][2]
Слово меконий происходит от греческого слова mēkōnion смысл сок из опийного мака поскольку седативный эффект, который он оказывает на плод, наблюдался Аристотель.[3]
Меконий - липкое вещество темно-зеленого цвета, содержащее желудочно-кишечные выделения, амниотическая жидкость, желчные кислоты, желчь, кровь, слизь, холестерин, панкреатический секрет, лануго, верникс казеоза и клеточный мусор.[1] Меконий накапливается в плоде желудочно-кишечный тракт на протяжении третьего триместра беременности, и это первые выделения из кишечника в течение первых 48 часов после родов.[4] Примечательно, что поскольку меконий и все содержимое желудочно-кишечного тракта расположены «экстракорпорально», его составляющие скрыты и обычно не распознаются иммунной системой плода.[5]
Чтобы меконий в околоплодных водах мог успешно вызвать МАС, он должен попасть в дыхательная система в период, когда наполненные жидкостью легкие переходят в наполненный воздухом орган, способный к газообмен.[1]
Причины
Основные теории перехода мекония в околоплодные воды вызваны зрелостью плода или стрессом плода в результате гипоксия или инфекция.[3] Другие факторы, способствующие прохождению мекония в утробе включают плацентарную недостаточность, материнскую гипертензию, преэклампсия и употребление наркотиков матери табак и кокаин.[6] Однако точный механизм перехода мекония в околоплодные воды до конца не изучен, и это может быть комбинация нескольких факторов.
Переход мекония в результате дистресса плода
Может быть важная связь между дистрессом плода и гипоксия с MSAF.[2] Считается, что дистресс плода перерастает в гипоксию плода, заставляя плод испражняться меконием, что приводит к MSAF, а затем, возможно, к MAS.[6] Другие факторы стресса, вызывающие дистресс плода и, следовательно, переход мекония, включают, когда насыщение кислородом пупочной вены ниже 30%.[3]
Гипоксический стресс плода во время родов может стимулировать активность толстой кишки за счет усиления кишечной перистальтика и расслабление анального сфинктера, что приводит к выходу мекония. Затем из-за внутриматочного вдоха или из-за первых нескольких вдохов после родов может развиться МАС. Кроме того, аспирация густого мекония приводит к обструкции дыхательных путей, что приводит к более тяжелому гипоксия.[6][7]
Важно отметить, что связь между патологическим состоянием плода и пассажем мекония не является определенной причинно-следственной связью, поскольку более четверти детей с MSAF активны при рождении и не имеют дистресса или гипоксии.[2] Кроме того, дистресс плода часто возникает без прохождения мекония.[3]
Переход мекония в результате созревания плода
Хотя меконий присутствует в желудочно-кишечный тракт на ранней стадии развития MSAF редко возникает раньше 34 недель. беременность.[3]
Перистальтика кишечника плода присутствует уже на 8 неделе беременности, а анальный сфинктер развивается примерно на 20–22 неделе. Ранние механизмы контроля анального сфинктера изучены недостаточно, однако есть свидетельства того, что плод регулярно испражняется в амниотическая полость даже при отсутствии бедствия. Присутствие кишечных ферментов плода было обнаружено в околоплодных водах у женщин на сроке беременности 14–22 недели. Таким образом, предполагается, что кишечное содержимое свободно попадает в амниотическую жидкость.[8]
Мотилин обнаруживается в более высоких концентрациях в желудочно-кишечном тракте плода после родов, чем у плода. Аналогичным образом кишечная парасимпатическая иннервация и миелинизация также увеличивается на более поздних сроках беременности. Следовательно, повышенная частота MAS при переношенных беременностях может отражать созревание и развитие перистальтики желудочно-кишечного тракта у новорожденного.[3]
Патофизиология
Поскольку MAS описывает спектр заболеваний у новорожденных, рожденных через MSAF, без каких-либо врожденных респираторных нарушений или другой основной патологии, существует множество предполагаемых механизмов и причин возникновения этого синдрома. Эти расстройства могут иметь долгосрочные последствия, например, у младенцев, у которых развивается МАС, более высокая частота развития дефектов нервного развития из-за плохого дыхания.[9]
Обструкция дыхательных путей
В первые 15 минут аспирации мекония наблюдается обструкция более крупных дыхательных путей, что вызывает повышение сопротивления легких, снижение податливость легких, острый гипоксемия, гиперкапния, ателектаз и респираторный ацидоз. После 60 минут воздействия меконий попадает в более мелкие дыхательные пути. Попадая в конечные бронхиолы и альвеолы, меконий вызывает воспаление, отек легких, вазоконстрикция, бронхоспазм, коллапс дыхательных путей и инактивация поверхностно-активное вещество[10][11].
Гипоксия плода
Области легких, которые не участвуют или участвуют лишь частично вентиляция из-за закупорки и / или разрушения станет гипоксическим, что может привести к воспалительной реакции. Частичное препятствие приведет к захвату воздуха и гиперинфляция определенных участков легких и пневмоторакс может последовать. Хроническая гипоксия приводит к повышению тонуса гладких мышц легочных сосудов и стойкая легочная гипертензия вызывая нарушение дыхания и кровообращения.[1]
Инфекционное заболевание
Микроорганизмы, чаще всего Грамотрицательный стержни и эндотоксины обнаруживаются в образцах MSAF чаще, чем в прозрачных околоплодных водах, например, у 46,9% пациентов с MSAF также присутствовали эндотоксины. Микробная инвазия в амниотическую полость (MIAC) чаще встречается у пациентов с MSAF, что в конечном итоге может привести к внутриамниотической воспалительной реакции. MIAC связан с высокими концентрациями цитокины (Такие как Ил-6 ), хемокины (Такие как Ил-8 и хемоаттрактантный белок-1 моноцитов ), дополнять, фосфолипаза А2 и ферменты, разрушающие матрицу. Следовательно, эти вышеупомянутые медиаторы в амниотической жидкости во время MIAC и внутриамниотической инфекции могут при аспирации в матка, вызывают воспаление легких у плода.[12]
Легочное воспаление
Меконий имеет сложный химический состав, поэтому сложно выделить один агент, ответственный за несколько возникающих заболеваний. Поскольку меконий хранится внутри кишечник, и частично не подвергается воздействию иммунная система, когда он становится аспирированным, врожденная иммунная система признает инородное и опасное вещество. Иммунная система, которая присутствует при рождении, реагирует в течение нескольких минут с низкой специфичностью и отсутствием памяти, чтобы попытаться устранить микробы. Меконий, возможно, приводит к химический пневмонит так как это мощный активатор медиаторов воспаления, которые включают цитокины, дополнять, простагландины и активные формы кислорода.[5]
Меконий является источником провоспалительных цитокины, включая фактор некроза опухоли (TNF) и интерлейкины (Ил-1, Ил-6, Ил-8 ), и медиаторов, производимых нейтрофилы, макрофаги и эпителиальные клетки, которые могут прямо или косвенно повредить легочную ткань. Например, протеолитические ферменты высвобождаются из нейтрофильных гранул, и они могут повредить легочную мембрану и сурфактантные белки. Дополнительно активирован лейкоциты и цитокины производят реактивный азот и формы кислорода который имеет цитотоксический последствия. Окислительный стресс приводит к вазоконстрикция, бронхоспазм, Скопление тромбоцитов и ускоренная сотовая апоптоз.[11] Недавно была выдвинута гипотеза, что меконий является мощным активатором толл-подобный рецептор (TLR) и дополнять, ключевые медиаторы воспаления и, таким образом, могут способствовать воспалительной реакции при МАС.[1][5]
Меконий содержит большое количество фосфолипаза А2 (PLA2), мощный провоспалительный фермент, который может напрямую (или посредством стимуляции арахидоновая кислота ) приводят к дисфункции сурфактанта, разрушению эпителия легких, тканей некроз и увеличение апоптоз.[1][11] Меконий также может активировать каскад коагуляции, изготовление фактор активации тромбоцитов (PAF) и другие вазоактивные вещества, которые могут привести к разрушению капилляров. эндотелий и подвальные мембраны. Повреждение альвеолокапиллярной мембраны приводит к утечке жидкости, белков плазмы и клеток в интерстиций и альвеолярный пробелы[11].
Инактивация поверхностно-активного вещества
Поверхностно-активное вещество синтезируется альвеолярные клетки II типа и состоит из комплекса фосфолипиды, белки и сахариды. Он функционирует для снижения поверхностное натяжение (чтобы облегчить расширение легких во время вдохновение ), стабилизировать альвеолы в конце истечение срока (для предотвращения коллапса альвеол) и предотвращает легкое отек. Поверхностно-активное вещество также способствует защите и защите легких, так как оно также является противовоспалительным средством. Поверхностно-активное вещество улучшает удаление вдыхаемых частиц и дряхлый клетки далеко от альвеолярной структуры.[13]
Степень ингибирования поверхностно-активного вещества зависит как от концентрации поверхностно-активного вещества, так и от концентрации мекония. Если концентрация поверхностно-активного вещества низкая, даже очень сильно разбавленный меконий может ингибировать функцию поверхностно-активного вещества, тогда как при высоких концентрациях поверхностно-активного вещества действие мекония ограничено. Меконий может влиять на механизмы сурфактанта, предотвращая распространение сурфактанта по альвеолярной поверхности, уменьшая концентрацию сурфактантных белков (СПА и СП-Б ), а также изменением вязкости и структуры ПАВ.[10] После воздействия мекония происходит несколько морфологических изменений, наиболее заметным из которых является отслоение эпителия дыхательных путей от строма и сброс эпителиальные клетки в дыхательные пути. Это указывает на прямое пагубное воздействие на альвеолярные клетки легких из-за попадания мекония в легкие.[1]
Стойкая легочная гипертензия
Стойкая легочная гипертензия (PPHN) - это неспособность кровообращения плода адаптироваться к внематочным условиям после рождения. PPHN ассоциируется с различными респираторными заболеваниями, включая MAS (поскольку у 15-20% младенцев с MAS развивается PPHN), но также пневмония и сепсис. Сочетание гипоксия, легочный вазоконстрикция и вентиляция /перфузия несоответствие может вызвать PPHN, в зависимости от концентрации мекония в дыхательные пути.[14][7] PPHN у новорожденных является ведущей причиной смерти при МАС.[5]
Апоптоз
Апоптоз является важным механизмом удаления поврежденных клеток и восстановления тканей, однако слишком сильный апоптоз может причинить вред, например, острое повреждение легких. Меконий вызывает апоптоз и ДНК расщепление эпителиальных клеток дыхательных путей легких, это обнаруживается по присутствию фрагментированной ДНК в дыхательных путях и в ядрах альвеолярного эпителия. Меконий вызывает воспалительную реакцию в легких, так как увеличивается аутофагоцитарный ячеек и уровней каспаза 3 после контакта. После 8 часов воздействия мекония у плодов кроликов общее количество апоптотических клеток составляет 54%.[15] Следовательно, большая часть повреждений легких, вызванных меконием, может быть вызвана апоптозом эпителия легких.[1]
Диагностика
Дыхательной недостаточности у ребенка, родившегося в результате темного окраса MSAF, а также мекония, закупоривающего дыхательные пути, обычно достаточно для диагностики MAS. Кроме того, у новорожденных с МАС могут быть другие типы респираторного дистресса, такие как тахипноэ и гиперкапния. Иногда сложно диагностировать МАС, поскольку его можно спутать с другими заболеваниями, которые также вызывают респираторный дистресс, например: пневмония. Кроме того, рентген и УЗИ легких могут быть быстрыми, простыми и дешевыми методами визуализации для диагностики заболеваний легких, таких как MAS.[16]
Профилактика
В целом, заболеваемость MAS значительно снизилась за последние два десятилетия, поскольку количество послеродовых родов сведено к минимуму. В настоящее время индуцируют роды у женщин, срок беременности которых превышает 41 неделю.[17]
Профилактика при беременности
Профилактика во время беременности может включать амниоинфузию и антибиотики, но эффективность этих методов лечения сомнительна.[2]
Профилактика во время родов
Как упоминалось ранее, ротоглоточный и носоглоточный отсасывание не является идеальным профилактическим лечением как для энергичных, так и для детей с депрессией (не дышащих).[2]
Уход
Большинство младенцев, рожденных в результате MSAF, не нуждаются в каком-либо лечении (кроме планового послеродового ухода), поскольку у них нет признаков респираторного дистресса, поскольку только примерно у 5% младенцев, рожденных в результате MSAF, развивается MAS.[1] Тем не менее, младенцы, у которых действительно развивается МАС, должны быть помещены в неонатальное отделение, где за ними будут внимательно наблюдать и предоставлять любое необходимое лечение. Наблюдения включают мониторинг частота сердцебиения, частота дыхания, насыщение кислородом и глюкоза в крови (чтобы обнаружить ухудшение респираторный ацидоз или развитие гипогликемия ).[18] В целом, лечение МАС носит более поддерживающий характер.
Техники вспомогательной вентиляции легких
Очистить дыхательные пути от мекония, трахея однако можно использовать отсасывание, эффективность этого метода под вопросом, и он может причинить вред.[19]
В случае MAS существует потребность в дополнительном кислороде в течение как минимум 12 часов, чтобы поддерживать кислородное насыщение гемоглобина на уровне 92% или более. Тяжесть респираторного дистресс-синдрома может значительно различаться у новорожденных с МАС, поскольку некоторым из них требуется минимальная потребность в дополнительном кислороде или вообще не требуется, а в тяжелых случаях может потребоваться искусственная вентиляция легких.[20][2] Желаемое насыщение кислородом составляет от 90-95% до PaO2 может достигать 90 мм рт.[17] В случаях, когда глубоко в легких находится густой меконий, механическая вентиляция может потребоваться. В крайних случаях экстракорпоральная мембранная оксигенация (ЭКМО) может использоваться у младенцев, которые не реагируют на вентиляционную терапию.[2] Находясь на ЭКМО, организм может успеть усвоить меконий и разрешить все связанные с этим расстройства. Это лечение было отличным ответом, поскольку выживаемость MAS при ЭКМО составляет более 94%.[21]
Вентиляция младенцев с MAS может быть сложной задачей, и, поскольку MAS может влиять на каждого человека по-разному, может потребоваться индивидуальная процедура вентиляции. У некоторых новорожденных с MAS могут быть однородные изменения в легких, а у других - непостоянные и неоднородные изменения в легких. Обычно седативные препараты и миорелаксанты используются для оптимизации вентиляции и минимизации риска пневмоторакс связано с диссинхронным дыханием.[18]
Вдыхаемый оксид азота
Вдохнул оксид азота (iNO) действует на гладкие мышцы сосудов вызывая селективный легочный расширение сосудов. Это идеально подходит для лечения PPHN поскольку он вызывает расширение сосудов в вентилируемых областях легких, уменьшая несоответствие вентиляции и перфузии и тем самым улучшая оксигенацию. Лечение с использованием iNO снижает потребность в ЭКМО и смертность новорожденных с гипоксической дыхательной недостаточностью и ПРГН в результате МАС. Однако примерно 30-50% младенцев с PPHN не отвечают на терапию iNO.[17]
Противовоспалительные
Поскольку воспаление является такой серьезной проблемой при MAS, лечение состояло из противовоспалительных средств.
Глюкокортикоиды
Глюкокортикоиды (ГК) обладают сильным противовоспалительным действием и снижают миграцию и активацию нейтрофилы, эозинофилы, мононуклеары и другие клетки. ГК уменьшают миграцию нейтрофилов в легкие, следовательно, уменьшая их прилипание к эндотелий. Таким образом, снижается действие медиаторов, высвобождаемых из этих клеток, и, следовательно, уменьшается воспалительная реакция.[22][11]
ГК также обладают геномным механизмом действия, в котором, будучи связанными с рецептор глюкокортикоидов, активированный комплекс переходит в ядро и подавляет транскрипция из мРНК. В конечном итоге, влияет на то, будут ли производиться различные белки или нет. Подавление транскрипции ядерного фактора (NF-κB ) и протеиновый активатор (АП-1 ) ослабляет экспрессию провоспалительных цитокинов (Ил-1, Ил-6, Ил-8 и TNF и др.), ферменты (PLA2, СОХ-2, iNOs др.) и другие биологически активные вещества.[23][22][11] Противовоспалительный эффект ГК также демонстрируется повышением активности липокортинов, которые ингибируют активность PLA.2 и, следовательно, уменьшить производство арахидоновая кислота и посредники липоксигеназа и циклооксигеназа пути[22].
Противовоспалительные средства необходимо вводить как можно быстрее, так как действие этих препаратов может ослабнуть даже через час после аспирации мекония. Например, раннее введение дексаметазон значительно улучшенный газообмен, снизилось давление на дыхание, уменьшилось количество нейтрофилы в бронхоальвеолярной области снижена отек образование и окислительное повреждение легких.[11]Однако глюкокортикоиды могут повышать риск инфицирования, и этот риск увеличивается с увеличением дозы и продолжительности лечения глюкокортикоидами. Могут возникнуть другие проблемы, например, обострение сахарный диабет, остеопороз, кожа атрофия и задержка роста у детей.[23]
Ингибиторы фосфодиэстеразы
Фосфодиэстеразы (PDE) деградирует лагерь и cGMP и в рамках дыхательная система новорожденного с MAS могут быть вовлечены различные изоформы PDE из-за их провоспалительных и гладкая мышца сократительная активность. Следовательно, неселективные и селективные ингибиторы ФДЭ потенциально могут использоваться в терапии МАС. Однако использование ингибиторов ФДЭ может вызвать сердечно-сосудистый побочные эффекты. Неселективные ингибиторы ФДЭ, такие как метилксантины, увеличивают концентрацию цАМФ и цГМФ в клетках, что приводит к бронходилатация и расширение сосудов. Кроме того, метилксантины снижают концентрацию кальция, ацетилхолин и моноамины, это контролирует высвобождение различных медиаторов воспаления и бронхоспазм, включая простагландины. Селективные ингибиторы PDE нацелены на один подтип фосфодиэстераза а в МАС деятельность PDE-3, ПДЭ-4, ПДЭ-5 и PDE-7 может стать усиленным.[11] Например, Милриноне (селективный ингибитор PDE3) улучшил оксигенацию и выживаемость новорожденных с MAS.[24]
Ингибиторы циклооксигеназы
Арахидоновая кислота метаболизируется через циклооксигеназа (COX) и липоксигеназа, к различным веществам, включая простагландины и лейкотриены, которые обладают сильными провоспалительными и вазоактивный последствия. Путем подавления ЦОГ, а точнее СОХ-2, (с помощью селективных или неселективных препаратов) воспаление и отек можно уменьшить. Однако ингибиторы ЦОГ могут вызывать пептические язвы и причина гиперкалиемия и гипернатриемия. Кроме того, ингибиторы ЦОГ не показали значительного ответа при лечении МАС.[11]
Антибиотики
Меконий обычно стерилен, однако он может содержать различные культуры бактерий, поэтому может потребоваться назначение соответствующих антибиотиков.[17]
Обработка сурфактантом
Промывание легких с разбавленным поверхностно-активное вещество это новый метод лечения, дающий потенциально положительные результаты в зависимости от того, как рано его вводить новорожденным с МАС. Эта обработка является многообещающей, поскольку она оказывает значительное влияние на утечки воздуха, пневмоторакс, нужда в ЭКМО и смерть. Раннее вмешательство и его использование у новорожденных с легким MAS более эффективно. Однако существуют риски, поскольку закапывание большого объема жидкости в легкие новорожденного может быть опасным (особенно в случаях тяжелого MAS с легочная гипертония ) так как это может усугубить гипоксия и приводят к смертности.[25]
Предыдущие процедуры
Первоначально считалось, что MAS возник в результате физической блокировки дыхательных путей меконием. Таким образом, чтобы предотвратить развитие МАС у новорожденных, рожденных через MSAF, отсасывание ротоглоточный и носоглоточный область перед поставкой плеч с последующим трахея аспирация использовалась 20 лет. Это лечение считалось эффективным, поскольку сообщалось, что оно значительно снижает частоту возникновения MAS по сравнению с новорожденными, рожденными через MSAF, которые не получали лечения.[26] Позже это утверждение было опровергнуто, и будущие исследования пришли к выводу, что отсасывание через ротоглотку и носоглотку до родоразрешения у младенцев, рожденных через MSAF, не предотвращает MAS или его осложнения.[2] Фактически, это может вызвать больше проблем и повреждений (например, слизистая оболочка повреждение), поэтому это не рекомендуется для профилактического лечения.[19] Отсасывание не может значительно снизить частоту возникновения МАС, поскольку может произойти прохождение мекония и аспирация. в утробе. Таким образом, отсасывание становится ненужным и бесполезным, поскольку меконий может находиться глубоко в легких во время рождения.[17]
Исторически, амниоинфузия использовался при наличии MSAF, который включает трансцервикальное вливание жидкости во время родов. Идея заключалась в том, чтобы разбавить толстый меконий, чтобы уменьшить его потенциальную патофизиологию и уменьшить количество случаев MAS, поскольку MAS более распространен в случаях толстого мекония.[2] Однако есть связанные риски, такие как: выпадение пуповины и продление родов. Руководящие принципы Национального института здравоохранения и клинической практики Великобритании (NICE) не рекомендуют использовать амниоинфузию у женщин с MSAF.[18]
Распространенность
У 1 из каждых 7 беременностей есть MSAF, и из этих случаев примерно у 5% этих младенцев развивается MAS.[1] MSAF наблюдается в 23-52% беременностей на 42 неделе, поэтому частота MAS увеличивается с увеличением продолжительности беременности. беременность увеличивается, так что распространенность наиболее высока при перенесенных беременностях. Наоборот, преждевременные роды не часто связаны с MSAF (только около 5% в общей сложности содержат MSAF). Частота MAS снижается в популяциях, в которых индуцируют роды у женщин, беременность которых превышает 41 неделю.[4] Есть много предполагаемых факторов, предшествующих выбрасыванию, которые, как считается, увеличивают риск MAS. Например, риск MSAF выше у матерей афроамериканцев, африканцев и жителей островов Тихого океана по сравнению с матерями из других этнических групп.[27][6]
Будущие исследования
Исследования сосредоточены на разработке как успешного метода предотвращения MAS, так и эффективного лечения. Например, проводятся исследования эффективности противовоспалительное средство агенты, заместительная терапия сурфактантами и антибиотик терапия. Необходимо провести дополнительные исследования фармакологических свойств, например, глюкокортикоиды, включая дозировку, введение, время или любые лекарственные взаимодействия.[22] Кроме того, все еще проводятся исследования относительно того, является ли интубация и отсасывание мекония у новорожденных с МАС полезным, вредным или просто избыточным и устаревшим лечением. В целом до сих пор не существует общепринятого терапевтического протокола и эффективного плана лечения МАС.
Смотрите также
Рекомендации
- ^ а б c d е ж грамм час я j Ван Иерланд, Y; Де Бофор, AJ (2009). «Почему меконий вызывает синдром аспирации мекония? Современные концепции патофизиологии MAS». Раннее человеческое развитие. 85: 617–620. Дои:10.1016 / j.earlhumdev.2009.09.009.
- ^ а б c d е ж грамм час я Напрасно, NE; Баттон, Д.Г. (2017). «Аспирация мекония» (или респираторный дистресс, связанный с околоплодными водами, окрашенными меконием?) ». Семинары по фетальной и неонатальной медицине. 22: 214–219. Дои:10.1016 / j.siny.2017.04.002.
- ^ а б c d е ж Рахман, S; Ансуорт, Дж; Vause, S (2013). «Меконий в труде». Акушерство, гинекология и репродуктивная медицина. 23 (8): 247–252. Дои:10.1016 / j.ogrm.2013.05.007.
- ^ а б Argyridis, S; Арулкумаран, S (2016). «Околоплодные воды, окрашенные меконием». Акушерство, гинекология и репродуктивная медицина. 26 (8): 227–230. Дои:10.1016 / j.ogrm.2016.05.001.
- ^ а б c d Линденсков, PHH; Кастельхейм, А; Саугстад, OD (2015). «Синдром аспирации мекония: возможные патофизиологические механизмы и будущие потенциальные методы лечения». Неонатология. 107: 225–230. Дои:10.1159/000369373.
- ^ а б c d Сварнам, К; Soraisham, AS; Шиванандан, S (2012). «Достижения в лечении синдрома аспирации мекония». Международный журнал педиатрии. 2012: 1–7. Дои:10.1155/2012/359571. ЧВК 3228378. PMID 22164183.
- ^ а б Фанаров, AA (2008). «Синдром аспирации мекония: исторические аспекты». Журнал перинатологии. 28: S3 – S7. Дои:10.1038 / jp.2008.162.
- ^ Погги, Ш; Гидини, А (2009). «Патофизиология перехода мекония в амниотическую жидкость». Раннее человеческое развитие. 85: 607–610. Дои:10.1016 / j.earlhumdev.2009.09.011.
- ^ Белигере, Н; Рао, Р. (2008). «Результаты нервного развития младенцев с синдромом аспирации мекония: отчет об исследовании и обзор литературы». Журнал перинатологии. 28: S93 – S101. Дои:10.1038 / jp.2008.154.
- ^ а б Мокра, Д; Калковска, А (2013). «Как преодолеть дисфункцию сурфактанта при синдроме аспирации мекония». Респираторная физиология и нейробиология. 187: 58–63. Дои:10.1016 / j.resp.2013.02.030.
- ^ а б c d е ж грамм час я Мокра, Д; Mokry, J; Тонхайзерова, I (2013). «Противовоспалительное лечение синдрома аспирации мекония: преимущества и риски». Респираторная физиология и нейробиология. 187: 52–57. Дои:10.1016 / j.resp.2013.02.025.
- ^ Ромеро, Р. Юн, BH; Chaemsaithong, P; Cortez, J; Парк, CW; Бенке, РГЭ; Хасан, СС; Чайворапонгса, Т; Йео, L (2014). «Бактерии и эндотоксины в околоплодных водах, окрашенных меконием, в срок: может ли внутриамниотическая инфекция вызвать прохождение мекония?». Журнал материнско-фетальной и неонатальной медицины. 27 (8): 775–788. Дои:10.3109/14767058.2013.844124. ЧВК 5881914. PMID 24028637.
- ^ Даргавилль, Пенсильвания; Миллс, Дж. Ф. (2005). «Сурфактантная терапия синдрома аспирации мекония: современное состояние». Наркотики. 65 (18): 2569–2591. Дои:10.2165/00003495-200565180-00003.
- ^ Брук-Винсент, Ф (2015). «Синдром аспирации мекония и стойкая легочная гипертензия у новорожденных». Журнал неонатального ухода. 21: 161–167. Дои:10.1016 / j.jnn.2015.05.002.
- ^ Загария, А; Bhat, R; Чари, G; Ухал, Б; Navale, S; Видьясагар, Д. (2005). «Апоптоз эпителиальных клеток дыхательных путей в ответ на меконий». Науки о жизни. 76: 1849–1858. Дои:10.1016 / j.lfs.2004.10.033.
- ^ Marco, P; Надя, Ы; Roselyne, B; Паоло, М; Мостафа, М; Де Лука, Д. (2014). «Результаты ультразвукового исследования легких при синдроме аспирации мекония». Раннее человеческое развитие. 90 (2): 41–43. Дои:10.1016 / S0378-3782 (14) 50011-4.
- ^ а б c d е Четтри, S; Bhat, BV; Адхисивам, Б. (2016). «Современные концепции лечения синдрома аспирации мекония». Индийский J Paediatr. 83 (10): 1125–1130. Дои:10.1007 / s12098-016-2128-9.
- ^ а б c Стенсон, Б.Дж.; Смит, CL (2012). «Управление синдромом аспирации мекония». Педиатрия и детское здоровье. 22 (12): 532–535. Дои:10.1016 / j.paed.2012.08.015.
- ^ а б Агилар, AM; Напрасно, NE (2011). «Дебаты о всасывании в родильном зале». Раннее человеческое развитие. 87S: S13 – S15. Дои:10.1016 / j.earlhumdev.2011.01.003.
- ^ Напрасно, NE; Szyld, EG; Prudent, LM; Wiswell, TE; Агилар, AM; Вивас, Н.И. (2004). «Орофарингеальное и назофарингеальное отсасывание новорожденных, окрашенных меконием, перед родоразрешением их плеч: многоцентровое рандомизированное контролируемое исследование». Ланцет. 364: 597–602. Дои:10.1016 / S0140-6736 (04) 16852-9.
- ^ Короткий, BL (2008). «Экстракорпоральная мембранная оксигенация: использование при синдроме аспирации мекония». Журнал перинатологии. 28: S79 – S83. Дои:10.1038 / jp.2008.152. PMID 19057615.
- ^ а б c d Мокра, Д; Мокры, Дж (2011). «Глюкокортикоиды в лечении неонатального синдрома аспирации мекония». Eur J Pediatr. 170: 1495–1505. Дои:10.1007 / s00431-011-1453-2. ЧВК 3221844. PMID 21465122.
- ^ а б Czock, D; Келлер, Ф; Раше, FM; Хаусслер, У (2005). «Фармакокинетика и фармакодинамика глюкокортикоидов, применяемых системно». Клиническая фармакокинетика.. 44 (1): 61–98. Дои:10.2165/00003088-200544010-00003. PMID 15634032.
- ^ Басслер, D; Чунг, К.; McNamara, P; Кирпалани, Х (2006). «Неонатальная стойкая легочная гипертензия, леченная милриноном: отчет о четырех случаях». Биология новорожденного. 89: 1–5. Дои:10.1159/000088192.
- ^ Choi, HJ; Hahn, S; Ли, Дж; Парк, Би Джей; Ли, С. М.; Кин, HS; Бэ, CW (2012). «Терапия сурфактантным лаважем при синдроме аспирации мекония: систематический обзор и метаанализ». Неонатология. 101 (3): 183–191. Дои:10.1159/000329822.
- ^ Карсон, Б.С.; Лоузи, RW; Боуз-младший, Вашингтон; Симмонс, Массачусетс (1976). «Комбинированный акушерский и педиатрический подход к профилактике синдрома аспирации мекония». Am J Obstet Gynecol. 15 (126): 172–175. Дои:10.1016/0002-9378(76)90525-1.
- ^ Сехагатян, MR; Осман, я; Hossain, MM; Видьясагар, Д. (2000). «Риск заражения меконием околоплодных вод у разных этнических групп». J Perinatol. 20: 257–261. Дои:10.1038 / sj.jp.7200367.
внешняя ссылка
| Классификация | |
|---|---|
| Внешние ресурсы |
