Абакавир - Википедия - Abacavir
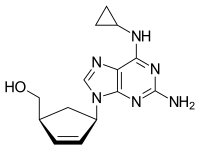 | |
 Химическая структура абакавира | |
| Клинические данные | |
|---|---|
| Произношение | /əˈбækəvɪər/ ( |
| Торговые наименования | Зиаген и др.[1] |
| AHFS /Drugs.com | Монография |
| MedlinePlus | a699012 |
| Данные лицензии | |
| Беременность категория |
|
| Маршруты администрация | Внутрь (раствор или таблетки) |
| Код УВД | |
| Легальное положение | |
| Легальное положение | |
| Фармакокинетический данные | |
| Биодоступность | 83% |
| Метаболизм | Печень |
| Устранение период полураспада | 1,54 ± 0,63 ч |
| Экскреция | Почка (1,2% абакавира, 30% метаболита 5'-карбоновой кислоты, 36% метаболита 5'-глюкуронида, 15% неустановленных минорных метаболитов). Фекальный (16%) |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| NIAID ChemDB | |
| Панель управления CompTox (EPA) | |
| ECHA InfoCard | 100.149.341 |
| Химические и физические данные | |
| Формула | C14ЧАС18N6О |
| Молярная масса | 286.339 г · моль−1 |
| 3D модель (JSmol ) | |
| Температура плавления | 165 ° С (329 ° F) |
| |
| |
| (проверять) | |
Абакавир, продается под торговой маркой Зиаген, это медикамент используется для профилактики и лечения ВИЧ / СПИД.[1][2] Подобно другим аналог нуклеозида ингибиторы обратной транскриптазы (НИОТ), абакавир используется вместе с другими Лекарства от ВИЧ, и не рекомендуется сам по себе.[3] Он принимается внутрь в виде таблеток или раствора и может применяться у детей в возрасте старше трех месяцев.[1][4]
Абакавир обычно хорошо переносится.[4] Общие побочные эффекты включают рвоту, проблемы со сном, лихорадка и чувство усталости.[1] Более серьезные побочные эффекты включают: гиперчувствительность, повреждение печени, и лактоацидоз.[1] Генетическое тестирование может указывать на повышенный риск развития гиперчувствительности у человека.[1] Симптомы гиперчувствительности включают сыпь, рвоту и одышку.[4] Абакавир относится к классу НИОТ, которые блокируют обратная транскриптаза, фермент, необходимый для Вирус ВИЧ репликация.[5] Абакавир относится к классу НИОТ. карбоциклический нуклеозид.[1]
Абакавир был запатентован в 1988 году и разрешен к применению в США в 1998 году.[6][7] Это на Список основных лекарственных средств Всемирной организации здравоохранения.[8] Он доступен как дженерик.[1] Обычно абакавир используется вместе с другими лекарствами от ВИЧ, такими как абакавир / ламивудин / зидовудин, абакавир / долутегравир / ламивудин, и абакавир / ламивудин.[4][5] Комбинация абакавир / ламивудин также является важным лекарством.[8]
Медицинское использование
Таблетки и раствор для приема внутрь абакавира в сочетании с другими антиретровирусными средствами показаны для лечения инфекции ВИЧ-1.
Абакавир всегда следует использовать в сочетании с другими антиретровирусными препаратами. Абакавир не следует добавлять в качестве единственного агента, когда схемы антиретровирусной терапии меняются из-за потери вирусологического ответа.
Побочные эффекты
Общие побочные реакции включают тошноту, головную боль, усталость, рвоту, диарею, потерю аппетита и проблемы со сном. Редкие, но серьезные побочные эффекты включают реакцию гиперчувствительности, такую как сыпь, повышенный уровень АСТ и АЛТ, депрессия, беспокойство, лихорадка / озноб, URI, лактоацидоз, гипертриглицеридемия и липодистрофия.[9][10]
Людям с заболеваниями печени следует с осторожностью применять абакавир, поскольку он может усугубить их состояние. Признаки проблем с печенью включают тошноту и рвоту, боль в животе, темную мочу, пожелтение кожи и пожелтение белков глаз. Использование нуклеозид такие препараты, как абакавир, очень редко могут вызывать лактоацидоз. Признаки лактоацидоза включают быстрое или нерегулярное сердцебиение, необычную мышечную боль, усталость, затрудненное дыхание и боль в животе с тошнотой и рвотой.[11] Абакавир также может привести к воспалительному синдрому восстановления иммунитета, изменению жировых отложений, а также к повышению риска сердечного приступа.[требуется медицинская цитата ]
Устойчивость к абакавиру развилась в лабораторных вариантах ВИЧ, которые также устойчивы к другим ВИЧ-специфическим антиретровирусным препаратам, таким как ламивудин, диданозин, и зальцитабин. Штаммы ВИЧ, устойчивые к ингибиторы протеазы вряд ли будут устойчивы к абакавиру.[требуется медицинская цитата ]
Абакавир противопоказан к применению у детей младше трех месяцев.[требуется медицинская цитата ]
Мало что известно о последствиях передозировки Абакавира. Пострадавших от передозировки следует доставить в отделение неотложной помощи больницы для лечения.[требуется медицинская цитата ]
Синдром гиперчувствительности
Гиперчувствительность к абакавиру прочно связан с конкретным аллелем в человеческий лейкоцитарный антиген B локус а именно HLA-B * 5701.[12][13][14] Существует связь между распространенностью HLA-B * 5701 и происхождением. Распространенность аллель оценивается в среднем от 3,4 до 5,8 процента в популяциях европейского происхождения, 17,6 процента в Американцы индийского происхождения, 3,0 процента среди испаноязычных американцев и 1,2 процента в Американцы китайского происхождения.[15][16] Распространенность HLA-B * 5701 среди африканского населения значительно различается. В афро-американцы, распространенность оценивается в среднем в 1,0 процента, в странах - 0 процентов. Йоруба из Нигерия, 3,3% в Лухья из Кения, и 13,6% в Масаи из Кении, хотя средние значения получены на основе сильно варьирующихся частот в группах выборки.[17]
Общие симптомы синдрома гиперчувствительности к абакавиру включают: высокая температура, недомогание, тошнота, и понос. У некоторых пациентов также может развиться кожная сыпь.[18] Симптомы AHS обычно проявляются в течение шести недель лечения абакавиром, хотя их можно спутать с симптомами ВИЧ, синдром восстановления иммунитета, синдромы гиперчувствительности, связанные с другими лекарствами или инфекциями.[19] Соединенные штаты. Управление по контролю за продуктами и лекарствами (FDA) опубликовало предупреждение о абакавире и препаратах, содержащих абакавир, 24 июля 2008 г.[20] и одобренная FDA этикетка для абакавира рекомендует предварительный скрининг на аллель HLA-B * 5701 и использование альтернативной терапии для пациентов с этим аллелем.[21] Кроме того, Консорциум по внедрению клинической фармакогенетики и Голландская рабочая группа по фармакогенетике рекомендуют использовать альтернативную терапию у лиц с аллелем HLA-B * 5701.[22][23]
Тестирование кожи может также использоваться для определения того, будет ли человек испытывать реакцию гиперчувствительности на абакавир, хотя некоторые пациенты, подверженные развитию АГЧ, могут не реагировать на тест с пластырем.[24]
Развитие подозреваемых реакций гиперчувствительности на абакавир требует немедленного и постоянного прекращения терапии абакавиром у всех пациентов, включая пациентов, не обладающих аллелем HLA-B * 5701. 1 марта 2011 года FDA проинформировало общественность о продолжающемся обзоре безопасности абакавира и о возможном повышенном риске сердечного приступа, связанного с этим препаратом.[25] А метаанализ однако из 26 исследований, проведенных FDA, не было обнаружено никакой связи между употреблением абакавира и сердечным приступом. [26][27]
Иммунопатогенез
Механизм, лежащий в основе синдрома гиперчувствительности к абакавиру, связан с изменением HLA-B * 5701 белок товар. Абакавир связывается с высокой специфичностью с белком HLA-B * 5701, изменяя форму и химический состав антигенсвязывающей щели. Это приводит к изменению иммунологическая толерантность и последующая активация специфического для абакавира цитотоксические Т-клетки, которые вызывают системную реакцию, известную как синдром гиперчувствительности к абакавиру.[28]
Взаимодействие
Абакавир и вообще НИОТ, не подвергаются метаболизму в печени и поэтому имеют очень ограниченное (или полное отсутствие) взаимодействие с ферментами CYP и лекарствами, которые влияют на эти ферменты. При этом существует еще несколько взаимодействий, которые могут повлиять на абсорбцию или доступность абакавира. Ниже приведены некоторые из общепринятых взаимодействий между лекарственными средствами и пищевыми продуктами, которые могут иметь место во время совместного приема абакавира:
- Ингибиторы протеазы Такие как типранавир или же ритоновир может снизить концентрацию абакавира в сыворотке за счет индукции глюкуронизация. Абакавир метаболизируется как алкогольдегидрогеназа и глюкуронизация.[29][30]
- Этиловый спирт может привести к повышению уровня абакавира за счет ингибирования алкогольдегидрогеназы. Абакавир метаболизируется как алкогольдегидрогеназой, так и глюкуронизацией.[29][31]
- Метадон может снизить терапевтический эффект абакавира. Абакавир может снизить концентрацию метадона в сыворотке крови.[32][33]
- Орлистат может снизить концентрацию антиретровирусных препаратов в сыворотке крови. Механизм этого взаимодействия полностью не установлен, но есть подозрения, что это связано со снижением абсорбции абакавира орлистатом.[34]
- Кабозантиниб: Препараты из семейства ингибиторов MPR2 (ингибиторы белка 2, ассоциированного с множественной лекарственной устойчивостью), такие как абакавир, могут повышать концентрацию кабозантиниба в сыворотке крови.[35]
Механизм действия
Абакавир - это нуклеозидный ингибитор обратной транскриптазы что тормозит вирусная репликация. Это гуанозин аналог, который фосфорилируется до карбовира трифосфата (CBV-TP). CBV-TP конкурирует с вирусными молекулами и включается в вирусные ДНК. Как только CBV-TP интегрирован в вирусную ДНК, транскрипция и ВИЧ обратная транскриптаза заблокирован.[36]
Фармакокинетика
Абакавир назначается перорально и быстро всасывается с высокой биодоступность 83%. Раствор и таблетка имеют сопоставимые концентрации и биодоступность. Абакавир можно принимать независимо от приема пищи.[требуется медицинская цитата ]
Абакавир может пересечь гематоэнцефалический барьер. Абакавир метаболизируется главным образом за счет ферментов. алкогольдегидрогеназа и глюкуронилтрансфераза бездействующему карбоксилат и глюкуронид метаболиты. Оно имеет период полураспада примерно 1,5-2,0 часа. Если у человека отказ печени, период полураспада абакавира увеличивается на 58%.[требуется медицинская цитата ]
Абакавир выводится с мочой (83%) и калом (16%). Неясно, можно ли удалить абакавир гемодиализ или же перитонеальный диализ.[36]
История
Роберт Винс и Сьюзан Далуге вместе с Мэй Хуа, приглашенным ученым из Китая, разработали лекарство в 80-х годах.[37][38][39]
Абакавир был одобрен США. Управление по контролю за продуктами и лекарствами (FDA) 18 декабря 1998 года и, таким образом, является пятнадцатым одобренным антиретровирусным препаратом в Соединенных Штатах.[нужна цитата ] Его патент истек в США 26 декабря 2009 года.[нужна цитата ]
Синтез

Рекомендации
- ^ а б c d е ж грамм час «Абакавир сульфат». Американское общество фармацевтов систем здравоохранения. В архиве с оригинала 21 августа 2017 г.. Получено 31 июля 2015.
- ^ «Рекомендации по сокращению названий лекарств для взрослых и подростков». AIDSinfo. В архиве из оригинала 9 ноября 2016 г.. Получено 8 ноября 2016.
- ^ «Рекомендации по использованию АРВ-препаратов для взрослых и подростков». AIDSinfo. В архиве из оригинала 9 ноября 2016 г.. Получено 8 ноября 2016.
- ^ а б c d Юэн Г.Дж., Веллер С., Пейкс Г.Е. (2008). «Обзор фармакокинетики абакавира». Клиническая фармакокинетика.. 47 (6): 351–71. Дои:10.2165/00003088-200847060-00001. PMID 18479171. S2CID 31107341.
- ^ а б «Нуклеозидные ингибиторы обратной транскриптазы (НИОТ или« ядерные бомбы ») - ВИЧ / СПИД». www.hiv.va.gov. В архиве из оригинала 9 ноября 2016 г.. Получено 8 ноября 2016.
- ^ Фишер, Янош; Ганеллин, С. Робин (2006). Открытие лекарств на основе аналогов. Джон Вили и сыновья. п. 505. ISBN 9783527607495. В архиве из оригинала от 8 сентября 2017 г.
- ^ Кейн, Бригид М. (2008). Препараты для лечения ВИЧ / СПИДа. Публикация информационной базы. п. 56. ISBN 9781438102078. В архиве из оригинала от 8 сентября 2017 г.
- ^ а б Всемирная организация здоровья (2019). Типовой список основных лекарственных средств Всемирной организации здравоохранения: 21-й список 2019 г.. Женева: Всемирная организация здравоохранения. HDL:10665/325771. WHO / MVP / EMP / IAU / 2019.06. Лицензия: CC BY-NC-SA 3.0 IGO.
- ^ «Побочные реакции на абакавир». Epocrates Online.
- ^ Факты о профессиональных наркотиках
- ^ «Абакавир». AIDSinfo. В архиве из оригинала 6 марта 2017 г.. Получено 8 ноября 2016.
- ^ Маллал С., Филлипс Э., Карози Дж. И др. (2008). «Скрининг HLA-B * 5701 на гиперчувствительность к абакавиру». Медицинский журнал Новой Англии. 358 (6): 568–579. Дои:10.1056 / nejmoa0706135. PMID 18256392.
- ^ Раух А., Нолан Д., Мартин А. и др. (2006). «Проспективный генетический скрининг снижает частоту реакций гиперчувствительности на абакавир в когортном исследовании ВИЧ в Западной Австралии». Клинические инфекционные заболевания. 43 (1): 99–102. Дои:10.1086/504874. PMID 16758424.
- ^ Дин Л. (2015). «Абакавир терапия и генотип HLA-B * 57: 01». В Pratt VM, McLeod HL, Rubinstein WS, et al. (ред.). Резюме по медицинской генетике. Национальный центр биотехнологической информации (NCBI). PMID 28520363. Код книжной полки: NBK315783. Получено 14 января 2019.
- ^ Хетерингтон С., Хьюз А.Р., Мостеллер М. и др. (2002). «Генетические вариации в области HLA-B и реакции гиперчувствительности к абакавиру». Ланцет. 359 (9312): 1121–1122. Дои:10.1016 / с0140-6736 (02) 08158-8. PMID 11943262. S2CID 9434238.
- ^ Маллал С., Нолан Д., Витт С. и др. (2002). «Связь между присутствием HLA * B5701, HLA-DR7 и HLA-DQ3 и гиперчувствительностью к ингибитору обратной транскриптазы ВИЧ-1 абакавиру». Ланцет. 359 (9308): 727–732. Дои:10.1016 / с0140-6736 (02) 07873-х. PMID 11888582. S2CID 12923232.
- ^ Rotimi CN, Jorde LB (2010). «Предки и болезни в эпоху геномной медицины». Медицинский журнал Новой Англии. 363 (16): 1551–1558. Дои:10.1056 / nejmra0911564. PMID 20942671.
- ^ Филлипс Э., Маллал С (2009). «Успешный перевод фармакогенетики в клинику: пример абакавира». Молекулярная диагностика и терапия. 13 (1): 1–9. Дои:10.1007 / bf03256308. ISSN 1177-1062. PMID 19351209. S2CID 45896364.
- ^ Филлипс Э., Маллал С (2007). «Лекарственная гиперчувствительность при ВИЧ». Текущее мнение в области аллергии и клинической иммунологии. 7 (4): 324–330. Дои:10.1097 / aci.0b013e32825ea68a. PMID 17620824. S2CID 37549824.
- ^ «Информация для медицинских работников: абакавир (продается как Ziagen) и препараты, содержащие абакавир». Управление по контролю за продуктами и лекарствами (FDA). 24 июля 2008 г. Архивировано с оригинал 11 декабря 2013 г.. Получено 29 ноября 2013.
- ^ «Зиаген-абакавира сульфат таблетка, этикетка с пленочным покрытием». DailyMed. 30 сентября 2015 г. В архиве из оригинала 11 января 2017 г.. Получено 9 сентября 2019.
- ^ Swen JJ, Nijenhuis M, de Boer A, et al. (Май 2011 г.). «Фармакогенетика: от скамейки к байту - обновление рекомендаций». Clin Pharmacol Ther. 89 (5): 662–73. Дои:10.1038 / clpt.2011.34. PMID 21412232. S2CID 2475005.
- ^ Мартин М.А., Хоффман Дж. М., Фреймут Р. Р. и др. (Май 2014 г.). «Рекомендации Консорциума по внедрению клинической фармакогенетики для генотипа HLA-B и дозирования абакавира: обновление 2014 г.». Clin Pharmacol Ther. 95 (5): 499–500. Дои:10.1038 / clpt.2014.38. ЧВК 3994233. PMID 24561393.
- ^ Shear NH, Milpied B, Bruynzeel DP и др. (2008). «Обзор тестирования на лекарственные пластыри и его значение для врачей, занимающихся ВИЧ». СПИД. 22 (9): 999–1007. Дои:10.1097 / qad.0b013e3282f7cb60. PMID 18520343. S2CID 2972984.
- ^ «Сообщение FDA по безопасности лекарств: обновленная информация в обзоре безопасности абакавира и возможное повышение риска сердечного приступа». Управление по контролю за продуктами и лекарствами (FDA). 1 марта 2011 г.. Получено 9 сентября 2019.
- ^ «Предупреждение FDA: абакавир - постоянный обзор безопасности: возможный повышенный риск сердечного приступа». Drugs.com. В архиве из оригинала 10 декабря 2013 г.. Получено 29 ноября 2013.
- ^ Динг Х, Андрака-Каррера Э, Купер С. и др. (Декабрь 2012 г.). «Нет связи между использованием абакавира и инфарктом миокарда: результаты метаанализа FDA». Синдр иммунодефицита J Acquir. 61 (4): 441–7. Дои:10.1097 / QAI.0b013e31826f993c. PMID 22932321. S2CID 7997822.
- ^ Иллинг П. Т., Вивиан Дж. П., Дудек Н. Л. и др. (2012). «Иммунная самореактивность, вызванная репертуаром HLA-пептидов, модифицированных лекарственными средствами». Природа. 486 (7404): 554–8. Bibcode:2012Натура.486..554I. Дои:10.1038 / природа11147. PMID 22722860. S2CID 4408811.
- ^ а б Прописная информация. Зиаген (абакавир). Research Triangle Park, NC: GlaxoSmithKline, июль 2002 г.
- ^ Вурвахис М, Кашуба А.Д. (2007). «Механизмы фармакокинетических и фармакодинамических лекарственных взаимодействий, связанных с типранавиром, усиленным ритонавиром». Фармакотерапия. 27 (6): 888–909. Дои:10.1592 / phco.27.6.888. PMID 17542771. S2CID 23591048.
- ^ McDowell JA, Chittick GE, Stevens CP и др. (2000). "", «Фармакокинетическое взаимодействие абакавира (1592U89) и этанола у взрослых, инфицированных вирусом иммунодефицита человека». Противомикробные агенты Chemother. 44 (6): 1686–90. Дои:10.1128 / aac.44.6.1686-1690.2000. ЧВК 89933. PMID 10817729.
- ^ Беренгер Дж., Перес-Элиас М. Дж., Беллон Дж. М. и др. (2006). «Эффективность и безопасность абакавира, ламивудина и зидовудина у ВИЧ-инфицированных пациентов, ранее не получавших антиретровирусную терапию: результаты большой многоцентровой наблюдательной когорты». Синдр иммунодефицита J Acquir. 41 (2): 154–159. Дои:10.1097 / 01.qai.0000194231.08207.8a. PMID 16394846. S2CID 17609676.
- ^ Долофин (метадон) [информация о назначении]. Колумбус, Огайо: Roxane Laboratories, Inc.; Март 2015 г.
- ^ Gervasoni C, Cattaneo D, Di Cristo V и др. (2016). «Орлистат: потеря веса за счет повторного заражения ВИЧ». J Antimicrob Chemother. 71 (6): 1739–1741. Дои:10.1093 / jac / dkw033. PMID 26945709.
- ^ Кометрик (кабозантиниб) [информация по назначению]. Южный Сан-Франциско, Калифорния: Exelixis, Inc.; Май 2016.
- ^ а б Информация о продукте: таблетки для приема внутрь ZIAGEN®, раствор для приема внутрь, таблетки для приема внутрь сульфата абакавира, раствор для приема внутрь. ViiV Healthcare (по производителям), Research Triangle Park, NC, 2015.
- ^ "Доктор Роберт Винс - призывник 2010 г.". Зал славы изобретателей Миннесоты. Архивировано из оригинал 15 февраля 2016 г.. Получено 10 февраля 2016.
- ^ «Роберт Винс, доктор философии (список преподавателей)». Университет Миннесоты. В архиве из оригинала 17 февраля 2016 г.
- ^ Далуге С.М., Гуд С.С., Фалетто М.Б. и др. (Май 1997 г.). «1592U89, новый аналог карбоциклического нуклеозида с сильной избирательной активностью против вируса иммунодефицита человека». Противомикробные препараты и химиотерапия. 41 (5): 1082–1093. Дои:10.1128 / AAC.41.5.1082. ЧВК 163855. PMID 9145874.
- ^ Crimmins MT, King BW (1996). «Эффективный асимметричный подход к карбоциклическим нуклеозидам: асимметричный синтез 1592U89, мощного ингибитора обратной транскриптазы ВИЧ». Журнал органической химии. 61 (13): 4192–4193. Дои:10.1021 / jo960708p. PMID 11667311.
дальнейшее чтение
- Дин Л. (апрель 2018 г.). «Абакавир терапия и генотип HLA-B * 57: 01». В Pratt VM, McLeod HL, Rubinstein WS, et al. (ред.). Резюме по медицинской генетике. Национальный центр биотехнологической информации (NCBI). PMID 28520363.
внешняя ссылка
- «Абакавир». Портал информации о наркотиках. Национальная медицинская библиотека США.
- Путь абакавира на PharmGKB
- Рекомендации по дозированию абакавира от Консорциума по внедрению клинической фармакогенетики (CPIC)
- Рекомендации по дозировке абакавира от Голландской рабочей группы по фармакогенетике (DPWG)

