Меленгестрол - Melengestrol
 | |
| Клинические данные | |
|---|---|
| Код УВД |
|
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| ChemSpider | |
| UNII | |
| Панель управления CompTox (EPA) | |
| ECHA InfoCard | 100.024.613 |
| Химические и физические данные | |
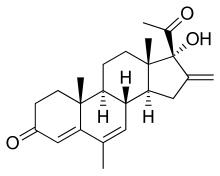
| Формула | C23ЧАС30О3 |
| Молярная масса | 354.490 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
| | |
Меленгестрол (ГОСТИНИЦА, БАН ) это стероидный прогестин из 17α-гидроксипрогестерон группа и противоопухолевый препарат, средство, медикамент который никогда не продавался.[1] An ацилированный производная меленгестрола ацетат, используется как стимулятор роста у животных.[1]
Пока меленгестрол иногда используется как синоним меленгестрола ацетат, то, что обычно называют ацетатом меленгестрола, а не меленгестролом.
Синтез
6-метил-16-дегидропрегненолона ацетат (5) является ключевым промежуточным продуктом для получения как ацетата меленгестерина, так и медрогестон. Петров и его сотрудники разработали несколько интересных схем, восходящих к диосгенин в качестве отправной точки. Эти схемы выполняют необходимые модификации в кольцах A и B с сохранением боковой цепи сапогенина. По сути, этот подход использует эту боковую цепь в качестве защитной группы для будущей функции 16-дегидро-20-кетона. По одному из этих способов диосгенин сначала превращается в 3-толуолсульфонат (1). Сольволиз этого гомоаллильного производного спирта дает 3,5-циклостероид (2), через циклопропил карбиниловый ион (ион карбения ) (не показано). (Эта общая реакция, вероятно, впервые была обнаружена на стероидах и носила название "я-стероидная перегруппировка. ") Окисление продукта посредством PCC дает кетон. Реакция этого с метилмагний йодид дает два изомерных карбинола с преобладающим α-изомером (3). Сольволиз в присутствии нуклеофила, такого как уксусная кислота, обращает циклопропилкарбинильное превращение с образованием гомоаллилового ацетата. Удаление боковой цепи сапогенина приводит к желаемому продукту (5).[2]

Было обнаружено, что замена в положении 16 приводит к дальнейшему усилению прогестагенной активности. Реакция с диазометан по сопряженной двойной связи в 16 дает сначала пиразол (6). Этот гетероцикл дает 16-метиловый Enone на пиролиз (7). Селективный эпоксидирование сопряженной двойной связи с 16,17α-эпоксидом по сравнению с 5,6 достигается окислением основным пероксид водорода (8). Открытие этого тетразамещенного оксиран кольцо в кислоте протекает с потерей протона из β-положения (16-метил) (9) с получением желаемой функциональной группы 16-метилен-17α-гидрокси-20-кетона в кольце D (10). Продукт омыляется, а затем подвергается Окисление Оппенауэра, который затем дегидрируется до 4,6-диена с хлоранил (11). Ацетилирование в форсирующих условиях завершает синтез ацетата меленгестерина.
Смотрите также
Рекомендации
- ^ а б Макдональд Ф (1997). Словарь фармакологических агентов. CRC Press. п. 1269. ISBN 978-0-412-46630-4. Получено 30 мая 2012.
- ^ Берн Д., Эллис Б., Петроу В., Стюарт-Уэбб И.А., Уильямсон Д.М. (1957). «809. Модифицированные стероидные гормоны. Часть IV. Производные 6-метилпрегнана». Журнал химического общества (возобновлено): 4092. Дои:10.1039 / JR9570004092.
- ^ Кирк Д. Н., Петроу В., Уильямсон Д. М. (1961). «550. Модифицированные стероидные гормоны. Часть XXII. 6α, 16β-Диметилпрогестерон и 17α-ацетокси-6β-метил-16-метиленпрогестерон». Журнал химического общества (возобновлено): 2821. Дои:10.1039 / JR9610002821.
| Этот препарат, средство, медикамент статья, касающаяся мочеполовая система это заглушка. Вы можете помочь Википедии расширяя это. |
| Эта статья о стероидный препарат это заглушка. Вы можете помочь Википедии расширяя это. |
