Фосфолипаза C - Phospholipase C

Фосфолипаза C (ПЛК) представляет собой класс мембранно-ассоциированных ферменты этот раскол фосфолипиды прямо перед фосфат группа (см. рисунок). Обычно его считают синонимом человеческих форм этого фермента, которые играют важную роль в эукариотический ячейка физиология, особенно преобразование сигнала пути. Существует тринадцать видов фосфолипазы С млекопитающих, которые классифицируются на шесть изотипов (β, γ, δ, ε, ζ, η) в зависимости от структуры. Каждый ПЛК имеет уникальные и частично совпадающие элементы управления экспрессией и субклеточным распределением. Активаторы каждого ПЛК различаются, но обычно включают гетеротримерный G-белок субъединицы, белок тирозинкиназы, маленькие G-белки, Ca2+и фосфолипиды.[1]
Варианты
Варианты млекопитающих
Обширное количество функций, выполняемых реакцией PLC, требует, чтобы она строго регулировалась и была способна реагировать на множественные внеклеточные и внутриклеточные входы с соответствующей кинетикой. Эта потребность руководила эволюцией шести изотипов PLC у животных, каждый из которых имел свой способ регуляции. Пре-мРНК PLC также может подвергаться дифференциальному сплайсингу, так что млекопитающее может иметь до 30 ферментов PLC.[2]
- бета: PLCB1, PLCB2, PLCB3, PLCB4
- гамма: PLCG1, PLCG2
- дельта: PLCD1, PLCD3, PLCD4
- эпсилон: PLCE1
- эта: PLCH1, PLCH2
- дзета: PLCZ1
- фосфолипаза C-подобная: PLCL1, PLCL2
Бактериальные варианты
Большинство бактериальных вариантов фосфолипазы С относятся к одной из четырех групп структурно родственных белков. Токсичные фосфолипазы C способны взаимодействовать с мембранами эукариотических клеток и гидролизовать фосфатидилхолин и сфингомиелин, что в конечном итоге приводит к лизису клеток.[3]
- Цинк-металлофосфолипазы C: Clostridium perfringens альфа-токсин, Bacillus cereus ПЛК (BC-PLC)
- Сфингомиелиназы: B. cereus, Золотистый стафилококк
- Ферменты, гидролизующие фосфатидилинозит: B. cereus, B. thuringiensis, L. monocytogenes (ПЛК-А)
- Псевдомонад фосфолипаза C: Синегнойная палочка (PLC-H и PLC-N)
Структура фермента

У млекопитающих PLC имеют общую консервативную структуру ядра и отличаются другими доменами, специфичными для каждого семейства. Основной фермент включает расщепленный ствол триозофосфатизомеразы (ТИМ), домен гомологии плекстрина (PH), четыре тандемных ручных домена EF и C2 домен.[1] Цилиндр TIM содержит активный центр, все каталитические остатки и Ca2+ сайт привязки. У него есть автоматическая вставка, которая прерывает его активность, называемая линкером X-Y. Было показано, что линкер X-Y закрывает активный сайт, и при его удалении активируется PLC.[4]
Гены, кодирующие альфа-токсин (Clostridium perfringens), Bacillus cereus ПЛК (BC-PLC) и ПЛК от Clostridium bifermentans и Listeria monocytogenes были выделены и нуклеотиды секвенированы. Наблюдается значительная гомология последовательностей, приблизительно 250 остатков, от N-конца. Альфа-токсин имеет еще 120 остатков на С-конце. О C-конце альфа-токсина сообщалось как о «C2-подобном» домене, ссылаясь на C2 домен обнаружены у эукариот, которые участвуют в передаче сигналов и присутствуют у млекопитающих фосфоинозитид фосфолипаза C.[5]
Ферментный механизм

Первичная катализируемая реакция PLC происходит на нерастворимом субстрате на границе раздела липид-вода. Остатки в активном сайте консервативны во всех изотипах PLC. У животных PLC избирательно катализирует гидролиз фосфолипидов. фосфатидилинозитол-4,5-бисфосфат (PIP2) на глицериновой стороне фосфодиэфирной связи. Происходит образование слабо связанного с ферментом промежуточного соединения, 1,2-циклического фосфодиэфира инозита, и высвобождение диацилглицерин (ДАГ). Промежуточный продукт затем гидролизуют до инозитол 1,4,5-трифосфат (IP3).[6] Таким образом, двумя конечными продуктами являются DAG и IP.3. Для кислотно-основного катализа требуются два консервативных остатка гистидина и Ca2+ ion необходим для PIP2 гидролиз. Было замечено, что активный центр Ca2+ координируется с четырьмя кислотными остатками, и если какой-либо из остатков мутирован, то большее количество Ca2+ концентрация необходима для катализа.[7]
Регулирование
Активация
Рецепторы, активирующие этот путь, в основном G-белковые рецепторы в сочетании с гαq подразделение, в том числе:
- 5-HT2 серотонинергические рецепторы
- α1 (Альфа-1) адренорецепторы[8]
- Рецепторы кальцитонина
- ЧАС1 гистаминовые рецепторы
- Метаботропные рецепторы глутамата, Группа I
- M1, M3, и M5 мускариновые рецепторы
- Рецептор тироид-высвобождающего гормона в передней доле гипофиза
Другие второстепенные активаторы, кроме Gαq находятся:
- MAP киназа. К активаторам этого пути относятся: PDGF и FGF.[8]
- βγ-комплекс из гетеротримерные G-белки, как в второстепенном пути гормон роста выпуск гормон, высвобождающий гормон роста.[9]
- Каннабиноидные рецепторы
Торможение
- Низкая молекула U73122: аминостероид, предполагаемый ингибитор PLC.[10][11] Однако специфичность U73122 подвергается сомнению.[12][13] Сообщалось, что U73122 активирует фосфолипазную активность очищенных PLC.[14]
- Эдельфозин: липидоподобное противоопухолевое средство (ET-18-OCH3)[15]
- Автоингибирование линкера X-Y в клетках млекопитающих: предполагается, что линкер X-Y состоит из длинных участков кислых аминокислот, которые образуют плотные области отрицательного заряда. Эти области могут отталкиваться отрицательно заряженной мембраной при связывании PLC с липидами мембраны. Считается, что сочетание отталкивания и стерических ограничений удаляет линкер X-Y рядом с активным сайтом и снимает аутоингибирование.[1]
- Соединения, содержащие каркас морфолинобензойной кислоты, относятся к классу лекарственно-подобных фосфатидилхолин-специфичных ингибиторов PLC.[16][17]
- о-фенантролин: гетероциклическое органическое соединение, ингибирующее цинк-металлоферменты[18]
- ЭДТА: молекула, хелатирующая Zn2+ ионов и эффективно инактивирует PLC, который, как известно, ингибирует цинк-металлоферменты[19]
Биологическая функция
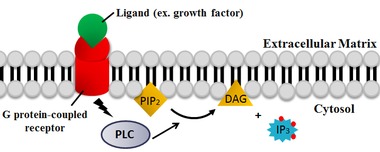
ПЛК расщепляет фосфолипид фосфатидилинозитол-4,5-бисфосфат (PIP2) в диацилглицерин (DAG) и инозитол 1,4,5-трифосфат (IP3). Таким образом, PLC оказывает глубокое влияние на истощение PIP.2, который действует как мембранный якорь или аллостерический регулятор.[20] PIP2 также действует как субстрат для синтеза более редких липидов фосфатидилинозитол 3,4,5-трифосфат (PIP3), который отвечает за передачу сигналов во множественных реакциях.[21] Следовательно, PIP2 истощение в результате реакции PLC имеет решающее значение для регулирования местного PIP3 концентрации как в плазматической мембране, так и в ядерной мембране.
Два продукта реакции, катализируемой PLC, DAG и IP3, являются важными вторичными посредниками, которые контролируют различные клеточные процессы и являются субстратами для синтеза других важных сигнальных молекул. Когда PIP2 расщепляется, DAG остается связанным с мембраной, а IP3 выделяется в виде растворимой структуры в цитозоль. IP3 затем диффундирует через цитозоль, чтобы связываться с IP3 рецепторы особенно кальциевые каналы в гладкая эндоплазматическая сеть (ER). Это вызывает повышение цитозольной концентрации кальция, вызывая каскад внутриклеточных изменений и активности.[22] Кроме того, кальций и DAG вместе работают для активации протеинкиназа C, который затем фосфорилирует другие молекулы, что приводит к изменению клеточной активности.[22] Конечные эффекты включают вкусовые ощущения, распространение опухоли, а также экзоцитоз пузырьков. супероксид производство из НАДФН оксидаза, и JNK активация.[22][23]
И DAG, и IP3 являются субстратами для синтеза регуляторных молекул. ДАГ - субстрат для синтеза фосфатидная кислота, регуляторная молекула. IP3 является ограничивающим скорость субстратом для синтеза полифосфатов инозита, которые стимулируют множественные протеинкиназы, транскрипцию и процессинг мРНК.[24] Таким образом, регуляция активности PLC жизненно важна для координации и регуляции других ферментов путей, которые являются центральными для контроля клеточной физиологии.
Кроме того, фосфолипаза C играет важную роль в пути воспаления. Связывание таких агонистов, как тромбин, адреналин, или коллаген, чтобы тромбоцит поверхностные рецепторы могут запускать активацию фосфолипазы C, чтобы катализировать высвобождение арахидоновая кислота из двух основных мембранных фосфолипидов, фосфатидилинозитол и фосфатидилхолин. Затем арахидоновая кислота может перейти в путь циклооксигеназы (производя простогландины (PGE1, PGE2, PGF2), простациклины (PGI2) или тромбоксаны (TXA2)) и липоксигеназный путь (продуцирующий лейкотриены (LTB4, LTC4, LTD4, LTE4)).[25]
Бактериальный вариант Clostridium perfringens тип А производит альфа-токсин. Токсин обладает активностью фосфолипазы C и вызывает гемолиз, летальность и дермонекроз. В высоких концентрациях альфа-токсин вызывает массовую деградацию фосфатидилхолин и сфингомиелин, производящий диацилглицерин и керамид соответственно. Затем эти молекулы участвуют в путях передачи сигнала.[5] Сообщалось, что токсин активирует каскад арахидоновой кислоты в изолированной аорте крысы.[26] Сокращение, вызванное токсином, было связано с образованием тромбоксана А.2 из арахидоновой кислоты. Таким образом, вероятно, что бактериальный PLC имитирует действие эндогенного PLC в мембранах эукариотических клеток.
Смотрите также
- Гликозилфосфатидилинозитолдиацилглицерин-лиаза EC 4.6.1.14 Трипаносомальный фермент.
- Фосфатидилинозитолдиацилглицерин-лиаза EC 4.6.1.13 Другой родственный бактериальный фермент
- Фосфоинозитид фосфолипаза C EC 3.1.4.11 Основная форма встречается у эукариот, особенно у млекопитающих.
- Цинк-зависимая фосфолипаза C семейство бактериальных ферментов EC 3.1.4.3 это включает альфа-токсины C. perfringens (также известен как лецитиназа ), P. aeruginosa, и S. aureus.
использованная литература
- ^ а б c Кадамур Г, Росс Э.М. (2013). «Фосфолипаза С млекопитающих». Ежегодный обзор физиологии. 75: 127–54. Дои:10.1146 / аннурев-физиол-030212-183750. PMID 23140367.
- ^ Suh, PG; Парк, JI; Manzoli, L; Cocco, L; Пик, JC; Катан, М; Фуками, К; Катаока, Т; Юн, S; Рю, SH (2008). «Множественные роли фосфоинозитид-специфических изоферментов фосфолипазы C». BMB отчеты. 41 (6): 415–34. Дои:10.5483 / bmbrep.2008.41.6.415. PMID 18593525.
- ^ Титболл, RW (1993). «Бактериальные фосфолипазы С.» Микробиологические обзоры. 57 (2): 347–66. Дои:10.1128 / MMBR.57.2.347-366.1993. ЧВК 372913. PMID 8336671.
- ^ Hicks SN, Jezyk MR, Gershburg S, Seifert JP, Harden TK, Sondek J (август 2008 г.). «Общее и универсальное автоингибирование изоферментов PLC». Молекулярная клетка. 31 (3): 383–94. Дои:10.1016 / j.molcel.2008.06.018. ЧВК 2702322. PMID 18691970.
- ^ а б Сакураи Дж., Нагахама М., Ода М. (ноябрь 2004 г.). «Альфа-токсин Clostridium perfringens: характеристика и механизм действия». Журнал биохимии. 136 (5): 569–74. Дои:10.1093 / jb / mvh161. PMID 15632295.
- ^ Essen LO, Perisic O, Katan M, Wu Y, Roberts MF, Williams RL (февраль 1997 г.). «Структурное картирование каталитического механизма для фосфоинозитид-специфической фосфолипазы C млекопитающих». Биохимия. 36 (7): 1704–18. Дои:10.1021 / bi962512p. PMID 9048554.
- ^ Эллис, М.В.; Джеймс, SR; Перишич, О; Даунс, ПК; Уильямс, Р.Л .; Катан, М. (1998). «Каталитический домен фосфоинозитид-специфической фосфолипазы C (PLC): анализ мутаций остатков в активном центре гидрофобного гребня PLCD1». Журнал биологической химии. 273 (19): 11650–9. Дои:10.1074 / jbc.273.19.11650. PMID 9565585.
- ^ а б Уолтер Ф. Борон (2003). Медицинская физиология: клеточный и молекулярный подход. Elsevier / Saunders. п. 1300. ISBN 978-1-4160-2328-9. Стр.104
- ^ GeneGlobe -> Сигнализация GHRH[постоянная мертвая ссылка ] Проверено 31 мая, 2009 г.
- ^ Блисдейл Дж. Э., Такур Н. Р., Грембан Р. С., Банди Г. Л., Фицпатрик Ф. А., Смит Р. Дж., Бантинг С. (ноябрь 1990 г.). «Селективное ингибирование рецептор-связанных фосфолипазных C-зависимых процессов в человеческих тромбоцитах и полиморфно-ядерных нейтрофилах». Журнал фармакологии и экспериментальной терапии. 255 (2): 756–68. PMID 2147038.
- ^ Макмиллан Д., Маккаррон Дж. Г. (июль 2010 г.). «Ингибитор фосфолипазы C U-73122 ингибирует высвобождение Ca (2+) из внутриклеточного хранилища Ca (2+) саркоплазматического ретикулума путем ингибирования накачки Ca (2+) в гладких мышцах». Британский журнал фармакологии. 160 (6): 1295–301. Дои:10.1111 / j.1476-5381.2010.00771.x. ЧВК 2938802. PMID 20590621.
- ^ Хуанг В., Барретт М., Хаджичек Н., Хикс С., Харден Т.К., Сондек Дж., Чжан К. (февраль 2013 г.). «Низкомолекулярные ингибиторы фосфолипазы C из нового высокопроизводительного скрининга». Журнал биологической химии. 288 (8): 5840–8. Дои:10.1074 / jbc.M112.422501. ЧВК 3581404. PMID 23297405.
- ^ Лейтнер М.Г., Мишель Н., Берендт М., Диерих М., Дембла С., Вилке Б.У., Конрад М., Линднер М., Обервинклер Дж., Оливер Д. (август 2016 г.). «Прямая модуляция каналов TRPM4 и TRPM3 ингибитором фосфолипазы C U73122». Британский журнал фармакологии. 173 (16): 2555–69. Дои:10.1111 / bph.13538. ЧВК 4959952. PMID 27328745.
- ^ Klein RR, Bourdon DM, Costales CL, Wagner CD, White WL, Williams JD, Hicks SN, Sondek J, Thakker DR (апрель 2011 г.). «Прямая активация фосфолипазы С человека ее хорошо известным ингибитором u73122». Журнал биологической химии. 286 (14): 12407–16. Дои:10.1074 / jbc.M110.191783. ЧВК 3069444. PMID 21266572.
- ^ Горовиц Л.Ф., Хирдес В., Сух BC, Хильгеманн Д.В., Маки К., Хилле Б. (сентябрь 2005 г.). «Фосфолипаза С в живых клетках: активация, ингибирование, потребность в Са2 + и регуляция М-тока». Журнал общей физиологии. 126 (3): 243–62. Дои:10.1085 / jgp.200509309. ЧВК 2266577. PMID 16129772.
- ^ Eurtivong, C .; Pilkington, L.I .; ван Ренсбург, М .; Уайт, Р. М .; Kaur Brar, H .; Rees, S .; Паулин, Э.К .; Xu, C. S .; Sharma, N .; Leung, I. K. H .; Leung, E .; Barker, D .; Рейниссон, Дж. (1 февраля 2020 г.). «Открытие новых ингибиторов фосфатидилхолин-специфической фосфолипазы C, подобных лекарственным средствам, в качестве потенциальных противораковых агентов». Европейский журнал медицинской химии. 187: 111919. Дои:10.1016 / j.ejmech.2019.111919. PMID 31810783.CS1 maint: использует параметр авторов (ссылка на сайт)
- ^ Pilkington, L.I .; Воробей, К .; Rees, S. W. P .; Паулин, Э.К .; ван Ренсбург, М .; Xu, C. S .; Langley, R.J .; Leung, I. K. H .; Reynisson, J .; Leung, E .; Баркер, Д. (2020). «Разработка, синтез и биологическое исследование нового класса мощных ингибиторов PC-PLC». Европейский журнал медицинской химии. 191: 112162. Дои:10.1016 / j.ejmech.2020.112162. PMID 32101781.CS1 maint: использует параметр авторов (ссылка на сайт)
- ^ Литтл К., Относ А.Б. (июнь 1975 г.). «Зависимость фосфолипазы С от ионов металлов Bacillus cereus». Biochimica et Biophysica Acta (BBA) - Энзимология. 391 (2): 326–33. Дои:10.1016/0005-2744(75)90256-9. PMID 807246.
- ^ «Фосфолипаза C, специфическая к фосфатидилинозитолу из Bacillus cereus» (PDF). информация о продукте. Сигма Олдрич.
- ^ Хильгеманн DW (октябрь 2007 г.). «Локальные сигналы PIP (2): когда, где и как?». Pflügers Archiv. 455 (1): 55–67. Дои:10.1007 / s00424-007-0280-9. PMID 17534652. S2CID 29839094.
- ^ Falkenburger BH, Jensen JB, Dickson EJ, Suh BC, Hille B (сентябрь 2010 г.). «Фосфоинозитиды: липидные регуляторы мембранных белков». Журнал физиологии. 588 (Pt 17): 3179–85. Дои:10.1113 / jphysiol.2010.192153. ЧВК 2976013. PMID 20519312.
- ^ а б c Альбертс Б., Льюис Дж., Рафф М., Робертс К., Уолтер П. (2002). Молекулярная биология клетки (4-е изд.). Нью-Йорк: Наука Гарланд. ISBN 978-0-8153-3218-3.
- ^ Ли З, Цзян Х, Се В., Чжан З, Смрка А. В., Ву Д. (февраль 2000 г.). «Роли PLC-beta2 и -beta3 и PI3Kgamma в передаче сигнала, опосредованной хемоаттрактантами». Наука. 287 (5455): 1046–9. Дои:10.1126 / science.287.5455.1046. PMID 10669417.
- ^ Грессет А., Сондек Дж., Харден Т.К. (2012). «Изоферменты фосфолипазы С и их регуляция». Фосфоинозитиды I: ферменты синтеза и распада. Субклеточная биохимия. 58. С. 61–94. Дои:10.1007/978-94-007-3012-0_3. ISBN 978-94-007-3011-3. ЧВК 3638883. PMID 22403074.
- ^ Пиомелли, Даниэле (1 апреля 1993 г.). «Арахидоновая кислота в передаче сигналов в клетке» (PDF). Текущее мнение в области клеточной биологии. 5 (2): 274–280. Дои:10.1016/0955-0674(93)90116-8. PMID 7685181.
- ^ Fujii Y, Sakurai J (май 1989 г.). «Сокращение изолированной аорты крысы, вызванное альфа-токсином Clostridium perfringens (фосфолипаза C): доказательства участия в метаболизме арахидоновой кислоты». Британский журнал фармакологии. 97 (1): 119–24. Дои:10.1111 / j.1476-5381.1989.tb11931.x. ЧВК 1854495. PMID 2497921.
