Rho-ассоциированная протеинкиназа - Википедия - Rho-associated protein kinase
| КАМЕНЬ | |
|---|---|
 Кристаллическая структура человека ROCK I | |
| Идентификаторы | |
| Символ | Rho-ассоциированная протеинкиназа |
| Альт. символы | Rho-ассоциированная протеинкиназа, содержащая спиральную спираль |
| Ген NCBI | 579202 |
| Прочие данные | |
| Номер ЕС | 2.7.11.1 |
Rho-ассоциированная протеинкиназа (КАМЕНЬ) это киназа принадлежащих к семейству AGC (PKA / PKG / PKC) серин-треониновые киназы. Он участвует в основном в регулировании формы и движения клеток, воздействуя на цитоскелет.
Горные породы (ROCK1 и ROCK2 ) встречаются у млекопитающих (человек, крыса, мышь, корова), рыбок данио, Xenopus, беспозвоночные (C. elegans, комар, Дрозофила ) и курица. Human ROCK1 имеет молекулярная масса из 158кДа и является основным последующим эффектором малых GTPase RhoA. ROCK млекопитающих состоит из киназного домена, спиральная катушка регион и Гомология Плекстрина (PH) домен, который снижает киназную активность ROCK за счет аутоингибиторной внутримолекулярной складки, если RhoA-GTP отсутствует.[1][2]
ROCK крысы были открыты как первые эффекторы Rho, и они индуцируют образование стрессовые волокна и очаговые спайки фосфорилированием MLC (легкая цепь миозина).[3]В связи с этим фосфорилирование, то актин привязка миозин II и, таким образом, сократимость увеличивается. Две изоформы ROCK мыши ROCK1 и ROCK2 были идентифицированы. ROCK1 в основном экспрессируется в легкое, печень, селезенка, почка и яички. Однако ROCK2 распространяется в основном в мозг и сердце.[1][2][4]
Протеинкиназа C и Rho-ассоциированная протеинкиназа участвуют в регуляции поступления ионов кальция; эти ионы кальция, в свою очередь, стимулируют киназу легкой цепи миозина, вызывая сокращение.[5]
Функция
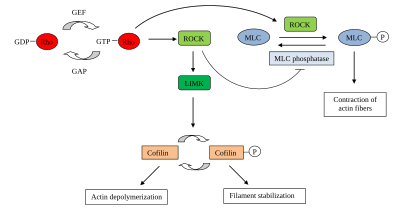
ROCK играет роль в широком спектре различных клеточных явлений, поскольку ROCK является последующим эффекторным белком небольшого GTPase Ро, который является одним из основных регуляторов цитоскелет.
1. ROCK является ключевым регулятором организации актина и, следовательно, регулятором миграция клеток следующее:
ROCK могут фосфорилировать различные субстраты, включая LIM. киназа, миозин легкая цепь (MLC) и MLC фосфатаза. Эти субстраты, после фосфорилирования, регулируют организацию и сократимость актиновых филаментов следующим образом:[2]
- Количество актиновых филаментов
ROCK косвенно подавляет деполимеризацию актиновых филаментов: ROCK фосфорилирует и активирует LIM киназа, который, в свою очередь, фосфорилирует АДФ / кофилин, тем самым инактивируя его активность деполимеризации актина. Это приводит к стабилизации актиновых филаментов и увеличению их количества. Таким образом, со временем количество мономеров актина, которые необходимы для продолжения полимеризации актина для миграции, становится ограниченным. Увеличение количества стабильных актиновых филаментов и потеря мономеров актина способствуют уменьшению миграции клеток.[2][6]
- Клеточная сократимость
ROCK также регулирует миграцию клеток, способствуя клеточной сокращение и, таким образом, контакты клетка-субстрат. ROCK увеличивает активность моторного белка миозин II двумя разными механизмами:
- Во-первых, фосфорилирование легкой цепи миозина (MLC ) увеличивает миозин II АТФаза Мероприятия. Таким образом, несколько связанных и активных миозинов, которые асинхронно активны на нескольких актиновых филаментах, перемещают актиновые филаменты друг против друга, что приводит к общему укорочению актиновых волокон.
- Во-вторых, ROCK инактивирует MLC. фосфатаза, что приводит к повышению уровня фосфорилированных MLC.
Таким образом, в обоих случаях активация ROCK с помощью Rho вызывает образование актина. стрессовые волокна, пучки актиновых нитей противоположной полярности, содержащие миозин II, тропомиозин, кальдесмон и MLC-киназу, и, следовательно, фокальные контакты, которые являются незрелыми интегрин -основные точки сцепления с внеклеточным субстратом.[2][7]
2. Другие функции и цели
- RhoA-GTP стимулирует активность фосфолипидфосфатазы PTEN (фосфатаза и гомолог тензина), человек опухоль белок-супрессор. Эта стимуляция, кажется, зависит от ROCK.[8][9] Таким образом, PTEN важен для предотвращения неконтролируемого деления клеток, как это имеет место в раковых клетках.
- ROCK играет важную роль в контроле клеточного цикла, он, по-видимому, препятствует преждевременному разделению двух центриоли в G1, и предполагается, что он необходим для сокращения борозды дробления, что необходимо для завершения цитокинез.[2][10][11][12][13][14]
- Скалы также, кажется, противодействуют инсулин сигнальный путь, приводящий к уменьшению размера клетки и влиянию на судьбу клетки.[2]
- Скалы играют роль в мембранные пузыри, морфологическое изменение, наблюдаемое в клетках, приверженных апоптоз. Проапоптотическая протеаза, каспаза 3, активирует активность киназы ROCK, отщепляя C-концевой домен PH. В результате аутоингибиторная внутримолекулярная складка ROCK отменяется. ROCK также регулирует фосфорилирование MLC и сократительную способность актомиозина, которые регулируют образование пузырей на мембране.[2]
- ROCK вносят свой вклад в нейрит отказ путем побуждения конус роста коллапс за счет активации сократимости актомиозина. Также возможно, что фосфорилирование белка-2 медиатора ответа на коллапсин (CRMP2) с помощью ROCK ингибирует функцию CRPM2, способствующую разрастанию аксонов, что приводит к коллапсу конуса роста.[2]
- ROCK регулируют межклеточную адгезию: потеря активности ROCK, по-видимому, приводит к потере целостности плотных контактов в эндотелиальных клетках. В эпителиальных клетках ингибирование ROCK, по-видимому, снижает целостность плотных соединений. Активный ROCK в этих клетках, по-видимому, стимулирует нарушение межклеточных контактов, опосредованных E-кадгерином, путем активации сократимости актомиозина.[2]
3. Другие цели ROCK
- NHE1 (водородообменник натрия, участвующий в фокальных адгезиях и организации актина)
- белки промежуточных филаментов: виментин, GFAP (глиальный фибриллярный кислый белок), NF-L (белок L нейрофиламента)
- Связывающие F-актин белки: аддуцин, EF-1 и альфа (фактор элонгации, кофактор трансляции), MARCKS (субстрат миристилированной аланин-богатой С-киназы), капонин (неизвестная функция) и ERM (участвующий в связывании цитоскелтона актина с плазматическая мембрана).
Гомологи
| Rho-ассоциированная, содержащая спиральную спираль протеинкиназа 1 | |||||||
|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||
| Символ | ROCK1 | ||||||
| Ген NCBI | 6093 | ||||||
| HGNC | 10251 | ||||||
| OMIM | 601702 | ||||||
| RefSeq | NM_005406 | ||||||
| UniProt | Q13464 | ||||||
| |||||||
| Rho-ассоциированная, содержащая спиральную спираль протеинкиназа 2 | |||||||
|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||
| Символ | ROCK2 | ||||||
| Ген NCBI | 9475 | ||||||
| HGNC | 10252 | ||||||
| OMIM | 604002 | ||||||
| RefSeq | NM_004850 | ||||||
| UniProt | O75116 | ||||||
| |||||||
Две изоформы ROCK мыши, ROCK1 и ROCK2 имеют высокий гомология. У них 65% аминокислота общие последовательности и 92% гомологии в их киназных доменах.[1][4]
ROCK гомологичны другим киназам многоклеточных животных, таким как киназа миотонической дистрофии (ДМПК ), DMPK-родственный белок контроля деления клеток 42 (Cdc42 ) -связывающие киназы (MRCK) и цитронкиназы. Все эти киназы состоят из N-концевого киназного домена, спиральной структуры и других функциональных элементов. мотивы на С-конце [2]
Регулирование
ROCK - это последующая эффекторная молекула Rho GTPase Rho, связанный с ним, увеличивает активность киназы ROCK.
Автоингибирование
Активность ROCK регулируется нарушением внутримолекулярного аутоингибирования. В общем, структура ROCK-белков состоит из N-концевого киназного домена, спирально-спиральной области и домена PH, содержащего богатый цистеином домен (CRD) на С-конце. Rho-связывающий домен (RBD) расположен в непосредственной близости от домена PH.
Активность киназы подавляется внутримолекулярный связывание между C-концевым кластером домена RBD и Домен PH к N-концевому киназному домену ROCK. Таким образом, активность киназы выключена, когда ROCK свернут внутримолекулярно. Активность киназы включается, когда Rho-GTP связывается с Rho-связывающим доменом ROCK, нарушая аутоингибирующее взаимодействие внутри ROCK, которое высвобождает киназный домен, потому что ROCK больше не сворачивается внутримолекулярно.[2]
Другие регуляторы
Также было показано, что Ро не единственный активатор РОК. ROCK также может регулироваться липидами, в частности арахидоновая кислота, и белок олигомеризация, который индуцирует N-концевое трансфосфорилирование.[2]
Болезнь
Эта секция нуждается в расширении. Вы можете помочь добавляя к этому. (Январь 2020) |
Исследования последних двух десятилетий показали, что передача сигналов ROCK играет важную роль во многих заболеваниях, включая сердечно-сосудистые заболевания,[15][16] нейродегенеративные заболевания, такие как Болезнь Альцгеймера, болезнь Паркинсона, и боковой амиотрофический склероз,[17] и рак.[18] Например, была выдвинута гипотеза, что ROCK играет важную роль в плейотропные эффекты статинов. ROCK1 / 2 вместе с киназами MRCKα / β вовлечены в пластичность миграции раковых клеток, феномен, который дает преимущество выживания раковых клеток во время лечения лекарственными препаратами (устойчивость к лекарству ).[19]
Исследователи разрабатывают Ингибиторы ROCK для лечения различных заболеваний, включая рак.[20][21] Например, такие лекарства обладают потенциалом предотвращения распространения рака, блокируя миграцию клеток, останавливая распространение раковых клеток в соседние ткани.[1]
Смотрите также
Рекомендации
- ^ а б c d Hahmann C, Schroeter T (январь 2010 г.). «Ингибиторы Rho-киназы как терапевтические средства: от пан-ингибирования до селективности изоформ». Клеточные и молекулярные науки о жизни. 67 (2): 171–7. Дои:10.1007 / s00018-009-0189-х. PMID 19907920. S2CID 6445354.
- ^ а б c d е ж грамм час я j k л м Риенто К., Ридли А.Дж. (июнь 2003 г.). «Камни: многофункциональные киназы в поведении клеток». Обзоры природы. Молекулярная клеточная биология. 4 (6): 446–56. Дои:10.1038 / nrm1128. PMID 12778124. S2CID 40665081.
- ^ Леунг Т., Чен XQ, Мансер Э, Лим Л. (октябрь 1996 г.). «РоА-связывающая киназа p160 ROK альфа является членом семейства киназ и участвует в реорганизации цитоскелета». Молекулярная и клеточная биология. 16 (10): 5313–27. Дои:10.1128 / mcb.16.10.5313. ЧВК 231530. PMID 8816443.
- ^ а б Накагава О, Фудзисава К., Исидзаки Т., Сайто Ю., Накао К., Нарумия С. (август 1996 г.). «ROCK-I и ROCK-II, две изоформы Rho-ассоциированной спиральной спирали, образующей серин / треонинкиназу у мышей». Письма FEBS. 392 (2): 189–93. Дои:10.1016/0014-5793(96)00811-3. PMID 8772201. S2CID 6684411.
- ^ Анджум I (июнь 2018 г.). «Механизмы сенсибилизации кальцием в гладких мышцах детрузора». Журнал фундаментальной и клинической физиологии и фармакологии. 29 (3): 227–235. Дои:10.1515 / jbcpp-2017-0071. PMID 29306925. S2CID 20486807.
- ^ Маэкава М., Ишизаки Т., Боку С., Ватанабэ Н., Фудзита А., Ивамацу А., Обината Т., Охаши К., Мизуно К., Нарумия С. (август 1999 г.). «Передача сигналов от Rho к актиновому цитоскелету через протеинкиназы ROCK и LIM-киназы». Наука. 285 (5429): 895–8. Дои:10.1126 / наука.285.5429.895. PMID 10436159.
- ^ Ван И, Чжэн XR, Риддик Н., Брайден М., Баур В., Чжан Х, Суркс, Гонконг (февраль 2009 г.). «Регулирование изоформ ROCK миозинфосфатазы и сократительной способности гладкомышечных клеток сосудов». Циркуляционные исследования. 104 (4): 531–40. Дои:10.1161 / CIRCRESAHA.108.188524. ЧВК 2649695. PMID 19131646.
- ^ Li Z, Dong X, Dong X, Wang Z, Liu W, Deng N, Ding Y, Tang L, Hla T, Zeng R, Li L, Wu D (апрель 2005 г.). «Регулирование PTEN с помощью малых GTPases Rho». Природа клеточной биологии. 7 (4): 399–404. Дои:10.1038 / ncb1236. PMID 15793569. S2CID 19316266.
- ^ «Ген Entrez: фосфатаза и гомолог тензина PTEN (мутировавший при множественных распространенных формах рака 1)».
- ^ Гао Си, Ли Си, Чен Дж, Пан Л., Сайто С., Терашита Т., Сайто К., Мияваки К., Шигемото К., Моминоки К., Мацуда С., Кобаяши Н. (2004). «Сигнальный путь Rho-ROCK регулирует основанный на микротрубочках процесс формирования культивируемых подоцитов - ингибирование удлинения процесса, вызванного ROCK». Нефрон Экспериментальная нефрология. 97 (2): e49–61. Дои:10.1159/000078406. PMID 15218323. S2CID 45342422.
- ^ Дрексел Д. Н., Хайман А. А., Холл А, Глоцер М. (январь 1997 г.). «Потребность в Rho и Cdc42 во время цитокинеза у эмбрионов Xenopus». Текущая биология. 7 (1): 12–23. Дои:10.1016 / S0960-9822 (06) 00023-6. PMID 8999996. S2CID 16144917.
- ^ Косако Х., Ёсида Т., Мацумура Ф., Ишизаки Т., Нарумия С., Инагаки М. (декабрь 2000 г.). «Rho-киназа / ROCK участвует в цитокинезе через фосфорилирование легкой цепи миозина, а не белков эзрин / радиксин / моэзин в борозде расщепления». Онкоген. 19 (52): 6059–64. Дои:10.1038 / sj.onc.1203987. PMID 11146558. S2CID 39115039.
- ^ Ясуи Ю., Амано М., Нагата К., Инагаки Н., Накамура Х., Сая Х., Кайбути К., Инагаки М. (ноябрь 1998 г.). «Роль Rho-ассоциированной киназы в цитокинезе; мутации в сайтах фосфорилирования Rho-ассоциированной киназы нарушают цитокинетическую сегрегацию глиальных филаментов». Журнал клеточной биологии. 143 (5): 1249–58. Дои:10.1083 / jcb.143.5.1249. ЧВК 2133074. PMID 9832553.
- ^ Пекны А.Ю., Сеть ЧП (июнь 2002 г.). «Rho-связывающая киназа (LET-502) и миозинфосфатаза (MEL-11) регулируют цитокинез в раннем эмбрионе Caenorhabditis elegans». Журнал клеточной науки. 115 (Pt 11): 2271–82. PMID 12006612.
- ^ Sladojevic N, Yu B, Liao JK (декабрь 2017 г.). «РОК как терапевтическая мишень при ишемическом инсульте». Экспертный обзор нейротерапии. 17 (12): 1167–1177. Дои:10.1080/14737175.2017.1395700. ЧВК 6221831. PMID 29057688.
- ^ Ю Б., Сладоевич Н., Блэр Дж. Э., Ляо Дж. К. (январь 2020 г.). «Нацеленность на Rho-ассоциированную спиралевидную формирующую протеинкиназу (ROCK) при сердечно-сосудистом фиброзе и повышении жесткости». Мнение экспертов о терапевтических целях. 24 (1): 47–62. Дои:10.1080/14728222.2020.1712593. ISSN 1744-7631. ЧВК 7662835. PMID 31906742. S2CID 210043399.
- ^ Чонг CM, Ай Н, Ли С.М. (2017). «РОК в ЦНС: различные роли изоформ и терапевтическая мишень для нейродегенеративных заболеваний». Текущие цели в отношении лекарств. 18 (4): 455–462. Дои:10.2174/1389450117666160401123825. ISSN 1873-5592. PMID 27033194.
- ^ Вэй Л., Сурма М., Ши С., Ламберт-Читам Н., Ши Дж. (Август 2016 г.). «Новое понимание роли Rho Kinase в раке». Archivum Immunologiae et Therapiae Experimentalis. 64 (4): 259–78. Дои:10.1007 / s00005-015-0382-6. ЧВК 4930737. PMID 26725045.
- ^ Кале, Виджай Пралхад; Hengst, Jeremy A .; Desai, Dhimant H .; Amin, Shantu G .; Юн, Чон К. (01.06.2015). «Регуляторная роль киназ ROCK и MRCK в пластичности миграции раковых клеток». Письма о раке. 361 (2): 185–196. Дои:10.1016 / j.canlet.2015.03.017. ISSN 0304-3835. PMID 25796438.
- ^ Кале, Виджай Пралхад; Hengst, Jeremy A .; Desai, Dhimant H .; Дик, Тарин Э .; Чоу, Кэтрин Н .; Колледж, Эшли Л .; Такахаши, Ёсинори; Сун, Шен-Шу; Amin, Shantu G .; Юн, Чон К. (28 ноября 2014 г.). «Новый селективный мультикиназный ингибитор ROCK и MRCK эффективно блокирует миграцию и инвазию раковых клеток». Письма о раке. 354 (2): 299–310. Дои:10.1016 / j.canlet.2014.08.032. ISSN 0304-3835. ЧВК 4182185. PMID 25172415.
- ^ Фэн Й., Лограссо П.В., Деферт О., Ли Р. (март 2016 г.). «Ингибиторы Rho-киназы (ROCK) и их терапевтический потенциал». Журнал медицинской химии. 59 (6): 2269–2300. Дои:10.1021 / acs.jmedchem.5b00683. ISSN 1520-4804. PMID 26486225.
