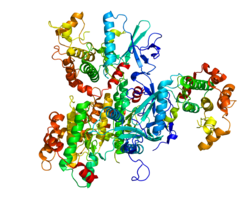
MAP2K6 - MAP2K6
Митоген-активированная протеинкиназа киназа 6 с двойной специфичностью также известный как MAP киназа киназа 6 (MAPKK 6) или MAPK / ERK киназа 6 является фермент что у людей кодируется MAP2K6 ген, на хромосома 17.[5]
Функция
MAPKK 6 является членом семейства протеинкиназ с двойной специфичностью, которое функционирует как митоген-активированный белок (MAP) киназа киназа. Киназы MAP, также известный как киназы, регулируемые внеклеточными сигналами (ERK), действуют как точка интеграции для множества биохимических сигналов. Этот белок фосфорилаты и активирует p38 MAP киназа в ответ на воспалительный цитокины или экологический стресс. Как важный компонент опосредованной киназой p38 MAP путь передачи сигнала, этот ген участвует во многих клеточных процессах, таких как остановка клеточного цикла, вызванная стрессом, транскрипция активация и апоптоз.[6]
Взаимодействия
MAP2K6 был показан взаимодействовать с ТАОК2,[7] ASK1,[8][9] MAPK14[7][10][11][12] и MAP3K7.[13][14][15][16]
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000108984 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000020623 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Хан Дж., Ли Дж. Д., Цзян Й, Ли З, Фэн Л., Улевич Р. Дж. (Февраль 1996 г.). «Характеристика структуры и функции новой киназы MAP-киназы (MKK6)». Журнал биологической химии. 271 (6): 2886–91. Дои:10.1074 / jbc.271.6.2886. PMID 8621675.
- ^ «Ген Entrez: MAP2K6 митоген-активированная протеинкиназа киназа 6».
- ^ а б Чен З., Кобб М.Х. (май 2001 г.). «Регулирование киназных путей митоген-активированного протеина (MAP), чувствительного к стрессу, с помощью TAO2». Журнал биологической химии. 276 (19): 16070–5. Дои:10.1074 / jbc.M100681200. PMID 11279118.
- ^ Хуанг С., Шу Л., Диллинг М.Б., Истон Дж., Харвуд ФК, Итиджо Х., Хоутон П.Дж. (июнь 2003 г.). «Устойчивая активация каскада JNK и апоптоз, индуцированный рапамицином, подавляются p53 / p21 (Cip1)». Молекулярная клетка. 11 (6): 1491–501. Дои:10.1016 / S1097-2765 (03) 00180-1. PMID 12820963.
- ^ Морита К., Сайто М., Тобиуме К., Мацуура Х., Эномото С., Нишито Х., Итиджо Х. (ноябрь 2001 г.). «Регулирование отрицательной обратной связи ASK1 протеинфосфатазой 5 (PP5) в ответ на окислительный стресс». Журнал EMBO. 20 (21): 6028–36. Дои:10.1093 / emboj / 20.21.6028. ЧВК 125685. PMID 11689443.
- ^ Санс-Морено В., Касар Б., Креспо П. (май 2003 г.). «Изоформа p38alpha Mxi2 связывается с регулируемой внеклеточными сигналами киназой 1 и митоген-активируемой протеинкиназой 2 и регулирует ее ядерную активность, поддерживая уровни фосфорилирования». Молекулярная и клеточная биология. 23 (9): 3079–90. Дои:10.1128 / MCB.23.9.3079-3090.2003. ЧВК 153192. PMID 12697810.
- ^ Рейнго Дж., Уитмарш А.Дж., Барретт Т., Дерихард Б., Дэвис Р.Дж. (март 1996 г.). «Экспрессия гена, регулируемая MKK3 и MKK6, опосредована сигнальным путем передачи сигнала митоген-активируемой протеинкиназы p38». Молекулярная и клеточная биология. 16 (3): 1247–55. Дои:10.1128 / mcb.16.3.1247. ЧВК 231107. PMID 8622669.
- ^ Штейн Б., Брэди Х., Ян М.Х., Янг Д. Б., Барбоза М. С. (май 1996 г.). «Клонирование и характеристика MEK6, нового члена каскада митоген-активируемых протеинкиназ-киназ». Журнал биологической химии. 271 (19): 11427–33. Дои:10.1074 / jbc.271.19.11427. PMID 8626699.
- ^ Иситани Т., Такаэсу Г., Ниномия-Цудзи Дж., Сибуя Х., Гейнор Р. Б., Мацумото К. (декабрь 2003 г.). «Роль TAB2-родственного белка TAB3 в передаче сигналов IL-1 и TNF». Журнал EMBO. 22 (23): 6277–88. Дои:10.1093 / emboj / cdg605. ЧВК 291846. PMID 14633987.
- ^ Ван С., Дэн Л., Хун М., Аккараджу Г.Р., Иноуэ Дж., Чен З.Дж. (июль 2001 г.). «TAK1 представляет собой убиквитин-зависимую киназу MKK и IKK». Природа. 412 (6844): 346–51. Дои:10.1038/35085597. PMID 11460167. S2CID 9641806.
- ^ Ниномия-Цудзи Дж., Кисимото К., Хияма А., Иноуэ Дж., Цао З., Мацумото К. (март 1999 г.). «Киназа TAK1 может активировать NIK-I kappaB, а также каскад киназ MAP в пути передачи сигнала IL-1». Природа. 398 (6724): 252–6. Дои:10.1038/18465. PMID 10094049. S2CID 4421236.
- ^ Сакурай Х., Миёси Х., Мизуками Дж., Сугита Т. (июнь 2000 г.). «Зависимая от фосфорилирования активация киназы киназы протеинкиназы, активируемой митогеном TAK1, с помощью TAB1». Письма FEBS. 474 (2–3): 141–5. Дои:10.1016 / S0014-5793 (00) 01588-X. PMID 10838074. S2CID 30831863.
дальнейшее чтение
- Бен-Леви Р., Хупер С., Уилсон Р., Патерсон Х. Ф., Маршалл С. Джей (сентябрь 1998 г.). «Ядерный экспорт стресс-активированной протеинкиназы p38, опосредованный ее субстратом MAPKAP kinase-2». Текущая биология. 8 (19): 1049–57. Дои:10.1016 / S0960-9822 (98) 70442-7. PMID 9768359. S2CID 15627349.
- Танака С., Накамура К., Такахаси Н., Суда Т. (декабрь 2005 г.). «Роль RANKL в физиологической и патологической резорбции кости и терапии, нацеленной на сигнальную систему RANKL-RANK». Иммунологические обзоры. 208: 30–49. Дои:10.1111 / j.0105-2896.2005.00327.x. PMID 16313339. S2CID 13811917.
- Доза Ю.Н., Куэнда А., Томас Г.М., Коэн П., Небреда А.Р. (май 1995 г.). «Активация RK, гомолога MAP-киназы, требует фосфорилирования Thr-180 и Tyr-182, и оба остатка фосфорилируются в химически стрессированных клетках KB». Письма FEBS. 364 (2): 223–8. Дои:10.1016 / 0014-5793 (95) 00346-Б. PMID 7750576. S2CID 25025858.
- Маруяма К., Сугано С. (январь 1994 г.). «Олиго-кэппинг: простой метод замены кэп-структуры эукариотических мРНК олигорибонуклеотидами». Ген. 138 (1–2): 171–4. Дои:10.1016/0378-1119(94)90802-8. PMID 8125298.
- Рейнго Дж., Уитмарш А.Дж., Барретт Т., Дерихард Б., Дэвис Р.Дж. (март 1996 г.). «Экспрессия гена, регулируемая MKK3 и MKK6, опосредована путем передачи сигнала митоген-активируемой протеинкиназы p38». Молекулярная и клеточная биология. 16 (3): 1247–55. Дои:10.1128 / mcb.16.3.1247. ЧВК 231107. PMID 8622669.
- Штейн Б., Брэди Х., Ян М.Х., Янг Д. Б., Барбоза М. С. (май 1996 г.). «Клонирование и характеристика MEK6, нового члена каскада митоген-активируемых протеинкиназ-киназ». Журнал биологической химии. 271 (19): 11427–33. Дои:10.1074 / jbc.271.19.11427. PMID 8626699.
- Моригути Т., Куроянаги Н., Ямагути К., Гото Й, Ирие К., Кано Т., Сиракабе К., Муро Ю., Сибуя Х., Мацумото К., Нисида Е., Хагивара М. (июнь 1996 г.). «Новый каскад киназ, опосредованный митоген-активированной протеинкиназой киназой 6 и MKK3». Журнал биологической химии. 271 (23): 13675–9. Дои:10.1074 / jbc.271.23.13675. PMID 8663074.
- Куэнда А., Алонсо Дж., Моррис Н., Джонс М., Мейер Р., Коэн П., Небреда А. Р. (август 1996 г.). «Очистка и клонирование кДНК SAPKK3, основного активатора RK / p38 в моноцитах и эпителиальных клетках, стимулированных стрессом и цитокинами». Журнал EMBO. 15 (16): 4156–64. Дои:10.1002 / j.1460-2075.1996.tb00790.x. ЧВК 452138. PMID 8861944.
- Годерт М., Куэнда А., Кракстон М., Джейкс Р., Коэн П. (июнь 1997 г.). «Активация новой стресс-активируемой протеинкиназы SAPK4 цитокинами и клеточными стрессами опосредуется SKK3 (MKK6); сравнение ее субстратной специфичности со специфичностью других киназ SAP». Журнал EMBO. 16 (12): 3563–71. Дои:10.1093 / emboj / 16.12.3563. ЧВК 1169981. PMID 9218798.
- Судзуки Ю., Ёситомо-Накагава К., Маруяма К., Суяма А., Сугано С. (октябрь 1997 г.). «Создание и характеристика полноразмерной библиотеки кДНК, обогащенной по 5'-концу». Ген. 200 (1–2): 149–56. Дои:10.1016 / S0378-1119 (97) 00411-3. PMID 9373149.
- Enslen H, Raingeaud J, Davis RJ (январь 1998 г.). «Селективная активация изоформ киназы митоген-активированного протеина p38 (MAP) киназами MAP-киназы MKK3 и MKK6». Журнал биологической химии. 273 (3): 1741–8. Дои:10.1074 / jbc.273.3.1741. PMID 9430721.
- Чан-Хуэй П.Ю., Уивер Р. (декабрь 1998 г.). «Киназа митоген-активируемой протеинкиназы человека опосредует вызванную стрессом активацию каскадов митоген-активируемой протеинкиназы». Биохимический журнал. 336 (Pt 3): 599–609. Дои:10.1042 / bj3360599. ЧВК 1219910. PMID 9841871.
- Чен З., Хатчисон М., Кобб М.Х. (октябрь 1999 г.). «Выделение протеинкиназы TAO2 и идентификация ее митоген-активируемой протеинкиназы / регулируемого внеклеточным сигналом киназного домена связывания киназы». Журнал биологической химии. 274 (40): 28803–7. Дои:10.1074 / jbc.274.40.28803. PMID 10497253.
- Cong F, Goff SP (ноябрь 1999 г.). «c-Abl-индуцированный апоптоз, но не остановка клеточного цикла, требует активации митоген-активируемой протеинкиназы киназы 6». Труды Национальной академии наук Соединенных Штатов Америки. 96 (24): 13819–24. Дои:10.1073 / пнас.96.24.13819. ЧВК 24148. PMID 10570156.
- Ван Х, Макгоуэн СН, Чжао М., Хе Л., Дауни Дж.С., Фернс К., Ван И, Хуанг С., Хан Дж. (Июль 2000 г.). «Участие каскада MKK6-p38gamma в остановке клеточного цикла, вызванной гамма-излучением». Молекулярная и клеточная биология. 20 (13): 4543–52. Дои:10.1128 / MCB.20.13.4543-4552.2000. ЧВК 85840. PMID 10848581.
- Висконти Р., Гадина М., Кьяриелло М., Чен Э. Х., Станкато Л. Ф., Гуткинд Дж. С., О'Ши Дж. Дж. (Сен 2000). «Важность пути MKK6 / p38 для индуцированного интерлейкином-12 фосфорилирования серина STAT4 и транскрипционной активности». Кровь. 96 (5): 1844–52. Дои:10.1182 / кровь.V96.5.1844. PMID 10961885.
- Флеминг Ю., Армстронг К. Г., Моррис Н., Патерсон А., Годерт М., Коэн П. (ноябрь 2000 г.). «Синергетическая активация изоформ N-концевой киназы (SAPK1 / JNK) активируемой стрессом протеинкиназы 1 / c-Jun» митоген-активируемой протеинкиназой киназы 4 (MKK4) и MKK7 ». Биохимический журнал. 352 Pt 1 (Pt 1): 145–54. Дои:10.1042/0264-6021:3520145. ЧВК 1221441. PMID 11062067.
- Витале Дж., Бернарди Л., Наполитани Дж., Мок М, Монтекукко С. (декабрь 2000 г.). «Чувствительность членов семейства митоген-активируемых протеинкиназ киназ к протеолизу летальным фактором сибирской язвы». Биохимический журнал. 352 Pt 3 (Pt 3): 739–45. Дои:10.1042/0264-6021:3520739. ЧВК 1221512. PMID 11104681.