Циклинзависимая киназа 5 - Cyclin-dependent kinase 5
Циклинзависимая киназа 5 представляет собой белок, а точнее фермент, который кодируется геном Cdk5. Он был открыт 15 лет назад, и он явно выражается в постмитотических нейронах центральной нервной системы (ЦНС).
Молекула относится к циклинзависимым киназа семья. Киназы - это ферменты, которые катализируют реакции фосфорилирования, процесс, который позволяет субстрату получать фосфатную группу, предоставленную органическим соединением, известным как АТФ. Фосфорилирование жизненно важно во время гликолиз Таким образом, киназы становятся важной частью клетки из-за их роли в метаболизме, передаче сигналов в клетке и многих других процессах.
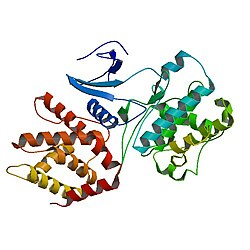
Структура
Cdk5 - это пролин-направленная серин / треониновая киназа, которая была впервые идентифицирована как член семейства CDK из-за ее структуры, аналогичной CDC2 / CDK1 у человека, белку, который играет решающую роль в регуляции клеточного цикла.
Ген Cdk5 содержит 12 экзонов в области, содержащей около 5000 нуклеотидов (5kb), как это было определено Ohshima после клонирования гена Cdk5, принадлежащего мыши.
Cdk5 содержит 292 аминокислоты и представляет собой структуру как α-спирали, так и β-цепи.[5]
Несмотря на то, что Cdk5 имеет структуру, аналогичную другим циклин-зависимым киназам, его активаторы очень специфичны (CDK5R1 и CDK5R2 ).
Некоторые расследования[6] сообщили, что активные состояния протеинкиназ структурно отличаются друг от друга, чтобы сохранить геометрию их механизмов, так что каталитический выход работает должным образом. Киназа Cdk5 также имеет оригинальный дизайн.
Cdk5 принадлежит к эукариотическим протеинкиназам (ePKs). Кристаллическая структура каталитического домена цАМФ-зависимая протеинкиназа показал, что держит 2 доли; с одной стороны, он имеет небольшую долю, N-конец, расположенный как антипараллельную структуру β-листа, кроме того, он содержит нуклеотидные мотивы как способ ориентировать нуклеотид для переноса фосфора. С другой стороны, большой лепесток, С-конец, спиральной формы, который помогает идентифицировать субстрат и включает важные остатки для переноса фосфора.

Физиологическая роль
Боль
Недавно Cdk5 стал важной киназой в сенсорных путях. Недавние сообщения Pareek et al. предполагают его необходимость в передаче сигналов боли. Фактически, CDK5 необходим для правильного развития мозга и для активации он должен ассоциироваться с CDK5R1 или же CDK5R2.[7][8] В отличие от других циклинзависимых киназ, CDK5 также не требует фосфорилирование на Т-петле, следовательно, связывания с активатором достаточно для активации киназы.[9]
Нейроны
Cdk5 присутствует в большом количестве и в основном экспрессируется в нейронах, где он фосфорилирует белковые полимеры с высокой молекулярной массой, называемые нейрофиламентами, и связанный с микротрубочками белок тау, которых много в ЦНС (центральной нервной системе).[10] Фермент участвует во многих аспектах развития и функций нейронов.
Когда речь идет о нейронах, основная роль Cdk5 заключается в обеспечении правильной миграции нейронов. Нейроны будут посылать и дендриты, и аксоны, чтобы формировать связи с другими нейронами для передачи информации, а Cdk5 регулирует этот процесс. Для работы Cdk5 должен быть активирован p35 (эти 3 аминокислоты, Asp-259, Asn-266 и Ser-270, участвуют в образовании водородных связей с Cdk5.[11]) или p39 (изоформа p35), которые являются двумя из его нейрон-специфичных регуляторных субъединиц. Это означает, что уровень экспрессии p35 и p39 будет связан с активностью фермента: если во время развития мозга наблюдается высокая активность Cdk5, будет высокая экспрессия его активаторов. Фактически, когда исследования проводились на мышах без p35 и p39, результаты были такими же, как и на мышах без Cdk5: наблюдались явные нарушения ламинарных структур в коре головного мозга, обонятельной луковице, гиппокампе. и мозжечок. Правильное развитие и функциональность этих областей полностью зависит от Cdk5, который зависит от правильной экспрессии p35 и p39. Также Cdk5 сотрудничает с Reelin передача сигналов, чтобы гарантировать правильную миграцию нейронов в развивающемся мозге.
Cdk5 не только участвует в миграции нейронов, фермент также помогает управлять расширением нейритов, образованием синапсов и синаптической передачей. Также стоит отметить, что Cdk5 также регулирует процесс апоптоза, который необходим для обеспечения правильности формируемых нейронных связей. Более того, из-за того, что Cdk5 также участвует в регуляции синаптической пластичности, он участвует в процессах обучения и формирования памяти, а также в создании наркозависимости.
Вдобавок к этому, Cdk5 модулирует динамику актина-цитоскелета, фосфорилируя Pak1 и филамин 1, и регулирует микротрубочки, также фосфорилируя тау, MAP1B, даблкортин, Nudel и CRMP, которые являются белками, связанными с микротрубочками. Неправильная экспрессия Cdk5 вызовет дефекты в этих субстратах, которые могут привести к множественным заболеваниям. Например, дефект филамина 1 у человека вызывает перивентрикулярную гетеротопию; а дефект Lis1 и даблкортинов вызовет лиссэнцефалию 1 типа. Фактически, четыре члена кровной израильской мусульманской семьи, страдающей лизэнцефалией-7 с гипоплазией мозжечка, имели мутация сайта сплайсинга в гене Cdk5.[12][13]
Злоупотребление наркотиками
Было доказано, что Cdk5 напрямую связан со злоупотреблением наркотиками. Мы знаем, что лекарства действуют в системе вознаграждения, достигая своего действия, нарушая пути передачи внутриклеточного сигнала. Cdk5 участвует в этих нейросигналах.[14] Пристрастие к наркотикам - явное следствие нейрональной зависимости и поведенческих пластичность. Когда потребление наркотиков становится повторяющейся привычкой, это изменяет несколько компонентов передачи сигналов дофамина, изменения в экспрессии генов и изменения в нейронных схемах дофаминоцептивных нейронов.
Если взять пример кокаина, его действие вызвано: CREB (Связывание ответного элемента цАМФ), что приводит к временному всплеску экспрессии немедленных ранних генов в полосатом теле, а также от ΔFosB (который накапливается и сохраняется в нейронах полосатого тела при регулярном употреблении препарата). Многие исследования показали, что сверхэкспрессия ΔFosB из-за злоупотребления наркотиками является причиной повышающей регуляции Cdk5 (поскольку он находится ниже ΔFosB в полосатом теле, включая прилежащее ядро).
Давайте теперь посмотрим на роль Cdk5 во всем этом. Было обнаружено, что при воздействии наркотиков, таких как кокаин, и при избыточном присутствии ΔFosB количество Cdk5 увеличивается. Это происходит из-за этих двух факторов, активирующих p35, который активирует выработку белка Cdk5.
Также было продемонстрировано, что этот фермент играет важную роль в регуляции нейротрансмиссии дофамина. Действительно, Cdk5 способен изменять дофаминовую систему путем фосфорилирования DARPP-32. Мы знаем, что прилежащее ядро связано с наркозависимостью. Как следствие увеличения количества Cdk5, также увеличивается количество точек ветвления дендритов и шипов, как средние шиповатые нейроны в прилежащее ядро и пирамидные нейроны в медиальная префронтальная кора. Следовательно, это связано со злоупотреблением наркотиками и, в частности, с системой вознаграждения, которая запускается потреблением наркотиков.

Дальнейший анализ взаимосвязи между долей Cdk5 и эффектами лекарств показал, что существуют значительные различия в зависимости от дозы и частоты употребления лекарства.[15] Например, если частота приема дозы кокаина действительно распределена во времени или сосредоточена в единичном и длительном периоде времени, эффекты кокаина будут присутствовать, даже если производство Cdk5 в прилежащем ядре, в вентральная тегментальная область и префронтальная кора не увеличится. Однако, когда дело доходит до частых доз, значительно близких по времени, эффекты кокаина не проявляются, несмотря на повышенную долю Cdk5. Эти различия можно объяснить тем фактом, что Cdk5 является переходным состоянием к чрезмерному воздействию наркотиков, таких как кокаин.
Теперь вся эта информация должна быть сосредоточена на поиске терапевтического применения Cdk5, которое может уменьшить чувство награды при регулярном употреблении наркотиков. Прежде всего, было доказано, что антагонист Cdk5 после длительного его использования работает как ингибитор роста шиповидных дендритов в нейронах прилежащего ядра. Таким образом, мы можем лечить зависимости. Во-вторых, его можно использовать как способ диагностики злоупотребления наркотиками, если мы решим контролировать количество Cdk5 у пациента. Это возможно, потому что Cdk5 производится только в качестве награды за употребление наркотиков, но не в качестве посредника или естественного вознаграждения.
Поджелудочная железа
Хотя основная роль Cdk5 связана с миграцией нейронов, его влияние на организм человека не ограничивается нервной системой. Действительно, Cdk5 играет важную роль в управлении инсулин секреция поджелудочной железы.
На самом деле этот фермент был обнаружен в поджелудочной железе. β клетки и было доказано, что снижает экзоцитоз инсулина за счет фосфорилирование L-VDCC (L-тип, зависимый от напряжения Ca2+ канал).[16]
Иммунная система
В течение Т-клетка активации, Cdk5 фосфорилирует коронин 1a, белок, который способствует процессу фагоцитоз и регулирует актин поляризация. Следовательно, эта киназа способствует выживанию и подвижности Т-клеток.[17]
Cdk5 также принимает участие в производстве интерлейкин 2 (IL-2), цитокин, участвующий в клеточная сигнализация, Т-клетками. Для этого он нарушает репрессию транскрипции интерлейкина 2 посредством Гистоновая деацетилаза 1 (HDAC1) через фосфорилирование белка mSin3a. Это снижает способность комплекса HDAC1 / mSin3a связываться с промотором IL-2, что приводит к увеличению продукции интерлейкина 2.[18]
Регуляция экзоцитоза
Экзоцитоз синаптических везикул также регулируется с помощью CdK5 с фосфорилированием белка munc-18-a, который необходим для секреции, поскольку он имеет большое сродство с производным рецептора SNAP (белок SNARE). Это фосфорилирование было продемонстрировано при моделировании секреции нейроэндокринных клеток, поскольку активность Cdk5 увеличивалась. Когда Cdk5 был удален, секреция норэпинефрина уменьшилась.[19]
объем памяти
Благодаря эксперименту на мышах была продемонстрирована связь между памятью и Cdk5. С одной стороны, мыши не проявляли страха, интегрированного с предыдущей активностью, когда Cdk5 был инактивирован. С другой стороны, когда активность ферментов увеличилась в гиппокампе, где хранятся воспоминания, страх снова появился.
Ремоделирование актинового цитоскелета в головном мозге
В течение эмбриогенез, Cdk5 необходим для развития мозга, так как он имеет решающее значение для регуляции цитоскелет это, в свою очередь, важно для ремоделирования мозга.[20] Несколько нейронных процессов: передача сигналов о боли, наркомания, изменения поведения, формирование воспоминаний и обучение, связанные с развитием мозга, происходят в результате быстрых изменений цитоскелета. Негативное ремоделирование цитоскелета нейронов будет связано с потерей синапсы и нейродегенерация при заболеваниях мозга, когда активность Cdk5 нарушена. Следовательно, большая часть субстратов Cdk5 связана с актиновым скелетом; как физиологические, так и патологические. Некоторые из них были идентифицированы в последние десятилетия: эфексин1, p27, Mst3, CaMKv, калирин-7, RasGRF2, Pak1, WAVE1, нейрабин-1, TrkB, 5-HT6R, талин, дребрин, синапсин I, синапсин III, CRMP1. , GKAP, SPAR, PSD-95 и LRRK2.[20]
Регулировка циркадных часов
Млекопитающее циркадные часы контролируется Cdk5 с фосфорилированием PER2.[21][22] В лаборатории Cdk5 был заблокирован в SCN (супрахиазматические ядра, главный осциллятор циркадной системы), следовательно, период автономной работы у мышей был сокращен. В течение суточного периода PER2[23] (по остатку серина 394) фосфорилировался Cdk5, таким образом, криптохром 1 (CRY1[24]) мог легко взаимодействовать с ним, и комплекс PER2-CRY1 перешел в ядро. Молекулярный циркадный цикл и период устанавливаются должным образом благодаря задаче Cdk5 как ядерного двигателя этих белков.
Регулятор апоптоза клеток и выживаемости клеток
В дополнение ко всем ранее упомянутым ролям, Cdk5 участвует во многих клеточных функциях, таких как выживание подвижности клеток, апоптоз, и генная регуляция.[25][26]
Плазматическая мембрана, цитозоль и перинуклеарная область - это места, где обнаруживаются активаторы Cdk5 / p35. Тем не менее, Cdk5 также можно активировать с помощью циклин I, этот регулятор вызывает увеличение экспрессии белков семейства BCl-2, которые связаны с антиапоптотическими функциями.
Роль в болезни
Химическое объяснение широкого спектра неврологических расстройств привело к появлению Cdk5; Аномальное фосфорилирование тау-белка - это патологическое действие, осуществляемое этой киназой, и нейрофибриллярные сплетения являются следствием.
Нейродегенеративные заболевания
Cdk5 играет важную роль в центральной нервной системе. В процессе эмбриогенеза эта киназа необходима для развития мозга; а во взрослом мозге Cdk5 необходим для многих нейрональных процессов; например, обучение и формирование воспоминаний. Тем не менее, если активность Cdk5 нарушена, это может привести к действительно серьезным неврологическим заболеваниям, включая болезнь Альцгеймера, Паркинсона, рассеянный склероз и болезнь Хантингтона.[27]
- Болезнь Альцгеймера (БА)[28] отвечает за 50-70% всех случаев деменции. Некоторые исследования показали, что избыток активности Cdk5, пролин-направленной протеинкиназы, приводит к тау гиперфосфорилирование - процесс, который наблюдается у многих пациентов с БА. Активаторы cdk5, p35 и p39 (оба являются миристоилированный белки, которые прикреплены к клеточным мембранам), могут расщепляться кальций-активированным кальпаином до p25 и p29. Это приведет к миграции белков из клеточной мембраны как в ядерную, так и в перинуклеарную области и к нарушению регуляции активности Cdk5. У p25 и p29 период полураспада в 5-10 раз больше, чем у p35 и p39. Это невероятно проблематично из-за того, что может привести к накоплению активаторов Cdk5 и избытку активности Cdk5, что затем вызывает гиперфосфорилирование тау. Вдобавок к этому повышение уровня Aβ также может приводить к гиперфосфорилированию тау-белка за счет стимуляции выработки p25. Следовательно, Cdk5 может быть потенциальной лекарственной мишенью для лечения пациентов с AD, поскольку его ингибирование может снизить гиперфосфорилирование тау-белка и, следовательно, уменьшить образование NFT (нейрофибриллярных клубков) и замедлить процесс нейродегенерации.[29]
- Болезнь Хантингтона (БХ) - еще одно нейродегенеративное заболевание, которое в некоторой степени связано с активностью Cdk5. Родственный динамину белок 1 (Drp1 ) является важным элементом деления митохондрий. Cdk5 может изменять субклеточное распределение Drp1 и его активность. Фактически, было замечено, что ингибирование чрезмерно активной киназы позволяет Drp1 функционировать должным образом при фрагментации митохондрий, чтобы избежать нейротоксичности в мозге. Вдобавок к этому, Cdk5 может влиять на изменение морфологии митохондрий или их трансмембранного потенциала, что может привести к гибели клеток и нейродегенерации. Это означает, что Cdk5 является возможной терапевтической мишенью для лечения митохондриальной дисфункции, которая приводит к развитию HD.[30]

- болезнь Паркинсона (PD):[31] Считается, что Cdk5 тесно связан с болезнью Паркинсона. Это нейродегенеративное заболевание вызвано прогрессирующей потерей нервных клеток в части мозга, называемой черная субстанция, среди прочего. Cdk5 способен образовывать комплекс с p25 (пептид расщепления p35): Cdk5 / p25. P25 приведет к гиперактивности Cdk5. Результатом образования этого комплекса является апоптоз нервных клеток и нейровоспаление. Это открытие можно использовать для лечения болезни Паркинсона. Чтобы ингибировать комплекс Cdk5 / p25, мы могли бы использовать антагонист Cdk5: CIP. Результаты этого лечения были на удивление положительными. Действительно, мы можем заметить, что не только симптомы болезни Паркинсона уменьшились, но также оказалось, что CIP защищает от потери дофаминергических нейронов в черной субстанции.
- Рассеянный склероз (РС):[32] одно из заболеваний, при котором не удается провести ремиелинизацию[33] может спровоцировать стойкое повреждение аксонов и необратимую потерю функции. Циклинзависимая киназа 5 участвует в этом процессе, поскольку регулирует олигодендроцит (Развитие OL9 и миелинизация в ЦНС). Ингибиторы Cdk5 препятствуют ремиелинизации и нарушают активность нервных клеток. Низкая экспрессия MBP и протеолипидного белка, а также уменьшение количества миелинизированных аксонов указывают на отсутствие репарации миелина.
Рак
Cdk5 участвует в инвазивном раке, по-видимому, за счет снижения активности актин регуляторный белок Caldesmon.[34]
Хотя Cdk5 не мутирует в раковых тканях, его активность и экспрессия нарушены. Киназы фосфорилируют опухолевые супрессоры и факторы транскрипции, которые участвуют в развитии клеточного цикла. Cdk5 участвует в пролиферации опухолей, миграции, ангиогенез а также устойчивость к химиотерапии и противоопухолевый иммунитет. Он также участвует в сигнальных путях, которые приводят к метастаз, и он регулирует цитоскелет и очаговые спайки.[35]
| Возможные механизмы ангиогенеза, опосредованные Cdk5 | |
|---|---|
| Согласно исследованию аденом гипофиза, Cdk5 способствует экспрессии фактора роста эндотелия сосудов (VEGF), белка, который регулирует васкулогенез и ангиогенез. VEGF стимулирует деление и миграцию эндотелиальных клеток, а также проницаемость сосудов.[36] | |
| Cdk5 способствует ангиогенезу путем ремоделирования актинового цитоскелета через Rac1, сигнальную GTPase. Он также может регулировать образование ламеллиподий, которые представляют собой выступы мембраны, участвующие в миграции клеток.[37] | |
| Фосфорилирование Cdk5 и активация пресенилина стимулирует NICD (внутриклеточный домен Notch). Как следствие, активируется Notch-зависимая передача сигналов, ключевой путь, способствующий ангиогенезу.[38] |
Возможное лечение рака может заключаться в нацеливании на Cdk5 и предотвращении его связывания с его активаторами и субстратами.
В недавних исследованиях[39] Что касается лучевой терапии у пациентов с крупноклеточным раком легких, было обнаружено, что истощение CDK5 снижает развитие рака легких и лучевую устойчивость in vitro и in vivo. Было продемонстрировано, что снижение Cdk5 снижает экспрессию TAZ,[40] компонент Гипоталамус путь. В результате эта потеря ослабляет активацию сигнала из гипоталамуса. Следовательно, Cdk5 можно рассматривать как мишень для борьбы с раком легких.
История
CDK5 изначально был назван NCLK (нейрональная CDC2-подобная киназа) из-за сходного мотива фосфорилирования. CDK5 в сочетании с активатором также называют тау-протеинкиназой II.[41] Кроме того, сообщалось, что Cdk5 участвует в Активация Т-клеток и играют важную роль в развитии аутоиммунных заболеваний, таких как рассеянный склероз.[42]
Интерактивная карта проезда
Нажмите на гены, белки и метаболиты ниже, чтобы ссылки на соответствующие статьи.[§ 1]
- ^ Интерактивную карту путей можно редактировать на WikiPathways: «НикотинДопаминергический_WP1602».
Взаимодействия
Было показано, что циклин-зависимая киназа 5 взаимодействовать с разными молекулами и субстратами:
- Он взаимодействует с LMTK2,[43] NDEL1,[44] CDK5R1,[9][45] Нестин[46] и PAK1.[47]
- Ген CABLES1 кодирует циклин-зависимый белок, связывающий киназу, полное название которого Cdk5 и Abl ферментный субстрат 1. Этот связывающий белок связывает Cdk5 и c-Abl, тирозинкиназа. Активный c-Abl фосфорилирует CDK5 по тирозину 15, процесс усиливается белком CABLES1. В результате увеличивается активность Cdk5 / p35 в развивающихся нейронах. CABLES1 и упомянутое фосфорилирование могут играть важную роль в аксон регулирование роста.[48]
- Ген CABLES2 кодирует другой связывающий белок, Cdk5 и Abl ферментный субстрат 2. Хотя его функция неизвестна, он может быть задействован в G1-S. клеточный цикл переход, стадия между ростом клеток и репликацией ДНК.[49]
- Более того, Cdk5 фосфорилирует тирозинкиназу, ассоциированную с апоптозом (AATK). Этот белок, вероятно, вызывает задержку роста и миелоидный клетки-предшественники апоптоз, а также активирует CdkR1.[50]
- Глутатион S-трансфераза P Фермент, кодируемый геном GSTP1, вызывает отрицательную регуляцию или снижение активности Cdk5. Это достигается за счет транслокации p25 / p35 для предотвращения нейродегенерация.[51]
- Cdk5 связывается с белком Гистоновая деацетилаза 1 (HDAC1). Когда Cdk5 / p25 дерегулирует HDAC1, появляется аномальная активность клеточного цикла и двухцепочечные разрывы ДНК, вызывающие нейротоксичность.[52]
- Cdk5 цитоплазматический Распределение определяется активаторами p35 и p39. Оба активатора имеют мотивы локализации, которые приводят к присутствию Cdk5 в плазматическая мембрана и в околоядерный область, край. p35 и p39 миристоилирование позволяет Cdk5 связываться с мембранами.[53]
- Cdk5 также взаимодействует с APEX1 эндонуклеаза. Киназа фосфорилирует Thr-233, вызывая накопление повреждений ДНК и, в конечном итоге, гибель нейронов.[54]
- Cdk5 фосфорилирует и регулирует белок-супрессор опухоли p53. В апоптотическом Клетки PC12 наблюдается одновременное увеличение уровней Cdk5 и p53, поэтому считается, что механизм, с помощью которого Cdk5 индуцирует апоптоз, может быть вызван фосфорилированием и активацией p53.[55]
- Как только Cdk5 фосфорилируется белком, называемым EPH рецептор A4, фосфорилирует Факторы обмена гуаниновых нуклеотидов (NGEF) регулирующий RhoA и морфогенез дендритного шипа.[56]
- Cdk5 также фосфорилирует Киназа фокальной адгезии (ФАК). Это может стимулировать ядерную транслокацию, которая играет важную роль в миграции нейронов, регулируя центросома -ассоциированный микротрубочка структура.[57]
- Рецептор 5-гидрокситриптамина 6 (HTR6), который, как полагают, контролирует холинергический нейрональная передача в головном мозге, управляет миграцией пирамидных нейронов во время кортикогенез. Для этого HTR6 регулирует активность Cdk5.[58]
- Cdk5 взаимодействует с CTNNB1 и CTNND2 также.[59]
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000164885 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000028969 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ «1D PFV: 1UNH». Банк данных белков RCSB. Получено 2020-11-06.
- ^ Циклинзависимая киназа 5. Springer. 19 августа 2008 г. ISBN 978-0-387-78886-9.
- ^ Патрик Г. Н., Цукерберг Л., Николич М., де ла Монте С., Диккес П., Цай Л. Х. (декабрь 1999 г.). «Превращение p35 в p25 нарушает регуляцию активности Cdk5 и способствует нейродегенерации». Природа. 402 (6762): 615–22. Bibcode:1999Натура402..615П. Дои:10.1038/45159. PMID 10604467. S2CID 4414281.
- ^ Paglini G, Cáceres A (март 2001 г.). «Роль киназы Cdk5 - p35 в развитии нейронов». Европейский журнал биохимии. 268 (6): 1528–33. Дои:10.1046 / j.1432-1327.2001.02023.x. PMID 11248669.
- ^ а б Tarricone C, Dhavan R, Peng J, Areces LB, Tsai LH, Musacchio A (сентябрь 2001 г.). «Структура и регуляция комплекса CDK5-p25 (nck5a)». Молекулярная клетка. 8 (3): 657–69. Дои:10.1016 / S1097-2765 (01) 00343-4. PMID 11583627.
- ^ Кортес Н., Гусман-Мартинес Л., Андраде В., Гонсалес А., Макчони РБ (2019). «CDK5: уникальный CDK и его многочисленные роли в нервной системе». Журнал болезни Альцгеймера. 68 (3): 843–855. Дои:10.3233 / JAD-180792. PMID 30856110.
- ^ Сайто Т., Яно М., Кавай Й, Асада А., Вада М., Дои Х, Хисанага С. (ноябрь 2013 г.). «Структурная основа для различной стабильности и активности комплексов Cdk5 с активаторами p35 и p39». Журнал биологической химии. 288 (45): 32433–9. Дои:10.1074 / jbc.M113.512293. ЧВК 3820878. PMID 24085300.
- ^ «Запись OMIM - * 123831 - ЦИКЛИНЗАВИСИМАЯ КИНАЗА 5; CDK5». omim.org. Получено 2020-11-02.
- ^ Цай, Ли-Хуэй. Циклинзависимая киназа 5 (Cdk5).
- ^ Бибб Дж. А. (2003). «Роль Cdk5 в передаче сигналов нейронов, пластичности и злоупотреблении наркотиками». Нейросигналы. 12 (4–5): 191–9. Дои:10.1159/000074620. PMID 14673205. S2CID 10403277.
- ^ Seiwell AP, Reveron ME, Duvauchelle CL (апрель 2007 г.). «Повышенная экспрессия accumbens Cdk5 у крыс после непродолжительного приема кокаина, но не после сеансов длительного доступа». Письма о неврологии. 417 (1): 100–5. Дои:10.1016 / j.neulet.2007.02.043. ЧВК 1876973. PMID 17339080.
- ^ Шупп А., Казимиро М.С., Пестелл Р.Г. (март 2017 г.). «Биологические функции CDK5 и потенциальные целевые клинические методы лечения CDK5». Oncotarget. 8 (10): 17373–17382. Дои:10.18632 / oncotarget.14538. ЧВК 5370047. PMID 28077789.
- ^ Pareek TK, Lam E, Zheng X, Askew D, Kulkarni AB, Chance MR, et al. (Октябрь 2010 г.). «Циклинзависимая активность киназы 5 необходима для активации Т-клеток и индукции экспериментального аутоиммунного энцефаломиелита». Журнал экспериментальной медицины. 207 (11): 2507–19. Дои:10.1084 / jem.20100876. ЧВК 2964575. PMID 20937706.
- ^ Лам Э, Парик Т.К., Леттерио Дж.Дж. (2015). «Cdk5 контролирует экспрессию гена IL-2 посредством репрессии комплекса mSin3a-HDAC». Клеточный цикл. 14 (8): 1327–36. Дои:10.4161/15384101.2014.987621. ЧВК 4614394. PMID 25785643.
- ^ Флетчер А.И., Шуанг Р., Джованнуччи Д.Р., Чжан Л., Биттнер М.А., Стуенкель Е.Л. (февраль 1999 г.). «Регулирование экзоцитоза с помощью циклин-зависимой киназы 5 посредством фосфорилирования Munc18». Журнал биологической химии. 274 (7): 4027–35. Дои:10.1074 / jbc.274.7.4027. PMID 9933594. S2CID 32098805.
- ^ а б Шах К., Росси С. (апрель 2018 г.). "Сказка о хорошем и плохом Cdk5: Реконструкция актинового цитоскелета в мозге". Молекулярная нейробиология. 55 (4): 3426–3438. Дои:10.1007 / s12035-017-0525-3. ЧВК 6370010. PMID 28502042.
- ^ Aryal RP, Kwak PB, Tamayo AG, Gebert M, Chiu PL, Walz T, Weitz CJ (сентябрь 2017 г.). «Макромолекулярные сборки циркадных часов млекопитающих». Молекулярная клетка. 67 (5): 770–782.e6. Дои:10.1016 / j.molcel.2017.07.017. ЧВК 5679067. PMID 28886335.
- ^ Бренна А., Олейничак И., Чаван Р., Рипперджер Дж. А., Лангмессер С., Камерони Е. и др. (Ноябрь 2019 г.). «Циклин-зависимая киназа 5 (CDK5) регулирует циркадные часы». eLife. 8. Дои:10.7554 / eLife.50925. ЧВК 6890458. PMID 31687929.
- ^ «Per2 - период циркадного гомолога белка 2 - Mus musculus (мышь) - ген и белок Per2». www.uniprot.org. Получено 2020-10-31.
- ^ "Ген CRY1 - GeneCards | Белок CRY1 | Антитело CRY1". www.genecards.org. Получено 2020-10-31.
- ^ Шупп А., Казимиро М.С., Пестелл Р.Г. (март 2017 г.). «Биологические функции CDK5 и потенциальные целевые клинические методы лечения CDK5». Oncotarget. 8 (10): 17373–17382. Дои:10.18632 / oncotarget.14538. ЧВК 5370047. PMID 28077789.
- ^ Руфайель Р., Муршид Н. (ноябрь 2019 г.). «CDK5: ключевой регулятор апоптоза и выживания клеток». Биомедицины. 7 (4): 88. Дои:10.3390 / biomedicines7040088. ЧВК 6966452. PMID 31698798.
- ^ Шах К., Лахири Д.К. (июнь 2014 г.). «Активность Cdk5 в головном мозге - несколько путей регуляции». Журнал клеточной науки. 127 (Pt 11): 2391–400. Дои:10.1242 / jcs.147553. ЧВК 4038939. PMID 24879856.
- ^ Лю С.Л., Ван Ц., Цзян Т., Тан Л., Син А., Ю. Дж. Т. (сентябрь 2016 г.). «Роль Cdk5 в болезни Альцгеймера». Молекулярная нейробиология. 53 (7): 4328–42. Дои:10.1007 / s12035-015-9369-х. PMID 26227906. S2CID 17269616.
- ^ Цай, Ли-Хуэй. Циклинзависимая киназа 5 (Cdk5).
- ^ Cherubini M, Puigdellívol M, Alberch J, Ginés S (октябрь 2015 г.). «Cdk5-опосредованное деление митохондрий: ключевой игрок в дофаминергической токсичности при болезни Хантингтона». Biochimica et Biophysica Acta (BBA) - Молекулярная основа болезни. 1852 (10 Pt A): 2145–60. Дои:10.1016 / j.bbadis.2015.06.025. PMID 26143143.
- ^ Хэ Р, Хуанг В., Хуанг И, Сюй М., Сонг П, Хуанг И и др. (2018). «Пептид, ингибирующий Cdk5, предотвращает потерю дофаминергических нейронов и облегчает поведенческие изменения на мышиной модели болезни Паркинсона, вызванной MPTP». Границы старения нейронауки. 10: 162. Дои:10.3389 / fnagi.2018.00162. ЧВК 5992349. PMID 29910724.
- ^ Луо Ф, Берк К., Кантор С., Миллер Р. Х., Ян Й. (июль 2014 г.). «Циклин-зависимая киназа 5 опосредует созревание OPC у взрослых и репарацию миелина посредством модуляции передачи сигналов Akt и GsK-3β». Журнал неврологии. 34 (31): 10415–29. Дои:10.1523 / JNEUROSCI.0710-14.2014. ЧВК 4115145. PMID 25080600.
- ^ Франклин Р.Дж., Ffrench-Constant C (ноябрь 2008 г.). «Ремиелинизация в ЦНС: от биологии к терапии». Обзоры природы. Неврология. 9 (11): 839–55. Дои:10.1038 / номер 2480. PMID 18931697. S2CID 1270678.
- ^ Quintavalle M, Elia L, Price JH, Heynen-Genel S, Courtneidge SA (июль 2011 г.). «Скрининговый анализ с высоким содержанием клеток выявляет активаторы и ингибиторы инвазии раковых клеток». Научная сигнализация. 4 (183): ra49. Дои:10.1126 / scisignal.2002032. ЧВК 3291516. PMID 21791703.
- ^ Посо К., Бибб Дж. А. (октябрь 2016 г.). «Возникающая роль Cdk5 в раке». Тенденции рака. 2 (10): 606–618. Дои:10.1016 / j.trecan.2016.09.001. ЧВК 5132345. PMID 27917404.
- ^ Се В., Ван Х, Хэ И, Ли Д., Гун Л., Чжан И (2014-01-25). «CDK5 и его активатор P35 в нормальном гипофизе и в аденомах гипофиза: связь с экспрессией VEGF». Международный журнал биологических наук. 10 (2): 192–9. Дои:10.7150 / ijbs.7770. ЧВК 3927131. PMID 24550687.
- ^ Либл Дж., Вайтенштайнер С.Б., Вереб Г., Такач Л., Фюрст Р., Фоллмар А.М., Захлер С. (ноябрь 2010 г.). «Циклин-зависимая киназа 5 регулирует миграцию эндотелиальных клеток и ангиогенез». Журнал биологической химии. 285 (46): 35932–43. Дои:10.1074 / jbc.M110.126177. ЧВК 2975216. PMID 20826806.
- ^ Мерк Х., Чжан С., Лер Т., Мюллер С., Ульрих М., Бибб Дж. А. и др. (Февраль 2016). «Ингибирование эндотелиального Cdk5 снижает рост опухоли, способствуя непродуктивному ангиогенезу». Oncotarget. 7 (5): 6088–104. Дои:10.18632 / oncotarget.6842. ЧВК 4868742. PMID 26755662.
- ^ «CDK5 активирует передачу сигналов от гиппопотама, чтобы обеспечить устойчивость к лучевой терапии через повышающую регуляцию ТАЗ при раке легких». Международный журнал радиационной онкологии, биологии, физики.
- ^ Piccolo S, Dupont S, Cordenonsi M (октябрь 2014 г.). «Биология YAP / TAZ: передача сигналов бегемота и не только». Физиологические обзоры. 94 (4): 1287–312. Дои:10.1152 / Physrev.00005.2014. PMID 25287865.
- ^ Кобаяси С., Исигуро К., Омори А., Такамацу М., Ариока М., Имахори К., Учида Т. (декабрь 1993 г.). «Родственная cdc2 киназа PSSALRE / cdk5 гомологична 30 кДа субъединице тау-протеинкиназы II, пролин-направленной протеинкиназы, связанной с микротрубочками». Письма FEBS. 335 (2): 171–5. Дои:10.1016/0014-5793(93)80723-8. PMID 8253190. S2CID 26474408.
- ^ Pareek TK, Lam E, Zheng X, Askew D, Kulkarni AB, Chance MR, Huang AY, Cooke KR, Letterio JJ (октябрь 2010 г.). «Циклинзависимая активность киназы 5 необходима для активации Т-клеток и индукции экспериментального аутоиммунного энцефаломиелита». Журнал экспериментальной медицины. 207 (11): 2507–19. Дои:10.1084 / jem.20100876. ЧВК 2964575. PMID 20937706.
- ^ Кесавапани С., Лау К.Ф., Акерли С., Баннер С.Дж., Шемилт С.Дж., Купер Д.Д., Ли П.Н., Шоу К.Э., Маклафлин Д.М., Миллер С.К. (июнь 2003 г.). «Идентификация новой мембраносвязанной нейрональной киназы, циклин-зависимой киназы 5 / p35-регулируемой киназы». Журнал неврологии. 23 (12): 4975–83. Дои:10.1523 / JNEUROSCI.23-12-04975.2003. ЧВК 6741199. PMID 12832520.
- ^ Нитхаммер М., Смит Д.С., Айала Р., Пэн Дж., Ко Дж., Ли М.С., Морабито М., Цай Л.Х. (декабрь 2000 г.). «NUDEL - это новый субстрат Cdk5, который связывается с LIS1 и цитоплазматическим динеином». Нейрон. 28 (3): 697–711. Дои:10.1016 / S0896-6273 (00) 00147-1. PMID 11163260. S2CID 11154069.
- ^ Чен Ф., Студзинский Г.П. (июнь 2001 г.). «Экспрессия нейронального активатора циклин-зависимой киназы 5 p35Nck5a в моноцитарных клетках человека связана с дифференцировкой». Кровь. 97 (12): 3763–7. Дои:10.1182 / blood.V97.12.3763. PMID 11389014.
- ^ Сальгрен К.М., Михайлов А., Вайттинен С., Паллари Х.М., Калимо Х., Пант Х.С., Эрикссон Дж. Э. (июль 2003 г.). «Cdk5 регулирует организацию Nestin и его связь с p35». Молекулярная и клеточная биология. 23 (14): 5090–106. Дои:10.1128 / MCB.23.14.5090-5106.2003. ЧВК 162223. PMID 12832492.
- ^ Рашид Т., Банерджи М., Николич М. (декабрь 2001 г.). «Фосфорилирование Pak1 киназой p35 / Cdk5 влияет на морфологию нейронов». Журнал биологической химии. 276 (52): 49043–52. Дои:10.1074 / jbc.M105599200. PMID 11604394.
- ^ Цукерберг Л. Р., Патрик Г. Н., Николич М., Хумберт С., Ву К. Л., Ланье Л. М. и др. (Июнь 2000 г.). «Кабели связывают Cdk5 и c-Abl и облегчают фосфорилирование тирозина Cdk5, активацию киназы и рост нейритов». Нейрон. 26 (3): 633–46. Дои:10.1016 / S0896-6273 (00) 81200-3. HDL:1721.1/83489. PMID 10896159. S2CID 15142577.
- ^ «Резюме экспрессии белка CABLES2 - Атлас человеческого белка». www.proteinatlas.org. Получено 2020-11-01.
- ^ «Ген AATK - GeneCards | Белок LMTK1 | Антитело LMTK1». www.genecards.org. Получено 2020-11-01.
- ^ "Ген GSTP1 - Генные карты | Белок GSTP1 | Антитело GSTP1". www.genecards.org. Получено 2020-11-01.
- ^ Ким Д., Франк К.Л., Доббин М.М., Цунемото Р.К., Ту В., Пэн П.Л. и др. (Декабрь 2008 г.). «Дерегуляция HDAC1 с помощью p25 / Cdk5 при нейротоксичности». Нейрон. 60 (5): 803–17. Дои:10.1016 / j.neuron.2008.10.015. ЧВК 2912147. PMID 19081376.
- ^ Асада А., Ямамото Н., Года М., Сайто Т., Хаяси Н., Хисанага С. (август 2008 г.). «Миристоилирование p39 и p35 является детерминантом цитоплазматической или ядерной локализации активных циклин-зависимых комплексов киназы 5». Журнал нейрохимии. 106 (3): 1325–36. Дои:10.1111 / j.1471-4159.2008.05500.x. PMID 18507738. S2CID 205619401.
- ^ «APEX1 - ДНК- (апуриновый или апиримидиновый сайт) эндонуклеаза - Homo sapiens (человек) - ген и белок APEX1». www.uniprot.org. Получено 2020-11-01.
- ^ Чжан Дж., Кришнамурти П.К., Джонсон Г.В. (апрель 2002 г.). «Cdk5 фосфорилирует p53 и регулирует его активность». Журнал нейрохимии. 81 (2): 307–13. Дои:10.1046 / j.1471-4159.2002.00824.x. PMID 12064478. S2CID 42188500.
- ^ «Ген EPHA4 - Генные карты | Белок EPHA4 | Антитело EPHA4». www.genecards.org. Получено 2020-11-01.
- ^ Xie Z, Tsai LH (февраль 2004 г.). «Cdk5 фосфорилирование FAK регулирует миокротубулы, ассоциированные с центросомами, и миграцию нейронов». Клеточный цикл. 3 (2): 108–10. Дои:10.4161 / cc.3.2.646. PMID 14712065. S2CID 29625072.
- ^ "Ген HTR6 - GeneCards | Белок 5HT6R | Антитело 5HT6R". www.genecards.org. Получено 2020-11-01.
- ^ «CDK5 - подобная циклиноподобной киназе 5 - Homo sapiens (человек) - ген и белок CDK5». www.uniprot.org. Получено 2020-11-01.
дальнейшее чтение
- Моришима-Кавасима М, Хасэгава М, Такио К., Судзуки М, Йошида Х, Ватанабэ А, Титани К., Ихара Y (1995). «Гиперфосфорилирование тау в PHF». Нейробиология старения. 16 (3): 365–71, обсуждение 371–80. Дои:10.1016 / 0197-4580 (95) 00027-C. PMID 7566346. S2CID 22471158.
- Перуцци Ф., Гордон Дж., Дарбинян Н., Амини С. (декабрь 2002 г.). «Tat-индуцированная дерегуляция нейрональной дифференцировки и выживания посредством пути фактора роста нервов». Журнал нейровирологии. 8 Дополнение 2 (2): 91–6. Дои:10.1080/13550280290167885. PMID 12491158.
внешняя ссылка
- Циклинзависимые + киназа + 5 в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- CDK5 расположение человеческого гена в Браузер генома UCSC.
- CDK5 детали человеческого гена в Браузер генома UCSC.