Металлоорганическая химия - Organometallic chemistry

Металлоорганическая химия это изучение металлоорганические соединения, химические соединения содержащий по крайней мере один химическая связь между углерод атом органической молекулы и металл, включая щелочные, щелочноземельные и переходные металлы, а иногда также расширены, чтобы включать металлоиды, такие как бор, кремний и олово.[1] Помимо связей с фрагментами или молекулами органила, они связаны с «неорганическим» углеродом, например монооксид углерода (карбонилы металлов), цианиды или карбиды, как правило, также считаются металлоорганическими. Некоторые родственные соединения, такие как гидриды переходных металлов и комплексы фосфинов металлов часто включаются в обсуждения металлоорганических соединений, хотя, строго говоря, они не обязательно являются металлоорганическими. Родственный, но отличный термин "металлоорганическое соединение "относится к металлосодержащим соединениям, у которых отсутствуют прямые связи металл-углерод, но которые содержат органические лиганды. β-дикетонаты металлов, алкоксиды, диалкиламиды и комплексы фосфинов металлов являются типичными членами этого класса. Область металлоорганической химии объединяет аспекты традиционных неорганический и органическая химия.[2]
Металлоорганические соединения широко используются как стехиометрически в исследованиях и промышленных химических реакциях, так и в качестве катализаторов для увеличения скорости таких реакций (например, при использовании гомогенный катализ ), где целевые молекулы включают полимеры, фармацевтические препараты и многие другие типы практических продуктов.
Металлоорганические соединения
Металлоорганические соединения обозначаются приставкой «органо-», например палладиевые соединения. Примеры таких металлоорганических соединений включают все Реактивы Гилмана, которые содержат литий и медь. Тетракарбонил никель, и ферроцен являются примерами металлоорганических соединений, содержащих переходные металлы. Другие примеры включают магнийорганические соединения, такие как йод (метил) магний MeMgI, диметилмагний (Мне2Mg), и все Реактивы Гриньяра; литийорганические соединения, такие как п-бутиллитий (n-BuLi), цинкорганические соединения, такие как диэтилцинк (Et2Zn) и хлор (этоксикарбонилметил) цинк (ClZnCH2C (= O) OEt); и медноорганические соединения, такие как диметилкупрат лития (Li+[CuMe2]−).
Помимо традиционных металлов, лантаноидов, актинидов и полуметаллов, такие элементы, как бор, кремний, мышьяк, и селен считаются образующими металлоорганические соединения, например органоборан такие соединения, как триэтилборан (Et3Б).
- Типичные металлоорганические соединения

Ферроцен представляет собой архетипический комплекс железоорганических соединений. Это стабильное на воздухе, возгоняемое соединение.

Кобальтоцен является структурным аналогом ферроцена, но обладает высокой реакционной способностью по отношению к воздуху.

Трис (трифенилфосфин) карбонилгидрид родия используется в промышленном производстве многих на основе альдегидов ароматы.

Соль Цейзе является примером алкеновый комплекс переходных металлов.

Триметилалюминий представляет собой металлоорганическое соединение с мосты метильная группа. Он используется в промышленном производстве некоторых спиртов.

Диметилцинк имеет линейную координацию. Это летучая пирофорная жидкость, которая используется для изготовления полупроводниковых пленок.
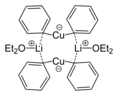
Бис (диэтилэфират) дифенилкупрата лития является примером Реактив Гилмана, тип медьорганического комплекса, часто применяемого в органическом синтезе.
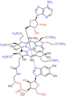
Аденозилкобаламин это кофактор требуется для нескольких важных ферментативных реакций, которые происходят в организме человека. Это редкий пример алкила металла (кобальта) в биологии.

Железо (0) пентакарбонил представляет собой красно-оранжевую жидкость, приготовленную непосредственно из соединения мелкодисперсного железа и газообразного монооксида углерода под давлением.

Технеций [99 мTc] сестамиби используется для изображения сердечной мышцы в ядерной медицине.
Координационные соединения с органическими лигандами
Много комплексы особенность координационные связи между металлом и органикой лиганды. Органические лиганды часто связывают металл через гетероатом такие как кислород или азот, и в этом случае такие соединения считаются координационными соединениями. Однако если какой-либо из лигандов образует прямую связь M-C, то комплекс считается металлоорганическим. IUPAC явно включает переходные металлы, металлы основной группы и полуметаллы, такие как бор, кремний, мышьяк и селен, как примеры центрального металла M.[3]
Хотя IUPAC не дал официального определения этому термину, некоторые химики используют термин «металлоорганический» для описания любого соединения, содержащего органический лиганд, независимо от наличия прямой связи M-C.[4]
Встречающийся в природе алкильный комплекс переходного металла является метилкобаламин (форма Витамин B12 ), с кобальт -метил связь. Это подмножество комплексов часто обсуждается в подполе биоорганометаллическая химия.[5] Наглядный пример многих функций B12-зависимые ферменты, MTR фермент катализирует перенос метильной группы с азота на N5-метил-тетрагидрофолат до серы гомоцистеин производить метионин.
Статус соединений, в которых канонический анион имеет делокализованную структуру, в которой отрицательный заряд разделяется с атомом более электроотрицательным, чем углерод, как в енолирует, может варьироваться в зависимости от природы анионного фрагмента, иона металла и, возможно, среды; в отсутствие прямых структурных доказательств наличия связи углерод-металл такие соединения не считаются металлоорганическими.[3] Например, еноляты лития часто содержат только связи Li-O и не являются металлоорганическими, в то время как еноляты цинка (реагенты Реформатского) содержат как связи Zn-O, так и Zn-C, и по своей природе являются металлоорганическими.
Структура и свойства
Связь металл-углерод в металлоорганических соединениях обычно высока. ковалентный. Для элементов с высокой электроположительностью, таких как литий и натрий, углеродный лиганд проявляет карбанионный характер, но свободные анионы на основе углерода чрезвычайно редки, например цианид.
Концепции и техники
Как и в других областях химии, счет электронов полезен для организации металлоорганической химии. В 18-электронное правило помогает в прогнозировании стабильности карбонилы металлов и родственные соединения. Однако большинство металлоорганических соединений не подчиняются правилу 18e. Химическая связь и реакционная способность в металлоорганических соединениях часто обсуждается с точки зрения изолобальный принцип.
А также дифракция рентгеновских лучей, ЯМР и ИК-спектроскопия - общие методы, используемые для определения структуры. Динамические свойства металлоорганических соединений часто исследуются с помощью ЯМР при переменной температуре и химической кинетики.
Металлоорганические соединения претерпевают несколько важных реакций:
- окислительная добавка и восстановительное устранение
- трансметалляция
- карбометализация
- гидрометалляция
- перенос электронов
- устранение β-гидрида
- реакция металлоорганического замещения
- активация углерод-водородной связи
- циклометалляция
- миграционная вставка
- нуклеофильная абстракция
История
Ранние разработки в области металлоорганической химии включают Луи Клод Кадет синтез соединений метил мышьяка, связанных с какодил, Уильям Кристофер Цейс с[6] платино-этиленовый комплекс,[7] Эдвард Франкленд открытие диэтил- и диметилцинк, Людвиг Монд открытие Ni (CO)4,[1] и Виктор Гриньяр Магнийорганические соединения. (Хотя не всегда признается металлоорганическим соединением, Берлинская лазурь железо-цианидный комплекс смешанной валентности был впервые получен в 1706 году мастером по производству красок. Иоганн Якоб Дисбах как первый координационный полимер и синтетический материал, содержащий связь металл-углерод.[1]) Обильные и разнообразные продукты из угля и нефти привели к Циглер – Натта, Фишер-Тропш, гидроформилирование катализ с использованием CO, H2, а также алкены в качестве сырья и лигандов.
Признание металлоорганической химии в качестве отдельной области привело к присуждению Нобелевской премии Эрнст Фишер и Джеффри Уилкинсон для работы над металлоцены. В 2005 году, Ив Шовен, Роберт Х. Граббс и Ричард Р. Шрок разделила Нобелевскую премию за катализируемые металлами метатезис олефинов.[8]
Хронология металлоорганической химии
- 1760 Луи Клод Кадет де Гассикур исследует чернила на основе кобальт соли и изоляты какодил из минерала кобальта, содержащего мышьяк
- 1827 Уильям Кристофер Цейс производит Соль Цейзе; первый платина / олефин сложный
- 1848 Эдвард Франкленд обнаруживает диэтилцинк
- 1863 Чарльз Фридель и Джеймс Крафтс приготовить хлорсиланы
- 1890 Людвиг Монд обнаруживает карбонил никеля
- 1899 г. - введение Реакция Гриньяра
- 1899 Джон Ульрик Неф обнаруживает алкинилирование с использованием натрия ацетилиды.
- 1900 Поль Сабатье работает на гидрирование органические соединения с металлическими катализаторами. Гидрирование жиры начинает продвижение пищевая промышленность, видеть маргарин
- 1909 Пол Эрлих вводит Сальварсан для лечения сифилиса, металлоорганическое соединение на основе раннего мышьяка
- 1912 Нобелевская премия Виктор Гриньяр и Поль Сабатье
- 1930 Генри Гилман работает с купратами лития, см. Реактив Гилмана
- 1951 Уолтер Хибер был награжден Альфред Сток приз за его работу с карбонил металла химия.
- 1951 Ферроцен обнаружен
- 1956 Дороти Кроуфут Ходжкин определяет структуру витамин B12, первая биомолекула, содержащая связь металл-углерод, см. биоорганометаллическая химия
- 1963 Нобелевская премия за Карл Циглер и Джулио Натта на Катализатор Циглера-Натта
- 1965 Открытие циклобутадиен, трикарбонил железа
- 1968 Чертовски реакция
- 1973 Нобелевская премия Джеффри Уилкинсон и Эрнст Отто Фишер на сэндвич-смеси
- 1981 Нобелевская премия Роальд Хоффманн и Кеничи Фукуи для создания правил Вудворда-Хоффмана
- 2001 Нобелевская премия У. С. Ноулз, Р. Нойори и Карл Барри Шарплесс для асимметричного гидрирования
- 2005 Нобелевская премия Ив Шовен, Роберт Граббс, и Ричард Шрок на катализируемом металлом метатезис алкенов
- 2010 Нобелевская премия Ричард Ф. Хек, Эй-ичи Негиси, Акира Сузуки для реакций кросс-сочетания, катализируемых палладием
Объем
К специальностям металлоорганической химии относятся:
- Период 2 элемента: литийорганическая химия, бериллийорганическая химия, органоборановая химия,
- Период 3 элемента: магнийорганическая химия, алюминийорганическая химия, кремнийорганическая химия
- Период 4 элемента: титаноорганическая химия, хроморганическая химия, химия марганца железоорганическая химия, органокобальтовая химия никельорганическая химия, медьорганическая химия, цинкорганическая химия, химия органо-галлия, химия германия
- Период 5 элементов: органорутениевая химия, палладиеорганическая химия, химия кремния, кадмийорганическая химия, органоиндиевая химия, оловоорганическая химия
- Период 6 элементов: химия органолантаноидов, химия органического углерода, органоиридий химия, платинорганическая химия, золотоорганическая химия, ртутьорганическая химия, химия органического вещества, химия свинца
- Период 7 элементов: органоорганическая химия
Промышленное применение
Металлоорганические соединения находят широкое применение в коммерческих реакциях, как в гомогенный катализ и как стехиометрические реагенты. Например, литийорганический, магнийорганический, и алюминийорганические соединения, примеры которых являются высокоосновными и сильно восстанавливающими, полезны стехиометрически, но также катализируют многие реакции полимеризации.[2]
Почти все процессы с участием окиси углерода основаны на катализаторах, известные примеры описаны как карбонилирование.[9] Производство уксусной кислоты из метанола и окиси углерода катализируется через карбонильные комплексы металлов в Монсанто процесс и Cativa процесс. Большинство синтетических альдегидов производятся гидроформилирование. Основная часть синтетических спиртов, по крайней мере, больше, чем этанол, производится гидрирование альдегидов, производных гидроформилирования. Точно так же Wacker процесс используется при окислении этилен к ацетальдегид.[10]
Практически все производственные процессы с участием алкен -производные полимеры основаны на металлоорганических катализаторах. Полиэтилен и полипропилен в мире производятся как на неоднородно через Циглер – Натта катализ и гомогенно, например, через катализаторы с ограниченной геометрией.[11]
В большинстве процессов с участием водорода используются катализаторы на основе металлов. В то время как объемное гидрирование, например производство маргарина, полагаться на гетерогенные катализаторы, для производства тонких химикатов, таких гидрогенизация полагаются на растворимые металлоорганические комплексы или включают металлоорганические промежуточные соединения.[12] Металлоорганические комплексы позволяют проводить эти гидрогенизации асимметрично.

Многие полупроводники производятся из триметилгаллий, триметилиндий, триметилалюминий, и триметилсурьма. Эти летучие соединения разлагаются вместе с аммиак, арсин, фосфин и родственные гидриды на нагретой подложке через эпитаксия из паровой фазы металлоорганических соединений (MOVPE) процесс производства светодиоды (Светодиоды).
Металлоорганические реакции
Синтезу многих органических молекул способствуют металлоорганические комплексы. Метатезис сигма-связи синтетический метод образования новых углерод-углерод сигма-облигации. Метатезис сигма-связи обычно используется с комплексами ранних переходных металлов, которые находятся в самой высокой степени окисления.[13] Использование переходных металлов с наивысшей степенью окисления предотвращает протекание других реакций, таких как окислительная добавка. Помимо метатезиса сигма-связи, метатезис олефинов используется для синтеза различных углерод-углеродных пи-облигации. Ни метатезис сигма-связи, ни метатезис олефинов не изменяют степень окисления металла.[14][15] Многие другие методы используются для образования новых углерод-углеродных связей, в том числе устранение бета-гидрида и реакции вставки.
Катализ
Металлоорганические комплексы обычно используются в катализе. Основные производственные процессы включают гидрирование, гидросилилирование, гидроцианирование, метатезис олефинов, полимеризация алкена, олигомеризация алкена, гидрокарбоксилирование, карбонилирование метанола, и гидроформилирование.[16] Металлоорганические промежуточные соединения также используются во многих гетерогенный катализ процессы, аналогичные перечисленным выше. Кроме того, предполагается, что металлоорганические промежуточные соединения Процесс Фишера-Тропша.
Металлоорганические комплексы также широко используются в мелкомасштабном тонком химическом синтезе, особенно в реакции кросс-сочетания[17] которые образуют углерод-углеродные связи, например Муфта Сузуки-Мияура,[18] Аминирование Бухвальда-Хартвига для получения ариламинов из арилгалогенидов,[19] и Муфта Соногашира, так далее.
Проблемы окружающей среды
Природные и загрязняющие металлоорганические соединения обнаруживаются в окружающей среде. Некоторые из них, такие как органический свинец и ртутьорганические соединения, являются остатками их использования человеком. Тетраэтилсвинец был подготовлен для использования в качестве бензин добавка, но вышла из употребления из-за токсичности свинца. Его заменителями являются другие металлоорганические соединения, такие как ферроцен и метилциклопентадиенил трикарбонил марганца (ММТ).[20] В мышьяковоорганическое соединение роксарсон - спорная добавка к корму для животных. В 2006 году только в США было произведено около миллиона килограммов этого продукта.[21]

Смотрите также
Рекомендации
- ^ а б c Крэбтри, Роберт Х. (2009). Металлоорганическая химия переходных металлов. (5-е изд.). Нью-Йорк, штат Нью-Йорк: Джон Уайли и сыновья. стр. 2, 560, и пассим. ISBN 978-0470257623. Получено 23 мая 2016.
- ^ а б Оливейра, Хосе; Эльшенбройх, Кристоф (2006). Металлоорганические соединения (3., полностью перераб. И доп. Ред.). Weinheim: Wiley-VCH-Verl. ISBN 978-3-527-29390-2.
- ^ а б «ИЮПАК - металлоорганические соединения (O04328)». goldbook.iupac.org. Получено 2020-03-23.
- ^ Энциклопедия межфазной химии: поверхностная наука и электрохимия. Том 1, 1.1 экспериментальные методы, 1.2 наука о поверхности в условиях окружающей среды. Вандельт, К. (Клаус), 1944-. Амстердам, Нидерланды. 29 марта 2018. с. 762. ISBN 978-0-12-809894-3. OCLC 1031373796.CS1 maint: другие (связь)
- ^ Берг, Джереми М .; Липпард, Стивен Дж. (1994). Основы биоинорганической химии ([Pbk. Ed.]. Ed.). Милл-Вэлли: университетские научные книги. ISBN 978-0-935702-73-6.
- ^ Хант, Л. Б. (1984). «Первые металлоорганические соединения: Уильям Кристофер Цейзе и его платиновые комплексы» (PDF). Platinum Metals Rev. 28 (2): 76–83.
- ^ Zeise, W.C. (1831). "Von der Wirkung zwischen Platinchlorid und Alkohol, und von den dabei entstehenden neuen Substanzen". Annalen der Physik. 97 (4): 497–541. Bibcode:1831АнП .... 97..497Z. Дои:10.1002 / andp.18310970402.
- ^ Драгутан, В .; Драгутан, И .; Балабан, А. Т. (2006). "Нобелевская премия по химии 2005 г.". Обзор платиновых металлов. 50 (1): 35–37. Дои:10.1595 / 147106706X94140. ISSN 0032-1400.
- ^ В. Бертлефф; М. Ропер; X. Сава. «Карбонилирование». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a05_217.
- ^ Леувен, Пит W.N.M. фургон (2004). Гомогенный катализ: понимание искусства. Дордрехт: Спрингер. ISBN 978-1-4020-3176-2.
- ^ Клосин, Ежи; Fontaine, Philip P .; Фигероа, Рут (2015). «Разработка молекулярных катализаторов группы IV для высокотемпературных реакций сополимеризации этилена-α-олефина». Отчеты о химических исследованиях. 48 (7): 2004–2016. Дои:10.1021 / acs.accounts.5b00065. ISSN 0001-4842. PMID 26151395.
- ^ Пол Н. Райландер, «Гидрирование и дегидрирование» в Энциклопедия промышленной химии Ульмана, Wiley-VCH, Weinheim, 2005. Дои:10.1002 / 14356007.a13_487
- ^ Уотерман, Рори (2013-12-23). «Метатезис σ-Бонда: 30-летняя ретроспектива». Металлоорганические соединения. 32 (24): 7249–7263. Дои:10.1021 / om400760k. ISSN 0276-7333.
- ^ "Металлоорганический гипертекстовая книга: метатезис олефинов". www.ilpi.com. Получено 2017-12-26.
- ^ "Металлоорганический HyperTextBook: Метатезис сигма-связи". www.ilpi.com. Получено 2017-12-26.
- ^ П. W.N.M. ван Леувен "Гомогенный катализ: понимание искусства", 2004 Kluwer, Dordrecht. ISBN 1-4020-2000-7
- ^ Джана, Ранджан; Pathak, Tejas P .; Сигман, Мэтью С. (09.03.2011). «Достижения в реакциях перекрестного связывания, катализируемых переходными металлами (Pd, Ni, Fe), с использованием алкилорганических соединений в качестве партнеров реакции». Химические обзоры. 111 (3): 1417–1492. Дои:10.1021 / cr100327p. ISSN 0009-2665. ЧВК 3075866. PMID 21319862.
- ^ Малуэнда, Ирэн; Наварро, Оскар (24 апреля 2015 г.). «Последние изменения в реакции Сузуки-Мияуры: 2010–2014 гг.». Молекулы. 20 (5): 7528–7557. Дои:10,3390 / молекул20057528. ЧВК 6272665. PMID 25919276.
- ^ Магано, Хавьер; Дунец, Джошуа Р. (09.03.2011). «Широкомасштабное применение соединений, катализируемых переходными металлами, для синтеза фармацевтических препаратов». Химические обзоры. 111 (3): 2177–2250. Дои:10.1021 / cr100346g. ISSN 0009-2665. PMID 21391570.
- ^ Сейферт, Д. (2003). "Взлет и падение тетраэтилсвинца. 2". Металлоорганические соединения. 22 (25): 5154–5178. Дои:10.1021 / om030621b.
- ^ Хайлман, Б. (9 апреля 2007 г.). «Мышьяк в курином производстве». Новости химии и техники. С. 34–35.
Эта научная статья требует дополнительных цитаты к вторичные или третичные источники (Май 2016) (Узнайте, как и когда удалить этот шаблон сообщения) |
дальнейшее чтение
- Эльшенбройх, Кристоф (2016). Металлоорганические соединения (3-е изд.). Нью-Йорк, штат Нью-Йорк: Джон Уайли и сыновья. ISBN 978-3527805143. Получено 23 мая 2016.
- Клейден, Джонатан; Гривс, Ник; Уоррен, Стюарт (2012). Органическая химия (2-е изд.). Оксфорд, Великобритания: Издательство Оксфордского университета. стр. 132f 182–196, 218ff. 444f, 509f, 656–693 пассим, 858, 1009, 1069–1101, 1107–1131 пассим. ISBN 978-0199270293. Получено 2 февраля 2016.
- Крэбтри, Роберт Х. (2009). Металлоорганическая химия переходных металлов. (5-е изд.). Нью-Йорк, штат Нью-Йорк: Джон Уайли и сыновья. ISBN 978-0470257623. Получено 23 мая 2016.
- Дженкинс, Пол Р. (1992). Металлоорганические реагенты в синтезе. Oxford Chemistry Primers, № 3. Оксфорд, Великобритания: Oxford University Press. ISBN 978-0198556664. ISSN 1367-109X. Получено 23 мая 2016.
- Пирсон, Энтони Дж. (1985). Металлоорганическая химия. Нью-Йорк, штат Нью-Йорк: Джон Уайли и сыновья. ISBN 978-0471904465. Получено 23 мая 2016.
- Гупта, Элиас А.Дж. (2016) Основы металлоорганической химии Universities Press (Индия) ISBN 978-81-7371-874-8










